i T.C.
SELÇUK ÜNĠVERSĠTESĠ SAĞLIK BĠLĠMLERĠ ENSTĠTÜSÜ
TĠROĠT KANSERLĠ HASTALARDA OPERASYON ÖNCESĠ VE SONRASI ESER ELEMENTLERĠN SERUMDAKĠ DEĞĠġĠKLĠKLERĠ
TUĞRUL KADĠR DÜNDAR
DOKTORA TEZĠ
FĠZYOLOJĠ (TIP) ANABĠLĠM DALI
DANIġMAN
PROF. DR. ABDÜLKERĠM KASIM BALTACI
ii T.C.
SELÇUK ÜNĠVERSĠTESĠ SAĞLIK BĠLĠMLERĠ ENSTĠTÜSÜ
TĠROĠT KANSERLĠ HASTALARDA OPERASYON ÖNCESĠ VE SONRASI ESER ELEMENTLERĠN SERUMDAKĠ DEĞĠġĠKLĠKLERĠ
TUĞRUL KADĠR DÜNDAR
DOKTORA TEZĠ
FĠZYOLOJĠ (TIP) ANABĠLĠM DALI
DANIġMAN
PROF. DR. ABDÜLKERĠM KASIM BALTACI
Bu çalıĢma Selçuk Üniversitesi Bilimsel AraĢtırma Programı (BAP) Koordinatörlüğü tarafından 09202081 nolu proje olarak desteklenmiĢtir.
i
i.ÖNSÖZ
Tiroit hormonları ile eser elementler arasında önemli bir iliĢki vardır. Hem eser elementler tiroit hormon metabolizmasına karıĢır, hem de tiroit fonksiyonundaki bozukluklar eser elementlerin kan ve dokulardaki düzeylerini değiĢtirebilir. Tiroit hormon metabolizmasına karıĢan bu eser elementlerin en önemlilerinden birisi de çinkodur. Çinkonun hem deney hayvanları, hem de insanlarda plazma tiroit hormon seviyelerini etkileyerek, tiroit aktivitesine karıĢtığı bilinmektedir. Çinkoya bağlı endokrin fonksiyonlardan birisi de, düĢük çinko diyeti alan insan ve hayvanlarda tiroit hormon metabolizması ve enerji tüketimindeki değiĢikliklerdir. Hem deney hayvanları, hem de insanlar üzerinde yapılan çalıĢmalar iyot yetersizliği durumunda, çinko yetersizliğinin guatr geliĢimi için bir stimulus olabileceğini göstermektedir. Ancak yine de sonuçlar arasında tam bir uyum yoktur. Bu çalıĢmanın amacı da tiroit kanserli hastalarda operasyon öncesi ve sonrası eser elementlerin serumdaki değiĢikliklerinin araĢtırılmasıdır.
Mevcut çalıĢma Selçuk Üniversitesi Bilimsel AraĢtırma Programı (BAP) Koordinatörlüğü tarafından 09202081 nolu proje olarak desteklenmiĢtir.
Tez çalıĢmam sırasında her türlü bilimsel desteğini ve katkısını gördüğüm danıĢman hocam Prof. Dr. Abdülkerim Kasım Baltacı‟ya teĢekkürü borç bilirim. Ayrıca çalıĢmam süresince hasta temini ve takibi konusunda yardımlarından dolayı Necmettin Erbakan Üniversitesi Meram Tıp Fakültesi Genel Cerrahi Anabilim Dalı Öğretim Üyesi Prof. Dr. Faruk Aksoy‟a, çalıĢmamın patolojik değerlendirmelerini yapan Necmettin Erbakan Üniversitesi Meram Tıp Fakültesi Patoloji Anabilim Dalı Öğretim Üyesi Prof. Dr. Mustafa Cihat Avunduk‟a, tez çalıĢmam boyunca desteğini gördüğüm Selçuk Üniversitesi Tıp Fakültesi Fizyoloji Anabilim Dalı Öğretim Üyesi Prof. Dr. Rasim Moğulkoç‟a, atomik emisyon cihazındaki eser elementlerin analizlerinde yardımcı olan Selçuk Üniversitesi Tıp Fakültesi Fizyoloji Anabilim Dalı Yüksek Lisans öğrencisi Mine Yılmaz‟a teĢekkürü bir borç bilirim.
ii
ii.ĠÇĠNDEKĠLER Sayfa
1.GĠRĠġ 1
1.1. Tiroit Bezi 2
1.1.1.Tiroit Bezinin Anatomisi ve Embriyolojisi 2
1.1.2.Tiroit Bezinin Histolojik Yapısı 4
1.1.3.Tiroit Hormonları 4
1.1.4.Tiroit Hormonlarının Sentez ve Salınımı 5
1.1.5.Tiroit Hormonlarının Metabolizması 8
1.1.6.Tiroit Hormon Sekresyonunun Düzenlenmesi 10
1.1.7.Tiroit Hormonlarının Fizyolojik Fonksiyonlar Üzerine Etkileri 11
1.2.Tiroit Bezinin Eser Elementlerle ĠliĢkisi 15
1.2.1.Tiroit Hastalıkları ve Ġyot 16
1.3.Tiroit Hormonları ve Selenyum 17
1.4.Tiroit Fonksiyonu ve Çinko 18
1.5.Diğer Elementler ve Tiroit 20
2.GEREÇ ve YÖNTEM 21
2.1. Grupların OluĢturulması 21
2.2. Kan ve Doku Örneklerinin Alınması 21
2.3.Serumda Element Analizleri 22
2.4. Tiroit Dokusunda Element Analizleri 22
2.5. Ġstatistiksel Değerlendirmeler 22
3.BULGULAR 23
3.1. Operasyon Öncesi Deneklerin Element Düzeyleri 23
3.2. Operasyon Sonrası Deneklerin Element Düzeyleri 24
3.3. Operasyon Sonrası Deneklerin Tiroit Element Düzeyleri 25
iii 4.TARTIġMA 27 5.SONUÇ ve ÖNERĠLER 30 6.ÖZET 31 7.SUMMARY 32 8.KAYNAKLAR 33 9.EKLER 37 10.ÖZGEÇMĠġ 46
1
1.GĠRĠġ
Tiroit hormonları ile eser elementler arasında önemli bir iliĢki vardır (Ravaglia ve ark 2000). Hem eser elementler tiroit hormon metabolizmasına karıĢır, hem de tiroit fonksiyonundaki bozukluklar eser elementlerin kan ve dokulardaki düzeylerini değiĢtirebilir (Arthur ve Beckett 1999, Ravaglia ve ark 2000). Tiroit hormon metabolizmasına karıĢan bu eser elementlerin en önemlilerinden birisi de çinkodur (Farooqi ve ark 2000). Çinko tip 1 5‟-deiyodinaz‟ın fonksiyonunda vazgeçilmez elementtir ve bu enzim T4‟ün aktif formu olan T3‟e dönüĢümü için gereklidir (Danforth ve Burger 1989). Çinko sadece tiroit hormonlarının aktivitesinde değil, aynı zamanda ön hipofizden TSH ve hipotalamustan TRH sentezi için de gereklidir (Brandao-Neto ve ark 2006, Pekary ve ark 1991).
Tiroit hormon aktivitesindeki değiĢikliklerin, selenyum düzeylerinde de önemli değiĢikliklere yol açtığı (Liu ve ark 2001), selenyum eksikliğinin tiroit hormonlarının düzenleyici fonksiyonları için bir risk oluĢturduğuna dikkat çekilmektedir (Kvícala ve Zamrazil 2003). Tiroit kanserli hastaların tiroit dokusundaki selenyum ve çinko konsantrasyonlarının önemli ölçüde düĢük bulunduğu, bahsedilen bu elementlerin karsinojenik süreçte rol oynayabilecekleri rapor edilmiĢtir (Kucharzewski ve ark 2003). Kralik ve ark. (1996)‟ı gerçekleĢtirdikleri çalıĢmalarında selenyum ve çinkonun tiroit hormon metabolizması için önemli olduğunu, bu elementlerin eksikliğinde tiroit aktivitesinin de olumsuz etkileneceğini rapor etmiĢlerdir.
Tiroit kanserli hastaların cerrahi operasyon sonrasında magnezyum düzeylerinin önemli ölçüde azaldığı (Al-Sayer ve ark 2004), yine deneysel hipertiroidide hem eritrositte, hem de plazmada magnezyum düzeylerinin kontrollerinden daha düĢük seviyede olduğu (Simsek ve ark 1997) rapor edilmiĢtir.
Tiroit aktivitesindeki değiĢikliklerin bakır metabolizmasını da etkilediği bilinmektedir (Zhang ve ark 2004). Tiroit kanserli hastaların kandaki bakır konsantrasyonunun yüksek bulunduğu ileri sürülürken (Kucharzewski ve ark 2003), tam tersi bir baĢka çalıĢmada tiroit kanserli hastaların operasyon öncesi kontrollerinden farklı olmayan serumdaki bakır seviyelerinin operasyon sonrası önemli ölçüde baskılandığı gösterilmiĢtir (Al-Sayer ve ark 2004).
2
Tiroit fonksiyonları ve eser elementler arasındaki iliĢkiyi araĢtıran çok sayıda yayın olmasına rağmen, yine de sonuçlar arasında tam bir uyum yoktur (Kralik ve ark 1996, Morley ve ark 1991). Buna karĢın, tiroit kanserli hastalarda eser element metabolizmasının nasıl etkilendiğiyle ilgili sınırlı sayıda rapor vardır (Al-Sayer ve ark 2004). Tiroit kanserli hastalarda serumdaki eser element düzeylerindeki değiĢikliklerin ortaya konulması ve bu değiĢikliklerin takibinin hastalığın seyri açısından önemli olabileceğine dikkat çekilmektedir (Al-Sayer ve ark 2004). Bu çalıĢmanın amacı da tiroit kanserli hastalarda eser element düzeyindeki değiĢikliklerin araĢtırılmasıdır.
1.1.Tiroit Bezi
Tiroit bezi tanımlanan ilk endokrin bezdir (Ata 1999). Tiroit bezini ilk tanımlayan M.S. ikinci yüzyılda Galen olmuĢtur. Beze tiroit ismini veren ise 1656 yılında bez üzerine ilk monografı yazan Thomas Wharton„dur. Organın fonksiyonu, kretinizim ve miksödem oluĢumunun aydınlatılması için klinik gözlemlerin ve deneysel tiroidektominin birleĢtirildiği on dokuzuncu yüzyılın sonlarına kadar bilinememiĢtir (Ata 1999).
Tiroit hormonunun modern bilgisinin temelini oluĢturan ise, tiroidin gliserin ekstremlerinin ve nihayet hafif piĢirilmiĢ koyun tiroidinin yenmesinin miksödeme iyi geldiğinin 1893‟de anlaĢılması olmuĢtur (Ata 1999).
Tiroit bezi temelde iki hormon üretir, bunlar tiroksin (T4) ve triiyodotironin (T3) dir. Bu hormonlar bazal oksijen kullanımını ve metabolizmasını ve buna bağlı olarak ısı üretim hızını artırırlar. Böylece enerji ihtiyacı, kalorik destek ve termal ortamlardaki değiĢikliklere karĢı vücudu ayarlarlar. Tiroit hormonları aynı zamanda uygun metabolik hızın devam etmesi için gerekli olan oksijen ihtiyacı artırırlar. Son olarak, tiroit hormonları fetus ve çocuğun normal büyüme ve olgunlaĢmasında kritik öneme sahiptir (Yanıçoğlu 2002; Yörükan ve ark 2001).
1.1.1. Tiroit Bezinin Anatomisi ve Embriyolojisi
Embriyonal hayatın 4. haftasında ağız boĢluğunda dil üzerinde endodermal hücre çoğalması Ģeklinde baĢlayan tiroid taslağı, aĢağı doğru göç ederek hyoid kıkırdağın altına ulaĢır. Tiroglossal kanalın her iki ucunda oluĢan çıkıntılar tiroid loblarını oluĢtururken, bu sürecin sonunda tiroglossal kanal kapanır. Embriyonal hayatın 8. haftasında tiroglobülin (Tg) sentezlenirken, 10. haftada iyot tutulmaya
3
baĢlanarak tiroid bezi fonksiyonel hale geçer (Rogers 1994). T4 ve tiroksin bağlayan globülin (TBG) ilk kez embriyonal hayatın 8-10. haftalarında görülür (Burrow ve ark 1994). Tiroid uyarıcı hormon (TSH) ise 12. haftadan sonra salgılanır ve bu dönemden itibaren fetal hipotalamus-hipofiz-tiroid ekseni, anneden bağımsız olarak çalıĢmaya baĢlar (Rogers 1994).
Tiroit bezi kahverengimsi-kırmızı renkte ve zengin damar ağına sahip bir bezdir. Bu bez 5. servikal ile 1. torakal vertebra‟lar arasında yer alır. Fascia servikalis (profunda)‟in lamina pretrachealis‟i ile örtülüdür. Bu bezin lobus dexter ile lobus sinister olmak üzere iki lobu ve bu iki lobu birbirine bağlayan isthmus glandulae thyroideae adı verilen bir parçası vardır. Nadiren, isthmus glandulae thyroideae bulunmayabilir ve bu durumda bez iki ayrı parçadan oluĢur. %40 olguda ise lobus pyramidalis adı verilen ve isthmus glandulae thyroideae‟dan hyoid kemiğine doğru uzanan bir lob bulunabilir. Lobus pyramidalis ductus thyroglosus‟un alt ucunun açık kalmasıyla oluĢur. Embriyoda bu ductus dilde bulunan foramen caecum linguae‟ye açılır.
Tiroit bezinin ağırlığı yaklaĢık 20-25 g olup kadınlarda erkeklere oranla biraz daha büyük ve ağırdır. Loblar piramit Ģeklindedir. Piramidin tepesi yukarıda ve tabanı aĢağıdadır. Tepesi tiroit kıkırdağın linea obliqua‟sına, tabanı ise aĢağıda trachea‟nın 4. ve 5. kıkırdak halkaları hizasına kadar uzanır. Her bir lobun ortalama uzunluğu 5 cm‟dir. Isthmus glandulae thyroideae ise ortalama 1,25 cm uzunlukta olup trachea‟nın 2. veya 3. kıkırdak halkalarının ön yüzünde yer alır. Lobların konveks olan dıĢ yüzü (facies superficialis), m. sternothyroideus, m sternohyoideus ve m. omohyoideus‟un venter superior‟u, aĢağıda ise m. sternocleidomastoideus ile örtülüdür. Ġç yüzleri larynx, trachea, m. cricothyroideus‟u inerve eden n. laryngeus externus, n. laryngeus recurrens ve oseophagaus ile komĢuluk yapar. Lobların arka-dıĢ yüzü carotis kılıfı ile komĢu olup a. carotis communis‟i sarar. Ġnce olan ön kenarları a. thyroidea superior‟un ramus anterior‟u ile, yuvarlak olan arka kenarları ise a. thyroidea superior‟un ramus glandularis posterior‟u ile komĢuluk yapar.
Tiroit bezi capsula fibrosa adı verilen bir kapsül ile sarılıdır. Bu kapsül bezin parankimasına uzantılar göndererek bezi loblara ve lobüllere ayırır. Fascia servikalis (profunda)‟in lamina pretrachealis‟i bu kapsülün dıĢında yer alır. Lamina pretrachealis krikoid kıkırdak ve tiroit kıkırdağının linea obliqua‟sına tutunarak sonlanır. Bu nedenle, tiroit bezi yutma iĢlemi esnasında larynx ile birlikte hareket eder. Capsula fibrosa ile lamina pretrachealis arasında bezi besleyen damarlar
4
seyreder. Beze gelen sempatik lifler ganglion cervicale superius, medium ve inferius‟dan, parasempatik lifler ise n. vagus‟tan gelir (Cumhur 2001).
1.1.2. Tiroit Bezinin Histolojik Yapısı
Tiroit bezi ince fibroelastik bağ dokusundan oluĢan bir iç kapsül ve trakeayı larinkse bağlayan pretrekal fasiya‟nın bir parçasını oluĢturan bir dıĢ fasiyal kılıfla çevrilidir. DıĢtaki fibröz kapsül beze gevĢek olarak tutunmuĢtur ve bezden kolayca ayrılabilir. Ġç kapsül ise beze sıkı olarak yapıĢıktır. Fibroelastik kapsülden organ içine uzanan septalar organa kan damarları, lenfatikler ve sinirleri taĢır ve organı 20-40 follikülden oluĢan lobcuklara böler.
Folliküllerin çapları ortalama 30 mikron kadardır ve yetiĢkin insan tiroidinde yaklaĢık 3 milyon follikül olduğu hesaplanmıĢtır. Folliküller, bezin yapısal
birimleridir. Folliküller, esas olarak tek sıra küboidal follikül epitel hücre dizisinden oluĢan depolama bölgeleridir. Her bir tiroit follikülü lümeninde glikoprotein
yapısında tiroglobulin olarak adlandırılan PAS+ ve asidofilik, visköz kolloit adı verilen salgı depolanır.
Folliküller ince bir retiküler fibril ağı ile çevrelenmiĢtir. Ayrıca yakın bir pencereli kapiller ağı ile desteklenmiĢtir. Folliküller genç kiĢilerde oldukça uniform olmakla birlikte, ileri yaĢta Ģekilleri düzensizleĢir. Folliküller epitel hücreler, esas yada folliküler hücreler ve parafolliküler veya C (Clear) hücreleri olmak üzere iki tiptir (Karagöz 2002).
1.1.3. Tiroit Hormonları
Tiroit bezi, iki molekül tirozin aminoasidini organik bir yapı oluĢturmak için
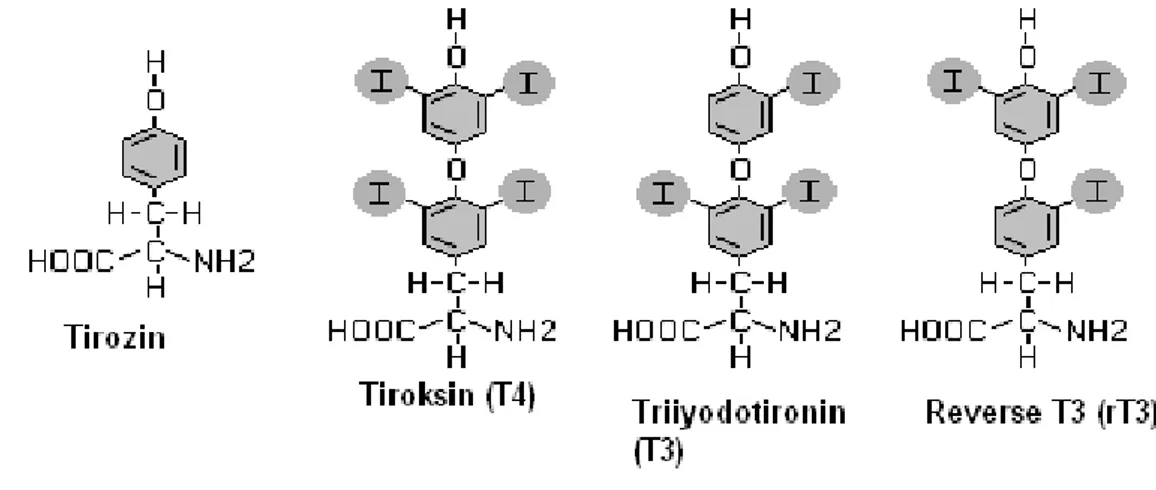
inorganik bir element olan iyotla birleĢtirmesi özelliği ile diğer bezlerden farklılık gösterir. Tiroit bezinin sekresyon ürünleri iyodotirozinler olarak adlandırılırlar. Tiroit bezinin temel ürünü T4 olarak ifade edilen ve tiroksin olarak bilinen 3,5,3‟,5‟-tetraiyodotironindir. Bu molekül fonksiyonlarını büyük oranda dolaĢımda prohormon olarak gerçekleĢtirir. Daha az miktarda ise T3 olarak ifade edilen ve basitçe triiyodotironin olarak bilinen 3,5,3‟-triiyodotironin salgılanır. Hedef dokudaki hemen hemen bütün tiroit aktivitesinden sorumlu olan bu hormon aslında çoğunlukla periferal dokularda prohormon T4‟den üretilir. TanımlanmıĢ bir hormonal etkisi olmayan ve önemsiz miktarlarda salgılanan diğer bir sekresyon ürünü ise 3,3‟,5‟-triiyodotironindir. Bu aynı zamanda rT3 veya reverse T3 olarak ifade edilir, çünkü bu
5
T3‟den sadece üç iyot atomundan birinin yerleĢiminin farklı olması ile ayrılır. Bu inaktif molekül daha az tiroit hormon etkisine ihtiyaç olduğu zaman üretilen prohormon T4‟ün değiĢken bir ürünüdür (Berne ve ark 1990).
ġekil 1: Tiroit hormonlarının kimyasal yapısı
1.1.4. Tiroit Hormonlarının Sentez ve Salınımı
Tiroit hormonlarının sentezi pek çok hormonun sentezinden daha
komplekstir. Bu sürecin 3 farklı özelliği vardır: (1) Tiroit hormonları yeterli miktarda diyetle alınması gereken çok büyük miktarlarda iyot içerirler, (2) tiroit hormonlarının sentezi, tamamlanmıĢ bir hormon tiroit bezinden salgılanmak için uyarılıncaya kadar foliküler lümende ekstraselüler olarak depolandığı için kısmen intraselüler ve kısmen ekstraselülerdir, (3) T4 tiroit bezinin temel sekresyon ürünü olmasına rağmen hormonun aktif formu değildir (Berne ve ark 1990).
Tiroit hormonlarının sentezinin üç temel basamağı vardır: (1) Ġyodun bez içerisine alınması ve konsantre edilmesi (iyodinasyon), (2) iyodun oksidasyonu ve tirozinin fenol halkası ile birleĢmesi ve (3) iki iyodine edilmiĢ tirozin molekülünün T4 veya T3 oluĢturmak için birleĢmesidir (Berne ve ark 1990).
1. Ġyodinasyon:
Ġyot, tiroit hormonları için temel yapısal eleman olduğundan tiroit hormonlarının biyosentezi iyot metabolizmasına bağlıdır. Ġçme suyu ve gıdalardan alınan iyodür ince bağırsaktan inorganik iyodür olarak absorbe edilir ve tiroit bezi tarafından alınır. Hormon sentezi için günlük minimal gereksinim 75 g dır. Ġyot
6
vücutta iyodotirozin ve iyodotironin olarak depolandığı için insanlar iyot yetersizliğine uzun süre dayanabilirler (Berne ve ark, 1990).
Ġyodür tiroit foliküler hücreleri içerisine kimyasal ve elektriksel çekime karĢı taĢınır, bu yüzden foliküler lümen içerisine hızlı bir Ģekilde difüze olur. Ġyodür taĢınması bazal membranın foliküler hücrelerinde, sodyum/iyodür (Na/I) yardımcı taĢıyıcılarıyla ve enerjiye bağlı ve saturable gerçekleĢir. Ġyodür alım hızı öyledir ki normal insanlarda intratiroidal iyodür konsantrasyonu 20 ile 100 kat daha fazladır. Ġyodür taĢınması tirotropin (TSH) tarafından uyarılır. Ġlaveten, TSH‟ dan bağımsız olarak aĢırı iyodür de inhibisyon ve iyodür yetersizliğinde ise artıĢ gerçekleĢir (Felig ve ark 2001).
Diyetle alınan iyodür, organik kombinasyona girmeden önce serbest iyoda dönüĢtürülmelidir (okside edilmelidir). Reaktif iyoda bu dönüĢüm temelde foliküler hücrenin apikal membranının yakınına yerleĢmiĢ olan tiroit peroksidaz enziminin varlığında gerçekleĢir. Serbest iyot foliküler hücre ve sonraki iyodinasyonun meydana geleceği yer olan foliküler lümendeki kolloidin arasından serbest bırakılır (Pocock ve ark 1999).
Ġyodun hücresel alımı TSH ve lokal kontrol mekanizmaları tarafından düzenlenir. Lokal otoregülatör mekanizmalar dolaĢımdaki iyot seviyesi düĢük olduğu zaman hormon sentezi için yeterli iyodu sağlamaya ve dolaĢımdaki iyot konsantrasyonu yüksek olduğu zaman aĢırı hormon sentezini önlemeye yardım ederler. Büyük miktarlardaki iyoda tepki olarak (2 mg veya daha fazlası) tiroglobulindeki tirozin kalıntılarının iyodinasyonunda keskin bir azalma olur. Yüksek iyot konsantrasyonu hala devam ederse tiroit hücreleri, hücre içine aktif iyot taĢınmasını azaltarak adapte olurlar (Pocock ve ark 1999).
2. Tirozinin Tiroglobulin Ġçerisinde Ġyodinasyonu:
Tiroglobulin, iki identical nonkovalent bağlanmıĢ alt ünitesi olan ve yaklaĢık %10 karbonhidrat içeren 660 kilodaltonluk (kDa) bir glikoproteindir. Tiroglobulin tiroit bezinin protein içeriğinin yaklaĢık %75 ini ve foliküler lümendekinin ise neredeyse tamamını oluĢturur (Felig ve ark 2001).
Tiroit hücrelerinde, ekzotoksik veziküllerden, membrana fuse ederek taĢınan iyodür apikal hücre membranına hücre lümeni ara yüzünün etkisi altında hızla difüze olur. Bu keselerde iyodür çok hızlı bir Ģekilde okside olur ve daha sonra
7
tiroglobulinin bazı tirozil parçalarına kovalent olarak bağlanır (organifiye olur). Ġyodür oksidasyonu, ekzositotik keselerin duvarlarına bağlanan bir heme içeren glikoprotein olan tiroit peroksidaz tarafından katalizlenir. Bu oksidasyon ve organifikasyon süreci, tiroglobulinin 134 tirozin kalıntısından yaklaĢık 15‟inin mono- veya diiyodinasyonuyla sonuçlanır (Pocock ve ark 1999).
Tirozin kalıntıları içeren kolloid, peptid bağlarıyla tiroglobulin molekülüne tutunur. Serbest iyot MIT oluĢturmak için 3-pozisyonunda tirozin kalıntılarına tutunur. 5-pozisyonundaki ikinci iyodinasyonda ise DIT oluĢturulur. Ġyodinasyonu takiben, hormonal aktif form olan T3 ve T4‟ü oluĢturmak için mono- ve di- iyodotirozinler arasında birleĢme reaksiyonu olur (Pocock ve ark 1999).
Ġyodine edilmiĢ protein, tiroit folikül lümeninde saklanır. Kayda değer miktarda hormon depolayamayan çoğu endokrin bezin aksine, tiroit bezi birkaç haftalık tiroit hormonu depolayabilir. Bu, diyetle iyot alımındaki geçici düĢmelerde tiroit hormonlarının normal seviyelerini koruması için önemlidir (Pocock ve ark 1999).
3. BirleĢme:
BirleĢme basamağı bir DIT molekülünün T4 oluĢturmak için tiroglobulin içerisinde diğer DIT molekülü ile veya T3 oluĢturmak için MIT molekülü ile birleĢmesi için peroksidaz tarafından yan yana getirilmesidir. Bezdeki genel T4:T3 oranı 10:1 dir (Berne ve ark 1990).
Tiroglobulin sadece T4 ve T3‟ün oluĢumunda görev almaz aynı zamanda bu iki hormonu depolar. T4 ve T3 sekresyon süreci, tiroglobulinin tiroit foliküler hücreleri içerisine geri alımını ve bunların enzimatik hidrolizini gerektirir (Felig ve ark 2001). Tiroit hormonları dolaĢıma salınmadan önce tiroglobulin hidroliz olmalıdır. Tiroit, ön hipofizden salgılanan TSH tarafından uyarıldığı zaman, kolloid damlacıkları, endositoz yoluyla apikal membranlar boyunca foliküler hücrelerden içeri alınırlar. Kolloid içeren endositotik vesiküller daha sonra sitoskeletal yapılar yardımıyla apikal membrandan uzaklaĢtırılır. Aynı zamanda lizozomlar endositotik vesiküllere doğru hareket ederler. BirleĢme daha sonra lizozom membranları ve kolloid içeren vesiküller arasında gerçekleĢir ve tiroglobulin bozulur. Sonuç olarak iyodotirozinler, aminoasitler ve Ģekerler serbest bırakılırlar. T3 ve T4, folikülü saran damarlardan muhtemelen difüzyon yolu ile serbest bırakılırlar. Tiroglobulinin kendisi, bezde bir hasar veya inflamasyon olmadıkça dolaĢıma bırakılmaz. Tiroglobulinin serum yarı ömrü 30 saattir (Pocock ve ark 1999).
8 ġekil 2: Tiroit hormonlarının sentezi
1.1.5. Tiroit Hormonlarının Metabolizması
T4 ve T3 suda çözünmezdir. Tiroit hormonlarının taĢınması için kan içinde çözünürlük kazanarak plazma proteinlerine tutunmaları gereklidir. Tiroidin temel sekresyon ürünü olan T4 serum proteinlerine bağlı olarak dolaĢımda bulunur.
9
Bağlayıcı proteinler, steroit hormon taĢıyıcıları gibi karaciğerde yapılır ve sentezleri östrojenler tarafından artırılır, androjenler tarafından azaltılır. T4‟ün %99‟undan fazlası üç proteine bağlanır: Bunlar tiroit bağlayıcı globulin (TBG), tiroit bağlayıcı prealbumin (TBPA) ve serum albumindir. DolaĢımdaki T4‟ün %75‟inin bağlandığı glikoprotein olan TBG en yüksek affiniteye sahiptir, TBPA‟nın affinitesi daha azdır. Serum albümin ise en düĢük affiniteye sahiptir ama en yüksek kapasiteye sahiptir. Yaygın Ģekilde protein bağlanmasından dolayı, T4‟ün dolaĢımdaki yarı ömrü yaklaĢık bir hafta iken proteine daha gevĢek bağlanan T3‟ün yarı ömrü 1,3 gündür (Felig ve ark 2001). DolaĢımdaki T4‟ün %0,05‟den azı serbest olarak bulunurken, T3‟ün yaklaĢık %0,5‟i serbest formdadır (Pocock ve ark 1999).
T4‟ün tiroidal sekresyondan türemiĢ bütün toplam günlük üretim hızı 80-100
g (100-130 nm)‟ dur. Her gün salgılanan T4‟ün yaklaĢık %80‟i deiyodinasyonla metabolize edilir, bunun yaklaĢık %40‟ı T3‟e ve %40‟ı da rT3‟e dönüĢtürülür. Kalan %20 ise tetraiodotyroasetik asit oluĢturmak için sülfat ve glucuronide ile konjugasyon, oksidatif deaminasyon ve dekarboksilasyon yolu ile metabolize edilir. T3 öncelikli olarak (%80) T4‟ün ekstratiroidal deiyodinasyonu ile üretilir, kalanı ise tiroitden gelir (Felig ve ark 2001).
Tiroksin bir prohormondur ve hedef dokuda 5‟-deiyodinasyon yoluyla metabolik açıdan aktif olan T3‟e dönüĢür. 5‟-deiyodinasyon, mikrozomal enzimler tarafından katalizlenir ki bunların aktivitesi için redüklenmiĢ thiollere ihtiyaç vardır. Tip I 5‟-deiodinaz aktif bölgesinde selenocyteine içerir (Berry ve ark 1991a). Çoğunlukla, karaciğer ve böbrekte bulunan bu enzim normal Ģartlar altında T3 üretiminin %80‟ine katılır. Sonuç olarak, T3 üretimi birçok faktörden etkilenir. Bunlardan birincisi, TSH‟ın T4 üretimini düzenlediği yer olan tiroit bezinde tiroit hormon sentezini kontrolüdür. Pek çok koĢul altında, periferde T4‟ün T3‟e dönüĢümü substrat T4 konsantrasyonu ile orantılıdır ama kontroldeki ikinci nokta karaciğer, böbrek gibi hedef organlarda bir çok anormal koĢul sonucunda T4‟ün T3‟e dönüĢümünün azalmasıdır. Açlık, hastalık, kortizol, propylthiouracil ve diğer birçok ilaçlar 5‟-deiodinaz aktivitesini azaltır. Açlık esnasında, ilk günün sonunda plazma T3 %20 oranında azalırken, üçüncü günün sonunda bu miktar %50‟ ye çıkar (Pocock ve ark 1999).
Tip II 5‟-deiyodinaz karaciğer ve böbrekten farklı olarak hipofiz ve merkezi sinir sisteminde bulunur. Tip II 5‟-deiyodinaz aktif bölgesinde selenocysteine yerine cysteine içerir (Berry ve ark 1991b). Tip II deiyodinaz, böbrek ve karaciğer
5‟-10
deiyodinazın inhibisyonundan dolayı dolaĢımdaki T3 konsantrasyonunun düĢtüğü açlık gibi durumlarda normal bir hipotalamus-hipofiz-tiroit ekseni sağlamak için hipofizde T4‟ü T3‟e çevirir. Hipofizdeki tip II 5‟-deiodinaz dolaĢımda T3 den ziyade T4 bulundurmak yoluyla feedback kontrol sağlar ve normal tiroit bezi üretiminin korunmasını sağlar (Felig ve ark 2001).
T4‟ün içteki halkasının, 5-deiodinaz tarafından deiyodinasyonu inaktif bir metabolit olan reverse T3 (rT3)‟ü oluĢturur. T4‟ten yaklaĢık eĢit miktarlarda T3 ve rT3 oluĢturulur ama rT3 daha hızlı temizlenir bu yüzden dolaĢımdaki konsantrasyonu daha düĢüktür. Açlıkta olduğu gibi 5-deiodinaz aktivitesi azaldığı zaman daha büyük miktarlarda T4, rT3 için metabolize edilir (Felig ve ark 2001). Tiroit bezinden günlük tiroksin üretimi 80 g, T3 üretimi yaklaĢık 4 g ve rT3 üretimi 2 g‟dır (Pocock ve ark 1999).
1.1.6. Tiroit Hormon Sekresyonunun Düzenlenmesi
Tiroit bezinin aktivitesi tiroit stimulan hormon (TSH) tarafından düzenlenir. TSH, ön hipofizin tirotrop hücrelerinde sentezlenen ve salgılanan 28 kDa‟lık bir glikoproteindir. Normal insanlarda hesaplanan TSH sekresyon hızı 75-150 mU/gün arasında değiĢir. TSH sekresyon seyri hem sirkadiyan hem de pulsatildir. TSH‟ın serum yarı ömrü 50-80 dakika arasında değiĢir ve temizlenme hızı da 40-60 ml/dk arasında farklılık gösterir (Felig ve ark 2001). TSH sekresyonu ise hipotalamusta bulunan tirotropin releasing hormon (TRH) tarafından kontrol edilir. TSH, tiroit foliküler hücrelerinin yüzeyinde bulunan spesifik reseptörlere bağlanarak ve membrana bağlı adenil siklazı uyarmak suretiyle etki eder ve bu suretle cAMP seviyesini artırır (Pocock ve ark 1999).
TSH, tiroit hormon sentezini ve sekresyonunu pek çok açıdan düzenler. Buna iyodür tutulması, peroksidaz aktivitesi, tiroglobulin sentezi ve tiroglobulin üzerinde tirozin iyodinasyonunun uyarılması da dahildir. TSH, aynı zamanda mono- ve di- iyodotirozin moleküllerinin birleĢmesini ve tiroit hormon sekresyonuna neden olan bütün faktörleri uyarır. TSH‟ın etkisinin net sonucu dolaĢımdaki tiroit hormon sekresyonunun artmasına ilave olarak folliküller içinde depolanmak üzere yeni tiroit hormon sentezini artırmaktır. TSH, tiroit bezi ve onun kan desteği üzerine tonik bakım etkisinden dolayı bir tropik hormondur. TSH yokluğunda tiroit bezi hızla atrofiye olur (Pocock ve ark 1999).
11
DolaĢımdaki tiroit hormonları TSH sekresyon hızını hem hipotalamus hem de ön hipofiz üzerine olan negatif feedback etkileri vasıtasıyla değiĢtirirler. Diğer hormonların da aynı zamanda TSH salınımını değiĢtirebildiği görülmektedir. Örneğin, büyük miktarlarda glikokortikoidler TSH salınımını inhibe ederken, östrojen ön hipofizdeki TSH salgılayan hücrelerin TRH‟a olan cevabını artırırlar (Pocock ve ark 1999).
Kimyasal kontrol mekanizmalarına ilave olarak, hipotalamustaki çeĢitli sinir inputları da TRH salgısının düzenlenmesinde ve böylece TSH ve tiroit hormonlarının üretiminde rol oynarlar. Soğuk stresinin de tiroit hormon sekresyonunu uyardığı bilinmektedir. Soğuk bir ortama girildikten sonra 24 saat içerisinde dolaĢımdaki T4 seviyelerinde birkaç gün içerisinde pik yapan bir artıĢ vardır (Pocock ve ark 1999).
1.1.7. Tiroit Hormonlarının Fizyolojik Fonksiyonlar Üzerine Etkileri
1.1.7.1. Bazal Metabolik Hız (BMR), Oksijen Tüketimi ve ATP Üretimi Üzerine Etkisi
Tiroit hormonlarının metabolizma üzerine etkisi komplekstir ve çoğu zaman tam olarak anlaĢılamamıĢtır. Tiroit hormonlarının muhtemelen en iyi bilinen fonksiyonu oksijen tüketimindeki artıĢla uyumlu olarak bazal metabolik hız üzerinedir. Ġnsanlar üzerinde yapılan çalıĢmalarda, hipotiroidizmde BMR‟ın düĢtüğü oysa hipertiroidizm durumunda arttığı genel olarak gösterilmiĢtir (Freake ve ark 1995).
Tiroit hormonları, ATP üretimindeki artıĢla birlikte, ATP tüketimini de artırarak etki ederler, böylece net etkileri oksijen tüketiminin ve BMR‟ın artmasıdır. Hücresel seviyede tiroit hormonları mitokondride pek çok değiĢikliğe sebep olurlar. Bunlara mitokondri içinden ADP taĢımakla görevli ADP-translokatör proteininin ekspresyonundaki artıĢa ilave olarak, elektron taĢıma sistemindeki elemanların durumunun azalması ve ekspresyonunun artması da dahildir. Bütün bu değiĢiklikler elektron taĢıma sistemi boyunca olan akıĢı artırmaya hizmet ederler ve böylece ATP üretimini artırırlar. AĢırı düzeydeki tiroit hormonunun mitokondrilerde hasara neden olduğu düĢünülmektedir (Freake ve ark 1995).
Tiroit hormonları aynı zamanda doku oksijen ihtiyacının artmasında olduğu gibi, oksijenlenmiĢ kan miktarının artması ile dokuya destek için kalp atım hızını artırmak gibi fizyolojik değiĢikliklere de neden olur. Artan kalp hızı için daha fazla
12
enerji gerekir ve tiroit hormonlarına cevap olarak mitokondride üretilen ATP‟nin bir kısmı harcanır. Enerji tüketimi aynı zamanda hücre membranında Na-K-ATPaz aktivitesinin artması suretiyle de artar. Bu enzim hücre membranı boyunca sodyum ve potasyum için iyon çekiminin korunmasından sorumludur ve hücresel enerji tüketir. Tiroit hormonlarının oksijen tüketimi, BMR ve ATP üretimi üzerine etkileri hakkında çok fazla Ģey bilinmesine rağmen tam mekanizma hala çözülememiĢtir (Freake ve ark 1995).
1.1.7.2. Tiroit Hormonlarının Gıda (Nutrient) Metabolizması Üzerine Etkisi
Tiroit hormonları karbonhidrat, lipit ve protein metabolizmasını etkilerler. Tiroit hormonları yağ asidi sentezini artırırlar. Tiroit hormonlarının lipogenesisi gerçekleĢtiren genlerin, özellikle fatty asit sentetaz ve asetil CoA karboksilazın ekspreyonunu artırdığı gösterilmiĢtir. Ġlave olarak, yağ asitlerinin trigliserit ve fosfolipidlere esterifikasyonu tiroit hormonları tarafından artırılır. Tiroit hormonları, lipolize neden olmak ve lipidlerin oksidasyonunu artırmak suretiyle etkili olurlar. Glikoliz ve glikoneogenezin her ikisi de tiroit hormonlarına tepki olarak artar. Tiroit hormonlarının, net protein sentezinde bir artıĢa neden olan total hücresel RNA sentezinde bir artıĢa neden olduğu gösterilmiĢtir. Bununla beraber yüksek seviyelerdeki tiroit hormonlarının proteinler üzerine katabolik etkisi ile BMR da artar. Tiroit hormonlarının makronutrientlerin hem katabolizması hem de anabolizması üzerine etkisi vardır (Freake ve ark 1995).
Günde 600 kalori veya daha az alan obez veya normal deneklerde iki ile dört gün arasında serum T3 konsantrasyonları yaklaĢık %40 düĢerken, serum rT3 konsantrasyonları %100 düĢer. Bu abnormalite denek karbonhidrat veya protein ile besleninceye kadar devam eder (Felig ve ark 2001).
1.1.7.3. Tiroit Hormonlarının Büyüme ve Gelişme Üzerine Etkisi
Tiroit hormonları özellikle bebeklik ve çocukluk esnasında büyüme ve geliĢmede temel rol oynarlar. Vücutta tiroit hormonlarının etkisi yaygın iken geliĢim için temel etkisi somatik doku ve kemik büyümesi, beyin geliĢimi, diĢ çıkması ve geliĢimi ve hipofiz-hipotalamus fonksiyonu üzerinedir. Fetal geliĢme ve erken postnatal periyot esnasındaki aĢırı hipotiroidizm, merkezi sinir sisteminde kretinizm olarak bilinen kalıcı hasara neden olur. Kretinizimin özellikleri zeka geriliği, kısa boy ve üreme anormallikleridir. Çocukluk döneminde tedavi edilmeyen
13
hipotiroidizm, lineer büyümede hasara ve iskelet geliĢiminde yetersizliğe yol açar ki bu bozukluk tiroit hormon tedavisi ile geri dönüĢtürülebilir (Boersma ve ark 1997). T3 çocukluk dönemindeki somatik büyümenin önemli bir düzenleyicisi olduğu kadar eriĢkin dönemde de kemik ve mineral metabolizmasında önemli rol oynar (Williams ve ark 1998).
a. Tiroit Hormonları ve Kemik Büyümesi:
Tiroit hormonlarının, kemik hücrelerinin farklılaĢmasını ve proliferasyonunu düzenlediği ve bu olaylarda diğer hormonlarla birlikte etki ettiğinden, bu etkisinin gerçek mekanizması tam olarak anlaĢılamamasına rağmen, diğer hormonların kalsemik hormonlar olduğu düĢünülmektedir. Kemirgen ve insan osteoblast hücre kültürü sistemlerinde yüksek seviyelerde T3‟ün hücre replikasyonunu inhibe ettiği oysa düĢük dozlardaki T3‟ün hücrelerin proliferasyonuna neden olduğu gösterilmiĢtir. T3‟ün bu çift etkisi iskelet sisteminin olgunlaĢmasının düzenlenmesi için fizyolojik açıdan önemli olabilir (Klaushofer ve ark 1995).
b. Kemik Büyümesi Üzerine T3, GH ve IGF-1 ĠliĢkisi:
T3 kemik büyümesini GH sekresyonunu artırmak suretiyle de etkiler. Tiroit hormonları olmaksızın kandrosit proliferasyonunun olmadığı bulunmuĢtur (Lewinson ve ark 1989). GH reseptörleri insan ve rat epiphyseal kandrositlerde bulunur ve GH‟nun hücre kültüründe kandrosit sayısını artırdığı gösterilmiĢtir. Bu GH‟nun iskelet büyümesi üzerine direk etkisi olduğunu, ama tiroit hormonlarının da iskelet olgunlaĢmasının tamamlanması için gerekli olduğunu gösterir (Lindahl ve ark 1986).
Tiroit hormonlarının perfuse edilmiĢ rat karaciğerinde IGF-1 üretimini artırdığı (Ikeda ve ark 1989) ve hipofizektomi yapılmıĢ ratların karaciğerinde IGF-1 mRNA‟yı artırdığı (Wolf ve ark 1989) gösterilmiĢtir. T3‟ün kartilajda IGF-1 etkisini (Lewinson ve ark 1994) ve rat kandrositlerinde IGF-1 reseptör mRNA‟sını (Ohlsson ve ark 1992) uyardığı bilinmektedir.
Bundan dolayı, tiroit hormonunun GH sekresyonunu artırdığı yerlerde, uzunlamasına kemik büyümesini veya indirek tiroit hormon etkisini sıra ile uyaran, IGF-1 üzerine direk bir tiroit hormon etkisinin varlığı muhtemeldir.
Tiroit hormonlarının fazla salgılanması kaslarda çok ince titreĢimlere (10-15/sn frekansta) neden olur. Tremor denilen bu kasılmalar, medulla spinaliste motor nöronların kas tonusu ile ilgili sinapslarında duyarlılığın artmasına bağlıdır. Tiroit hormonları kaslarda, özellikle kalp kasında adenilat siklaz yolu ile cAMP‟yi artırır.
14
Ancak aĢırı hormon salgısı ATP sentezini bozarak enerji yetmezliği oluĢturabilir (Rooyackers ve ark 1997).
1.1.7.4. Üreme Fonksiyonları Üzerine Etkisi
Tiroit hormonları tarihsel olarak gonadların temel bir düzenleyicisi olarak görülmemiĢtir. Bu paradigma geçen 15 yıl içerisinde yeniden gözden geçirilerek değiĢime uğramıĢtır ve Ģimdilerde tiroit hormonlarının özellikle erkeklerde geliĢme esnasında olmak üzere testisler ve kadınlarda ovaryum üzerine kritik bir etkisi olduğu açıklanmıĢtır (Cooke ve ark 2004).
Tiroit hormonlarının uygun gonadal geliĢme ve fonksiyondaki rolünü destekleyen çok sayıda delil vardır. Neonatal testiste, tiroit hormonlarının hem sertoli hem de leydig hücrelerinin çoğalma kapasitesi üzerine etkisi vardır. Oysa neonatal hipotiroidizm sertoli hücre proliferasyonunun uzamasına ve tüm yetiĢkin sertoli, leydig ve germ hücre populasyonlarının artmasına yol açar, neonatal hipertiroidizm ise sertoli hücre proliferasyonunun erken durdurulmasını uyarır. Gerçek mekanizma olduğu gibi kalmasına rağmen, proliferasyondaki değiĢiklik tiroit hormonlarının p27Kip1 gibi anahtar hücre siklusu proteinlerini düzenleme yeteneğinin bir sonucu olabilir. Tiroit hormonlarının ovaryumlar üzerine etkisi daha az açıktır. Normal euthyroid durumundaki rahatsızlığın normal ovaryum fonksiyonunu açıkça inhibe ettiği ve ovulasyona ilave olarak granülosa hücre farklılaĢmasını ve foliküler olgunlaĢmayı spesifik olarak değiĢtirdiği görülmektedir (Cooke ve ark 2004) .
Tiroit hastalıklarının bütün formları diĢilerde erkeklerden 4-5 kat daha fazladır. Hem hipotiroidizmin hem de hipertiroidizminin östrojen ve androjen metabolizması, menstural fonksiyon ve üreme üzerine önemli etkileri vardır. Plazma östrojen seviyeleri hipertiroit bireylerde menstural siklusun bütün safhalarında normal kadınlardan 2 veya 3 kat daha yüksektir. Hipertiroitli kadınlarda testosteron ve androsteneidon üretim hızı normal diĢilere kıyasla önemli ölçüde yükselmiĢtir. Testosteronun östradiol‟e dönüĢümüne ilave olarak andresteneidone‟un östrona dönüĢüm hızı hipertiroit kadınlarda artmıĢtır (Gerasimos ve ark 2000). Akande ve Hockaday (1972), menstural siklusun hem foliküler hem de luteal fazında ortalama LH seviyelerinin hipertiroit kadınlarda normal kadınlara kıyasla daha yüksek olduğunu bulmuĢlardır.
Bebeklikte ortaya çıkan hipotiroidizm eğer tedavi edilmezse cinsel olgunlaĢmanın bozulmasına yol açar, puberteye girmeden önce ortaya çıkan
15
hipotiroidizm ise anovulatuar siklusları takiben puberteye girmenin ertelenmesine neden olur. Hipotiroidizmli kadınlarda androsteneidone ve östron‟un metabolik olarak temizlenme hızı azalır ve periferal aromatizasyon artar. Hipotiroidizmde ise gonadotropin seviyeleri genellikle normaldir. Bununla beraber bazı hipotiroitli kadınlarda GnRH‟a LH cevabı ertelenir veya yok olur. AĢırı hipotiroidizmli kadınlarda ve erkeklerde genellikle libido kaybı görülür ve kadınlarda ovulasyonda baĢarısızlık meydana gelir (Gerasimos ve ark 2000).
Serum T4 ve T3 konsantrasyonları hamileliğin ilk üç aylık döneminde hamile olmayan kadınlara ve erkeklere göre %30-50 daha yüksektir ve sonraki ikinci ve üçüncü üç aylık dönemlerde ise sabit kalır. Hamilelik, iyodür ihtiyacını artırır çünkü maternal tiroit hormon sentezi ve böbreklerden iyodür temizliği artar ve iyodürün bir kısmı fetusta kaybolur. Tiroit büyüklüğü iyot alımı yeterli olan kadınlarda çok az değiĢir ama iyot alım düĢük olanlarda biraz artar, bu değiĢiklik iyot takviyesi ile önlenir (Felig ve ark 2001).
Hem hipotiroidizm hem de hipertiroidizm menstural anormalliklerle sonuçlanabilir. Hipotiroidizmde menstural düzensizliklerin sıklığı, çalıĢılan 171 hipotiroit hastanın %23,4‟ünde rapor edilmiĢtir (Gerasimos ve ark 2000).
Ratlara, tiroidekektomi uygulamasından 2 hafta ve propilthiourasil uygulamasından 3 hafta sonra ratların östrus sikluslarının düzensizleĢtiği ve yaklaĢık 1 ay sonra diöstrus-1 safhasında serum LH seviyelerinin önemli ölçüde düĢtüğü bulunmuĢtur. Hipotiroit ratlar yüksek progesteron ve düĢük testosteron seviyeleri gösterirler. Düzensiz östrus sikluslarının ve hormon seviyelerindeki değiĢikliklerin T4 verilmesi ile düzeltildiği bulunmuĢtur (Hatsuta ve ark 2004).
1.2.Tiroit Bezinin Eser Elementlerle ĠliĢkisi
Tiroit bezinin fonksiyonunu devam ettirebilmesi, tiroid hormonlarının hem metabolizması hem de sentezi için gerekli olan birçok eser elementin mevcut olmasına bağlıdır (Arthur ve Beckett 1999). Ġyot, tiroit hormonlarının vazgeçilmez bir hammaddesidir. Tiroksin (T4), triiyodotironin (T3) ve iyot eksikliği dünyada yaklaĢık bir milyar kadar insanı etkileyebilmektedir (Arthur ve Beckett 1999). Tiroksin (T4) hormonunun, biyolojik açıdan aktif hormon olan triiyodotronine (T3) dönüĢümünu sağlayan deiyododinaz enziminin biyolojik aktivitesi için selenyum gereklidir (Arthur ve Beckett 1999). Selenyumun dıĢında demir, çinko ve bakır gibi elementler de tiroit hormon metabolizmasını belirgin Ģekilde etkileyebilmektedir (Arthur ve Beckett 1999).
16
Ġnsan sağlığının sürdürülmesinde tiroit bezinin önemi iyi bir Ģekilde tanımlanmıĢtır. Ġyot tiroit hormonlarının çok önemli bir ögesi olduğu için, tiroit disfonksiyonunun iyodun yetersiz olduğu coğrafik bölgelerde oldukça yaygın olması ĢaĢırtıcı değildir. Fakat bu eser elementin yeterli düzeyde alınması durumunda bile toplumun %3-5‟inde tiroit fonksiyon bozuklukları görülebilmektedir (Zagrodzki ve ark 1998). Bunun dıĢında tiroit hormonlarının düzenli olarak sentezlenmesi fetal geliĢim sırasındaki özel dokular için de oldukça önemlidir (Zagrodzki ve ark 1998). Hem normal koĢullar altında hem de tiroit hormon metabolizmasının anormal olduğu durumlarda tiroit bezi biyokimyası ve kontrolü birçok araĢtırmanın da ilgi odağı olmuĢtur. Tiroit hormonlarının metabolizma ve fonksiyonu kompleks bir süreçtir. Bu süreç tiroit bezindeki ön hormonlar ve hormonların sentezi, salınımı ve vücut dokularında deiyodinaz enzimi tarafından dönüĢümü ile T3‟ün nükleer reseptörlerin gen ekspresyonunun kontrolü de dahil bir çok olayı içerir (Arthur ve Beckett 1999). Tiroit bezinin fonksiyonu ve hormon metabolizması birçok enzim ve proteinlerin varlığına bağlıdır ve eser elementler bu olaylarda oldukça önemlidirler (Arthur ve Beckett 1999; Zagrodzki ve ark 1998).
Tiroitle en yakından iliĢkisi olan elementler iyot, çinko ve selenyumdur. Ek olarak demir ve bakır da diyetteki seviyelerinin etkileri çok açık olmamasına rağmen tiroit metabolizmasını etkilemektedir (Arthur ve Beckett 1999; Zagrodzki ve ark 1998).
1.2.1.Tiroit Hastalıkları ve Ġyot
Tiroit bezinin fonksiyonunu etkileyen iyot, tiroit hormonlarının önemli bir bileĢenidir. Tiroit bezinin hormonal fonksiyonunun devamı için diyetle günlük 150– 200 µg civarında iyoda ihtiyaç vardır. Ġyot yetersizliği guatr, hipotiroidizm, zihinsel ve fiziksel geliĢim geriliği (kretinizm) gibi çeĢitli klinik belirtilerle kendini gösteren bir dünya sağlık probleminin de nedenidir (Arthur ve Beckett 1999; Zagrodzki ve ark 1998).
1.2.1.1.Düşük İyot Alımının Etkileri
Ġyot yetersizliğinin sıklıkla görüldüğü bölgelerde yaklaĢık 1 milyar insan yaĢamaktadır. Bunlardan yaklaĢık olarak 211 milyonunda guatr ve 20 milyon kadarında da beyin fonksiyonlarında zayıflıklar vardır (Arthur ve Beckett 1999; Zagrodzki ve ark 1998). Ġnsanları her yaĢta etkileyebilecek pek çok iyot yetersizliği hastalıkları vardır. Bunların içinde en tehlikesi özellikle fetal geliĢimde ve küçük çocuklardaki hızlı büyüme esnasında ortaya çıkan kretinizm‟dir. Ġyot yetersizliğinin
17
kliniksel belirtileri orta seviyedeki hipotiroidizmden Ģiddetli endemik kretinizme doğru sıralanabilir. Kretinizm tamamen iki farklı biçimde ortaya çıkmaktadır (Arthur ve Beckett 1999; Zagrodzki ve ark 1998). Miksodematus kretinizmde, Ģiddetli hipotroidizm ve engellenmiĢ büyüme vardır. Aynı zamanda tiroit dokusu palbe olmadan tiroit atrofisi mevcuttur. Tipik bir Ģekilde plazmada T4 ve T3 oldukça düĢüktür, TSH ise aĢırı derecede yüksektir (Arthur ve Beckett 1999; Zagrodzki ve ark 1998). Bu vakalarda tiroit yıkımı uterus içi yaĢamda ya da doğumdan hemen sonra baĢlayabilir. Hastalığın miksodematous biçiminden daha yaygın görülen nörolojik kretinizmde ise duyma ve konuĢma kusurlarını da içeren zihinsel yetersizlikler oluĢabilir. Kretinizmin patogenezi açık olmasa da bu fonksiyon bozukluklarının temelinde iyot yetersizliği büyük bir rol oynamaktadır(Arthur ve Beckett 1999; Zagrodzki ve ark 1998).
1.3.Tiroit Hormonları ve Selenyum
Doğada yaygın olarak bulunan selenyum (Se); insan ve hayvan organizmalarının normal geliĢmesi için gerekli olan esansiyel iz elementlerden birisidir (Shamberger 1986). Selenyum ilk olarak 1818 yılında Ġsveçli kimyacı Berzelius tarafından sülfirik asit artıklarından tanımlanmıĢtır (Oldfield 1987). Uzun süre toksik madde olarak kabul edilen selenyumun, canlı organizmasının ihtiyaç duyduğu bir element olduğu, ilk defa Schwartz ve Foltz (1957) tarafından 1957‟de karaciğer dejenerasyonunun oluĢmasında selenyum yetersizliğinin rol oynadığının anlaĢılmasıyla keĢfedilmiĢtir. 1960‟lı yılların sonunda selenyumun insan sağlığındaki rolü ilgi toplamaya baĢlamıĢ ve selenyuma yanıt veren hayvan hastalıklarına benzer olan insan hastalıkları araĢtırılmaya baĢlanmıĢtır (Combs ve Combs 1986). YaklaĢık 50 yıl öncesinde selenyumun insan beslenmesi için önemli olduğu tanımlanmasına rağmen, günlük ihtiyaç miktarı hala tam olarak bilinmemektedir. Hem kısa hem de uzun dönem insan sağlığına dair etkileri olan selenyuma atfedilen gerekli fonksiyonel roller hakkındaki bilgilerimiz her geçen gün geniĢlemektedir (Brown ve Arthur 2001).
Selenyum konsantrasyonu tiroitte diğer dokulardan özellikle de karaciğer ve böbrekten daha yüksektir. Bu da selenyumun tiroit bezi için fonksiyonel olduğunu gösterir. Selenyum, proteinlerin geniĢ alanının aktif bölümünde selenosistein olarak toplanır. Fizyolojik durumlar altında, selenosisteindeki selenyum, hemen hemen iyonlaĢmıĢtır ve sonuç olarak bu oldukça etkili bir biyolojik katalisttir (Arthur ve ark.
18
1997). Selenoproteinlerin en önemlilerinden biri iyodotironin deiyodinazlar‟dır. Bunlar aktif olmayan T3‟ün 3' diiyodotironine dönüĢümünü ve pro-hormon olan tiroksinin (T4) aktif tiroit hormonu 3,3′ 5 triiyodotironine dönüĢümünü katalize ederler. Tiroit hormonları hepatik enzim ekspresyonunda ve nötrofil iĢlevinde düzenleyici rol oynamaktadır. Sonuç olarak; selenyum hayvan replesyonu çalıĢmalarında; karaciğerdeki glutatyon metabolizması ve enzimleri metabolize eden ilacın etkisi arasındaki iliĢki eksikliği, nötrofil iĢlevi, GPx aktivitesindeki değiĢiklik araĢtırmaları selenyum ve tiroit durumu arasındaki iliĢkinin ortaya konulmasını sağlamıĢtır (Arthur ve ark. 1993). Tiroit hormonlarının tam aktivitesi tiroksinin triiyodotironine (T3) dönüĢümüne bağlıdır. Çoğu T3, birinci tür selenoenzim iyodotironin 5′ deiyodinaz tarafından katalize edilen T4„ün periferal deiyonizasyonu tarafından üretilir. Plazmayı ve tiroid hormonu dengesini korumak için beyin ve karaciğer gibi özel dokularda iĢlevselliğe sahip iyodotironin deiyonize enzimlerine bağlı selenyumun 3 türü vardır: T4„ün T3‟e dönüĢü kandaki T3/T4 oranlarını gözleyerek değerlendirilebilir. Bu oranda selenyum ilaveleriyle değiĢtirilebilen ve yaĢlanmaya bağlı olarak ortaya çıkan progresif bir azalma vardır. Bundan dolayı toplam T3 ve T4 oranı insan çalıĢmalarında selenyum durumu için iĢlevsel bir belirleyici olarak yardım edebilir. Bu gelinen aĢamada tiroid hormonlarının hücresel metabolik oran üzerindeki düzenleyici rolünün, yükselen hücre aktivitesine yanıt olarak gereksinimi artacak olan selenyum statüsü tarafından modüle edileceği belirtilmektedir (Olivieri ve ark. 1995).
1.4. Tiroit Fonksiyonu ve Çinko
Çinkoya bağlı endokrin fonksiyonlardan birisi de, düĢük çinko diyeti alan insan ve hayvanlarda tiroit hormon metabolizması ve enerji tüketimindeki değiĢikliklerdir (Ganapathy ve Volpe 1999). Çinkonun tiroit hormon metabolizmasını etkilemesiyle ilgili pek çok hipotez ileri sürülmüĢtür:
1.Çinko tiroit hormon sentezini direkt etkileyebilir. Gupta ve ark. (1997) çinko defektli hayvanlarda tiroit bezlerindeki küçülmeye paralel olarak, tiroit foliküllerinde atrofi ve dejeneratif değiĢikliklerin oluĢmasından yola çıkarak çinko eksikliğinin tiroit hormon sentezini direkt etkileyebileceğini rapor etmiĢlerdir. Çinko defekti esnasında tiroit atrofisi ve dejenerasyonundan sorumlu biyokimyasal mekanizmalar tam olarak bilinmemektedir. Ancak çinko defektinde en azından tiroit dejenerasyonu
19
kısmen antioksidan fonksiyonların zayıflamasıyla iliĢkili olabilir (Ganapathy ve Volpe 1999).
2.Çinkonun tiroit hormonlarının (özellikle T3) reseptör aktivitesi için gerekli olduğu kabul edilir. T3 hormon reseptörünün biyolojik olarak aktif olan durumunu muhafaza edebilmesi için çinkoya ihtiyaç olduğu ileri sürülmüĢtür (Freake ve ark. 2001).
3.Çinko tiroksin bağlayıcı protein yapımını artırarak T4 hormon seviyelerini etkileyebilir (Hartoma ve ark. 1979).
4.Çinko T4 hormonunun T3‟e dönüĢümü için gereklidir (Wada ve King 1986). T4‟ü aktif form olan T3‟çeviren hepatik tip I-5‟ deiyodinaz (5‟D-1) tiroit hormon metabolizmasında anahtar bir enzimdir. Ve tip I-5‟ deiyodinaz‟ın fonksiyonunda çinko vazgeçilmez bir elementtir (Wada ve King 1986). Çinko eksikliğinde tip I-5‟deiyodinaz enzim aktivitesi ve sonuç olarak T4‟ün T3‟e dönüĢümü azalır (Wada ve King 1986).
5.Hem hipotalamus, hem de hipofiz çinko eksikliğine karĢı hassastır (Pekary ve ark. 1991). Bu durumda da çinkonun TRH ve TSH sentezinde rol alan enzimler için gerekli olabileceği ileri sürülmüĢtür (Pekary ve ark. 1991). Ancak bu bulgu tartıĢmalıdır. Çinkonun sağlıklı erkeklerde TRH ve/veya TSH salgısını değiĢtirmediği Brandao-Neto ve ark. (2006) tarafından rapor edilmiĢtir.
Çinko ile tiroit hormonları arasındaki iliĢkinin tek yönlü olmadığı söylenebilir. Zira tiroit fonksiyonlarındaki bir bozulma da vücut çinko düzeylerini etkilemektedir (Maxwell ve Volpe 2007). Tiroit bezi hastalıklarından hipotiroidizmde düĢük, hipertiroidizmde yüksek çinko konsantrasyonlarının bildirilmesi (Ganapathy ve Volpe 1999) bu iliĢkinin tek yönlü olmadığının delilidir.
Pawan ve ark. (2007)‟nın bildirdiğine göre, hipertiroid ratlarda hem intestinal, hem de böbrek çinko alımı önemli ölçüde artmakta ve bu nedenle kontrollerine oranla hipertiroid ratlar daha yüksek çinko düzeylerine sahip olmaktadır. Bu olayın temel nedeninin de çinko taĢıyıcı bir protein olan Zip 10‟un barsak ve böbrekte tiroit hormonları ile pozitif korelasyonlu olmasından kaynaklandığı kabul edilmektedir (Pawan ve ark. 2007).
Buna karĢın hipotiroidi hastası 34 denek üzerinde gerçekleĢtirilen çalıĢmada serum çinko içeriğinin önemli ölçüde azaldığı ortaya konulmuĢtur (Buchinger ve ark. 1988). Hipotiroit hastalarda serumdaki azalmıĢ çinko düzeylerinin iki önemli
20
nedenden kaynaklandığı; bunlardan birincisinin azalmıĢ çinko emilimi, ikincisinin de idrarla çinko atılımındaki artıĢ olduğu gösterilmiĢtir (Kandhro ve ark. 2009).
Tiroit kanseri hastalarında sağlıklı deneklerden düĢük olan serum çinko düzeylerinin, operasyon sonrası normal düzeylere yükseldiği bildirilmiĢtir (Al-Sayer ve ark. 2004). Tiroit kanserli hastalarda operasyondan sonra yükselen serum çinko düzeylerinin baĢarılı bir operasyonun göstergesi olmasının yanı sıra, tiroit kanserli hastalarda çinko düzeylerinin hastalığın uzun süre takip edilmesinde önemli olabileceği sonucuna varılmıĢtır (Al-Sayer ve ark. 2004).
1.5.Diğer Elementler ve Tiroit
Demir ve bakır seviyeleri insanlar ve hayvanlarda plazma T3 konsantrasyonları ile iliĢkilendirilmektedir (Arthur ve Beckett 1999). Çinkoda olduğu gibi bu değiĢiklikler halen daha tiroit hormonu metabolizmasındaki enzimlerde meydana gelen değiĢikliklerle iliĢkilendirilememiĢtir. Tiroit metabolizmasındaki değiĢikliklerin demir ve bakır yetersizlikleri ile direk iliĢkili mi veya değil mi olduğu hala belirlenemeyen bir durumdur (Arthur ve Beckett 1999).
21
2.GEREÇ ve YÖNTEM
2.1.Grupların OluĢturulması
Bu çalıĢma, Selçuk Üniversitesi Meram Tıp Fakültesi Genel Cerrahi Anabilim Dalında opere edilen tiroit kanserli hastalar üzerinde gerçekleĢtirildi. ÇalıĢma protokolü Selçuk Üniversitesi Meram Tıp Fakültesi Etik Kurulu tarafından onaylandı.
15 kadın ve 15 erkek olmak üzere toplam 30 tiroit kanserli denek çalıĢmaya alındı. Aynı zamanda yine aynı klinikte opere edilen ancak patoloji sonucuna göre kanser teĢhisi konulmayan 10 kadın ve 10 erkek olmak üzere toplam 20 denek de kontrol grubu olarak çalıĢmaya dahil edildi. ÇalıĢma grupları Ģu Ģekilde oluĢturuldu.
Grup 1:Tiroit kanserli erkek hasta grubu (n=15):Bu gruptaki denekler operasyon sonrası alınan tiroit doku örneklerinde patolojik inceleme sonucu malignite teĢhisi konulan hastalardan oluĢtu.
Grup 2: Tiroit kanserli kadın hasta grubu (n=15):Bu gruptaki denekler operasyon sonrası alınan tiroit doku örneklerinde patolojik inceleme sonucu malignite teĢhisi konulan hastalardan oluĢtu.
Grup 3:Erkek Kontrol Grubu (n=10): Bu gruptaki denekler operasyon sonrası alınan tiroit doku örneklerinde patolojik inceleme sonucu kanser teĢhisi konulmayan hastalardan oluĢtu.
Grup 4:Kadın Kontrol Grubu (n=10): Bu gruptaki denekler operasyon sonrası alınan tiroit doku örneklerinde patolojik inceleme sonucu kanser teĢhisi konulmayan hastalardan oluĢtu.
2.2.Kan ve Doku Örneklerinin Alınması
AraĢtırmaya katılacak deneklerin tamamından operasyon öncesi, operasyondan hemen sonra ve operasyondan 15 gün sonra olmak üzere ön kol venalarından kan örnekleri alındı. Kan örnekleri santrifüj edilip serumları ayrıĢtırıldıktan sonra, plastik kapaklı tüpler içerisinde analiz anına kadar –80 0C‟de muhafaza edildi. Yine tüm deneklerden operasyon sonrası elde edilen tiroit doku örnekleri NHO3 ve deiyonize su ile yıkanmıĢ polietilen ağzı kapaklı tüplere alınarak kontaminasyonu engellendi. Analiz gününe kadar -35 0C‟de muhafaza edildi.
22
2.3.Serumda çinko, selenyum, bakır, demir, magnezyum, mangan, fosfor, kurĢun, kobalt, krom, sodyum, potasyum ve kalsiyum tayinleri:
Serum örnekleri, %1‟lik Triton X-100 (Sigma Chemical Co: T-9284 ) çözeltisi ile 1/50 oranında dilue edilmek suretiyle çinko, selenyum, bakır, demir, magnezyum, mangan, fosfor, kurĢun, kobalt, krom, sodyum, potasyum ve kalsiyum düzeylerinin tayini Selçuk Üniversitesi Ziraat Fakültesi Toprak bölümünde bulunan inductively coupled plasma emission spectrophotometry (ICP-AES; Varian Australia Pty LTD, Australia) atomik emisyon cihazında gerçekleĢtirildi (Saygi ve ark 1991).
2.4.Tiroit Dokusunda çinko, selenyum, bakır, demir, magnezyum, mangan, fosfor, kurĢun, kobalt, krom, sodyum, potasyum ve kalsiyum tayinleri:
Tiroit doku örnekleri, NHO3 ve deiyonize su ile yıkanmıĢ polietilen ağzı kapaklı tüplere alınarak kontaminasyonu engellendi. Analiz gününe kadar -350C‟de muhafaza edildi. Analiz yapılmak üzere, tiroit dokusu havanda dövülerek toz haline getirilerek yaĢ ağırlıkları kaydedildi. Üzerine konsantre H2SO4 ve konsantre HNO3 ilave edildi.(gram doku /ml H2SO4/ ml HNO3 = 1 / 1 / 10). Kapalı sistem mikro dalga fırında (CEM – Marsx5) 170 psa basınçta 2000C‟de 20 dakika bekletildi. Daha sonra, 25 ml deiyonize su ile son hacimleri tamamlanarak numuneler maksimum yarım saat bekletilerek okutuldu. Analiz iĢlemi, S. Ü. Ziraat Fakültesi Toprak Bölümünde bulunan Atomik Emisyon (ICP – AES) cihazında gerçekleĢtirildi (Saygi ve ark 1991). Tiroit dokusundaki kalsiyum, fosfat ve çinko değerleri mg/g/yaĢ doku, magnezyum değerleri μg/g/ yaĢ doku cinsinden hesaplandı.
2.5.Ġstatistiksel Değerlendirmeler
Bulguların istatistiksel değerlendirilmesi bilgisayar paket programı ile yapıldı. Diğer bütün parametrelerin aritmetik ortalamaları ve standart hataları hesaplandı. Gruplar arasındaki farklılıkların tespiti için varyans analizi uygulandı. Ġstatistiksel açıdan önemli bulunan varyans analizi sonuçlarında, grup ortalamalarını karĢılaĢtırmak için Asgari Önemli Fark (Least Significant Difference “LSD”) Testi kullanıldı. P<0.05 düzeyindeki farklılıklar anlamlı olarak kabul edildi.
23
3.BULGULAR
3.1.Operasyon Öncesi Deneklerin Element Düzeyleri
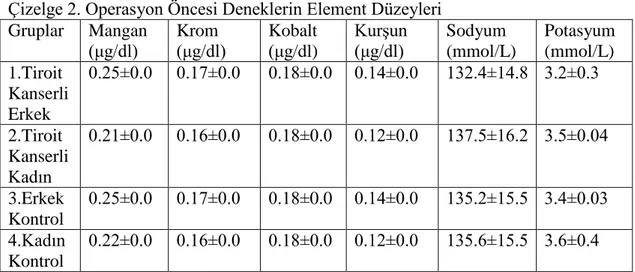
Operasyon öncesi tiroit kanserli erkek (grup 1) ve kadın (grup 2) hastaların serum çinko ve selenyum düzeyleri kontrol gruplarına oranla (grup 3 ve 4) önemli Ģekilde düĢüktü (P<0.05). Buna karĢın tiroit kanserli erkek (grup 1) ve kadın (grup 2) hastaların serum bakır değerleri kontrol gruplarından (grup 3 ve 4) daha yüksekti (p<0.05) (Çizelge 1). Operasyon öncesi çalıĢma gruplarının ölçümü yapılan diğer parametreleri arasında anlamlı bir farklılık yoktu (Çizelge 1 ve 2).
Çizelge 1. Operasyon Öncesi Deneklerin Element Düzeyleri Gruplar Çinko
(μg/dl) Selenyum (μg/dl) Bakır (μg/dl) Demir (μg/dl) Magnezyum (mg/dl)
Fosfor (mg/dl) Kalsiyum (mg/dl) 1.Tiroit Kanserli Erkek 65.5±6.8b 52.4±5.6b 85.4±8.7a 98.7±11.2 2.2±0.4 3.5±0.4 10.4±2.9 2.Tiroit Kanserli Kadın 66.2±7.2b 50.5±4.8b 86.8±8.4a 95.9±10.7 2.1±0.5 3.3±0.3 9.6±3.2 3.Erkek Kontrol 98.5±11.4a 70.1±6.9a 75.5±8.1b 102.9±10.8 2.5±0.8 3.5±0.3 10.2±2.8 4.Kadın Kontrol 92.7±10.2a 66.9±7.3a 74.2±7.5b 98.7±11.5 2.2±0.7 3.1±0.2 9.4±2.6 *Aynı sütunda değiĢik harf taĢıyan ortalamalar arasındaki farklılık istatistiksel olarak
önemlidir (p>0.005.)
Çizelge 2. Operasyon Öncesi Deneklerin Element Düzeyleri Gruplar Mangan (μg/dl) Krom (μg/dl) Kobalt (μg/dl) KurĢun (μg/dl) Sodyum (mmol/L) Potasyum (mmol/L) 1.Tiroit Kanserli Erkek 0.25±0.0 0.17±0.0 0.18±0.0 0.14±0.0 132.4±14.8 3.2±0.3 2.Tiroit Kanserli Kadın 0.21±0.0 0.16±0.0 0.18±0.0 0.12±0.0 137.5±16.2 3.5±0.04 3.Erkek Kontrol 0.25±0.0 0.17±0.0 0.18±0.0 0.14±0.0 135.2±15.5 3.4±0.03 4.Kadın Kontrol 0.22±0.0 0.16±0.0 0.18±0.0 0.12±0.0 135.6±15.5 3.6±0.4 *Aynı sütunda değiĢik harf taĢıyan ortalamalar arasındaki farklılık istatistiksel olarak önemlidir (p>0.005.)
24
3.2.Operasyon Sonrası Deneklerin Element Düzeyleri
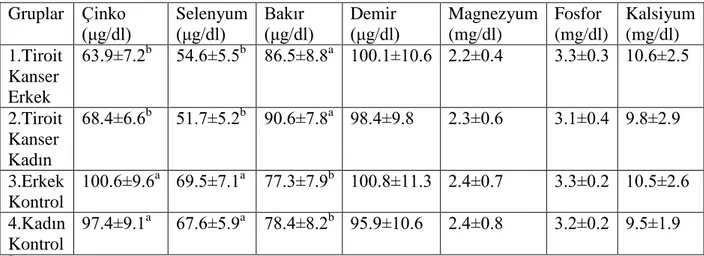
Operasyon sonrası tiroit kanserli erkek (grup 1) ve kadın (grup 2) hastaların serum çinko ve selenyum düzeyleri kontrol gruplarına oranla (grup 3 ve 4) önemli Ģekilde düĢüktü (P<0.05). Buna karĢın tiroit kanserli erkek (grup 1) ve kadın (grup 2) hastaların serum bakır değerleri kontrol gruplarından (grup 3 ve 4) daha yüksekti (p<0.05) (Çizelge 3). Operasyon sonrası çalıĢma gruplarının ölçümü yapılan diğer parametreleri arasında anlamlı bir farklılık yoktu (Çizelge 3 ve 4).
Çizelge 3. Operasyon Sonrası Deneklerin Element Düzeyleri Gruplar Çinko (μg/dl) Selenyum (μg/dl) Bakır (μg/dl) Demir (μg/dl) Magnezyum (mg/dl) Fosfor (mg/dl) Kalsiyum (mg/dl) 1.Tiroit Kanser Erkek 63.9±7.2b 54.6±5.5b 86.5±8.8a 100.1±10.6 2.2±0.4 3.3±0.3 10.6±2.5 2.Tiroit Kanser Kadın 68.4±6.6b 51.7±5.2b 90.6±7.8a 98.4±9.8 2.3±0.6 3.1±0.4 9.8±2.9 3.Erkek Kontrol 100.6±9.6a 69.5±7.1a 77.3±7.9b 100.8±11.3 2.4±0.7 3.3±0.2 10.5±2.6 4.Kadın Kontrol 97.4±9.1a 67.6±5.9a 78.4±8.2b 95.9±10.6 2.4±0.8 3.2±0.2 9.5±1.9 *Aynı sütunda değiĢik harf taĢıyan ortalamalar arasındaki farklılık istatistiksel olarak
önemlidir (p>0.005.)
Çizelge 4. Operasyon Sonrası Deneklerin Element Düzeyleri Gruplar Mangan (μg/dl) Krom (μg/dl) Kobalt (μg/dl) KurĢun (μg/dl) Sodyum (mmol/L) Potasyum (mmol/L) 1.Tiroit Kanserli Erkek 0.22±0.0 0.16±0.0 0.17±0.0 0.15±0.0 132.6±14.9 3.5±0.3 2.Tiroit Kanserli Kadın 0.20±0.0 0.15±0.0 0.15±0.0 0.10±0.0 136.7±14.4 3.8±0.05 3.Erkek Kontrol 0.22±0.0 0.16±0.0 0.17±0.0 0.15±0.0 133.8±15.2 3.4±0.3 4.Kadın Kontrol 0.20±0.0 0.15±0.0 0.15±0.0 0.10±0.0 138.4±14.8 3.7±0.3 *Aynı sütunda değiĢik harf taĢıyan ortalamalar arasındaki farklılık istatistiksel olarak önemlidir (p>0.005.)
25
3.3.Operasyon Sonrası Deneklerin Tiroit dokusundaki Element Düzeyleri
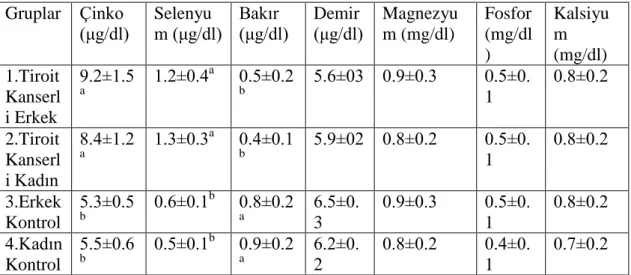
Operasyon sonrası tiroit kanserli erkek (grup 1) ve kadın (grup 2) hastaların tiroit dokusundaki çinko ve selenyum düzeyleri kontrol gruplarına oranla (grup 3 ve 4) önemli Ģekilde yüksekti (P<0.05). Buna karĢın tiroit kanserli erkek (grup 1) ve kadın (grup 2) hastaların tiroit dokusundaki bakır değerleri kontrol gruplarından (grup 3 ve 4) daha düĢüktü (p<0.05) (Çizelge 5). Operasyon sonrası çalıĢma gruplarının tiroit dokusunda ölçümü yapılan diğer parametreleri arasında anlamlı bir farklılık yoktu (Çizelge 5 ve 6).
Çizelge 5. Operasyon Sonrası Deneklerin Tiroit dokusundaki Element Düzeyleri Gruplar Çinko (μg/dl) Selenyu m (μg/dl) Bakır (μg/dl) Demir (μg/dl) Magnezyu m (mg/dl) Fosfor (mg/dl ) Kalsiyu m (mg/dl) 1.Tiroit Kanserl i Erkek 9.2±1.5 a 1.2±0.4 a 0.5±0.2 b 5.6±03 0.9±0.3 0.5±0. 1 0.8±0.2 2.Tiroit Kanserl i Kadın 8.4±1.2 a 1.3±0.3 a 0.4±0.1 b 5.9±02 0.8±0.2 0.5±0. 1 0.8±0.2 3.Erkek Kontrol 5.3±0.5 b 0.6±0.1 b 0.8±0.2 a 6.5±0. 3 0.9±0.3 0.5±0. 1 0.8±0.2 4.Kadın Kontrol 5.5±0.6 b 0.5±0.1 b 0.9±0.2 a 6.2±0. 2 0.8±0.2 0.4±0. 1 0.7±0.2 *Aynı sütunda değiĢik harf taĢıyan ortalamalar arasındaki farklılık istatistiksel olarak önemlidir (p>0.005.)
Çizelge 6. Operasyon Sonrası Deneklerin Tiroit dokusundaki Element Düzeyleri Gruplar Mangan (μg/dl) Krom (μg/dl) Kobalt (μg/dl) KurĢun (μg/dl) Sodyum (mmol/L) Potasyum (mmol/L) 1.Tiroit Kanserli Erkek 0.7±0.0 0.5±0.0 0.4±0.0 0.3±0.0 0.90±0.4 0.40±0.1 2.Tiroit Kanserli Kadın 0.6±0.0 0.4±0.0 0.4±0.0 0.2±0.0 0.87±0.3 0.38±0.1 3.Erkek Kontrol 0.7±0.0 0.5±0.0 0.4±0.0 0.3±0.0 0.90±0.4 0.40±0.1 4.Kadın Kontrol 0.6±0.0 0.5±0.0 0.4±0.0 0.2±0.0 0.85±0.3 0.36±0.1 *Aynı sütunda değiĢik harf taĢıyan ortalamalar arasındaki farklılık istatistiksel olarak önemlidir (p>0.005.)
26
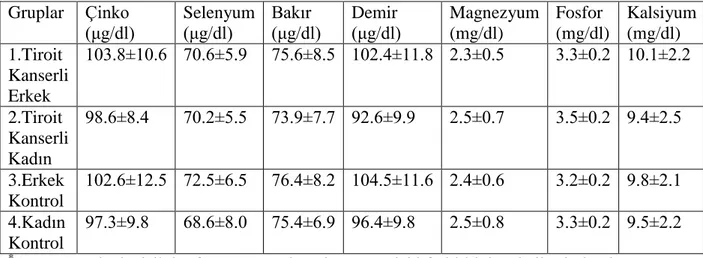
3.4.Operasyondan 15 Gün Sonra Deneklerin Serum Element Düzeyleri
Operasyondan 15 gün sonra çalıĢma gruplarının ölçümü yapılan parametrelerinin tamamı birbirinden farklı değildi (Çizelge 7 ve 8).
Çizelge 7. Operasyondan 15 Gün Sonra Deneklerin Serum Element Düzeyleri Gruplar Çinko (μg/dl) Selenyum (μg/dl) Bakır (μg/dl) Demir (μg/dl) Magnezyum (mg/dl) Fosfor (mg/dl) Kalsiyum (mg/dl) 1.Tiroit Kanserli Erkek 103.8±10.6 70.6±5.9 75.6±8.5 102.4±11.8 2.3±0.5 3.3±0.2 10.1±2.2 2.Tiroit Kanserli Kadın 98.6±8.4 70.2±5.5 73.9±7.7 92.6±9.9 2.5±0.7 3.5±0.2 9.4±2.5 3.Erkek Kontrol 102.6±12.5 72.5±6.5 76.4±8.2 104.5±11.6 2.4±0.6 3.2±0.2 9.8±2.1 4.Kadın Kontrol 97.3±9.8 68.6±8.0 75.4±6.9 96.4±9.8 2.5±0.8 3.3±0.2 9.5±2.2 *Aynı sütunda değiĢik harf taĢıyan ortalamalar arasındaki farklılık istatistiksel olarak
önemlidir (p>0.005.)
Çizelge 8. Operasyondan 15 Gün Sonra Deneklerin Element Düzeyleri Gruplar Mangan (μg/dl) Krom (μg/dl) Kobalt (μg/dl) KurĢun (μg/dl) Sodyum (mmol/L) Potasyum (mmol/L) 1.Tiroit Kanserli Erkek 0.23±0.0 0.15±0.0 0.15±0.0 0.12±0.0 140.6±15.2 3.7±0.4 2.Tiroit Kanserli Kadın 0.21±0.0 0.16±0.0 0.15±0.0 0.11±0.0 138.8±15.1 3.6±0.4 3.Erkek Kontrol 0.23±0.0 0.15±0.0 0.15±0.0 0.12±0.0 140.5±14.9 3.7±0.4 4.Kadın Kontrol 0.22±0.0 0.16±0.0 0.14±0.0 0.11±0.0 141.6±15.2 3.5±0.3 *Aynı sütunda değiĢik harf taĢıyan ortalamalar arasındaki farklılık istatistiksel olarak önemlidir (p>0.00
27
4.TARTIġMA
Çinko eksikliği, geliĢmekte olan ülkelerde majör halk sağlığı sorunlarından biri olmasına karĢın; çinko eksikliğiyle guatr problemleri arasındaki korelasyon daha sınırlıdır. Çinko, tiroksini daha aktif formu olan triiyodotironine dönüĢtürmek için gerekli olan tip1 5‟- deiyodinaz enziminin düzenli fonksiyon görmesi için gereklidir (Maxwell ve Volpe 2007). Wada ve King (1986) tarafından yapılan çalıĢma, çinko değerleri ile tiroit hormon değerleri arasındaki iliĢkiyi ve tiroit hormon fonksiyonlarına çinko desteğinin etkisini keĢfeden araĢtırmaların ilk olanıdır. Bu araĢtırmacılar guatrlı erkek ve kadın hastalarda çinko eksikliği olduğunda, serbest triiyodotironin (FT3) ve serbest tiroksin (FT4) değerlerinin belirgin olarak düĢüklüğünü rapor etmiĢlerdir. Bu sebeple çinko alımı belki de guatrlı hastalarda düĢük tiroit hormon değerleri ile iliĢkilidir (Wada ve King 1986).
Tiroit hastalıkları insan ve hayvan çalıĢmalarında en sık rastlanan ikinci endokrinopatidir. Normal tiroit düzeyi, tiroit hormonlarının sentez ve metabolizması için pek çok eser elementin varlığına bağlıdır (Kandhro ve ark 2009). Bunun yanında iyot ve bazı eser elementler tiroit hormon metabolizmasına katılmaktadır (Arthur ve Beckett 1999). Fakat sadece birkaç çalıĢma, bazı eser elementlerin eksikliğinin ilerleyen yaĢlarda izlenen tiroit fonksiyon değiĢimlerini açıklamasının mümkün olabileceğini göstermiĢtir (Arthur ve Beckett 1999, Kandhro ve ark 2009). Çinkonun suboptimal veya supraoptimal olarak diyetle alımının tiroit hormon metabolizmasına etki edebildiği ve aynı zamanda çinko eksikliğinin guatr oluĢumunda sinerjistik etkisinin olduğu gösterilmiĢtir (Arthur ve Beckett 1999).
Birçok hormonun fizyolojik ve biyokimyasal seviyeleri çinko metabolizmasından etkilenmektedir (Ravaglia ve ark 2000). Bu hormonlardan en önemlisi, çinko ile birbirini etkilemesi araĢtırılan tiroit hormonlarıdır (Ravaglia ve ark 2000). Büyümenin bozulması ve bazı endokrin hastalıklar çinko eksikliğine bağlıdır (Kandhro ve ark 2009). Tiroit hormonlarıyla çinko arasındaki etkileĢimin önemli olduğu ve çinko eksikliğinin guatr baĢlangıcı için uyarıcı bir faktör olabileceği düĢünülmektedir (Arthur ve Beckett 1999, Kandhro ve ark 2009).
Ġnsan dokularında ve sıvılarında çinko analizleri; çeĢitli hastalıkların teĢhisinde, beslenme durumunun saptanmasında, sistemik intoksikasyonun belirlenmesi ve çevre maruziyeti gibi olaylar hakkında bilgi edinilmesine imkan sunmakta ve bu konularda fayda sağlamak için kullanılabilmektedir (Kandhro ve ark 2009).