T.C
EGE ÜNVERSĠTESĠ TIP FAKÜLTESĠ ĠÇ HASTALIKLARI ANABĠLĠM DALI
Prof. Dr. Fehmi AKÇĠÇEK
DĠYABETĠK AYAKLI OLGULARDA KAN HĠPOKSĠ ĠLE ĠNDÜKLENEBĠLĠR FAKTÖR- 1ALFA, FETUĠN- A, FĠBRĠNOJEN VE HOMOSĠSTEĠN DÜZEYLERĠNĠN
AMPÜTASYON SEVĠYESĠYLE ĠLĠġKĠSĠ
UZMANLIK TEZĠ Dr. Nur Sinem ŞENGÖZ COŞKUN
TEZ DANIġMANI Prof. Dr. Şevki ÇETİNKALP
T.C
EGE ÜNVERSĠTESĠ TIP FAKÜLTESĠ ĠÇ HASTALIKLARI ANABĠLĠM DALI
Prof. Dr. Fehmi AKÇĠÇEK
DĠYABETĠK AYAKLI OLGULARDA KAN HĠPOKSĠ ĠLE ĠNDÜKLENEBĠLĠR FAKTÖR- 1ALFA, FETUĠN- A, FĠBRĠNOJEN VE HOMOSĠSTEĠN DÜZEYLERĠNĠN
AMPÜTASYON SEVĠYESĠYLE ĠLĠġKĠSĠ
UZMANLIK TEZĠ Dr. Nur Sinem ŞENGÖZ COŞKUN
TEZ DANIġMANI Prof. Dr. Şevki ÇETİNKALP
DEĞERLENDĠRME KURULU ÜYELERĠ
Adı Soyadı İmza
Başkan (Danışman): Prof.Dr. Şevki ÇETİNKALP …………...………...
Üye: Prof.Dr. Fehmi AKÇİÇEK …...………...
Üye: Prof.Dr. A. Gökhan ÖZGEN ...………...
Üye: Prof.Dr. Zeliha HEKİMSOY …………...
TEġEKKÜR
Uzmanlık eğitimim boyunca büyük bir aile olduğumuzu hissettiren, iyi hekimlik, etik kavramlarını bize ilgi ve sevgiyle öğreten, her anımızda desteğini esirgemeyen Anabilim Dalı Başkanı Sayın Prof. Dr. Fehmi AKÇİÇEK‟ e,
Tez hazırlama sürecimde güler yüzü ve pozitif motivasyonu sayesinde bu zorlu süreci kolayca atlatmama yardımcı olan, bakış açılarıyla bilim ufkumu geliştiren tez danışmanım Sayın Prof. Dr. Şevki ÇETİNKALP‟ e ve yardımları sayesinde doğru yolda ilerlememi sağlayan her daim güler yüzlü uzmanım Sayın Uzm. Dr. Ilgın YILDIRIM ŞİMŞİR‟ e,
Bugünkü donanım ve hekimlik becerilerimin kaynağı olan, uzmanlık eğitimi sürecimde bana doğru yolu gösterip bilgi ve birikimimi geliştiren, gereğinde manevi anlamda da desteğini esirgemeyen, bana bu yolu seçtiren başta Sayın Prof. Dr. Güray SAYDAM olmak üzere tüm İç Hastalıkları öğretim üyelerine,
Hastanede geçirdiğim süre zarfında birlikte çalıştığım tüm asistan arkadaşlarıma, hemşirelerimize ve personelimize,
Tez sürecimin her aşamasında en az benim kadar uğraşıp, bu dönem boyunca bana yeri geldiğinde öğretmenlik, yeri geldiğinde de ablalık yapan, Tıbbi Biyokimya Anabilim Dalı Öğretim Üyesi Sayın Prof. Dr. Yasemin AKÇAY‟ a,
Eğitim hayatım boyunca benim kendi gelişimime odaklanabilmem için her türlü fedakarlıkta bulunan, dualarını esirgemeyen ve bana güç veren canım aileme ve iyi kötü her anımda varlığıyla yüzümü güldüren sevgili eşim Celaleddin Çağrı COŞKUN‟ a sonsuz teşekkürlerimi sunarım.
Dr. Nur Sinem ŞENGÖZ COŞKUN
i
ĠÇĠNDEKĠLERTABLO VE ŞEKİL LİSTESİ ……….…iii
KISALTMALAR LİSTESİ ………...………...v ÖZET ……….……vii ABSTRACT ………ix 1 - GİRİŞ VE AMAÇ ………...….1 2 – GENEL BİLGİLER ………...3 2.1 Diabetes Mellitus ……….3 2.1.1 Tanım ………...3 2.1.2 Epidemiyoloji ………...3 2.1.3 Sınıflandırma ………4 2.1.4 Etyoloji ………...………..5 2.1.5 Tanı ………..7 2.1.6 Komplikasyonlar ………...7 2.1.6.1 Makrovasküler Komplikasyonlar……….8 2.1.6.1.1 Kardiyovasküler Hastalıklar………...………..8 2.1.6.1.2 Serebrovasküler Hastalıklar………10
2.1.6.1.3 Periferik Damar Hastalığı………...11
2.1.6.2 Mikrovasküler Komplikasyonlar……….………..12 2.1.6.2.1 Diyabetik Nefropati………...12 2.1.6.2.2 Diyabetik Retinopati………...13 2.1.6.2.3 Diyabetik Nöropati………..13 2.2 Diyabetik Ayak ………..18 2.2.1 Tanım ……….18 2.2.2 Epidemiyoloji ………...18 2.2.3 Etyoloji ………...19
ii
2.2.3.1 Metabolik ve Biyokimyasal Patogenez………...21
2.2.3.2 Yapısal ve Biyomekanik Patogenez………...22
2.2.3.3 Diyabetik Ayak Enfeksiyonu………...23
2.2.4 Sınıflandırma ………..25
2.2.5 Tedavi ………...30
2.3 Diyabetik Ayak Ampütasyonları ………...32
2.3.1 Tanım ………...32
2.3.2 Epidemiyoloji ………32
2.3.3 Sınıflandırma ………...33
2.4 Hipoksi ile İndüklenebilir Faktör- 1alfa (HIF- 1α) ………...34
2.5 Fetuin- A ……….35
2.6 Fibrinojen ………...37
2.7 Homosistein ………37
2.7.1 Homosistein Metabolizması………37
2.7.2 Hiperhomosisteinemi ve Nedenleri……….38
2.7.3 Hiperhomosisteineminin Fizyopatolojik Mekanizmaları ve Klinik Sonuçları……….39 3 – GEREÇ VE YÖNTEM….. ………..41 4 – BULGULAR ………42 5 – TARTIŞMA ……….59 6 – SONUÇ VE ÖNERİLER ………...68 7 – KAYNAKLAR ………...69
iii
TABLO, ġEKĠL VE GRAFĠK LĠSTESĠTablo- 1: Hastaların ortalama yaş ve DM süreleri
Tablo- 2: Hastaların ortalama boy, kilo ve BMI ölçümleri
Tablo- 3: Hastaların ortalama bilek- önkol indeksleri
Tablo- 4: Hastaların anamnez ve fizik muayeneleri bulgular
Tablo- 5: Hastaların kanında bakılan diyabetik belirteçleri
Tablo- 6: Hastaların kanında bakılan inflamatuvar belirteçleri
Tablo- 7: Hastaların kanında bakılan lipid profilleri
Tablo- 8: Hastaların kanında bakılan diğer biyokimyasal parametreleri
Tablo- 9: Hastaların kanında çalışma için bakılan parametrelerin özeti
Tablo- 10: Hastaların biyokimyasal parametrelerinin yara Wagner evrelerine göre ortalamaları
Tablo- 11: Hastaların biyokimyasal parametrelerinin ampütasyon seviyelerine göre ortalamaları
Tablo- 12: Biyokimyasal parametrelerin yara Wagner evresi ile ilişkisi (p > 0.05)
Tablo- 13: Biyokimyasal parametrelerin ampütasyon seviyesi ile ilişkisi
Şekil- 1: Nasırları olan diyabetik bir hasta ayağı (Wagner Evre- 0) Şekil- 2: Yüzeyel diyabetik ayak ülseri (Wagner Evre- 1)
Şekil- 3: Osteomyelit olmaksızın derin ülser bulunan diyabetik ayak yarası (Wagner Evre- 2) Şekil- 4: Osteomyelit ve yumuşak doku enfeksiyonu ile birlikte diyabetik ayak ülseri (Wagner Evre- 3)
Şekil- 5: 1- 2. parmaklarda nekroz geliştirmiş diyabetik ayak ülseri (Wagner Evre- 4)
Şekil- 6: Ayağın büyük bir bölümünde nekroz geliştirmiş olan diyabetik ayak yarası (Wagner Evre- 5)
Grafik- 1: Olguların cinsiyet dağılımı
Grafik- 2: Hastaların DM tiplerine göre dağılımı
iv
Grafik- 4: Olgulardaki eşlik eden komorbiditelerin sıklık dağılımıGrafik- 5: Olguların ampütasyon seviyelerine göre dağılımı
Grafik- 6: Ortalama Homosistein düzeyi ve yara Wagner evresi arasındaki ilişki
Grafik- 7: Ortalama Fibrinojen düzeyi ve yara Wagner evresi arasındaki ilişki
Grafik- 8: Ortalama HIF- 1α düzeyi ve yara Wagner evresi arasındaki ilişki
Grafik- 9: Ortalama Fetuin- A düzeyi ve yara Wagner evresi arasındaki ilişki
Grafik-10: Ortalama Homosistein düzeyi ve ampütasyon seviyesi arasındaki ilişki
Grafik-11: Ortalama Fibrinojen düzeyi ve ampütasyon seviyesi arasındaki ilişki
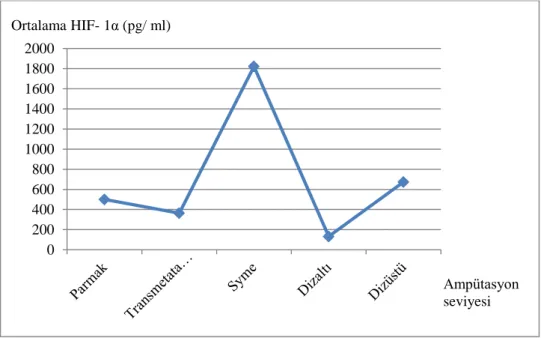
Grafik-12: Ortalama HIF- 1α düzeyi ve ampütasyon seviyesi arasındaki ilişki
Grafik-13: Ortalama Fetuin- A düzeyi ve ampütasyon seviyesi arasındaki ilişki
Grafik- 14: Her bir hastanın fetuin- A düzeyi ve ampütasyon seviyesi arasındaki ilişki (n= 30)
Grafik- 15: Her bir hastanın fibrinojen düzeyi ve ampütasyon seviyesi arasındaki ilişki (n= 28)
Grafik- 16: Her bir hastanın homosistein düzeyi ve ampütasyon seviyesi arasındaki ilişki (n= 29)
v
KISALTMALAR LĠSTESĠABD: Amerika Birleşik Devletleri ABI: Bilek- Önkol İndeksi
ACE: Anjiotensin Dönüştürücü Enzim AKŞ: Açlık Kan Şekeri
ATP: Adenozin Trifosfat
BMI: Beden Kitle İndeksi
CABG: Koroner Arter Bypass Grefti
CRP: C- Reaktif Protein
DM: Diabetes Mellitus
ESH: Eritrosit Sedimentasyon Hızı
FGF: Fibroblast Büyüme Faktörü FMF: Ailesel Akdeniz Ateşi GAD: Glutamik asit dekarboksilaz
GF: Büyüme Faktörü
GFR: Glomerüler Filtrasyon Hızı GLUT- 4: Glukoz taşıyıcısı- 4
HbA1c: Glikozile Hemoglobin (%)
HBO: Hiperbarik Oksijen
HDL: Yüksek dansiteli lipoprotein
HIF- 1α: Hipoksi ile indüklenebilir faktör- 1alfa
HLA: İnsan lökosit antijeni HPL: Hiperlipidemi
vi
ICA: Adacık hücre otoantikoruIDF: Uluslararası Diyabet Cemiyeti Ig: İmmunglobulin
IGF: İnsülin Benzeri Büyüme Faktörü IGT: Bozulmuş Glukoz Toleransı IL: İnterlökin
KAH: Koroner Arter Hastalığı KBY: Kronik Böbrek Yetmezliği KTS: Karpal Tünel Sendromu KY: Kalp Yetmezliği
LDL: Düşük dansiteli lipoprotein MI: Myokard İnfarktüsü
MODY: Gençlerdeki Erişkin Tip Diyabet
MRSA: Metisilin Rezistan Staphylococcus Aureus
NO: Nitrik Oksit
OAD: Oral Antidiyabetik
OGTT: Oral Glukoz Tolerans Testi
PAH: Periferik Arter Hastalığı PAI: Plazminojen Aktivatör İnhibitörü PHD: Prolil Hidroksilaz Domain
PI3K: Fosfatidil İnozitol- 3 Kinaz SYA: Serbest Yağ Asitleri SVO: Serebrovasküler Olay
vii
TG: TrigliseridTGF: Dönüştürücü Büyüme Faktörü TNF: Tümör Nekroz Faktörü
TURDEP: Türk Diyabet Epidemiyoloji Çalışma Grubu UKPDS: Birleşik Krallık Prospektif Diyabet Çalışması
USG: Ultrasonografi
VEGF: Vasküler Endotelyal Büyüme Faktörü VLDL: Çok Düşük Dansiteli Lipoprotein VRE: Vankomisin Rezistan Enterokok
viii
ÖZETDĠYABETĠK AYAKLI OLGULARDA KAN HĠPOKSĠ ĠLE ĠNDÜKLENEBĠLĠR FAKTÖR- 1ALFA, FETUĠN- A, FĠBRĠNOJEN VE HOMOSĠSTEĠN DÜZEYLERĠNĠN
AMPÜTASYON SEVĠYESĠYLE ĠLĠġKĠSĠ
Diabetes Mellitus‟ lu hastaların yaşam süresinin artmasına bağlı gelişen kronik komplikasyonların görülme sıklığı artmıştır. Bu önemli komplikasyonlardan birisi olan diyabetik ayak sendromu, çoğunlukla diyabetik nöropati ve vasküler yetersizliğin birlikte olmasının bir sonucu olarak ortaya çıkar ve travmatik olmayan ayak ampütasyonlarının % 60‟ ını oluşturmaktadır. Ayrıca dünyanın her yerinde hastanede kalış süresi uzunluğu, maliyeti, mortalite ve morbiditenin yüksekliği nedeniyle en önemli halk sağlığı sorunlarından birisidir.
Hipoksi ile indüklenebilir faktör- 1alfa (HIF- 1α) hipoksiye adaptasyon cevabının gelişiminde anahtar rol oynar, yaralardaki epitel restorasyonunu ve keratinosit göçünü düzenleyerek iyileşmeyi hızlandırmaktadır. Yapılmış olan çalışmalarda diyabetik bireylerde hiperglisemik çevrede transaktivasyonda bozulma sonucu HIF- 1α disfonksiyonu olduğu gösterilmiştir.
Fetuin- A, albumin gibi karaciğerden sentezlenen ve insülin aktivitesi ile vasküler ve ektopik kalsifikasyonları inhibe eden bir taşıyıcı proteindir. Diyabetiklerdeki fetuin- A düşüklüğünün vasküler kalsifikasyona yol açarak periferik arter hastalığı ile, yükselişinin ise ılımlı inflamasyon ve metabolik sendrom gelişimi ile ilişkili olduğu gözlenmiştir.
Fibrinojen, karaciğerden sentezlenen; hemostazda, doku onarımı ve yara iyileşmesinde önemli işlevleri olan bir akut faz reaktanıdır. Diyabetik bireylerde kandaki düzeyi artan fibrinojen, hiperkoagülabilite ortamı oluşumunu kolaylaştıran faktörlerden birisidir.
Homosistein metiyonin metabolizması esnasında oluşan, aterojenik özelliği olan (endotel disfonksiyonu ve hasar sonrası gelişen trombosit aktivasyonu ve trombüs oluşumu ile ilişkili), ayrıca LDL oksidasyonunu arttırarak vasküler toksisite yaratan bir aminoasittir. Homosisteinin bu toksik etkiler neticesinde endotelyumun normal antikoagülan fenotipini değiştirerek damarsal hastalığa zemin hazırlayabilmektedir.
Çalışmamızda; Diabetes Mellitus tanısına sahip ve buna bağlı sık görülen bir komplikasyon olan diyabetik ayak yarası olup Diyabetik Ayak Konseyi kararıyla ampütasyon planlanmış 31 hastada biyokimyasal olarak serum hipoksi ile indüklenebilir faktör- 1alfa (HIF- 1α), fetuin- A, fibrinojen ve homosistein düzeylerini belirleyerek bu kriterlerin ampütasyon seviyesi ile korelasyonunu inceledik.
Çalışmamızın sonucunda, fetuin- A düzeyi ile ampütasyon seviyesi arasında istatistiksel olarak anlamlı negatif korelasyon saptandı (p: 0.012, r: -0.450). Ancak HIF- 1α, fibrinojen ve homosistein ile ampütasyon seviyesi arasında anlamlı bir ilişki izlenmedi (p > 0.05).
Bu sonuçlarla diyabetik ayak patogenezinde fetuin- A eksikliğinin neden olduğu vasküler kalsifikasyonun önemli role sahip olabileceği, ayrıca fetuin- A düzeyinin ampütasyon seviyesini öngördürecek bir belirteç olabileceği düşünülmüştür. Bu bilgi ışığında patogeneze yönelik hayvan çalışmaları ve fetuin- A cut- off değerini belirleyecek büyük ölçekli insan çalışmaları yapılabilir.
ix
ABSTRACTTHE RELATIONSHIP BETWEEN AMPUTATION LEVEL AND BLOOD HYPOXIA- INDUCIBLE FACTOR- 1ALPHA, FETUIN- A, FIBRINOGEN AND HOMOCYSTEINE LEVEL
IN PATĠENTS WITH DIABETĠC FOOT
Cause of increased survival in patient with diabetes mellitus, incidence of chronic complications in this patient group has increased. The diabetic foot syndrome, which is one of those important complications, occurs usually as a result of presence both of diabetic neuropathy and vascular failure and it‟s reason % 60 of nontraumatic lower extremity amputations. Also that‟s one of the most important public health problems everywhere in the world cause of its increased cost, mortality, morbidity and hospitalization time.
Hypoxia- inducible factor- 1 alpha (HIF- 1α), plays a key role at developing adaptation response to hypoxia and it‟s expedites healing by arranging epithelium restoration and keratinocyte migration. In studies, HIF- 1α disfunction has shown in diabetic patients cause of faulty transactivation at hyperglycemic environment.
Fetuin- A is a carrier protein that has produced from liver as albumine and inhibates of vascular and ectopic calcifications with its insulin activity. It has observed that lower fetuin- A levels is related with peripheral artery disease causing vascular calcification and upper fetuin- A levels is related with developing minimal inflammation and metabolic syndrome in diabetic patients.
Fibrinogen is an acut phase reactant that‟s produced from liver and it has important functions in hemostasis, tissue repair amd wound healing. Increased blood fibrinogen level in diabetic patients is one of the factors that facilitates developing prothrombotic status.
Homocysteine is an aminoacid that occurs during methionine metabolism and has atherogenic characteristic (related with endothelial disfunction; thrombocyte activation and thrombosis formation after injury), also it crauses vascular toxicity by increasing oxidation of LDL. As a result of this toxic effects, homocysteine can cause vascular disease by changing normal anticoagulant phenotype of endothelium.
In our study, we investigated correlations between amputation level and biochemical criteria by measuring levels of blood HIF- 1alfa, fetuin- A, fibrinogen and homocysteine in 31 patients those have DM, diabetic foot wound, amputation decision was taken in Diabetic Foot Council
As a result of our study, there was statistically negative correlation between blood fetuin- A level and amputation level (p: 0.012, r: -0.450). But there was no significant correlation between amputation level and other biochemical parameters, HIF- 1alfa, fibrinogen and homocysteine (p > 0.05).
With these results, it has thought that vascular calcifications cause of decreased fetuin- A levels may be probably important role in diabetic foot pathogenesis. Also it has thinked that fetuin- A can be a marker that predicts amputation level. Based on this information, animal studies for pathogenesis and large- scale human studies that determines cutoff level of fetuin- A can be do.
1
1. GĠRĠġ VE AMAÇ
Diabetes Mellitus tüm dünyada en sık rastlanan, endojen insülinin mutlak veya göreceli eksikliği veya periferik etkisizliği sonucu ortaya çıkan kronik hiperglisemi, karbonhidrat, protein ve yağ metabolizmasında bozukluk, kapiller membran değişiklikleri ve hızlanmış arter sklerozu ile seyreden endokrin bir hastalıktır. İnsülin ve oral antidiyabetik ilaçların keşfiyle diyabetli bireylerin yaşam süreleri belirgin olarak uzamıştır. Bu sebeple, diyabetli bireylerin yaşam süresinin artmasına bağlı gelişen kronik komplikasyonların görülme sıklığı da artmıştır (1).
Diyabetik Ayak Sendromu, diyabetik nöropati ve vasküler yetersizliğe enfeksiyonun da eşlik etmesi sonucu ortaya çıkar. Tüm diyabet hastalarının % 10- % 25‟ inde diyabetik ayak ülseri gelişme riski vardır. Travmatik olmayan ayak ampütasyonlarının % 60‟ ını diyabetik ayak ülseri oluşturmaktadır (2, 3). Diyabetik ayaklı olgularda ampütasyon kararı ve seviyesi hastanın komorbiditeleri, performansı, doppler ultrasonografi bulguları ve klinik muayene sonuçlarıyla alınmakta olup henüz objektif ampütasyon kriterleri geliştirilememiştir (4). Ampütasyonların % 24‟ ü topuk, % 6‟ sı ayak ortası, % 39‟ u diz altı, % 21‟ i diz üstü ampütasyon şeklindedir (5). Diyabetik ayak lezyonlarının ABD‟ de yıllık maliyeti yaklaşık olarak 200- 500 milyon dolar olarak hesaplanmıştır. ABD‟ de yılda yaklaşık olarak 50.000‟ den fazla ampütasyon yapılmakta ve bunun maliyeti de yaklaşık 1 milyar dolar olarak bildirilmektedir (6, 7, 8). Ayrıca, yerli ve yabancı literatür incelendiğinde; reampütasyon oranlarının da % 16.4- % 43 arasında olduğu bildirilmiştir (9, 10). Diyabetik bireylerin % 9- 13‟ ünde ilk ampütasyon sonrası ilk 1 yıl içerisinde yeni bir ipsilateral veya kontralateral ampütasyon uygulanır. İlk ampütasyon sonrası 5 yıl içerisinde ise % 28- 51‟ i yeni bir ampütasyona gider (10). Diyabetik ayak dünyanın her yerinde hastanede kalış süresi uzunluğu, maliyeti, mortalite ve morbiditenin yüksekliği nedeniyle en önemli halk sağlığı sorunlarından birisidir. Diyabetik ayak yarası oluşumu ve buna bağlı ampütasyon gelişiminde periferik arter hastalığı en sık görülen komorbid faktörler arasında sayılmaktadır. Vasküler yetersizlik yani damar tıkanıklığı; özellikle damarlar, arterioller ve kapillerleri etkiler, prekapiller seviyede yaygın arteriyovenöz şantlar olur ve riskli bölgelerde doku oksijenlenmesinin azalmasına neden olur.
Diyabetik nöropati de diyabetik ayak gelişiminde çok önemlidir. Başlıca sensöriyel olup ağrı hissi, vibrasyon hissi ve pozisyon duygusunda azalmaya neden olur. Ayrıca diyabetik otonom nöropatiden dolayı terleme hissi de bozulur, cilt kurur, yüzeyel inflamasyon ve kronik dermatit olur. Diyabetik nöropatiden dolayı ayakta his kusuru olunca minimal travma veya inflamasyon iyileşmesi için oraya gelen kanın artması gerekir, ancak vasküler yetersizlikten dolayı bu olmaz. Ayrıca yine diyabetik nöropatiden dolayı ayakta basıncın anormal dağılımından kaynaklanan kallus teşekkülü olur; bu da iskemi, mikrotrombüs ve ileride ülser veya gangren oluşumuna neden olur (11). Yani hipoksi, nöropati ve vaskülarizasyon bozukluğu, diyabetik ayak yarası oluşumundaki en önemli faktörlerdir.
Hipoksi ile indüklenebilir faktör- 1alfa (HIF- 1α) hipoksiye adaptasyon cevabının gelişiminde anahtar rol oynayan bir transkripsiyon faktörüdür (12). Alfa ve beta alt ünitelerinden
2
oluşan bu faktörün alfa subüniti hücredeki oksijen konsantrasyonunun azalmasına bağlı olarak aktive olur (13). Yaralardaki epitel restorasyonunu ve keratinosit göçünü düzenleyerek iyileşmeyi hızlandırır, yaşamsal öneme sahiptir. Yapılmış olan çalışmalarda diyabetik bireylerde hiperglisemik çevrede transaktivasyonda bozulma sonucu HIF- 1α disfonksiyonu olduğu gösterilmiştir (14, 15, 16). Bu da hipoksinin derinleşmesine bağlı diyabetik ayak yarası gelişiminde HIF- 1α‟ nın önemi olabileceğini düşündürmektedir.Fetuin- A, albumin gibi karaciğerden sentezlenen ancak fetal serumda daha yüksek oranda olan ve insülin aktivitesini inhibe eden bir taşıyıcı proteindir. Postprandiyal glukoz düzeyinin ayarlanmasında, insülin sensitivitesinde, kilo alımı ve yağ birikiminde önemli bir role sahip olduğu düşünülmektedir (17, 18). Fareler üzerinde yapılan çalışmalarda, fetuin- A geninden yoksun farelerde ektopik kalsifikasyonların çok yüksek oranda olduğu gösterilmiş, in vitro ortamda kalsiyum fosfat çökeltilerine sonradan eklenen fetuin- A‟nın bu yapılara bağlanmak suretiyle sistemik kalsifikasyon üzerine negatif etkisi olduğu belirtilmiştir (19). Fetuin- A eksikliğine bağlı vasküler (özellikle arteriyal) kalsifikasyonun diyabetik ayak yarasının vaskülarizasyonunu bozarak iyileşmeyi zorlaştırdığı düşünülmektedir.
Fibrinojen, koagülasyon mekanizmasında rol oynayan ve karaciğerden sentezlenen bir akut faz reaktanıdır. Hemostazda doku onarımı ve yara iyileşmesinde önemli işlevleri vardır (20). Yapılan çalışmalarda koroner arter hastalığı ile yüksek fibrinojen düzeyi arasında anlamlı ilişki olduğu gösterilmiştir (21). Diyabetik bireylerde kandaki düzeyi artan fibrinojen, hiperkoagülabilite ortamı oluşumunu kolaylaştıran faktörlerden birisidir. Fibrinojen artışının yol açtığı hiperkoagülabilite de periferik damar kan akımını azaltıp doku iskemisine neden olarak diyabetik ayak iyileşme sürecini yavaşlatabilir.
Homosistein metiyonin metabolizması esnasında oluşan, yapısında sülfür bulunduran bir aminoasittir (22). Aterojenik olma özelliği endotel disfonksiyonu ve hasar sonrası gelişen trombosit aktivasyonu ve trombüs oluşumu ile ilişkilidir. Ayrıca LDL oksidasyonunu arttırarak vasküler toksisite yaratır. Yapılan çalışmalarda yüksek plazma homosistein düzeyinin aterosklerotik damar hastalığına yol açabileceği belirtilmiştir (23, 24). İskemi sonucunda da diyabetik olgularda yara gelişme riski artar, yara iyileşmesi bozulur.
Biz bu çalışma ile, hem Diabetes Mellitus„ a bağlı olarak yaygın görülen bir klinik sorun olan diyabetik ayağın patofizyolojisinde rol oynadığı düşünülen HIF- 1α, fetuin- A, fibrinojen ve homosistein düzeylerinin bu komplikasyonun gelişiminde katkısının olup olmadığının gösterilmesini, hem de serumda kolaylıkla ölçülebilen bu parametreler ile ampütasyonun seviyesinin objektif olarak öngörülebilirliğinin değerlendirilmesini amaçladık.
3
2. GENEL BĠLGĠLER
2.1 DĠABETES MELLĠTUS
2.1.1 Tanım
Diabetes mellitus (DM), insülin hormon sekresyonunun ve/ veya insüline karşı doku cevabının mutlak ve göreceli azlığı sonucu karbonhidrat, protein ve yağ metabolizmasında bozukluklara yol açan kronik hiperglisemik bir grup metabolizma hastalığıdır (25). Bu durumun sonucu olarak kronik hiperglisemi, karbonhidrat, yağ ve protein metabolizması bozuklukları, kapiller membran değişiklikleri ve hızlanmış ateroskleroz oluşur. İnsülin ve oral antidiyabetik ilaçların keşfiyle diyabetli bireylerin yaşam süreleri belirgin uzamıştır. Yaşam süresinin artmasına bağlı gelişen kronik komplikasyonların görülme sıklığı artmıştır (1).
2.1.2 Epidemiyoloji
Aralık 2015‟ te güncellenen IDF (Uluslararası Diyabet Federasyonu) verilerine göre; bu tarih itibariyle DM tanısına sahip 415 milyon erişkin olduğu belirtilmekte (215.2 milyonu erkek, 199.5 milyonu kadın), 2040 yılı itibariyle bu sayının 642 milyona ulaşması (328.4 milyonu erkek, 313.3 milyonu kadın) beklenmektedir. Bu da, yaklaşık olarak 11 erişkinden 1‟ inin DM tanısına sahip olduğu, 2040‟ta ise 10 erişkinden 1‟ inin diyabetli olacağı anlamına gelmektedir. Her 6 saniyede 1 kişi olmak üzere toplam 5 milyon ölümün DM nedeniyle olduğu belirtilmektedir (26).
Diyabet, hem gelişmiş hem de gelişmekte olan ülkelerde yaygındır (27). Ancak az gelişmiş ülkelerde yaygın değildir (28). 2015 yılı itibariyle en çok diyabet hastasına sahip beş ülke; 109.6 milyonla Çin, 69.2 milyonla Hindistan, 29.3 milyonla ABD, 14.3 milyonla Brezilya ve 12.1 milyonla Rusya olmuştur (29).
Diabetes Mellitus batı toplumlarının yaklaşık % 3- 5' ini ilgilendiren bir metabolik bozukluktur ve önemli olan bir nokta da hastalığın prevalansının yaşlanma ile birlikte hızlı bir şekilde artış göstermesidir. Aslen bir yetişkin hastalığı olarak görülen Tip 2 DM, obezite oranlarının artışıyla paralel olarak çocuklarda da artış göstermiştir (27). Tip 2 DM artık ABD‟ deki ergenlik çağındaki çocuklarda, Tip 1 DM kadar sık teşhis edilmektedir (28).
Türkiye' de populasyona dayalı ilk diyabet taraması olup 1997- 1998 yıllarında Türk Diyabet Epidemiyoloji Çalışma Grubu (TURDEP) tarafından 24.788 kişinin katılımıyla yapılan TURDEP- I çalışmasında erişkin yaş nüfusta (≥ 19 yıl) Tip- 2 diyabetin prevalansının % 7.2 ve bozulmuş glukoz toleransının prevalansı % 6.7 olarak bildirilmiştir (30). 2010 yılında yapılan TURDEP- II çalışmasında ise ülke genelinde 20 yaş üzerinde 26.499 kişi incelenmiş ve tip 2 diyabet sıklığının geçen yıllarda önemli derecede arttığı ve % 13.7‟ ye, BGT‟ nin ise % 7.9‟ a vardığı görülmüştür. TURDEP –I ve TURDEP- II‟ yi karşılaştıracak olursak;
4
TURDEP – I‟ de kentsel bölgede yaşayanlarda DM oranı biraz daha yüksek iken, TURDEP- II‟ de kentsel ve kırsal kesimde yaşayanlar arasında anlamlı bir fark kalmadığı gözlenmektedir. Bilinen diyabet ve yeni diyabet oranları birbirine yakındır (% 45 ve % 55).
Diyabet sıklığı erkeklerde kadınlarda hafifçe daha düşük bulunmuş olup kadın ve erkekler arasında çok anlamlı bir fark görülmemiştir.
Bölgesel diyabet prevalansı Kuzey Anadolu‟ da % 14.5 ile en az, Doğu Anadolu‟ da ise % 18.2 ile en fazladır.
Diyabet farkındalığı Batı Anadolu‟ da en yüksek (Bilinen diyabetlilerin toplam diyabetlilere oranı % 61.6), Doğu Anadolu Bölgesi‟ nde ise en düşüktür (Bilinen/ toplam diyabet oranı % 47.2).
TURDEP- II çalışmasına göre 40- 44 yaş grubundan itibaren nüfusun en az % 10‟ u diyabetlidir (TURDEP- I‟ de ise % 10‟ un üzerindeki diyabet sıklığı 45- 49 yaş grubunda başlamaktaydı). Buna dayanarak Türkiye‟ de diyabetin 1998 yılına göre yaklaşık olarak 5 yaş daha erken başladığı düşünülebilir.
Kentsel ve kırsal arasında prediyabet açısından anlamlı bir fark kalmamıştır (30, 31).
Sonuç olarak 1998‟ de yapılan TURDEP- I‟ e göre, yeni tamamlanan TURDEP- II çalışmasında Türkiye‟de diyabet sıklığı 12 yılda % 90 artmıştır.
Yine Türkiye‟ de KBH hastalarına yönelik 2006‟ da yapılan ve toplam 5 yıllık dönemdeki değişim oranlarını gösteren CREDIT İnsidans çalışmasına göre, 2006‟ da % 12,7 olan diyabet sıklığı, 2011 yılında % 18,3‟ e yükselmiştir (32).
2.1.3 Sınıflandırma
Tip 1 DM (Beta hücre yıkımına bağlı, insülinin azlığı veya tamamen yokluğu)
Tip 2 DM (İnsülin rezistansı zemininde progresif insülin sekresyon azlığı)
Diğer durumlara bağlı spesifik DM tipleri (Monogenik DM- Neonatal DM/ MODY-, Ekzokrin pankreas hastalıkları, ilaç- kimyasal maddelere bağlı durumlar vb.)
Sekonder DM
5
2.1.4 EtyolojiPankreastan salgılanan endojen insülinin zamanla yetmezliğine bağlı olarak gelişen Tip 1 DM sıklıkla pankreas beta hücrelerinin idiyopatik otoimmün yıkımı ile gelişir. Hastalık ani başlangıçlıdır. İmmünolojik olarak beta hücrelerinin % 80‟ i harap olduktan sonra klinik tablo ani olarak oluşur. Polidipsi, poliüri, kilo kaybı yakınmaları veya ketoasidoz koması ilk bulgu olabilir.
Tip 1 DM poligenetik bir eğilim gösterir. Çeşitli ırklarda Tip 1 DM‟ ye yatkınlık sağlayan antijenin tipi değişiktir. Beyaz ırk için HLA B8, HLA B15, HLA DR3 ve HLA DR4, zenci ırk için HLA DR7, Japonlar için HLA DR9 diyabete yatkınlık sağlayan antijenlerdir. Genetik yatkınlığı olan çocukta genelde 5- 15 yaşları arasında tetiği çeken bir olaydan sonra hastalık hızla gelişmektedir. Tetik çeken olay viral enfeksiyonlar, özellikle kabakulak, konjenital rubella ve koksaki B, diyet, toksinler ve strestir. Büyük çoğunlukta ise otoimmun mekanizmayı başlatan faktörün ne olduğu bilinmemektedir. Bu hastalarda klinik yakınmaların başlaması ile beraber dolaşımda adacık hücrelerine karşı otoantikorlar (islet cell autoantibodies- ICA) yüksek oranda (% 65- 85) saptanır. Otoantikorların çoğu IgG tipindedir. ICA titresi zamanla düşen Tip 1 DM‟ li hastalarda ICA (-) olduğu için Tip 1 DM ile Tip 2 DM‟ nin erken yaşta başlayan formunun ayırıcı tanısında kullanılan otoantikorlar olan anti- GAD, ICA ve anti- IA2 (anti- insülin antikor), erken dönemde önemli bir laboratuar bulgusudur.
Yine bu hastalarda adacık hücrelerine karşı otoantikorlardan başka daha az sıklıkla insülin, proinsülin, glukagon, glutamik asit dekorbaksilaz (GAD), mikrobakteriyal ısı şoku proteini ve karboksipeptidaz H proteinlerine karşı da otoantikorlar saptanmıştır. Bu hastalarda humoral immuniteden başka hücresel immunitenin de uyarıldığı ve etyopatogenezde rol oynadığı bilinmektedir. Hastalığın başlangıcında pankreasın özellikle lenfositleri içeren mononükleer hücreler tarafından infiltrasyonu ile tanımlanan insülinitis görülür (34).
Tip 2 DM poligenik kalıtımlı, başlamasında sıklıkla obezite ve sedanter yaşama ilişkin veya obezite olmadan da varolan insülin rezistansı bulunan, β hücresinin bu rezistansı kompanse etmek için rölatif olarak fazla insülin salgıladığı ve hastalık ilerledikçe insülin salgılama fonksiyonunda olası bir genetik defekt nedeniyle zaten bozukluk olan β hücresinin insülin salgılama kapasitesinin daha da azalıp hipergliseminin artarak muhtemelen beta hücre apoptozunu tetiklemek suretiyle kısır bir döngü yarattığı durumdur (35). Bugün Tip 2 DM‟ de primer fizyopatolojinin insülin rezistansı ve bunun sonucunda gelişen β hücresinin yorgunluğu mu, yoksa β hücresinin insülin salgılama kapasitesini belli bir evreden sonra arttırmasını engelleyen genetik kökenli bir bozukluk mu olduğu konusunda tam bir fikir birliği yoktur. Fakat çevre faktörlerinin değiştirilmesi, fizik aktivitenin arttırılıp az da olsa kilo verilmesinin Tip 2 DM gelişimini engellediği, en azından daha ileri yaşlara ertelediği gösterilmiştir (36, 37).
Obezite, vücut kitle indeksinin (BMI= kg/ m²) 30‟ un üstünde olmasıdır. Özellikle bu düzeyde viseral yağ artışı, ciddi bir insülin rezistansına neden olur. İnsülin rezistansı, belli miktardaki glukozu kas, karaciğer, yağ dokusuna sokup metabolize etmek için toplum ortalamasının daha üstünde
6
insülinemi seviyelerine gereksinim duyulması halidir. Obezite ile insülin rezistansı J şeklinde bir korelasyon gösterir. Bununla birlikte toplumda nonobez şahısların bir bölümünde de insülin rezistansı mevcuttur.Viseral yağ dokusundan portal dolaşıma fazla miktarda esterifiye olmamış serbest yağ asidi (SYA) geçer. SYA' lar karaciğerde insülin rezistansına neden olurlar. Bunun dışında SYA' lar karaciğerde asetil koenzim A' ya metabolize olup piruvat yapımını arttırırlar. Piruvattan da glukoz üretilir. Keza çoğunlukla hepatosteatozu olan obezlerde yağ depolanmasının glukoneogenezi arttırdığı saptanmıştır (38, 39).
İnsülin glikojenolizi baskılayan bir hormon, glukagon ise stimüle eden bir hormondur. Tip 2 DM‟ de relatif bir hipoinsülinemi ve relatif bir hiperglukagonemi mevcuttur. Bütün bu olayların sonucunda karaciğer glukoz çıkışı diyabetiklerde artmıştır. Sabah açlık glisemisinin en önemli nedeni gece insülin ile baskılanamayan karaciğerden artmış glukoz çıkışıdır. Sabah açlık glisemisi ile geceki karaciğer glukoz çıkışı arasında direkt bir korelasyon mevcuttur.
Karaciğerde yüksek SYA düzeyleri ve azalmış insülin etkisi sonucunda VLDL üretimi artar. Hipertrigliseridemi HDL düzeyi düşüklüğüne neden olur. Tip 2 DM‟ ye eşlik eden tipik dislipidemi yüksek trigliserid düzeyleri ve azalmış HDL düzeyidir. LDL ise aterojen olan kolesteroldür. Hipertrigliseridemi bazı mekanizmalar ile klinikte rutin biyokimya yöntemleri ile ölçemediğimiz bu subfraksiyonlardan aterojen olan küçük yoğun LDL partikülleri lehine artış yapar. Rutin yöntemler ile ölçülen total LDL normal veya hafif yüksek olsa da genel olarak aterojenitesi artmıştır. Kas dokusunda fazla miktara ulaşan SYA' lar okside olup glukoz oksidayonunda görevli heksokinazı inhibe ederek glukoz metabolizmasını baskılarlar. Yine kas dokusunda depolanan trigliseridler ve SYA da kas dokusunda insülinin etkisini azaltır.
İnsülin dokuya geldiği zaman spesifik reseptörüne bağlanır. Reseptörün hücre içindeki parçası insülinin hücre içinde etkisini göstermesi için ilk basamak olan fosforilizasyon kaskadını başlatır. Bu fosforilizasyondan sonra insülin sinyalinin hücre içinde ulaşması gereken yerlere iletilmesinde belli bir düzeyde zayıflama hem obez hem de nonobez diyabetiklerde saptanmıştır. Bu durum diyabetiklerde insülin etkisinin postreseptör düzeyde bozukluk göstermesi olarak adlandırılır. Hala hücre içinde insülin sinyalinin tüm iletim mekanizmaları ve diyabette hangi düzeyde ne tür bir bozukluk olduğu tam olarak bilinmemektedir. İnsülinin kas hücresindeki en önemli görevi glukoz taşıyıcılarından biri olan ve iskelet kasında fazla miktarda bulunan GLUT- 4 (Glukoz transporter- 4) üzerinedir. GLUT- 4 hücre içinden hücre membranına transloke olur, ortamdaki glukozu alıp hücre içine sokar. Hücre içine yeterli sinyali gönderemeyen insülin gerekli miktarda GLUT- 4 translokasyonunu da sağlayamaz. Dolayısı ile kapillerlerdeki glukoz yeterli miktarda hücre içine giremez.
Kronik hiperglisemi genel olarak insülin rezistansını arttırır, β hücre fonksiyonlarını bozar. Hiperglisemi çeşitli yöntemler ile normal veya normale yakın glisemik düzeylere indirilirse hem β hücre fonksiyonlarında düzelme, hem de insülinin etkenliğinde artış olur (40).
7
Kronik hipergliseminin zaten normal hız ve kapasitede işlemeyen mekanizmaları daha fazla bozmasına glukoz toksisitesi adı verilmiştir. Artmış SYA konsantrasyonunda yukarıda glukoz toksitesi için bahsedilen kademeler ve yerlerde inhibisyon olur. Bu durum da lipotoksisite olarak adlandırılmıştır. Yani glisemik ayarı sağlanamamış Tip 2 DM‟ de hiperglisemi ve artmış sirkülan SYA' lar bir kısır döngü yaratıp metabolik bozukluğu arttırırlar (41).β hücresi normalde insülini bifazik olarak salgılar. Glukoz, aminoasit, SYA ve gastrointestinal hormonların uyarısı sonucunda önce β hücresi içinde granüllerde bulunan insülin salgılanır, takiben uyarı yeni insülin sentezi ve salgılanmasına neden olur. Birinci faz insülin sekresyonu 10 dakika kadar sürer. Tip 2 DM‟ de insülin salınımının ilk fazı bozulur. Postprandiyal hipergliseminin nedeni de yetersiz olan erken faz insülin sekresyonudur. Hastalık ilerledikçe ikinci faz salınımında da yetersizlikler gelişir, β hücresi disfonksiyonu için daha öncede bahsedilen genetik, glukotoksisite, lipotoksisite gibi nedenler dışında fetal ve süt çocukluğu dönemindeki malnütrisyonun da etkisi olduğu kabul edilmektedir. Erken fetal dönem malnütrisyonunun β hücre gelişimini engellediği ve/ veya β hücresinin normal miktarda gıda alımına vereceği cevabı sınırladığı düşünülmektedir (42).
Sonuç olarak insülin sekresyonu % 50‟ ye düşüp, insülin duyarlılığı % 70 azalınca Tip 2 DM ortaya çıkar.
Diyabetin nadir görülen bir tipi olan MODY (Maturity Onset of Diabetes of the Young = genç kişide erişkin tipi diyabet); subtipleri olan, otozomal dominant geçen, genç yaşlarda insülin sekresyonu defekti ile seyreden, fakat tedavisinde hemen hiç bir zaman insülin gereksinimi duyulmayan, sorumlu gen lokuslarının kesin olarak gösterildiği bir diyabet tipidir.
2.1.5 Tanı
Aşağıdaki kriterlerin en az 1‟ inin karşılanması DM tanısını koydurur;
En az 2 ölçümde AKŞ≥ 126 mg/ dl olması (En az 8 saat kalorili gıda alımı olmaksızın açlık olmalı)
75 gr. OGTT‟ de 2. saat KŞ≥ 200 mg/ dl olması
Klasik hiperglisemik semptomları olan bir kişide rastgele bakılan KŞ≥ 200 mg/ dl olması
HbA1c≥ % 6.5 olması (33).
2.1.6 Komplikasyonlar
Akut (Metabolik) Komplikasyonlar (Diyabetik Ketoasidoz, Hiperosmolar Non- Ketotik Koma, Laktik Asidoz, Hipoglisemi)
Kronik (Dejeneratif) Komplikasyonlar (Makrovasküler– Kardiyovasküler, Serebrovasküler, Periferik Damar Hastalıkları- , Mikrovasküler– Nefropati, Retinopati, Nöropati, Diyabetik ayak- )
8
2.1.6.1 Makrovasküler KomplikasyonlarDiyabetin makrovasküler komplikasyonları, Tip 2 DM için henüz aşikar diyabetin ortaya çıkmadığı IGT (bozulmuş glukoz toleransı) döneminde başlar. Bu dönemde mikrovasküler komplikasyonlar gelişmemekle birlikte koroner arter hastalığı (KAH) için önemli risk faktörleri olan hipertansiyon, yüksek trigliserid (TG) düzeyi, HDL kolesterol düzeyinin düşüklüğü sık görülmekte, bu nedenlerden dolayı makrovasküler komplikasyonlar gelişebilmektedir. Makrovasküler komplikasyonlar açısından kadın erkek farkı yoktur (34). Makrovasküler hastalık için tanımlanmış risk faktörleri; sigara kullanımı, HT, dislipidemi, hiperglisemi, metabolik sendrom, mikroalbuminüri, periferik aterosklerotik damar hastalığı, koroner aterosklerotik damar hastalığı, hiperkoagulabilite ve karotid aterosklerotik damar hastalığıdır. Makrovasküler komplikasyonun erken başlatıcısı endotel disfonksiyonudur (43).
2.1.6.1.1 Kardiyovasküler Hastalıklar
Diyabet, kardiyovasküler morbidite ve mortalite açısından önemli ve bağımsız bir risk faktörüdür. Tip 2 DM‟ de mortalite nedeni, başta KAH olmak üzere kardiyovasküler hastalıklardır. Diyabetik kadınlarda KAH riski yükselmekte, nondiyabetik erkeklere yaklaşmaktadır. Diyabetlilerde aynı zamanda trombosit adhezyon ve agregasyonu artmış, fibrinoliz aktivitesi azalmış ve kan viskozitesi artmıştır. Bütün bunlar ateromlu hastalarda intravasküler tromboza ortam yaratan faktörlerdir (44). Otonom nöropati gelişmiş diyabetiklerde asemptomatik koroner arter hastalığı olacağı ve sessiz infarktüs gelişebileceği bilinmelidir. Tip 2 DM; yaygın aterosklerotik damar hastalığına, inflamatuvar ortama ve trombogeneze yatkınlık oluşturması açısından bakıldığında gerçek bir vaskülopati durumudur.
Diyabetik bireylerde KAH ile serebrovasküler hastalık ve periferik arter hastalığı mevcudiyeti arasında güçlü bir ilişki vardır. Diyabetli bireylerde karotid aterosklerotik damar hastalığı olma olasılıkları daha yüksektir ve diyabet, inmenin tekrarlama olasılığını iki katına çıkarmaktadır. Diyabetik bireyler 2- 4 kat daha fazla periferik ateroosklerotik damar hastalığı riskine sahiptir ve kladikasyon riski erkeklerde 3.5 kat, kadınlarda ise 8.6 kat daha fazladır. Kadınların erkeklerde olduğundan daha fazla aterojen olma eğiliminde olan küçük- yoğun lipoprotein kolesterolüne sahip olma riskleri daha yüksek gibi göründüğünden, diyabetik kadınlardaki KAH riski belirgin olabilir. Bu nedenle, kadınlardaki risk faktörlerine karşı agresif bir biçimde mücadele verilmesi son derece önemlidir (45).
Bir çalışma 1069 diyabetli bireyi inceleyerek 3.5 yıllık bir dönemdeki KAH mortalitesi ile tüm olayların insidansını değerlendirmiştir. Hastalar HbA1c değerlerine göre üç gruba ayrılmış; en yüksek A1C değerine sahip üçte birlik gruptakiler, en düşük HbA1c değerlerine sahip üçte birlik gruptakilere göre daha yüksek KAH mortalitesine sahip olmuşlardır. Ölümcül ve ölümcül olmayan miyokard enfarktüsü insidansı diyabeti olmayanlarda % 3.4 iken, diyabeti olanlarda % 14.8' e kadar yükselmiştir. KAH açısından en yüksek üçte birlik grupta olanların HbA1c değerleri > % 7.9 olmuştur (46). Vasküler hastalıkların altında yatan genel anlamdaki ve koroner arter hastalıklarının altında
9
yatan özel anlamdaki dislipidemi, hipertansiyon, bozulmuş endotel fonksiyonu, sigara içme, yaşam biçimi, hiperinsülinemi, insülin direnci, oksidatif stres, obezite, hiperhomosisteinemi, lipoprotein (a) yükseklikleri ve damar inflamasyonu gibi çok sayıda risk faktörünün var olduğu göz önünde bulundurulduğunda bu sonuç anlaşılabilir. Birden fazla risk faktörünün varlığı kardiyovasküler riski katlamalı olarak arttırmaktadır.UKPDS çalışması; miyokard enfarktüsü için en önemli risk faktörünün LDL düzeyi olduğunu ve bunu diyastolik kan basıncı, sigara içme, düşük HDL düzeyleri ve yüksek HbA1c düzeylerinin izlediğini göstermiştir (47). Koagulopatilerle mücadele ederken kan basıncı, lipid ve glukoz kontrolüne en fazla öncelik verilmelidir.
Sigara içme diyabet hastalarında makrovasküler hastalık riskini iki katına çıkarmaktadır ve yine mikrovasküler komplikasyonların gelişme ve ağırlaşma olasılığını anlamlı bir biçimde artırmaktadır. Bunun nedeni, sigara içmenin endotel disfonksiyonunu ve aterosklerotik depolanmaları artırması ve diyabetin vasküler komplikasyonlarını arttıran ileri glikozillenme son ürünleri için bir kaynak olmasıdır. Sigara içme, LDL kolesterolün oksidasyonunu artırarak intimaya depolanmasını hızlandırmaktadır. Sigara içmeyle birlikte plak instabilitesi artmaktadır ve tüm MI' ların % 68' inin, % 50' nin altındaki KAH stenozuyla birlikte oluştuğu düşünüldüğünde bu durum özellikle önemlidir. Çoklu Risk Faktörü Girişimi Çalışması günlük sigara tüketimi arttıkça koroner hastalık mortalitesinin de arttığını göstermiştir. Sigara içen diyabetli bireylerde erken ölüm riski diyabeti olmayan ve sigara içmeyen bireylere göre 11 kat daha fazla bulunmuştur (48).
Diyabetli bireylerde, endotelde bulunan vasküler düz kaslardaki aterojenik değişiklikler, diyabetin seyri sırasında oluşan dislipidemiyle artmaktadır. İnsülinin lipoprotein lipaz üzerindeki etkisinin ve glukozun hücreler tarafından alımının azalması adipositler tarafından serbest yağ asidi, gliserol ve plazminojen aktivatör inhibitörü 1 (PAI- 1) üretimini artırır. Böylece pıhtının çözünmesini ve fıbrinolizi baskılayarak hemostatik dengeyi trombotik duruma doğru kaydırır. Yüksek PAI- 1 düzeyleri dislipidemi, hipertansiyon ve hiperinsülinemi ile de ilişkili olup; kardiyovasküler hastalık riskinde artışa işaret eder (49) . Kilo verme, lipid düşürücü tedavi, ACE inhibitörü tedavisi (plağı stabilize eder) ya da yükselmiş trigliserid düzeylerinin düşürülmesiyle dolaşımdaki PAI- 1 düzeyleri düşürülebilmekte ve böylece hiperkoagülabilite azaltılabilmektedir (50, 51).
Ayrıca, adipoz doku düzeyindeki insülin direnci, karaciğerin aşırı miktarda VLDL üretmesine neden olur. Hepatik lipaz ile HDL‟ nin fazla yıkımı, hipertrigliseridemi ve küçük- yoğun LDL partiküllerinin baskın olmasıyla ilişkilidir. Grundy tarafından yayınlanan Framingham çalışmasının sonuçları, diyabeti olan bireylerde diyabeti olmayanlara göre daha fazla oranda lipid anormalliği bulunduğunu göstermiştir. Bu anormalliklerin en yaygın olanları diyabetli bireylerde % 34, diyabetik olmayanlarda ise % 25 oranında görülen ≥ 40 mg/ dl' lik VLDL yükseklikleri; diyabetli bireylerde % 19, diyabetik olmayanlarda ise % 9 oranında görülen ≥ 325 mg/ dl' lik trigliserid düzeyleri ve diyabetli bireylerde diyabetik olmayanlara göre % 21 oranında daha fazla görülen < 31 mg/ dl' lik HDL düzeyleri olmuştur (52).
10
Diyabeti olmayan kadınların sadece % 8' i hipertrigliseridemiye sahipken bu oran diyabetli kadınlarda % 17 olmuştur, diyabeti olmayan kadınların % 10' u ≤ 41 mg/ dl' lik HDL düzeylerine sahipken bu oran diyabetli bireylerde % 25 olmuştur. Diyabetli kadınlarda, Framingham Kalp Çalışması‟ nda yer alan diyabeti olmayan kadınlarla karşılaştırıldığında ≥ 35 mg/ dl düzeyinde VLDL‟ ye sahip olma olasılığı daha yüksek bulunmuştur (53).Hiperinsülinemi, hipertrigliseridemi ve düşük HDL kolesterolü arasında bir ilişki olduğu ilk kez 1994 yılında tanımlanmıştır. 64 olguyu içeren bir çalışmada, hiperinsülinemik olan hastalarda HDL kolesterol düzeyleri; insülin düzeyleri normal olan hastalara göre ağırlık, yaş, cinsiyet, fizik aktivite ve sigara içmeden bağımsız olarak anlamlı derecede daha düşük bulunmuştur. Toplam 1059 (581 erkek, 478 kadın) hastayı içeren geniş kapsamlı bir prospektif çalışma, HDL konsantrasyonlarının KAH olayları ve mortalitesi ile anlamlı ve ters bir biçimde ilişkili olduğunu göstermiştir. 45- 64 yaş arası hastaların 7 yıl boyunca izlendiği bu çalışma, toplam kolesterol arttıkça KAH olaylarının ve mortalitesinin de arttığını göstermiştir. Tersine, HDL düzeyleri azaldıkça KAH olayları ve mortalitesi artmıştır (54).
Hiperhomosisteinemi, özellikle diyabeti olmayan homosisteinemik hastalara göre riskin yaklaşık olarak iki kat artmış olduğu diyabet hastalarında başta olmak üzere, bağımsız bir kardiyovasküler risk faktörüdür. Ancak homosistein düzeylerinin düşürülmesinin yararı tartışmalı olup, bazı çalışmalar yarar ortaya koyarken diğerleri böyle bir yarar gösterememişlerdir. Hiperhomosisteineminin doku hipoksisi, lokal doku perfüzyonunda bozukluklar, artmış SYA, sistemik hipertansiyon, dislipidemi ve hiperglisemi gibi konakçı faktörlerden bir tanesi olduğu ve hasar oluşturucu serbest radikallerin üretimi ile endoteldeki vazodilatörlerle vazokonstriktörler arasındaki dengesizliği artıran oksidatif stresi güçlendirdiği açıktır. Endotel fonksiyonunda oluşan anormallik ACE' yi ve anjiyotensin II‟ yi artırmak suretiyle inflamatuvar mediatörleri arttırarak nitrik oksit üretimini azaltır. Proteolizin hızlanması plağın sağlamlığını azaltır ve yırtılmasını kolaylaştırırken, akabinde oluşan vazokonstriksiyon endotel fonksiyonunu bozar. Homosisteinemik hastalarda artmış PAI- 1 trombozu ve kardiyak yeniden yapılanma; vasküler ve hatta renal hipertrofi, endotel hasarı ve artmış CRP ile karakterize olan inflamasyonun hızlanmasından sorumlu olan ve anjiyotensin II tarafından oluşturulan büyüme faktörlerinin üretimini artırır (55).
2.1.6.1.2 Serebrovasküler Hastalıklar
Diyabetli bireylerde serebrovasküler hastalıklar normal popülasyona göre daha sık gözlenir, daha ağır seyreder ve daha yaygın lezyonlar oluşturur. Diyabette trombosit agregasyonu artmıştır. Diyabetiklerde fibrinojenin yarı ömrünün kısalmış olmasına rağmen fibrinojen düzeyinin yüksek oluşu, karaciğerde fibrinojen üretiminin artışı ile açıklanabilir. Yüksek fibrinojen düzeyleri, plazma viskozitesini yükseltip eritrositlerin agregasyonunu arttırarak trombozu arttırabilir, mikrosirkülasyonu güçleştirebilir. Bazen diyabetik bireyin geçici iskemik atakları, diyabetik hipoglisemi semptomlarıyla karışabilir. İyi metabolik kontrol ve risk faktörlerinin ortadan kaldırılması gerekmektedir. Tedavide antiagregan ajanlardan faydalanılabilir (25).
11
2.1.6.1.3 Periferik Damar HastalığıTip 2 DM hastaları aterojenik dislipidemiye ve metabolik sendroma daha yatkın olup periferik arter hastalığı riski 4 kat artmıştır ve diyabetli bireylerdeki semptomlar glisemik kontrolle doğrudan ilişkili değildir.
Ateroskleroz normalde erkeklerde kadınlara oranla daha sık ve ilerleyicidir. Diyabetiklerde ise her iki cinste de aynı sıklıkta görülür. Orta ve büyük arterleri tutan ateroskleroz yanında diyabetik bireylerde ikinci bir arter hastalığı daha görülür ki bu hastalık diyabete hastır, orta ve küçük arterleri tutar, endotel hücrelerinde proliferasyonla seyreden tıkayıcı bir arterittir. Küçük arterleri tuttuğu için lokal gangrenlere yol açabilir. Tip 2 diyabette makroanjiopati lezyonları daha çok distal arterlerde görülür. Bacaklardaki gangren insidansı diyabetiklerde, aynı yaştaki kontrol grubundan 30 kat daha fazladır (25).
Diyabetin neden olduğu veya hızlandırdığı periferik arter hastalığının klinikte en sık karşımıza çıkan şekli diyabetik ayaktır. Ortopedi kliniklerindeki non- travmatik alt ekstremite ampütasyonlarının % 50‟ sinin nedeni diyabetik ayaktır (56).
Periferik arter hastalığı; embolizm ya da arter tıkanıklığı sonucunda oluşan parestezi, paralizi, vücut ısısında bozulma, ağrı ve soluklukla seyreden akut ciddi iskemi ile kendini gösteren akut damar sorunları gibi çeşitli damar komplikasyonlarıyla bir arada olabilmektedir. Klinik bulgular arasında impotans ve intestinal anjina da olabilir. Periferik arter hastalığının yaygın görüldüğü bölgeler kalça, uyluk ve gluteal bölgede iskemi oluşturan aortoiliyak arter tıkanıklığı; uyluk ve bacakta iskemi oluşturan femoral arter ya da dallarının tıkanıklığı ve ayak, ayak bileği ve bacakta kendini gösteren popliteal arter tıkanıklıklarıdır (57).
Periferik damar hastalığı için değiştirilebilir risk faktörleri; dislipidemi, diyabet, HT, obezite, sigara içme ve artmış homosistein düzeyleridir.
Hiatt tarafından 2001 yılında yayınlanan verilere göre, periferik arter hastalığına sahip hastaların yaklaşık olarak yarısı kladikasyona ait semptomlara sahiptir. Hastanın yaşı ilerledikçe bu hastalığa bağlı semptomlara sahip olma olasılığı artmakta olup, 70 yaşın üzerindeki hastalarda semptomların görülme oranı en yüksektir (58). Kladikasyonu olan hastaların % 1- 3' ü 5 yıllık süre içerisinde ampütasyona gereksinim duyabilmektedir. Kladikasyon yakınması olan hastaların 5 yıllık mortalitesi % 30' lara yaklaşmaktadır. Kladikasyona karşı ayrıntılı bir tedavi yaklaşımı şarttır ve bu yaklaşım semptomları iyileştirebilmektedir. Bu ayrıntılı yaklaşım; lipid profilini, glisemik kontrolü, kan basıncı kontrolünü, kilo vermeyi ve ilaçları içermektedir.
Periferik damar hastalığına halen olduğundan daha az tanı konmakta, diğer bir ifadeyle bu tanı atlanmaya devam etmektedir. Ayrıntılı bir derlemede, ya 70 yaşın üzerinde, ya da 50- 69 yaşları arasında olup da sigara içme veya diyabet öyküsü olan 6979 hasta değerlendirilmiştir. Periferik arter hastalığı tanısı almış olan hastaların yalnızca % 79' u kendilerini tedavi eden hekim tarafından ortaya çıkarılabilmiş olup bu çalışmada periferik arter hastalığı tanısı konan hastaların % 45' ine daha önceden tanı konamamıştır (59).
12
Periferik damar hastalığının tanısında önemli olan bir nokta, alt ekstremitelerde arteriyel doppler ve ankle/ brakiyal (ayak bileği/ önkol) indeks (ABI) ile aterosklerotik depolanmaların gösterilmesidir. ABI, dorsalis pedis ile posteriyor tibial arterlerde ölçülen sistolik basınçların brakiyal arterden alınan sistolik basınçla karşılaştırılmasıdır. Kanada' da Anjiyoplasti ve Stent Yerleştirme Girişimleri (TASC) çalışma grubuna göre; ABI, periferik arter hastalığı tanısı için % 95 oranında duyarlı ve % 99 oranında özgündür (60). ABI oranının ≥ 0.9 olması normal olup 0.89- 0.75 arası hafif periferal damar hastalığını, 0.75- 0.50 arası orta dereceli bir damar hastalığını ve < 0.50 olması ise ağır hastalığı düşündürmektedir (61). Ayrıca semptomatik periferik damar hastalığı olan hastaların % 90' ının aynı zamanda KAH‟ a da sahip olabileceğinin bilinmesi gerekir (62).Sigara içme periferik hastalık için en güçlü değiştirilebilir risk faktörüdür; kladikasyon, sigara içenlerde içmeyenlere göre 3 kat daha yaygındır. Hastalığın ciddiyeti içilen sigara sayısına bağlı olarak artmaktadır. Sigarayı bırakmanın istirahatte ağrı, MI, kalple ilişkili ölümler ve genel anlamdaki 10 yıllık sağkalım oranlarında anlamlı azalmalarla ilişkili olduğu bildirilmiştir (63). Diyabet ve sigara içme, aterosklerotik damar hastalığı riskini % 25- 50 oranında artırmaktadır ve önemli başvuru semptomlarını sıklıkla maskelemektedir. Periferik damar hastalığının tedavi yaklaşımında katkıda bulunan risk faktörlerinin dikkatli bir biçimde kontrolü son derece önemlidir (64).
2.1.6.2. Mikrovasküler Komplikasyonlar
Diyabetin süresi arttıkça, özellikle de genetik yatkınlığı olan bireylerde; kapiller bazal membran kalınlaşması, kapiller permeabilite artışı, kan akımı ve viskozitesinde artış ve trombosit fonksiyonlarında bozulma gözlenir. Bu değişimlerin sonucu olarak kapiller protein sızıntısı (mikroalbuminüri), mikrotrombüs oluşumu ve dokularda iskemik hasar gelişebilir. Kronik hiperglisemi ve artan ileri glikozillenme son ürünleri, bu tip lezyonların oluşmasında önemli rol oynar. Mikrovasküler komplikasyonlar diyabetik nöropati, nefropati ve retinopatidir (65).
2.1.6.2.1 Diyabetik Nefropati
Diyabetik nefropati diyabetli bireylerde önemli bir mortalite nedenidir. Gelişmiş ülkelerde renal replasman ünitelerinde tedavi gören son dönem böbrek yetersizliği hastalarının 1/ 3‟ ünü diyabetikler oluşturur. Bu gelişmiş ülkelerdeki son dönem böbrek yetersizliğinin en sık nedeninin diyabetik nefropati olduğu anlamına gelir (66).
Diyabetik böbrekte ilk etapta diffüz, daha sonra da eksüdatif lezyon gelişir. Arteriollerde hyalinizasyon olur. Efferent arteriolde oluşan hyalinizasyon diyabete özgü histopatolojik lezyondur. Diffüz nodüler interkapiller glomerüloskleroz (Kimmelstiel- Wilson sendromu) dışında renal papilla nekrozu, kronik piyelonefrit, aterosklerotik renal arter darlığı, toksik nefropati gibi nedenlere bağlı olarak da diyabetik süreçte renal tutulum görülebilir.
13
Evre- 1‟ de glomerüler hiperfiltrasyon (ılımlı GFR artışı) ve böbreklerde hipertrofi mevcut olup, patolojik olarak glomerüler bazal membranda hafif kalınlaşma dışında önemli bir morfolojik değişiklik yoktur (67). Evre- 2‟ de GFR normal aralığa iner, patolojik olarak glomerüler bazal membranda kalınlaşma ve mezangiumda sınırlı ekspansiyondan ibaret morfolojik değişiklikler izlenir. Çoğu hasta iyi glisemik kontrolle bu evreden 3. evreye geçmez, nefropati gelişimi halen geri döndürülebilir (68).
Evre- 3‟ te GFR normaldir. Üriner albumin ekskresyonu mikroalbuminürik düzeyde, yani 30- 300 mg/ 24 saat arasındadır. Bu dönemde birçok hastada hipertansiyon sınırına varmayan progresif kan basıncı artışı gözlenir. İyi glisemik kontrol, protein kısıtlaması ve ACE inhibitörleri ile mikroalbuminüri azaltılarak klinik nefropatiye gidiş süresi geciktirilebilir (25, 67- 69).
Evre- 4‟ te proteinüri > 0,5 gr/ gün ile karakterizedir. Sıklıkla hipertansiyon da vardır. HT sıkı kontrol edilmezse renal fonksiyon kaybı hızlanır. GFR‟ nin düşme hızı, ayda 1 ml/ dk‟ dır. Böbrekte morfolojik olarak glomerüllerde skleroz da izlenmeye başlanır (25, 67, 68).
Evre- 5‟ te üremi gelişmesi ile birlikte sıvı retansiyonu gibi komplikasyonlar görülmeye başlar. Hemen hepsinde büyük damar kalsifikasyonları (Mönckeberg sklerozu) gelişir. GFR 15- 20 ml/ dk‟ nın altına indiğinde renal replasman programına alınmalıdır.
Arteriyal hipertansiyon ve böbrek yetersizliği olsun veya olmasın proteinüri varlığı en az beş yıldır diyabeti olan hastada, başka bir nedene bağlı değilse, diyabetik nefropati olarak değerlendirilir (25, 68).
2.1.6.2.2 Diyabetik Retinopati
Diyabetik retinopati, gelişmiş ülkelerde halen 20- 74 yaş arasında önde gelen körlük nedenlerindendir. Tipik mikroanjiopatik lezyonlar retinopatiyi oluşturur. Diyabetin süresi arttıkça retinopati sıklığı ve derecesi artar. Diyabetik retinopatide kapiller permabilite artışı, kan viskozitesinde artış ve trombosit agregasyonu artışı büyük önem taşır. Bunların sonucunda retinada mikrooklüzyonlar ve iskemik alanlar gelişir. Diyabetik bireylerde retinopati dışında vitröz kanama, rubeozis iridis, glokom, juvenil katarakt ve oküler kas felcine (3.- 4.- 6. kafa çiftlerinin felci) bağlı olarak da göz tutulumu olabilir. Permeabilite artışına bağlı olarak da eksuda, hemoraji ve retina ödemi izlenir (70, 71).
2.1.6.2.3 Diyabetik Nöropati
Diyabetik nöropati terimi; diğer periferik nöropati nedenleri dışında DM seyrinde klinik veya subklinik düzeyde ortaya çıkabilen, periferik, somatik ya da otonom sinir tutulumlarını ifade eder. Bulgular hem periferik hem de otonom sinir sistemi ile ilgili olarak ortaya çıkar.
Nöropati diyabetin en sık rastlanan komplikasyonları arasındadır. Diyabet tanısı konduğunda hastaların % 10‟ unda nöropati bulunurken; diyabet yaşının artmasıyla, örneğin 20 yılın sonunda, bu
14
oran % 50 olmaktadır. Bir başka deyişle diyabetik nöropati, diyabet yaşı ile birlikte görülme sıklığı artan bir komplikasyondur. Tip 2 DM tanısı konduktan sonra 9 yıl içinde nöropati başladığını gösteren güçlü deliller vardır. Bir başka çalışmada; DM‟ de nöropati prevelansı % 5 ile % 60 arasında bildirilmiştir (72). Nöropati bulgu ve semptomları olmaksızın sinir ileti anormalikleri katıldığında bu oran % 100‟ e çıkmaktadır (73). Yıllık insidans, diyabetin bilinen süresi ile ilgilidir ve plato yapmaya eğilim göstermez. Semptomatik yaşam kalitesini bozan nöropati diyabetik bireylerin % 50‟ sinde mevcutur. DM, tüm dünyada ve gelişmiş ülkelerde nöropatinin en sık nedeni olup, iyileşmeyen cilt ülserasyonlarının ve ekstremite ampütasyonlarının da en önemli nedenidir.Genellikle nöropatiler simetrik olmasına rağmen fokal de olabilir ve beraberinde otonom sinir sistemini de etkileyebilir. En sık görülen nöropati formu distal duyusal ve otonomik polinöropatidir. Mononöropatilerden ise en sık olarak karpal tünel sendromu (KTS) görülür (73). Tip 1 ve Tip 2 DM‟ de simetrik nöropatinin prevalansı benzerken, fokal sendromlar daha yaşlı diyabetiklerde daha sık görülür. Semptomatik polinöropati prevelansı Tip 1 DM‟ de % 15, Tip 2 DM‟ de % 13 olarak bulunmuştur (74). Diyabette görülen periferik nöropatiler özellikle alt ekstremitede simetrik yerleşim gösterir (75).
Cinsiyet, bölge, ırk farklılığı göstermekle beraber; bazı hastalarda kötü kontrole karşın daha geç görülmesi ya da görülmemesi, genetik katkıya yatkınlık telkin etmektedir (76). 18 ve üstü yaş grubunda; diyabet süresi, glikozillenmiş HbA1c, sigara içme ve HDL kolestrolün düşüklüğünün nöropati ile birlikteliği saptanmış ve bu 30 yaş ve üstünde daha fazla oranda bulunmuştur. Boy uzunluğu, maksimal vücut kitle indeksi, etanol kullanımı, sigara içme, sistolik ve diastolik kan basıncı, östradiol ve kolestrol düzeyleri nöropatili olan ve olmayanlarda farklı bulunmamıştır. Açlık plazma glukoz düzeyi nöropatiyi belirleyen en önemli faktördür (73).
Diyabetik nöropati patogenezinde öncelikle metabolik ve vasküler faktörler olmak üzere, genetik, immünite ve nörotropizm gibi birçok faktör rol oynamaktadır.
Vasküler Hipotezler: Yapılan çalışmalarda; kapiller endotel hücrelerinin şişmesi, damar duvarının kalınlaşması ve kapiller lümenin fibrin veya agregasyona uğramış plataletlerle oklüzyonu gösterilmiştir (77, 78). Hidrojen klirens metodu ile periferik kan akımının diyabet oluşturulan farelerde ilk birkaç günde % 80 kadar azaldığı, daha uzun sürede ise % 40 kadar azaldığı görülmüştür (79). Diyabetiklerde, fokal nöropatinin klinik bulgularının ani başlangıcı vasküler nedeni destekler. Nitrik oksit yapımında azalma, eikozanoid yapımında anormallikler ve oksidatif yolakta artış; endonöral mikrovaskülarizasyonda vazokontriksiyona ve sinir hipoksisine neden olur (79).
Metabolik Hipotezler: Hiperglisemi sinirleri birkaç yoldan etkileyebilir. Son zamanlara kadar dikkatler polyol yolu üzerindeydi, fakat bu hipotezle ilgili hayvan deneylerindeki veriler insanlara tamamı ile uygulanamamaktadır. Bununla birlikte metabolitlerin polyol yoluna artmış akışı, indirekt yol ile sinir hasarını etkileyebilir. Hipergliseminin bir sonucu da proteinlerin nonenzimatik glikozilasyonudur. Hiperglisemi periferik sinirlerde artmış glukoz konsantrasyonlarına neden olur ve sonra aldoz redüktazın aktivitesinin artması ile sorbitol ve fruktozun konsantrasyonları yükselir. Diyabetik hayvanların periferik sinirlerindeki sorbitol ve fruktozun yükselmesi ile myoinozitolun
15
konsantrasyonu azalır ve anormal fosfoinozitoller ortaya çıkar. Membran Na- K- ATPaz aktivitesi azalır (80). Ancak insanlarda periferik sinirde sorbitol birikimi ile myoinositolde azalma gösterilememişir (80).Diyabette diğer bir bozukluk karnitin azalmasıdır. Karnitin, yağlı açil koenzim- A derivelerinin oksidasyon için mitokondriye taşınmasında rol oynar, karnitin yetmezliği ATP üretimini bozar. Diyabetik farelere karnitin verilmesi sinir fonksiyonlarını değişik oranlarda düzeltmiştir (80).
Hiperglisemi, sinir gibi insülinden bağımsız dokularda, intraselüler proteinlerin glikozilasyonunu artırır. Nöronda glikozilasyondan en fazla etkilenen proteinler, aksonal transport için gerekli olan mikrotübüllerin tübülinleridir. Tübülinlerin glikozilasyonu, diyabetik sinirde aksonal transportun yavaşlamasına neden olur. Nonenzimatik glikozilasyon inhibitörü olan aminoguanidinin deney hayvanlarında endonöral kan damarlarının ve sinir liflerinin fonksiyonunu iyileştirdiği, sinir ileti değerlerini düzelttiği gösterilmiştir (79).
Ġmmünolojik Mekanizmalar: Diyabetik otonomik ve lumbosakral radikülopleksonöropatide immünolojik faktörler ön plandadır (72). İnsüline bağımlı diyabetik bireylerde, sempatik gangliyona karşı otoantikorlar gelişmektedir. Diyabetik bireylerin sural sinir biopsisinde endonöral veya epinöral lenfositik infiltrasyon gösterilmiştir.
Nörotrofik Faktörler: Büyüme faktörlerinin (GF) ikinci ailesi olan IGF‟ nin insüline benzer metabolik aktivitesi vardır (IGF- 1 ve IGF- 2). IGF- 1 ve IGF- 2 ile yapılan, in vitro ve nöropatili hayvan modellerindeki çalışmalar, bu faktörlerin sinir dejenerasyonunu etkilediğini göstermektedir. Nörotrofik faktörlerle nöropatilerin önlenmesi tedavisini amaçlayan preklinik araştırmalar olumlu sonuçlar vermekle birlikte, bu güne kadar yapılan klinik çalışmalarda birbiri ile uyumsuz sonuçlar elde edilmiştir (81).
Diğer Faktörler: Kardiyovasküler otonom nöropati ile HLADR3 ve DR4 haplotipleri arasında birliktelik vardır. Epidemiyolojik çalışmalar, sigaranın diyabetik nöropatiyi kolaylaştırdığını düşündürmektedir (73).
Ekstremite distalindeki ilerleyici duyu kaybına bağlı hastanın hissedemediği mekanik, termal ve kimyasal tekrarlayıcı travmalar ile otonom disfonksiyon sonucu terlemeyen ayakta oluşan fissür ve çatlaklar bakteriler için giriş yolu oluşturur. Tekrarlayan travmalar basınç noktalarında oluşan nasırların lokal basıncı % 30 oranında artırmasına bağlı bası nekrozlarının gelişmesine neden olması, ayağa uygun olmayan ayakkabılar giyildiğinde hastaların ayakkabının ayağını sıktığını hissetmemesi gibi faktörler diyabetik nöropatisi olan hastadaki diyabetik ayak yarası gelişiminde rol oynayan faktörlerdir.
Ağrı, ısı duyusunun kaybına ve otonom nöropatiye bağlı olarak ortaya çıkabilen ülserasyonlar; ayak baş parmaklarında, topuk veya malleollerde olabilir. Nöropatik ülserli ayak normal renkte ve sıcaktır, nabızları kolayca palpe edilebilir. İskemik ayakta ise ayak soğuk, ayak rengi soluk veya siyanotik olup nabızlar palpe edilemez. Lokal arteriovenöz şantın sonucu ayağa giden kan akımının arttığı gösterilmiştir. Periferik nöropati iskemik ağrıyı maskeleyebilir (72).
16
Diyabetik nöropatinin tanımından beri çeşitli sınıflandırmalar öne sürülmüştür. En kabul gören ve pratik sınıflandırma Thomas tarafından ileri sürülen, nöropatilerin; simetrik polinöropati, fokal ve multipl fokal nöropatiler olarak ayrılmasıdır (82). Kronik Progresif Distal Simetrik Polinöropati: Distal duysal ve sensorimotor polinöropati, diyabetik olgularda en sık ortaya çıkan sinsi başlangıçlı nöropati formudur. En erken duyu etkilenmesi ayak baş parmağında ortaya çıkar ve yukarı ilerler. Üst ekstremiteler daha nadir etkilenir. Daha ciddi olgularda duysal kayıp gövdeye yayılır. Sırtın korunduğu saptanmazsa myelopati ile karışabilir. Semptomu olmayan hastalarda bile aşil refleksi kaybı ve vibrasyon duyusunda azalma vardır. Geniş lif ve küçük lif tutulumu olabilirse de sıklıkla bu iki form birlikte olur.
a) Miks sensori- otonomik motor polinöropati: Diyabette en sık görülen nöropatidir. Genellikle simetrik tutulum vardır. Böylece klasik “eldiven- çorap” tarzı duysal azalma veya kayıp meydana gelir. Reflekslerde zaman içinde kaybolma gelişirken, ilk kaybolan refleks aşil refleksidir. Daha sonra ayak intrinsik kaslarında zayıflık ve atrofi gelişir. Bununla birlikte hasta ayakta durabilme ve yürüyebilme yetisini kaybetmez (75).
b) Miks polinöropati varyantları
Otonomik Polinöropati: Duysal nöropatinin otonomik anormalliklerle birlikte olması nadir değildir, fakat semptomatik otonom nöropati nadirdir. Somatik sinir içindeki otonomik lifler, organlara giden liflerden daha kolay tutulur. Otonom nöropati semptomu olmayan hastalarda kardiovasküler reflekslerde anormallikler saptanabilir ve bu durum, diyabet tanısından çok kısa bir süre sonra gözlenebilir. Bu klinik tablo subklinik otonom nöropati olarak tanımlanır.
Otonom nöropati diyabetin ilk yılında % 4, beşinci yılında % 20- 30 olup, ortalama % 30- 40 sıklıktadır (83). C lifleri nörojenik inflamasyonun başlangıcında etkilenebilir, bunun neticesinde travmaya cevap olarak oluşan nörojenik inflamasyon miktarı azalır. Terleme kaybına bağlı olarak kuru ayak oluşur, böylece ayakta fissür ve çatlaklar gelişebilir. Normal sempatik tonüsün kaybı periferal kan akımını artırır ve arteriovenöz şantların oluşmasına neden olur. Tonüsün kaybolmasıyla şantlar açılır ve kan akımı kapiller yatağa (by- pass) uğramadan geçer. Böylece arteriovenöz şantlar cilt kan akımının azalmasına yol açar (75). Tüm bunlar diyabetik ayak lezyonlarının orijinini oluşturabilir (72).
Hipogliseminin farkına varılamaması, ani açıklanamayan kardiorespiratuar arrestler ve mesane atonisine sekonder renal infeksiyonlar; diyabette yüksek mortalite nedenleridir (84).
Küçük (İnce) Lif Tipi (Ağrılı) Duysal Polinöropati: Sıklıkla derin ağrı, yanma, batma, burkulma, acı duyusu, spontan şimşekvari ağrı ve ağrı duyarlılığında artış (allodini) ile birliktedir. Ağrı özellikle akşamları şiddetlenir (75). Bu nöropatide; otonom dokulara karşı otoantikorlar ve aktive T lenfositlerin varlığı ile olguların 1/ 3‟ ünde iritis saptanması, etyolojide otoimmuniteyi düşündürmektedir (72, 84).