RADYASYON ONKOLOJİSİ
ANABİLİM DALI
AKCİĞER KANSERLİ HASTALARDA
RADYOTERAPİNİN SEBEP OLDUĞU AKUT
ÖZEFAJİTİN ÖNLENMESİNDE ORAL
GLUTAMİNİN ETKİNLİĞİ
UZMANLIK TEZİ
Dr. Öznur DÖNMEZ TUTANÇ
TEZ DANIŞMANI
Yrd. Doç. Dr. S. Burhanedtin ZİNCİRCİOĞLU
DİYARBAKIR-2010
TEŞEKKÜR
Tıpta uzmanlık eğitimim süresince üzerimde büyük emekleri olan, bilgi ve tecrübelerinden faydalandığım, derin hoşgörü anlayışı ile kendileriyle çalışmaktan kıvanç duyduğum değerli hocam Sayın Yrd. Doç. Dr. S. Burhanedtin ZİNCİRCİOĞLU’na, her zaman desteklerini hissettiğim değerli hocam Sayın Prof. Dr. Abdurrahman IŞIKDOĞAN’a teşekkür eder, saygılarımı sunarım.
Eğitimim sürecinde kısa bir süre çalışma olanağı bulsam da yardımlarını hiç bir zaman esirgemeyen Yrd. Doç. Dr. Ahmet DİRİER’e teşekkür ederim.
Tezimin hazırlanma aşamasında emekleri olan Yrd. Doç. Dr. Mehmet Ali KAPLAN’a, Dr. Müslüm GÜNEŞ’e, Dr. Ali ÜZEL’e ve birlikte çalışmaktan her zaman zevk duyduğum doktor, hemşire, fizik mühendisi, teknisyen ve tüm radyasyon onkolojisi kliniği çalışanlarına, tezimin istatistiksel açıdan değerlendirilmesi aşamasında büyük katkıları olan Sayın Prof. Dr. Melikşah ERTEM’e teşekkür ederim. Ayrıca bu günlere gelmemde büyük pay sahibi olan, maddi ve manevi desteklerini her an yanımda hissettiğim aileme teşekkür ederim.
İÇİNDEKİLER
Sayfa Teşekkür……….…...I İçindekiler……….………. II
Kısaltmalar Dizini……….………... III Tablolar Dizini.…...………... IV Şekiller Dizini……….………... V 1.Giriş ve Amaç ………..1 2.Genel Bilgiler ………..………...……...3 2.1. Anatomi………..3 2.2. Epidemiyoloji……….5 2.3. Etiyoloji………..5 2.4. Patoloji…………..……….6 2.5. Klinik ………..………...9 2.6. Tanısal Çalışmalar……….………14 2.7. Evreleme ………….………...16 2.8. Tedavi………...19
2.9. Konvansiyonel Radyoterapi Teknikleri...…..………..………..…………22
2.10. Radyoterapinin Etkileri ve Akut Özefajit………..……..25
2.11. Glutamin………..27 3. Materyal ve Metod………..29 4. Bulgular ………..33 5. Tartışma ………..………...43 6. Sonuç ………...48 7. Özet ………49 8.Summary ……….51 9.Kaynaklar………...53
KISALTMALAR DİZİNİ
KHDAK……: Küçük Hücreli Dışı Akciğer Kanseri KHAK……...: Küçük Hücreli Akciğer Kanseri AJCC……….: American Joint Committee on Cancer TNM………...: Tümör, Nod, Metastaz
KOAH………: Kronik Obstrüktif Akciğer Hastalığı PET………….: Pozitron Emisyon Tomografisi FDG…………: Flurodeoksiglukoz
BT………: Bilgisayarlı Tomografi RT…………...: Radyoterapi
KT…………..: Kemoterapi KRT………...: Kemoradyoterapi
VCSS………..: Venacava Süperior Sendromu SSS…………..: Santral Sinir Sistemi
EGFR……….: Endothelial Growth Factor Reseptor VEGF………..: Vascular Endothelial Growth Factor WHO…………: World Health Organization
RTOG………..: Radiation Therapy Oncology Group VALG………..: Veterans Administration Lung Cancer Gy………: Gray
DNA………….: Deoksiribo Nükleik Asit ADH…………..: Antidiüretik Hormon ALT…………..: Alanin Aminotransferaz AST…………...: Aspartat Aminotransferaz LDH…………..: Laktat Dehidrogenaz ALP…………...: Alkalen Fosfataz
GGT…………..: Gama Glutamin Transferaz ACTH………....: Adrenokortikotropik Hormon VATS………….: Video Assisted Thoracic Surgery AP/PA…………: Anterior Posterior/ Posterior Anterior LAP………: Lenfadenopati
TABLOLAR DİZİNİ
Tablo 1: Akciğer kanserinin etiyolojisi
Tablo 2: Akciğer kanserinde başvuruda saptanan semptom ve bulguların sıklığı sebepleri
Tablo 3: Akciğer tümörlerinin WHO patolojik sınıflaması
Tablo 4: Akciğer kanserinde metastatik hastalığı düşündüren klinik bulgular Tablo 5: Akciğer kanserinde TNM evrelemesi
Tablo 6: TNM evre gruplaması
Tablo 7: KHAK evrelemesinde VALG’ın önerdiği ikili sistem evrelemesi Tablo 8: RTOG akut özefajit toksisite kriterleri
Tablo 9: Hasta ve tümör özellikleri
Tablo 10:Her iki gruptaki hastaların yaşa göre dağılımı
Tablo 11: Her iki gruptaki hastaların cinsiyete göre dağılımı
Tablo 12:Her iki gruptaki hastaların histopatolojik tanılarına göre dağılımı
Tablo 13: Her iki gruptaki hastaların evrelere göre dağılımı
Tablo 14: Her iki gruptaki hastaların tedavi seçimlerine göre dağılımı Tablo 15: Her iki gruptaki hastaların aldıkları RT dozlarına göre dağılımı
Tablo 16: Her iki gruptaki hastaların tümörlerinin lokalizasyonuna göre dağılımı Tablo 17: Her iki gruptaki hastaların RT alanlarına giren özefagus uzunluğuna göre
dağılımı
Tablo 18: Hasta ve tümör özelliklerinin gruplara göre genel dağılımı
Tablo 19: Her iki gruptaki hastaların tedavi sonuçlarına göre dağılımı
Tablo 20: Tedavi sonucunda oluşan özefajit derecelerinin kemoterapi alma durumu
ile ilişkisi
Tablo 21: Tedavi sonucunda oluşan özefajit derecelerinin histopatolojik tiple ilişkisi Tablo 22: Tedavi sonucunda oluşan özefajit derecelerinin hastaların aldığı RT
dozları ile ilişkisi
Tablo 23: Tedavi sonucunda oluşan özefajit derecelerinin hastaların RT
alanlarındaki özefagusun uzunluğu ile ilişkisi
Tablo 24: Tedavi sonucunda oluşan özefajit derecelerinin KHDAK tanılı hastalarda
ŞEKİLLER DİZİNİ
Şekil 1: Akciğer kanserinin evrelendirilmesinde kullanılan lenf nodu istasyonları ve
akciğerin primer lenfatik drenajı
Şekil 2: Akciğer kanserinde primer tümörün yerleşim yerine göre konvansiyonel
saha çizimleri
Şekil 3: Tümör hücrelerinde glutamin metabolizması
1. GİRİŞ VE AMAÇ
Akciğer kanseri erkeklerde prostat, kadınlarda meme kanserinden sonra ikinci
en sık görülen kanser tipidir.2,4 Her yıl bir milyondan fazla sayıda ölümle tüm
dünyada, hem kadınlarda hem de erkeklerde kanser ölümlerinin en sık ve en önemli sebebidir.8,9 Akciğer kanseri etiyolojisindeki faktörler göz önüne alınırsa önlenebilir
bir hastalıktır. Sigara içimi en büyük risk faktörünü oluşturmaktadır.6,12 Akciğer
kanseri gelişiminden %94 oranında sigara ve tütün ürünleri sorumludur.6
Akciğer kanserli hastaların tedavisine histopatolojik tanısı, evresi ve performans durumu göz önüne alınarak karar verilir. Kemoterapi (KT), radyoterapi (RT), cerrahi ya da kombine tedaviler kullanılır.6
Torakal radyoterapinin amacı; komşu normal dokulara uygun RT dozunu verirken, tümöre terapötik aralıktaki en efektif RT dozunu vermektir.57 Etkili
RT dozunu vermek isterken çeşitli yan etkiler ortaya çıkmaktadır.51,52
Özefagus; santral bölgede olduğu için, özellikle akciğer kanseri hastalarında torakal RT uygulandığında önemli ölçüde radyasyona maruz kalmaktadır.53
Radyoterapinin sebep olduğu akut özefajit; torakal RT alan hastalarda görülen yan etkilerden biridir.51,52
Akut özefajiti önlemek için özefagusun aldığı RT dozunu organ tolerans değerlerinin altında tutmalı, IMRT (Intensity Modulated Radiotion Therapy) gibi ileri RT tekniklerini kullanıp, özefagusun tamamını alan dışına çıkarmaya çalışarak planlama yapılmalıdır. Ancak özefagusun tutulu lenf nodlarına yakınlığı ve mediastendeki pozisyonundan dolayı bu yaklaşımı sıklıkla kullanmak mümkün değildir. Bundan dolayı akut özefajiti önlemek ya da kontrol altında tutabilmek için öncelikli yaklaşım olarak, etkili bir radyokoruyucu ajan saptamaya çalışılmaktadır.52
Glutamin; güçlü radyokoruyucu özellikleri olan bir ajandır. Kanser gibi hiper katabolik durumlarda glutaminin önemli miktarı; iskelet kasları tarafından
sağlanır. Ancak zaman geçtikçe sentez artışı ile kompanse edilemeyecek derecede belirgin glutamin deplesyonu olur.55 Glutamin deplesyonu oluşunca,
RT ve/veya KT ile oluşan doku hasarının genişliği artabilir.57
Bundan dolayı; radyoterapinin sebep olduğu akut özefajiti önlemede glutamin verilmesinin yararlı olabileceği akla uygundur.52
Bu çalışmada; torakal RT alan akciğer kanseri tanılı hastalarda gelişen akut özefajitin önlenmesinde oral glutaminin etkinliğini araştırmak amaçlanmıştır.
2. GENEL BİLGİLER
2.1. Anatomi
Alt solunum sistemi trakea ve akciğerlerden oluşmaktadır. Trakea torasik
kavitedeki ana hava yoludur. Duvarı, kıkırdak halkalar, düz kas ve bağ dokusundan ibarettir ve trakeanın iç yüzeyi epitel hücreleriyle örtülüdür. Trakea, larenksin alt ucundan başlayıp bifürkasyon yaptığı 5. torasik vertebra seviyesinde sonlanmaktadır. Bu bifürkasyona karina denir. Karina hem anatomik hem de radyografik olarak torasik 4 ve 5. vertebra seviyesine denk gelmektedir. Trakea, bifürkasyonda sağ ve sol ana bronşlara bölünmektedir. Bu bronşlar daha sonra ağaç yapısına benzeyen bir dallanma sürecine başlamaktadırlar. Ana bronşlar sekonder bronş olarak bilinen lobar bronş dallarını oluştururlar ve lobar bronşlar daha küçük olan segmenter bronşlara bölünmeye devam ederler. Segmenter bronşlar ise mikroskobik yapılar olan bronşiollere bölünürler ve bronşiollerde alveolar duktusları oluştururlar. Bu düzeyde pek çok kapiller damar alveolar duktusları beslemektedirler. Gazlar alveolar-kapiller membrandan difüzyon yapmaktadırlar. Oksijen ve karbondioksit değişimi bu mikroskobik seviyede gerçekleşir.1
Sağ akciğer üst, orta ve alt lob olmak üzere üç lobdan oluşur. Bu loblar oblik veya majör fissür ve horizontal veya minör fissür adı verilen iki fissür ile birbirinden ayrılır. Sol akciğer tek bir fissür ile ayrılan iki lobdan oluşur. Sol üst lobun lingular parçası sağ akciğerde orta loba karşılık gelir.2 Akciğerlerin hilusu, kan damarları,
lenfatik damarlar ve sinirlerin akciğere girdiği ve çıktığı yerdir.1 Bronşları, pulmoner
arter ve venleri, pulmoner pleksusun çeşitli dallarını, bronşial arter ve venleri ve lenfatikleri içerir2 (Şekil 1).
Akciğer çeşitli lenf bezi bölgelerine drene olan zengin bir lenfatik damar ağına
sahiptir. Bu lenf bezi bölgeleri beş gruba ayrılabilir; intrapulmoner, bronkopulmoner (hiler), mediastinal, supraklavikuler ve skalen lenf bezleri.2
1) Süperior mediastinal lenf bezleri; üst paratrakeal, pretrakeal, retrotrakeal, alt paratrakeal (azygos nodları) ve aortik pencerede yerleşik bir grup bezleri içeren trakea bifurkasyonu (karina) üzerinde yerleşik bezler.
2) İnferior mediastinal lenf bezleri; subkarinal, paraözefageal ve pulmoner ligament bezlerini içeren subkarinal bölge ve inferior mediastende yerleşik bezler.
Sağ üst lob lenfatikleri, trakeobronşial lenf bezlerine, sol üst lob lenfatikleri sadece aynı tarafa değil, aynı zamanda karşı üst mediastene de drene olurken, sağ ve sol alt lob lenfatikleri ise subkarinal bezlere ve buradan sağ üst mediastene ve direk olarak alt mediastinal lenf bezlerine drene olur.2
Şekil 1: Akciğer kanserinin evrelendirilmesinde kullanılan lenf nodu istasyonları ve
2.2. Epidemiyoloji
Akciğer kanseri erkeklerde prostat, kadınlarda meme kanserinden sonra ikinci en sık görülen kanser tipidir.2,3 Tüm dünyada yeni kanser olgularının % 12,4’ünden
akciğer kanseri sorumludur.5,6
Ülkemizde Sağlık Bakanlığının tüm sağlık kuruluşlarında tanı alan kanser olgularının kaydedildiği pasif kanser kayıt sistemi verilerine göre akciğer kanseri insidansı 11,5/ 100.000’dir.6
Amerika Birleşik Devletleri (ABD)’inde 2002 yılında 169.400 kişi akciğer kanseri
tanısı almıştır, 2003 yılında 154.900 kişi bu hastalığa yakalanmıştır.7
Akciğer kanseri insidansı yaşla birlikte artmakta ve altıncı-yedinci dekadlarda pik
yapmaktadır.6
Akciğer kanseri her yıl bir milyondan fazla sayıda ölümle tüm dünyada, hem
kadınlarda hem de erkeklerde kanser ölümlerinin en sık ve en önemli sebebidir.8,9 Tüm dünyada kanser ölümlerinin % 17,8’inden akciğer kanseri sorumludur.5,6
ABD’de de akciğer kanseri halen kansere bağlı ölüm sebeplerinden hem erkeklerde hem kadınlarda 1.sırada yer almaktadır. Erkeklerde kansere bağlı ölümlerin % 31’i, kadınlarda % 22’si akciğer kanserine bağlıdır. Akciğer kanseri diğer sık görülen üç kanserden (kolon, meme ve prostat kanseri) daha fazla ölüm nedenidir.10
Akciğer kanserli hastaların yalnızca % 13’ünün, 5 yıl yaşaması beklenmektedir.11
2.3. Etiyoloji
Akciğer kanseri etiyolojisindeki faktörler göz önüne alınırsa önlenebilir bir
gelişiminden % 94 oranında sigara ve tütün ürünleri sorumludur.6 Tütün dumanı
içinde 3000’den fazla mutajen, karsinojen ve bunlarla ilişkili kimyasal maddeler saptanmıştır.12
Sigara kullananlarda akciğer kanseri riski kullanmayanlardan 24-36 kat daha
fazladır. Sigaraya başlama yaşı, sigara içme süresi, içilen sigara sayısı ile tütün ve sigara tipi ( filtreli, filtresiz, puro vb.) akciğer kanseri gelişme riskini etkiler. Pasif sigara içiminde risk % 3,5’dir.6,13 Akciğer kanserinin tüm histolojik tiplerinin
insidansı sigara içimi ile artmaktadır. İstemli yada istemsiz sigara içimine bağlı en çok görülen akciğer kanseri tipleri skuamöz (yassı) ve küçük hücreli kanserlerdir. Sigara içmeyenlerde bu tipler nadir olup, adenokanserler daha fazla görülür.14
Türkiye’ de akciğer kanseri oluşumunda rol oynayan diğer önemli bir faktör asbest ile temastır. Havayla taşınan küçük partiküllere bölünen bir mineral bileşiği olan asbest, havayoluyla taşınan liflerle karşılaşan kişilerde, özellikle de sigara içenlerde, akciğer kanserini arttırdığı bilinen bir karsinojendir. Sigara içenlerde asbest ile temas kanser riskini 90 kat arttırmaktadır ve akciğer kanserlerinin % 3-4 kadarının asbeste maruz kalınmasından kaynaklandığı düşünülmektedir.15
Krom, arsenik, nikel, klormetileter gibi diğer mesleksel etkenlerle de akciğer kanseri riski artmakta ve sigara ile sinerjistik etki göstermektedir.9,15,16
Yüksek doz iyonize radyasyon, vitamin A’dan fakir diyet, iç ve dış ortam hava kirliliği, genetik yatkınlık, başta tüberküloz olmak üzere akciğerde skar dokusu bırakan hastalıklar ve KOAH’da akciğer kanseri gelişme riskini arttırabilmektedir.6
Akciğer kanserinin etiyolojisi daha geniş ve toplu olarak Tablo 1’de özetlenmiştir.
2.4. Patoloji ve Doğal Gidiş
Akciğer kanseri; bronş epiteli, salgı hücreleri, nöroendokrin hücreler ve
alveollerin tip I, II pnömositleri gibi birçok hücreye farklılaşabilen epitelyal kök hücrelerden gelişmektedir.12
Patolojik olarak akciğer kanserlerinde 4 ana grup bilinmektedir: Skuamöz hücreli karsinom, adenokarsinom, büyük hücreli karsinom ve küçük hücreli karsinom.
Akciğer Kanserinin Etiyolojisi
a. Sigara (% 94) b. Çevresel faktörler Atmosfer kirliliği Biyolojik yakıt Radon Asbestoz
Kimyasal ürünler (böcek ilaçları, formaldehit) c. Mesleki karsinojenler İyonize radyasyon Asbest Krom Kadmiyum Nikel d. Besin maddeleri
Vitamin A ve β-karotenden fakir diyet Yüksek yağlı diyet
e. Akciğer hastalıkları Tüberküloz Bronşektazi Pnömoni Apse Pulmoner emboli
İnterstisyel akciğer hastalıkları gibi akciğerde skatris bırakan hastalıklar Genetik predispozisyon
Aril hidrokarbon hidroksilaz enziminin artmış aktivitesi
_________________________________________________________________
Tablo 1: Akciğer kanserinin etiyolojisi 6
Akciğer tümörünün WHO (World Health Organization) tarafından yapılan patolojik sınıflaması toplu olarak Tablo 3’de görülmektedir.2
Ancak klinisyenler akciğer kanserini, küçük hücreli akciğer kanseri (KHAK) ve küçük hücre dışı akciğer kanseri (KHDAK) olmak üzere iki grupta sınıflandırmaktadır.12 Tüm akciğer kanseri olgularının % 80-85 kadarından KHDAK sorumludur. Başlıca üç tipi vardır: yassı hücreli, adenokarsinoma ve büyük hücreli kanser tipleridir.
Yassı hücreli kanser tüm akciğer kanserlerinin yaklaşık % 30’unu oluşturur ve ülkemizde en sık görülen akciğer kanseri tipidir. Erkeklerde daha fazladır. Genellikle santral yerleşimlidir. Lokal kalma eğilimi gösterirler. Ayrıca tedavilerden sonra da lokal tekrarlamalar daha fazladır.9 Yıllar süren karsinogenezis sonucu bronş
epitelinde yavaş yavaş gelişir. Bu yüzden radyolojik ve klinik bulgu olmadığı halde, balgam ve bronş lavaj örneklerinde atipik hücreler görülebilir. Metastaz yapmadan, endobronşial kitle lezyonu oluşturup ana bronşları tıkayarak semptom verdiğinden, teşhisi daha erken ve prognozu daha iyidir.2 Histolojik olarak iyi veya kötü
diferansiye epitelyal hücre katmanlarından oluşur ve sıklıkla proksimal bronştan köken alır.16 % 27,4’ünde adrenal metastaz görülebilir.2
Adenokarsinomlar ve büyük hücreli kanserler tüm akciğer kanserlerinin yaklaşık
% 60’ını oluştururlar. Aynı doğal gidişe sahiptirler. Sigara içmeyenlerde ve kadınlarda en sık görülen tip adenokarsinomdur. Çoğunlukla akciğerin periferinden kaynaklanır ve skar veya fibrozis zemininde gelişebilir. Yüzey epitelindeki bronşial mukozal glandlardan köken alır.15,16,17
KHAK tüm akciğer kanserlerinin % 15’ini oluşturur. Klinik ve morfolojik özellikleri, kemoterapi ve radyoterapiye duyarlı oluşları nedeniyle diğer akciğer kanseri alt tiplerinden ayrılırlar. Hastaların üçte ikisi tanı anında toraks dışında belirgin metastatik hastalıkla gelirken, yalnızca üçte biri toraksa sınırlı hastalık olarak başvurur.15,16 Yaklaşık % 95 hiler yada santral, % 5 periferik yerleşimli olur.
Hızlı büyüyen, geniş infiltrasyon yapabilen ve erken yayılan lezyonlardır. Agresif bir tiptir ve erkenden hiler, mediastinal ve uzak bölgelere metastaz yapar.Nöroendokrin özellikler gösterir. Paraneoplastik sendromların en sık görüldüğü akciğer kanseri tipidir (Uygunsuz ADH [Antidiüretik hormon] salınımı, Eaton Lambert sendromu gibi).17,18
Akciğer kanserinin orjinini belirlemek zordur. % 58 sağ akciğerden, % 42 sol akciğerden orjin alır. Akciğer kanserinin yayılım yolları intratorasik, lenfatik ve hematojen olmak üzere üçe ayrılır. KHDAK’da en fazla uzak metastaz adenokarsinom tipinde izlenir. Histopatolojik tipe bakmaksızın toplam metastaz oranı % 75-80’i bulur.2
Toplam lenf nodu tutulum oranı % 37-94 arasında değişir. Sağ üst lob ve orta
lob lezyonlarında hiler lenf nodu tutulumu % 60 izlenirken, alt lobların hiler lenf nodu metastaz oranı yaklaşık % 75 civarındadır. Supraklavikuler (skalen) lenf nodlarının tutulum oranı % 2-37 arasında değişir.2
2.5. Klinik
Akciğer kanserinin belirti ve bulguları, tümör lokalizasyonuna, lokorejyonel
yayılımına, uzak metastazlara veya gelişen paraneoplastik sendromlara bağlı olarak değişir. Akciğer kanserli hastaların büyük çoğunluğu tanı anında semptomatiktir. Öksürük hastaların % 75’inde önemli bir semptomdur ve bunların % 40’ı ciddidir. Diğer semptomlar % 57 hastada hemoptizi, % 40 hastada dispne ve göğüs ağrısı, % 10-15 olguda kilo kaybı, halsizlik ve iştahsızlıktır.2
Apikal yerleşimli tümörlerde servikal ve torasik sinirlerin tutulumuna bağlı Claud Bernard Horner sendromu, mediastinal yerleşimli lenf nodlarının basısına bağlı VCSS (Vena Kava Süperior Sendromu) gelişebilir. Nadiren de bazı hastalarda paraneoplastik sendrom izlenebilir.2
Başvuru anında saptanan semptom ve bulguların sıklığı ve muhtemel sebepleri Tablo 2’de görülmektedir.
Semptom,bulgu Sıklık(%) Potansiyel sebep
Öksürük 75 Obstrüksiyon, bası, tümör infiltrasyonu Kilo kaybı 68 İlerlemiş kanser, karaciğerin metastatik tutulumu
Dispne 55-60 Büyük hava yolu obstrüksiyonu, plevral sıvı Göğüs ağrısı 45-50 Torasik sinirlere invazyon ve bası, brakial pleksus
infiltrasyonu
Hemoptizi 25-35 Hava yollarının tümör infiltrasyonu Kemik ağrısı 25 Kemik metastazı
Çomak parmak 20 El ve ayak parmaklarının periostunun iç kesimi
boyunca osteoid depolanması, yeni kemik oluşumu
Ateş 15-20 Obstrüktif pnömoni,karaciğer metastazı Güçsüzlük 10 Periferik nöropati, myastenik sendrom VCSS 4 VCS’un neoplastik infiltrasyonu
Disfaji 2 Özefagus basısı veya infiltrasyonu Wheezing, stridor 2 Tümör kitlesi ile trake,ana bronş obstrüksiyonu
____________________________________________________________________
Tablo 2: Akciğer kanserinde başvuruda saptanan semptom ve bulguların sıklığı ve
sebepleri20
Tümörün intrapulmoner yayılımına bağlı semptom ve bulgular
Primer tümörün akciğerde büyümesi santral ve periferik olarak ikiye ayrılmaktadır. Santral tümörler ana bronş, lober ve proksimal segmental bronşlardan, periferal tümörler ise daha distal hava yollarından kaynaklanmaktadır.19
Öksürük santral yerleşimli tümörlerde daha sıktır. Büyük bronşlardaki küçük bir tümör yabancı cisim etkisiyle veya bronşial mukozada ülserasyon oluşturarak öksürüğe sebep olmaktadır. Yeni ortaya çıkabileceği gibi, daha önceden kronik bronşit sebebiyle var olan öksürüğün karakter değiştirmesi, eşlik eden semptomların değişmesi, tedaviye yanıt vermemesi şeklinde de görülebilmektedir.19
Hemoptizi göğüs radyografisi normal olan bir hastada tek ipucu olabilir. Hemoptizi ile gelen olguların yaklaşık % 20’sinde sebep akciğer kanseridir.19 Dispne genellikle trakea veya ana bronşların tümör tarafından obstrüksiyonuna
bağlı oluşmaktadır. Periferal tümörlerde görülen dispne yalnızca masif plevral sıvı sonucu veya yaygın lenfanjitis karsinomatoza sonucu pulmoner fonksiyonların etkilenmesiyle oluşmaktadır.20
Akciğer Tümörlerinin Patolojik Sınıflaması:
I. Epitelial tümörler
A. Benign tümörler 1. Papillomlar 2. Adenomlar
B. Displazi ve in situ karsinom C. Malign tümörler
1. Epidermoid karsinom a. İğ hücreli (Spindle cell) 2. Küçük hücreli karsinom a. Yulaf hücreli (Oat cell)
b. Ara hücreli (İntermediate cell) c. Kombine yulaf hücreli
3. Adenokarsinom a. Asiner
b. Papiller
c. Bronkoalveoler
d. Mukus salgılayan solid karsinom 4. Büyük hücreli karsinom
a. Dev hücreli (Giant cell) b. Berrak hücreli (Clear cell) 5. Adenosquamöz karsinom 6. Karsinoid tümör
7. Bronş bezi karsinomu
a. Mukoepidermoid karsinom b. Adenokistik karsinom 8. Diğerleri
II. Yumuşak doku tümörleri III. Mezotelyal tümörler
A. Benign tümörler B. Malign tümörler
IV. Karışık tümörler
A. Benign tümörler B. Malign tümörler
V. İkincil tümörler
VIII. Tümör benzeri lezyonlar
Tablo 3: Akciğer tümörlerinin WHO patolojik sınıflaması 2
Wheezing ana bronşun daralmasıyla oluşmakta ve özellikle tek taraflı ve sabit olduğunda önem kazanmaktadır. Stridor trakeanın alt kısmı ve ana bronşun şiddetli, tama yakın tıkanması sonucu oluşmakta ve ciddi klinik tabloya neden olmaktadır.20
Ateş hava yollarının kısmen veya tamamen tıkanması ile oluşan obstrüktif pnömoni veya atelektazi sonucu oluşmaktadır. Ayrıca kitlenin nekrozu sonucu oluşan akciğer apsesi de ateş yapabilir.20
Tümörün intratorasik yayılımına bağlı semptom ve bulgular
Akciğer kanseri direk genişlemeyle veya lenfatiklerle yayılabilmekte ve sinirler
büyük damarlar, organlar, diyafragma ve göğüs duvarına bağlı semptomlara neden olmaktadır.20
Süperior sulcus tümörü (pancoast tümörü) genellikle üst lob apeksinin posterior bölümüne ve brakial pleksusa yakın yerleşmekte, 8. servikal ve 1. ve 2. torasik sinir kökünü infiltre ederek ağrı, ciltte ısı değişikliğine neden olmaktadır. Tümör plevra ve göğüs duvarına kadar yayılabilmekte, 1. ve 2. kostada, vertebrada destrüksiyon yapabilmekte ve sempatik sinir tutulumu sonucunda tek taraflı enoftalmus, pitozis, ulnar alana yayılan omuz ağrısı ve ipsilateral yüz ve üst ekstremitede anhidroza neden olan Horner sendromu’ na yol açabilmektedir.2 Akciğer kanserlerinde ilk
bulgu olarak görülme sıklığı % 4’dür. Çoğunlukla yassı hücreli akciğer kanserinde görülür.20
Akciğer kanserli olgularda VCSS; tümörün basısı veya lenf nodu invazyonuna bağlı oluşmaktadır.1 Yüz, boyun ve göz kapaklarında ödem, omuz ve boyun
venlerinde genişleme ve daha az sıklıkla boyun üst kısmında siyanoz görülmektedir. Bu bulgulara baş ağrısı, baş dönmesi, uyuşukluk, göğüs ağrısı, nefes darlığı eşlik edebilmektedir. Akciğer kanserine bağlı gelişen VCSS’ lu vakaların % 40’ında
sebep KHAK’dir.20
Nervus laringeus rekürrensin tutulumu sonucu ses kısıklığı gelişebilmekte ve sol
nervus laringeus rekürrensin yerleşimi sebebiyle sol hemitoraksa yerleşmiş tümörlerde daha sık görülmektedir.20
Göğüs ağrısı genellikle künt, intermittan, saatlerce sürebilen, nefes darlığı veya öksürükten bağımsız, tümörle aynı tarafta veya orta hatta lokalizedir. Ağrı şiddetli, devamlı, iyi lokalize edilebilen özellikteyse plevra ve kosta erozyonu sonucu göğüs duvarı invazyonu söz konusudur.20,21
Perikard ve myokard tutulumu sonucunda ani başlangıçlı aritmi, kalp yetmezliği, kardiak tamponad gelişebilmektedir.20,21
Tümörün ekstratorasik yayılımına bağlı semptom ve bulgular
Oldukça kötü diferansiye olan KHAK en fazla metastaz yapan tipidir. KHDAK de en çok metastaz yapan adenokarsinomdur, bunu büyük hücreli karsinom ve yassı hücreli karsinom izler.22 Tablo 4’de metastatik akciğer hastalığını düşündüren klinik
bulgular gösterilmiştir.
Hastaların % 10’unda tanı anında SSS metastazı mevcuttur. Bunların % 80-85’i supratentorial bölgededir ve sıklıkla frontal loblarda lokalizedir. Baş ağrısı, mental değişiklik, halsizlik, hemiparezi, jeneralize nöbet, konuşma, görme bozukluğu gibi bir çok semptom ve bulguya neden olmaktadır. Beyin metastazı en sık KHAK’de görülür. 22 Kemik metastazı akciğer kanserinin ilk bulgusu olarak görülebilmekte ve
ağrı, patolojik kırık, nörolojik defisit, hiperkalsemi ve immobiliteye neden olarak hastanın yaşam kalitesini azaltabilmektedir. En sık vertebra, pelvis, kostalar ve femur tutulmaktadır. Tanıda klinik veriler, laboratuar sonuçları, radyografi ve kemik sintigrafisi kullanılmaktadır. Karaciğer metastazı hastaların % 1-35’inde görülmekte, sıklıkla anoreksi, hepatomegali, epigastrik ağrıya neden olmaktadır. Daha az sıklıkla sarılık ve asit görülmektedir. ALT, AST, LDH, ALP yükselebilmektedir. Adrenal metastazın tanınması zordur ancak tomografi ile tespit edilme duyarlılığı % 41-90 arasındadır. Pankreas metastazı sıklıkla KHAK’ de görülmektedir ve obstrüktif sarılığa neden olabilmektedir.20,23
Semptomlar Kilo kaybı( >%10 )
Fokal iskelet ağrısı
Fizik muayene bulguları Lenfadenopati ( >1cm )
Ses kısıklığı, VCSS Kemik hassasiyeti Hepatomegali ( >13cm )
Fokal nörolojik bulgu, papil ödem Yumuşak doku kitlesi
Laboratuar testleri Hematokrit düşüklüğü
(erkeklerde <%40, kadınlarda <%35) ALP, GGT, AST ve kalsiyum yüksekliği
Tablo 4: Akciğer kanserinde metastatik hastalığı düşündüren klinik bulgular 22
Paraneoplastik sendromlara bağlı semptom ve bulgular
Tümörden salınan polipeptid hormanlar, hormona benzer peptitler, antikorlar,
immunkompleksler, prostaglandinler ve sitokinlerin sistemik etkileri sonucunda oluşmaktadır. Akciğer kanseri ile ilgili bir çok paraneoplastik sendrom vardır.20,23
En sık görülen endokrin paraneoplastik sendromlar Cushing sendromu, nonmetastatik hiperkalsemi, uygunsuz ADH sendromudur. ACTH (Adrenokortikotropik Hormon); akciğer kanserinde oluşan en sık ektopik hormon olmasına rağmen klinik olarak Cushing sendromu vakaların % 2-7’sinde görülmektedir. En sık olarak KHAK’de görülmektedir. Paraneoplastik Cushing sendromu kötü prognostik faktördür ve kemoterapi sonrası fırsatçı enfeksiyonlar için büyük risk oluşturur. Hiperglisemi, kas güçsüzlüğü, hipokalemi, alkaloz, ACTH yüksekliği vardır ve deksametazon depresyonu görülmez. Hiperkalsemi en sık yassı hücreli kanserde görülmektedir. Konfüzyon, baş ağrısı, konstipasyon, karın ağrısı, dehidratasyon, poliüri gibi semptomlarla görülebilmektedir. Akciğer kanserli hastaların % 70’inde ADH salınımı artmakta, ancak uygunsuz ADH sendromunun klinik bulguları sık görülmemektedir. Vakaların % 10-60’ını KHAK oluşturmaktadır. Çomak parmak ve hipertrofik osteoartropati en sık yassı hücreli kanserde ve adenokarsinomda görülmektedir. KHAK’de nispeten daha nadir görülmektedir.20
Tanı çalışmaları kan biyokimyası ve tam kan sayımını (kalsiyum, kan üre nitrojeni, kreatinin, laktat dehidrogenaz, ALT, AST, total bilirubin, protrombin zamanı) içermelidir.12
Rutin akciğer filmi (PA ve lateral ) en yaygın kullanılan radyolojik görüntüleme yöntemidir. İki yönlü akciğer grafisi, tümörün yerleşim bölgesini, kot veya vertebra destrüksiyonunu tümör büyüklüğünü, atelektazi, plevral sıvı ve akciğer içi metastatik oluşumları gösterebilir.2
BT (Bilgisayarlı Tomografi) akciğer kanseri tanısında ve tedavisinin planlanmasında en önemli radyolojik yöntemlerden biridir. Tümörün mediasteni, kalbi, büyük damarları, trakeayı, özefagusu, veya karinayı tutup tutmamasına bağlı olarak T3 ve T4’ü birbirinden ayırarak rezektabilitesinin değerlendirilmesini sağlar. Komşu yapılarla ilişkisini göstermekle diğer radyolojik tetkiklere açıkça üstündür. 1,9 Ancak neoplazi ile inflamatuar olayı ayırdetmede yetersiz kalmaktadır.1 Toraks BT’ de kısa eksen çapı 1cm.’den büyük
olan medistinal lenf nodları patolojik sayılmaktadır.24
PET (Pozitron Emisyon Tomografisi) taramasında en sık FDG (floro-deoksi glukoz) kullanılmaktadır. Akciğer kanserinde; fokal pulmoner lezyonların, mediastinal lenf nodlarının malign benign ayrımında, uzak metastazların ve nükslerin belirlenmesinde, tedaviye yanıtın değerlendirilmesinde, prognoz hakkında bilgi sağlanmasında kullanımı vardır. 15,25
PET’ in sensitivitesi BT ile tespit edilemeyen primer lezyonların ortaya
çıkarılmasında % 90’dan fazladır.9 Çalışmalar, evrelemede PET ile birlikte BT kullanılmasıyla sensitivite ve spesifitenin % 60’dan % 85’lere çıktığını göstermiştir.26
Balgam sitolojisi santral lezyonlarda % 70, periferik lezyonlarda %10-20 oranında tanı değerine sahiptir.27
Tanı konulmamış şüpheli periferik akciğer lezyonlarında perkütan iğne biyopsisi sitolojik ve histolojik materyal elde etmek için iyi bir yöntemdir. Floroskopi veya BT eşliğinde yapılabilir.2
Bronkoskopi akciğer kanseri kuşkusu olan hastada tanı, evreleme, tedavi ve tedaviyi takip etmekte kullanılmaktadır. Tümörün bronşlardaki yerleşim yeri, karina tutulumu olup olmadığı veya karinaya olan uzaklığı, dıştan bası ile oluşan değişiklikler tanımlanabilir ve genellikle patolojik bir tanı sağlanır.
Bronkoskopi ile saptanan lezyon tipine göre bronş biyopsisi, transbronşial biyopsi, bronşial fırçalama, bronş lavajı, bronkoalveolar lavaj yapılmaktadır.2,28
Plevral sıvının sitolojik incelenmesi plevral sıvı aspirasyonu ile olur ve tanısal
değeri % 60-75’dir.27
Video eşliğinde torakoskopi (VATS); tanı konulamamış plevral sıvı ve kalınlaşmalarda, periferik parankimal lezyonlarda, mediastinal kitlelerde tanıda, aortiko-pulmoner pencere, azigos ve subkarinal lenf bezlerinde tanı ve evrelemede %100 duyarlılık ve özgüllüğe sahiptir.29 Alt lob tümörlerinde, periferik yerleşimli sol
üst lob tümörlerinde ve her iki hemitorakstaki ilave patolojileri aydınlatmak için tercih edilmelidir.15
Mediastinal nodların değerlendirilmesi hastanın daha ileri evrelenmesinde mediastinoskopi anahtar bir basamaktır. Eğer görüntüleme yöntemiyle elde edilen sonuçlara göre bir karara varılamıyorsa ve tümörün boyutları ve yerleşimine göre mediastinal tutulum olasılığı yüksekse mediastinoskopi önerilmektedir.15
Palpabl lenf bezi varlığında lenf bezi biyopsisi yapılır ve pozitifse inoperabilite kriteridir. Tanı ve rezeksiyon amacıyla torakotomi yapılabilmektedir. Daha az invazif yöntemlerle doğru tanı konabilmesine rağmen, hala küçük bir hasta grubunda akciğer tanısı sadece torakotomi ile konmaktadır.16
2.7. Evreleme
“American Joint Committee on Cancer (AJCC)”, ilk olarak Mountain ve
arkadaşları30 tarafından ileri sürülen ve genel olarak cerrahi bulguları temel alan
TNM sınıflamasını kabul etmiştir. Ancak 2009 yılında son olarak düzenlenmiştir.3,31
(Tablo 5,6).
________________________________________________________
PRİMER TÜMÖR (T)
Tx: Primer tümörün belirlenememesi veya balgam yada bronş lavajında malign
hücrelerin tespit edilip görüntüleme teknikleri yada bronkoskopi ile tümörün gösterilememesi
To: Primer tümör belirtisi yok. Tis: Karsinoma in situ
T1: T1a: ≤2cm tümör
T1b: >2cm fakat ≤3cm
Akciğer ve visseral plevra ile çevrili, bronkoskopik olarak lob bronşundan daha proksimale (ana bronşa ) invazyon göstermeyen tümör.
T2: T2a: >3cm fakat ≤5cm (herhangi T2 özelliklerinden birine sahip ancak ≤5cm) T2b: >5cm fakat ≤7cm
Ana bronş invaze ancak ana karinaya uzaklık 2cm veya daha uzak olması; veya visseral plevra invazyonu olması; veya hiler bölgeye ulaşan ancak tüm akciğeri kapsamayan atelektazi yada obstrüktif pnömoni ile birlikte olması
T3: > 7cm.
Göğüs duvarı ( superior sulcus tümörleri dahil ) diafragma, frenik sinir, mediastinal plevra, parietal perikard gibi yapılardan herhangi birine direkt invazyon göstermesi; veya karinaya 2 cm’ den daha yakın ancak karinayı tutmayan ana bronştaki tümör; veya bütün bir akciğeri kapsayan atelektazi veya obstrüktif pnömoni ile birlikte olan tümör veya tümörle aynı lob içinde satellit tümör nodül olması
T4: Tümörün herhangi bir büyüklükte olup mediasten, kalp, büyük damarlar, trakea , özefagus vertebral kolon, karina gibi yapılardan herhangi birini invaze etmesi ; veya farklı ipsilateral lobda satellit nodül olması
BÖLGESEL LENF NODU (N)
N0: Bölgesel lenf bezi metastazı yok.
N1: Aynı taraf peribronşial ve/veya aynı taraf hiler lenf bezlerine metastaz ve primer tümörün direkt yayılması ile intrapulmoner bezlerin tutulması
N2: Aynı taraf mediastinal ve/veya subkarinal lenf bezlerine metastaz
N3: Karşı taraf mediastinal , hiler ; aynı veya karşı taraf supraklaviculer veya skalen lenf bezi metastazı
UZAK METASTAZ (M)
Mx: Uzak metastaz varlığının değerlendirilememesi MO: Uzak metastaz yok
M1: Uzak metastaz var.
M1a: Karşı lobta satellit tümör nodülü olması ya da plevral nodülle birlikte olan veya malign plevral effüzyon gösteren tümör
M1b: Uzak metastaz
__________________________________________________________________
Tablo 5: Akciğer kanserinde TNM evrelemesi31
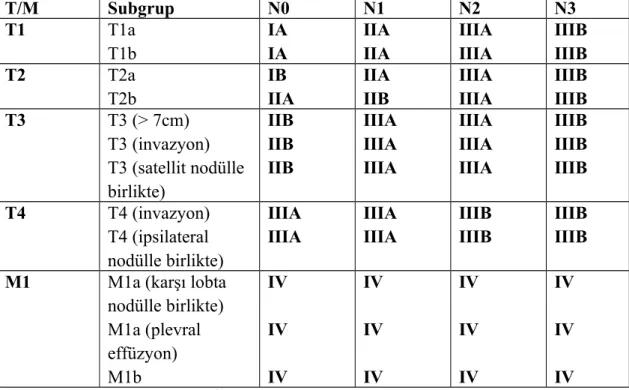
T/M Subgrup N0 N1 N2 N3 T1 T1a T1b IA IA IIA IIA IIIA IIIA IIIB IIIB T2 T2a T2b IB IIA IIA IIB IIIA IIIA IIIB IIIB T3 T3 (> 7cm) T3 (invazyon) T3 (satellit nodülle birlikte) IIB IIB IIB IIIA IIIA IIIA IIIA IIIA IIIA IIIB IIIB IIIB T4 T4 (invazyon) T4 (ipsilateral nodülle birlikte) IIIA IIIA IIIA IIIA IIIB IIIB IIIB IIIB M1 M1a (karşı lobta
nodülle birlikte) M1a (plevral effüzyon) M1b IV IV IV IV IV IV IV IV IV IV IV IV
Tablo 6: TNM evre gruplaması31
AJCC tarafından kabul edilen TNM evrelemesinin KHAK’ de de kullanılması önerilmiştir ve son yıllarda ‘’Uluslararası Akciğer Kanseri Çalışma Grubu’’ sınırlı evre hastalığı, TNM evresine göre evre I-IIIB hastalık olarak tanımlamaktadır.32
Ancak ‘’Veterans Administration Lung Cancer Group’’ un (VALG) önerdiği ikili sistem evrelemesi pratikte daha çok kullanılmaktadır (Tablo 7).6,33
Sınırlı hastalık Bir hemitoraksa sınırlı tümör; aynı yada karşı tarafa hiler, mediastinal ve supraklavikuler lenf bezi metastazı; aynı taraf malign plevral effüzyon (TNM ye göre evre I, II, III)
Yaygın hastalık Sınırlı hastalık kapsamına girmeyen tümör (evre IV)
Tablo 7: KHAK evrelemesinde VALG’ ın önerdiği ikili sistem evrelemesi6
2.8. Tedavi
Akciğer kanserli hastaların tedavisine histopatolojik tanısı, evresi ve performans durumu göz önüne alınarak karar verilir.6
2.8.1. KHDAK’ de evrelere göre tedavi yaklaşımı:
Evre IA ve IB’de standart yaklaşım cerrahi olarak tümörün ilgili akciğer dokusuyla beraber çıkartılması ve hiler, mediastinal lenf bezi diseksiyonu ile tam rezeksiyondur. Tercih edilen rezeksiyon tipi lobektomidir, gerekirse daha geniş rezeksiyon yapılabilir.6 Tam olarak rezeke edilmiş evre I hastalıkta
postoperatif torasik RT veya sistemik KT önerilmez. Tam olmayan rezeksiyonda (cerrahi sınır pozitifliğinde), kardiyopulmoner rezervi uygunsa tamamlayıcı cerrahi, değilse radikal RT düşünülmelidir. Medikal inoperabl olan ya da operasyonu kabul etmeyen olgularda torasik RT uygulanır.15,34
Evre IIA ve IIB’ de tümörlerin tedavisinde standart yaklaşım cerrahi ( lobektomi, sleeve lobektomi veya pnömonektomi) olarak tümörün tam rezeksiyonudur. Lenf bezi diseksiyonu rutin olarak yapılmalıdır. Negatif cerrahi marjinleri bulunan N1 hastalıkta olumsuz faktörler (yetersiz mediastinal lenf nodu diseksiyonu, ekstrakapsüler yayılım, multipl pozitif hiler nodlar ve yakın marjinler) taşıyan hastalarda KT veya KRT önerilmektedir. Pozitif cerrahi marjinleri bulunan N1 hastalıkta, yeniden rezeksiyon sonrasında kemoterapi ya da radyoterapi ile birlikte kemoterapi adjuvan olarak uygulanmalıdır. Göğüs duvarında lezyonu bulunan veya proksimal havayolundaki veya mediastendeki T3, N0-1 tümörlü hastalarda başlangıçta
cerrahi ile tedavi edilenler, cerrahi marjinler negatifse sadece KT almalıdır ve cerrahi marjinler pozitifse yeniden rezeksiyonla KT veya RT ile birlikte KT almalıdır.15
Evre III hastalarda tümör yerleşimine göre cerrahi rezektabilite ile ilgili karar verilmelidir. T3N1 olgularda önerilen tedavi cerrahidir. Rezektabl lezyonları olan hastalarda cerrahi sırasında mediastinal lenf nodu diseksiyonu yapılmalıdır. Tam olarak rezeke edilmiş N0-1 hastalıkta postoperatif radyoterapinin sağkalımı uzattığına dair kanıt olmamakla birlikte lokal nüksü azalttığı bildirilmiştir, bu yüzden bu durumda postoperatif RT önerilmez.6,15
Aynı lobda satellit nodülü olan ve N0-1 olan hastalar öncelikle cerrahi açıdan
değerlendirilmelidir. Karinal invazyonu olan ve N0-1 hastalar öncelikle cerrahi açıdan değerlendirilmelidir. Damar invazyonu olan ve N0-1 hastalar öncelikle cerrahi açıdan değerlendirilmelidir.15
N2 saptanan olgularda tam rezeksiyon sağlanabilecekse operasyona devam
edilir ve tam rezeke edililirse lokal nüksü engellemek için torasik RT programına alınır. Rezeke edilemez evre IIIA “bulky” N2’li hastalarda (BT’ de
pozitif tümörlü mediastinal lenf nodu 2-3cm üzerinde olan ve özellikle ekstranodal yayılımı olan veya paket oluşturmuş çok sayıda küçük pozitif lenf nodu olan hastalar) veya rezeke edilemez T4 tümörlü hastalarda (malign plevral effüzyonu olmayanlar) standart tedavi kemoradyoterapidir. Eş zamanlı KRT; birinci seçenek tedavi yöntemi olmalıdır. Radyoterapinin, tedavinin erken döneminde başlaması tercih edilmelidir. Tedavinin başlangıcında KRT’ ye başlanamayacak hastalarda indüksiyon kemoterapisi verilerek, daha sonra KRT şeklinde devam edilebilir. Ardışık KRT; eşzamanlı tedaviyi tolere edemeyecek olan hastalarda uygulanmalıdır. 2-3 siklus KT daha sonra torakal RT uygulanır. Kemoterapiye yanıt veren hastalara RT sonrası KT devam edilebilir. RT öncesi ve sonrasında toplam en fazla 6 kür KT verilir. Radikal RT, KT yapılamayacak hastalarda konvansiyonel veya akselere olarak tek başına uygulanabilir.15
Neoadjuvan tedavi sonrası operasyon için değerlendirilmesi düşünülen seçilmiş olgularda (T4N0M0, T4N1M0, rezeke edilemez evre IIIA N2’li hastalar) indüksiyon tedavisi olarak KRT veya KT uygulanabilir. Primer tümörde küçülme varsa operasyon için değerlendirilir. Stabil ya da progresyon varsa radikal torasik RT veya
eş zamanlı KRT programına alınır. Radyoterapinin küratif etkinliğini azaltmamak için cerrahi değerlendirmenin gecikmeden yapılması gerekir. Tercih edilen yaklaşım, başlangıçta operasyon yapılmasına karar verilen hastalarda neoadjuvan tedavi sonrası progresyon olmadığı takdirde operasyonun yapılmasıdır (çünkü opere edilemediği takdirde radyoterapiye ara vermeden küratif radyoterapinin tamamlanması gerekmektedir). Mediasteni pozitif hastaların neoadjuvan tedavi sonrası mediastenin negatif hale gelmesi başarı şansını arttırır.15
Evre IV hastalarda mevcut tedavi olanakları ile kür sağlamak mümkün değildir. İyi performans statüsü olan hastalarda KT uygun bir tedavidir. Primer tümöre bağlı ağrı, hemoptizi, dispne, total atelektazi, kemik, beyin metastazı, spinal kord kompresyonları ve süperior sulkus tümörleri gibi durumlarda palyatif RT endikasyonu bulunur.15
Son yıllarda ilerlemiş akciğer kanseri tedavisi için hedefe yönelik spesifik tedaviler geliştirilmiştir.35,36 Bevasizumab, vasküler endoteliyal büyüme faktörünü
(VEGF) bloke eden bir rekombinant monoklonal antikordur.35 Erlotinib, epidermal
büyüme faktörü reseptörünün (EGFR) inhibitörü olan küçük bir moleküldür.36 2.8.2. KHAK’de tedavi
Kemosensitif ve radyosensitif bir tümördür. Genellikle cerrahi uygulama yapılamaz. Çünkü bu kanserlerde ilk tanı sırasında % 80 olguda toraks dışında yayılım mevcuttur. KHAK‘de primer tedavi KT’dir. Sınırlı evrede KT’ye RT ilavesiyle hem sağkalım oranları, hem de lokal kontrol artar. Sınırlı evre hastalıkta önerilen standart tedavi eşzamanlı KRT’dir, bu tedavi ile hem sağkalım oranları, hem de lokal kontrol artar. Genel olarak bugün için kabul gören uygulama şekli; 1. veya 2. kürden itibaren radyoterapinin kemoterapiye eklenmesi ile eşzamanlı KRT uygulanmasıdır. 6, 37
Sınırlı hastalıkta KT ve RT kombinasyonu ile ortalama yaşam 20 ay, 2 yıllık
sağkalım % 45, 5 yıllık sağkalım % 15-20 arasındadır.33,38 Torasik radyoterapinin
sağkalımı uzattığı bildirilmiştir.39 Radyoterapinin teknik özellikleri KHDAK’den
farklı değildir. Fakat uygulanan RT dozu daha azdır.40 Tam yanıt alınan sınırlı evre
hastalarda profilaktik kranial RT yapılmalıdır.15
Yaygın hastalıkta 2 kür KT uygulanır. Yanıt varsa 4-6 küre tamamlanır. Yaygın hastalıkta tam yanıt varsa, sınırlı hastalıktaki gibi torasik RT ve profilaktik kranial
RT düşünülebilir. Lokal semptomlar varsa, toraksa palyatif dozlarda RT uygulanır.15
Yaygın hastalıkta tedavi verilmezse yaşam 1-3 ay, kombine kemoradyoterapisiyle 9-12 ay arasında yaşam beklenir. 41,42
2.9. Konvansiyonel Radyoterapi Teknikleri
2.9.1. Volüm, Alanlar ve RT Düzenlemeleri
Tedavi edilecek volüm ve radyoterapi sahaları, primer tümörün yerleşimine, büyüklüğüne, lenfatik drenaj alanlarına, histolojik tipe ve mevcut cihaz ve ışın enerjilerine göre ayarlanmaktadır.2
Akciğer kanserinin tedavisinde kullanılan tipik radyoterapi alanı, primer tümör volümünü ve komşu mediasteni içeren karşılıklı paralel ön-arka mediastinal sahalardan oluşur. Tipik olarak AP/PA saha dizaynı, her hangi bir gros tümör etrafında 2cm. sınırla ve eğer ışınlanacaksa elektif lenf nodlarının etrafında 1cm sınırla ayarlanır. Düzensiz şekilli alanlar tercih edilmelidir ve normal dokuları mümkün olduğu kadar korumak için özel ikincil bloklar kullanılmalıdır.
Eğer tedavi sahalarına potansiyel lenfatik drenaj da dahil edilecekse şu hususlar önerilmektedir:
1. Eğer primer tümör üst lobda ise, aynı taraf supraklaviküler bölge de tedavi sahasına dahil edilmelidir ve alt saha sınırı karinanın 5-6cm altına çekilmelidir. 2. Eğer primer tümör orta veya alt lobda ise ve mediastinal LAP yoksa supraklaviküler bölgeyi tedavi etmeye gerek yoktur.
3. Eğer BT'de veya mediastinoskopide gösterilmiş gros üst mediastinal tümör varsa, ayni taraf supraklaviküler bölge de tedavi sahasına dahil edilmelidir.
4. Aynı taraf hilus genellikle ışınlanan volüme dahil edilir ancak eğer kontralateral hiler bölge nodları tutulu değilse karşı hilus saha dışı bırakılır.
5. Eğer indüksiyon kemoterapisi uygulanmışsa primer tümör volümünün tanımı kemoterapi öncesi belirlenen volüme göre yapılmalıdır.2
Şekil 2: Akciğer kanserinde primer tümörün yerleşim yerine göre, konvansiyonel 2-boyutlu
radyoterapi için klasik saha çizimleri. Bu sahalar subklinik hastalığı da hedef alan geniş saha ışınlamalarıdır. 2
Geleneksel radyoterapi saha dizayn örnekleri Şekil 2’de görülmektedir.
Çeşitli çalışmalarda, klinik evre I seçilmiş KHDAK’li vakalarda, bölgesel
ve sağkalım görülmüştür ve bu nedenle elektif nodal ışınlama bu çalışmalarca önerilmemektedir.
Lateral alanlar bazı merkezlerde primer tümör ve hiler ve mediastinal lenf nodlarına ek doz vermek amacıyla kullanılmaktadır. Ancak, göğüsün lateraldeki kalınlığı nedeniyle, bu alanlardan uygulanacak doza bağlı olarak, normal akciğer dokusuna belirgin olarak daha fazla ışın dozları verilmiş olur.43 2.9.2. Tümör Dozları
Temel olarak akciğer karsinomunda konvansiyonel olarak uygulanan yöntem;
primer tümör ile bölgesel hiler ve mediastinal lenfatiklerden oluşan geniş volüme günde 1,8-2 Gy (Gray) ile haftada 5 gün, toplam 25 günde 45-50 Gy RT uygulanması ve daha sonra küçük alanlardan primer tümöre 5-7 günde 10-14 Gy boost (ek tedavi) dozu verilmesidir. Torasik radyoterapinin toplam tedavi süresinin uzaması sağkalımı olumsuz etkiler. Tümör evresi, hastanın durumu ve radyoterapi fraksiyonasyonuna bağlı olarak tümör dozları uygulanmaktadır.2 KHAK’de KHDAK’e göre RT dozu
daha azdır ve konvansiyonel fraksinasyon ile 23-25 seansta toplam 45-50 Gy RT dozu, primer tümör ve mediastinal lenfatik saha için yeterli kabul edilmektedir. Kemoterapiye kısmi cevap veren veya RT sırasında gerileme izlenmeyen vakalarda primer tümöre yönelik doz 60 Gy’e yükseltilebilir.44
Unrezektabl, lokal ileri evre KHDAK’ de son 30 yıldır kullanılagelmiş standart RT dozu RTOG (Radiation Oncology Group) 73-01 çalışmasında öngörülen günlük 2 Gy fraksiyonlarda toplam 60 Gy’dir.39
Çoğu “split-course” fraksiyonasyon şemasında 2-3 haftada 25-30 Gy tümör dozu (2.5-3 Gy fraksiyonlarla) verilmekte ve iki tedavi arasında 2-4 haftalık dinlenme periyodu uygulanmaktadır. Hiperfraksiyone radyoterapi (2x1.2-1.5 Gy/gün) normal dokularda morbiditeyi artırmadan tümöre daha fazla RT dozları vermek üzere (79.2 Gy) denenmiştir.45 Akselere fraksiyonasyon ile (1.5-1.6 Gy bid
veya tid) 50-79.2 Gy dozlar, bir faz II randomize olmayan çalışmada test edilmiş46
2.10. Radyoterapinin Etkileri ve Radyasyon Özefajiti
Memeli hücrelerin çoğalması mitoz bölünme ile gerçekleşir. Memeli
hücrelerin siklusu; mitoz (M), senteze hazırlık (G1), sentez (S), mitoza hazırlık (G2) fazlarından oluşur. Değişik hücre tiplerine göre her bir fazın süresi ve toplam mitotik siklus süresi farklıdır. Hücre sikluslarının farklı fazlarının radyasyon duyarlılıklarının birbirinden farklı olduğu gösterilmiştir. Mitoz (M) ve mitoza hazırlık (G2) fazındaki hücrelerin radyasyona karşı en duyarlı hücreler oldukları, buna karşın geç sentez (S) fazındaki hücrelerin radyasyona karşı en dirençli hücreler olduğu bulunmuştur.48,49,50
Radyoterapinin etkisi radyasyonun dokular tarafından absorbe edilmesiyle açığa çıkar. Moleküler ortamda eksitasyon ve iyonizasyon oluşturarak hücrelere etki söz konusudur. Bu etki değişikliğin meydana geldiği molekülün hücre içindeki görevine bağlı olarak ya doğrudan ya da dolaylı ölümcül etkiyi oluşturur. Doğrudan etki için etkilenen moleküller DNA gibi hücre döngüsünde primer role sahip olan bölgede olabilir. Bu süreçte o hücrenin bölünmesi mümkün olmaz veya hücrenin ölümüne yol açacak süreç aktive edilmiş olabilir ve direk radyasyon hasarı meydana gelir. Dolaylı etkide ise değişime uğrayan molekül kısa sürede hücrenin çoğalmasına etki etmese de, ilerleyen bölümlerde yapısal hasar oluşturarak hücrenin normal fonksiyon görmesini önleyecektir.50
Radyoterapinin amacı; iyonizan radyasyon kullanılarak malign hücrelerin ortadan kaldırılmasıdır ve bunu yaparken normal dokulara zarar vermemektir. Ancak çoğunlukla malign hücrelerin yakınındaki sağlıklı hücrelerin de yüksek radyasyon dozlarına maruz kalması kaçınılmazdır.51 Etkili RT dozunu vermek
isterken çeşitli yan etkiler ortaya çıkmaktadır. Radyoterapinin sebep olduğu akut özefajit; torakal RT alan hastalarda görülen yan etkilerden biridir.52
Özefagus; santral bölgede olduğu için, özellikle akciğer kanseri hastalarında torakal RT uygulandığında önemli ölçüde radyasyona maruz kalmaktadır.
Radyasyonun sebep olduğu akut özefajitin torakal radyoterapide en önemli doz sınırlayıcı toksisite olduğu kabul edilmektedir.53
Radyasyon özefajitinde özefagusta iritasyon ve inflamasyon ortaya çıkar ve özefagus peristaltizmi bozulur. Disfaji, odinofaji ve sternum arkasında yanma hissi en önemli semptomlarıdır. Radyasyon özefajiti tanısı genelde klinik olarak
konmaktadır. Özefagus mukozası çok hızlı bir şekilde rejenere olduğu için RT tamamlandıktan birkaç hafta sonra düzelmekte ve semptomlar kaybolmakta, dört altı haftadada da tamamen düzelmektedir. 53
RTOG’nin kabul ettiği akut özefajit toksisite derecelendirmesi Tablo 8’de belirtilmiştir.53 Tablo 8: RTOG akut özefajit toksisite kriterleri 52 Radyasyon özefajitini önlemek için çeşitli ilaçlar kullanılmakla birlikte oral glutamin de kullanılan ajanlardan biridir.52 Grade 0 Değişiklik yok
Grade I Hafif disfaji/ odinofaji
Topikal anestezik, nonnarkotik ajan veya yumuşak diet gerekebilir.
Grade II Orta disfaji/ odinofaji
Narkotik ajan veya pure/ sıvı diet gerekebilir
Grade III Şiddetli disfaji/ odinofaji
Dehidratasyon veya % 15 den fazla kilo kaybı eşlik edebilir.
NG beslenmeye gerekebilir.
Grade IV Komplet obstrüksiyon, ülserasyon, perforasyon/ fistül
2.11. GLUTAMİN
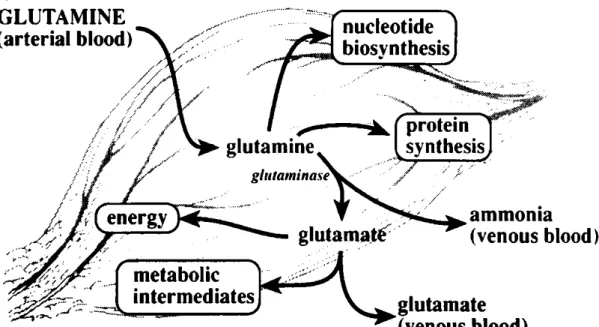
Glutamin insan dokularında en sık bulunan serbest aminoasittir.52 Proteinlerin en önemli kompanentidir. Enerji kaynağı ve nitrojen taşıyıcı olarak fonksiyonu vardır. Glikoneogenez ve protein sentezinin en önemli regülatörüdür. Glutamin kaslarda hızla sentezlenebilirken, metabolizması barsaklardan olur.Güçlü radyokoruyucu özellikleri olan bir ajandır. Kas depoları; barsak epiteli için gerekli glutaminin direk kaynağıdır. Barsak epitelinin başlıca oksidatif yakıtıdır, stres
durumlarında ve normal durumlarda barsak yapısının bütünlüğünün korunması için gereklidir. 54,55
Şekil 3: Tümör hücrelerinde glutamin metabolizması 56
Kanser gibi hiper katabolik durumlarda glutaminin önemli miktarı; iskelet kasları tarafından sağlanır. Ancak zaman geçtikçe sentez artışı ile kompanse edilemeyecek derecede belirgin glutamin deplesyonu olur. Glutamin deplesyonu gibi durumlar; radyasyon toleransında azalmaya yol açabilir.55 Glutaminin
normal dokulardaki oksidatif hasara karşı koruma fonksiyonu da vardır. Glutamin deplesyonu oluşunca, glutamin metabolizmasında üretilen bir ürün
olan glutatyon da deplese olur ve RT ve/veya KT ile oluşan doku hasarının genişliği artabilir.56,57 Kanser hastalarında kastaki glutaminin progresif
tüketimine eğilim vardır ve bu tüketim kanserin sebep olduğu kaşeksi için önemli bir faktördür.55
Destek amaçlı glutamin enteral veya parenteral verilmelidir. Aktif tümör büyümesi gibi metabolik stres esnasında günlük 20-40gram verilir. Kapsül ve hap formları ile toz formu kıyaslandığında toz tercih edilmelidir. Çünkü daha ucuz ve daha etkilidir. Kullanımı kolaydır, daha iyi absorbe edilip, daha iyi tolere edilir, daha yüksek dozlarda alınabilir, barsak epitelinde koruma sağlar.57,58,59
3. MATERYAL VE METOD
Bu çalışmada Ocak 2008-Ocak 2010 tarihleri arasında Dicle Üniversitesi Tıp Fakültesi Radyasyon Onkolojisi Anabilim Dalı’ nda tedavi ve takip edilmiş akciğer kanseri tanılı 316 hasta dosyası retrospektif olarak incelendi ve değerlendirildi. Torakal RT alan, tedavi öncesi bilinen disfaji rahatsızlığı bulunmayan, bilinen glutamin alerjisi olmayan ve glutaminden başka herhangi bir diet ürünü kullanmayan 46 hasta çalışmaya dahil edildi. Hastaların tamamının Karnofsky Performans Statüsü (KPS) %60 ve üstüydü.
3.1. Çalışmanın amacı
Bu çalışmada; torakal RT alan akciğer kanseri tanılı hastalarda gelişen akut
özefajitinin önlenmesinde oral glutaminin etkinliğini araştırmak amaçlanmıştır.
3.2. Hasta ve tümör özellikleri
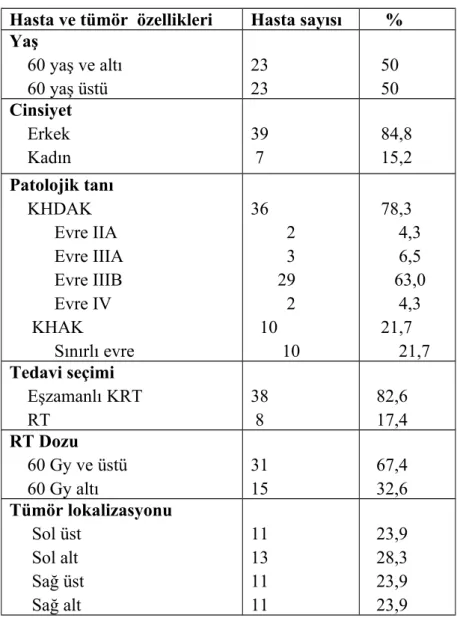
Çalışmadaki hastaların 39’u erkek, 7’si kadın idi. Hasta grubunda minimum yaş 34, maksimum yaş 80 olarak tespit edildi. Hastaların 23’ü 60 yaş ve altında, 23’ü ise 60 yaş üzerindeydi. Histolojik dağılım dikkate alındığında 36 hasta KHDAK, 10 hasta KHAK olarak tespit edildi. KHDAK tanılı hastaların 20’sinin alt tipi belirlenmişti ve bunların 13’ü yassı hücreli karsinom, 7’si adenokarsinom tanılıydı. KHDAK tanılı 36 hastanın 2’si evre IIA, 3’ü evre IIIA, 29’u evre IIIB, 2’si evre IV idi. KHAK tanılı 10 hastanın tamamı sınırlı evre idi. Tedavi seçimleri dikkate alındığında 38 hasta eş zamanlı KRT, 8 hasta sadece RT aldı. Tümörün 11 hastada sağ alt, 11 hastada sağ üst, 13 hastada sol alt, 11 hastada sol üst yerleşimli olduğu tespit edildi.
Tablo 9’da hasta ve tümör özellikleri özetlenmiştir.
3.3. Radyoterapi
Tüm hastaların RT alanları, koronal ve sagital planda iki boyutlu görüntü veren
Nucletron Oldelft marka Simulix-HP model simülatör cihazı ile planlandı. Toraks BT’ den yararlanılarak gross tümör volümü, klinik hedef volüm ve tedavi volümü belirlendi. Hastaların ilk tedavisine ilgili doktorun katılımı ile set up değerlendirildi ve tedavi alanı doğrulandı. Hastaların tamamı haftanın 5 günü torakal radyoterapisini günlük aldılar. Hastalara General Electric marka Saturn 43 F model lineer akseleratör tedavi cihazının 10 mV foton enerjisi kullanılarak, SAD tekniği ile günlük 2 Gy’lik ya da 3 Gy’lik fraksiyonlarla, hastanın histolojik tipine, evresine göre farklı dozlarda RT uygulandı.
Radyoterapi sahası olarak; primer tümör ve tutulu lenf nodlarını 2cm. sınırla içermiş, tüm mediasten saha içine alınmış, üst ve orta lob tümörlerinde subkarinal lenf nodu tutulumu yok ise karinanın 5cm altına kadar lenf nodları saha içine alınmış, alt lob lezyonlarında diyafram saha içine alınmış, ipsilateral supraklaviküler fossa, tümör sadece üst lob yerleşimli veya supraklaviküler fossada lenf nodu var ise dahil edilmiştir (Şekil 3). Medulla spinalis 46 Gy’de alan dışına çıkarılarak RT dozu tamamlanmıştır.
Çalışmadaki hastaların RT alanına giren özefagus uzunlukları 18cm. ve üstü ile 18cm. altı olarak, ayrıca aldıkları RT dozları da 60 Gy ve altı ile 60 Gy üstü olarak sınıflandırıldı.
3.4. Glutamin kullanımı
Çalışmaya alınan hastalar iki gruba ayrıldı. Profilaktik toz oral glutamin
1.gruptaki 21 hastaya; günlük 30gram olacak şekilde (10gr/8h su içinde oral olarak) torakal RT’ nin ilk günü başlanıp, RT süresince ve RT’den sonra 3 hafta devam edilerek verildi. 2.gruptaki 25 hastaya oral glutamin verilmedi. Her iki gruptaki hastalar özefajit ile ilgili ek başka bir tedavi almadı.
Tablo 9: Hasta ve Tümör özellikleri
3.5. Hasta değerlendirilmesi ve akut özefajit skorlaması
Tüm hastalara torakal RT sırasında haftalık muayene ve sorgulamalarla semptom ve toksisite değerlendirilmesi yapıldı. Hastalarda gelişen akut özefajit; RTOG akut özefajit toksisite kriterlerine göre derecelendirildi (Tablo 9).
Hasta ve tümör özellikleri Hasta sayısı % Yaş 60 yaş ve altı 60 yaş üstü 23 23 50 50 Cinsiyet Erkek Kadın 39 7 84,8 15,2 Patolojik tanı KHDAK Evre IIA Evre IIIA Evre IIIB Evre IV KHAK Sınırlı evre 36 2 3 29 2 10 10 78,3 4,3 6,5 63,0 4,3 21,7 21,7 Tedavi seçimi Eşzamanlı KRT RT 38 8 82,6 17,4 RT Dozu 60 Gy ve üstü 60 Gy altı 31 15 67,4 32,6 Tümör lokalizasyonu Sol üst Sol alt Sağ üst Sağ alt 11 13 11 11 23,9 28,3 23,9 23,9
3.6. Verilerin toplanışı ve istatistiki analizler
Veriler “SPSS 11,5 for Windows” programı yardımıyla veri tabanına girildi
ve istatistiki testler yine bu program üzerinden yapıldı. Hasta ve tümör özellikleri ve tedavi sonuçları ile ilgili tablolar spearman khi-kare analizi uygulanarak yapıldı ve yorumlandı.
Beklenen ve gözlenen değerlerin 5’ten aşağı olduğu durumlarda p değeri
fisher’in kesinlik testine göre (fisher’s exact test) hesaplandı. p< 0,05 değeri anlamlı olarak kabul edildi.
4. BULGULAR
Bu çalışma için uygun 46 hasta çalışmaya dahil edildi ve tamamı istatistiksel
analize dahil edildi. Hastalarda glutamine bağlı toksisite ya da glutamin intoleransı gözlenmedi. Çalışma popülasyonunun tamamının tedavi öncesi karakteristik özellikleri ve tümör özellikleri toplu olarak Tablo 18’de gösterilmiştir. İki grup arasında hasta ve tümör özellikleri açısından istatistiksel olarak anlamlı fark gözlenmemiştir (p> 0,05).
4.1. Hasta ve tümör özelliklerinin gruplara göre ilişkisi
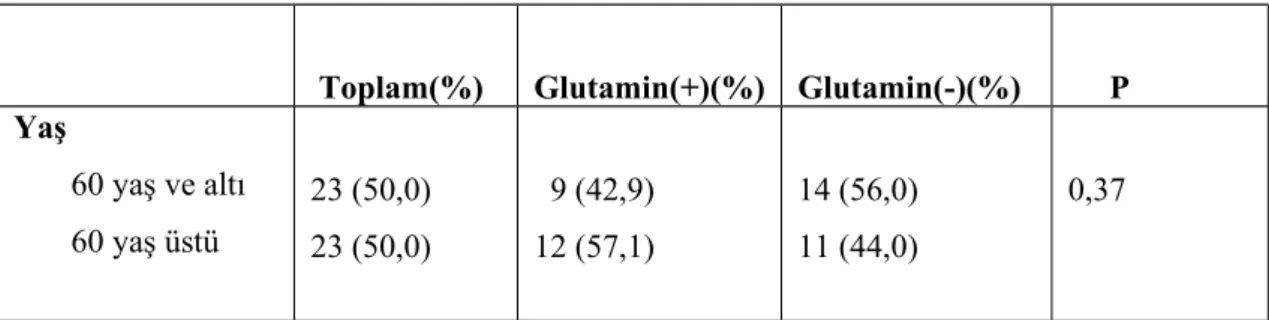
Toplam(%) Glutamin(+)(%) Glutamin(-)(%) P Yaş 60 yaş ve altı 60 yaş üstü 23 (50,0) 23 (50,0) 9 (42,9) 12 (57,1) 14 (56,0) 11 (44,0) 0,37
Tablo 10: Her iki gruptaki hastaların yaşa göre dağılımı
Yaş: Çalışmada glutamin verdiğimiz 1.grupta 9 hasta (% 42,9) 60 yaş ve altında,
12 hasta (% 57,1) 60 yaş üzerinde, 2.grupta 14 hasta (% 56,0) 60 yaş ve altında, 11 hasta (% 44,0) 60 yaş üzerinde belirlendi. Her iki grup arasında yaş bakımından istatistiksel olarak anlamlı farklılık bulunamamıştır (p:0,37).
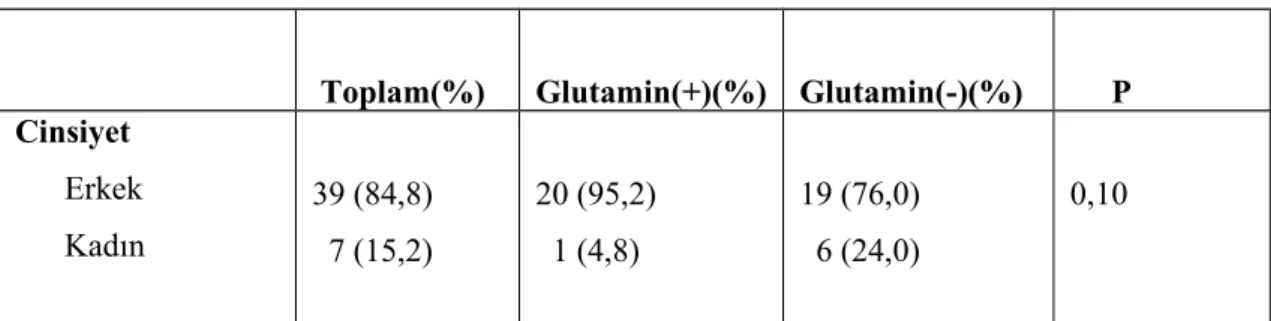
Toplam(%) Glutamin(+)(%) Glutamin(-)(%) P Cinsiyet Erkek Kadın 39 (84,8) 7 (15,2) 20 (95,2) 1 (4,8) 19 (76,0) 6 (24,0) 0,10
Tablo 11: Her iki gruptaki hastaların cinsiyete göre dağılımı
Cinsiyet: 1.grupta olguların 20’si (% 95,2) erkek, 1’i (% 4,8) kadın, 2.grupta
19’u (% 76,0) erkek, 6’sı (% 24,0) kadın olarak tespit edildi. Her iki grup arasında cinsiyet dağılımı açısından istatistiksel olarak anlamlı farklılık bulunamamıştır (p:0,10).
Toplam(%) Glutamin(+)(%) Glutamin(-)(%) P
Histopatolojik tanı KHDAK KHAK 37 (80,4) 9 (19,6) 18 (85,7) 3 (14,3) 18 (72,0) 7 (28,0) 0,26
Tablo 12: Her iki gruptaki hastaların histopatolojik tanılarına göre dağılımı
Histopatolojik tanı: 1.gruptaki hastaların histopatolojik dağılımı; 18’i (% 85,7)
KHDAK, 3’ü (% 14,3) KHAK olarak, 2.gruptaki hastaların histopatolojik dağılımı ise 18’i (% 72,0) KHDAK, 7’si (% 28,0) KHAK olarak belirlendi. Her iki grup arasında histopatolojik tanıları açısından istatistiksel olarak anlamlı farklılık bulunamamıştır (p:0,26).
Ayrıca KHDAK tanılı 36 hastanın 20’sinin (% 55,6) alt tipi belirlenmişti. Alt tipi belirli olan 20 hastanın 13’ü (% 65,0) yassı hücreli karsinom, 7’si (% 35,0) adenokarsinom tanılı idi.
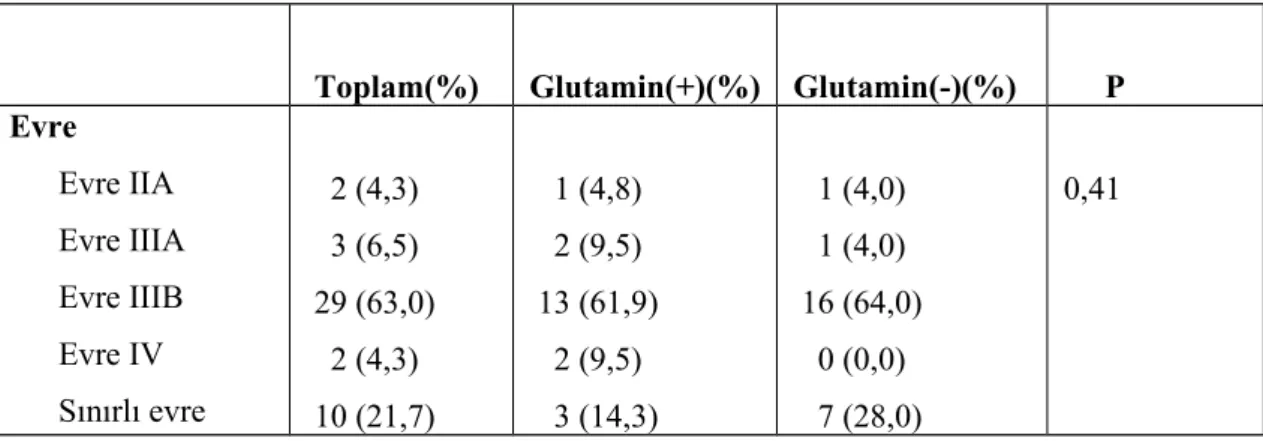
Toplam(%) Glutamin(+)(%) Glutamin(-)(%) P Evre Evre IIA Evre IIIA Evre IIIB Evre IV Sınırlı evre 2 (4,3) 3 (6,5) 29 (63,0) 2 (4,3) 10 (21,7) 1 (4,8) 2 (9,5) 13 (61,9) 2 (9,5) 3 (14,3) 1 (4,0) 1 (4,0) 16 (64,0) 0 (0,0) 7 (28,0) 0,41
Tablo 13: Her iki gruptaki hastaların evrelere göre dağılımı
Evre: Grup 1’de evre IIA 1 hasta (% 4,8), evre IIIA 2 hasta (% 9,5), evre IIIB 13 hasta (% 61,9), evre IV 2 hasta (% 9,5) ve sınırlı evre olan 3 hasta (% 14,3), 2.grupta evre IIA 1 hasta (% 4,0), evre IIIA 1 hasta (% 4,0), evre IIIB 16 hasta (% 64,0), evre IV olan hasta yoktu ve sınırlı evre olan 7 hasta (% 28,0) belirlendi. Her iki grup arasında evreleri açısından istatistiksel olarak anlamlı farklılık bulunamamıştır (p:0,41).
Toplam(%) Glutamin(+)(%) Glutamin(-)(%) P Tedavi seçimi Eşzamanlı KRT RT 38 (82,6) 8 (17,4) 16 (76,2) 5 (23,8) 22 (88,0) 3 (12,0) 0,43
Tablo 14: Her iki gruptaki hastaların tedavi seçimlerine göre dağılımı
Tedavi seçimi: Glutamin verdiğimiz 1.grupta RT ile birlikte eşzamanlı KT alan 16 hasta (% 76,2), sadece RT alan 5 hasta (% 23,8), 2.grupta RT ile birlikte eşzamanlı KT alan 22 hasta (% 88,0), sadece RT alan 3 hasta (% 12,0) tespit edildi. Her iki grup arasında eş zamanlı KT eklenip eklenmemesi açısından istatistiksel olarak anlamlı farklılık bulunamamıştır (p:0,43).