Yoğun bakım ünitesinde akut böbrek yetmezliği gelişen hastalarda mortaliteyi etkileyen faktörler
Tam metin
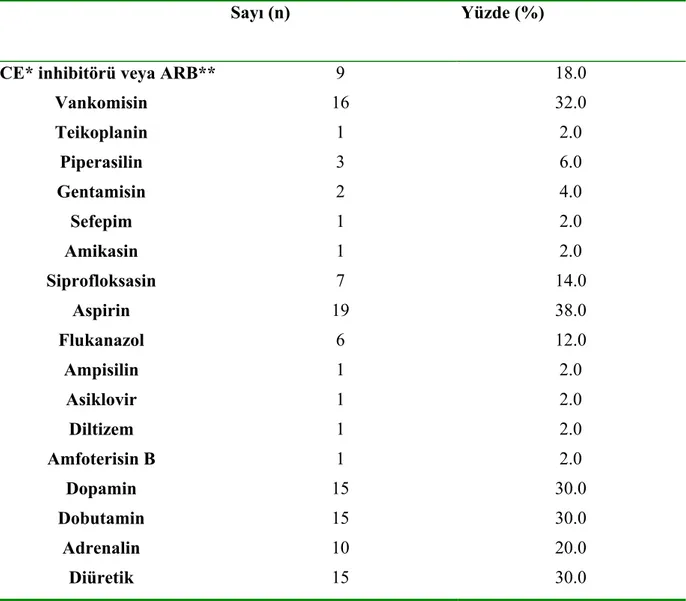
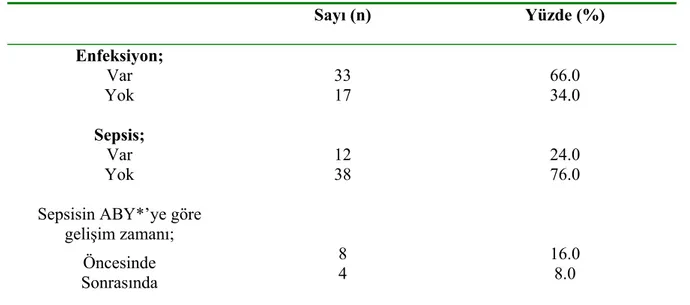
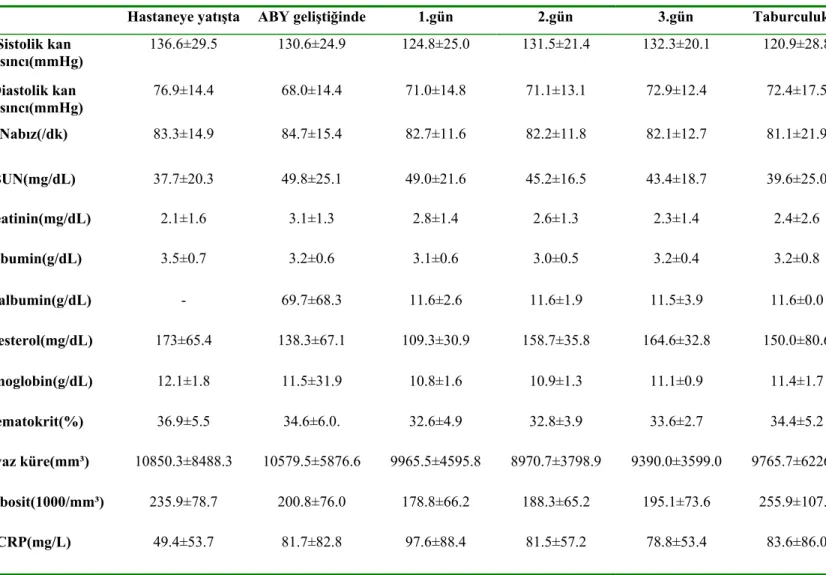
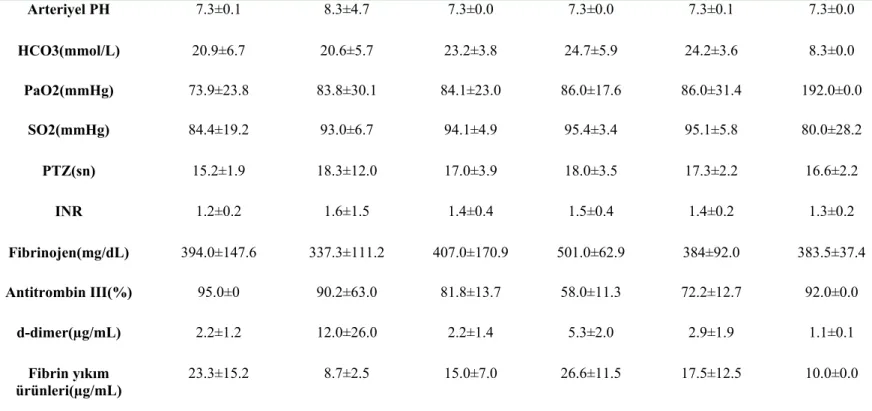
Şekil
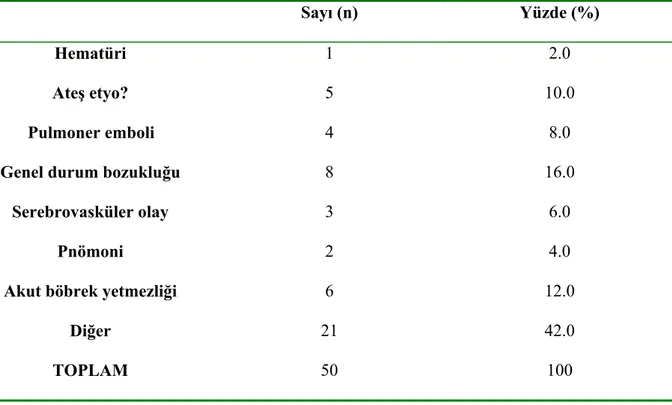
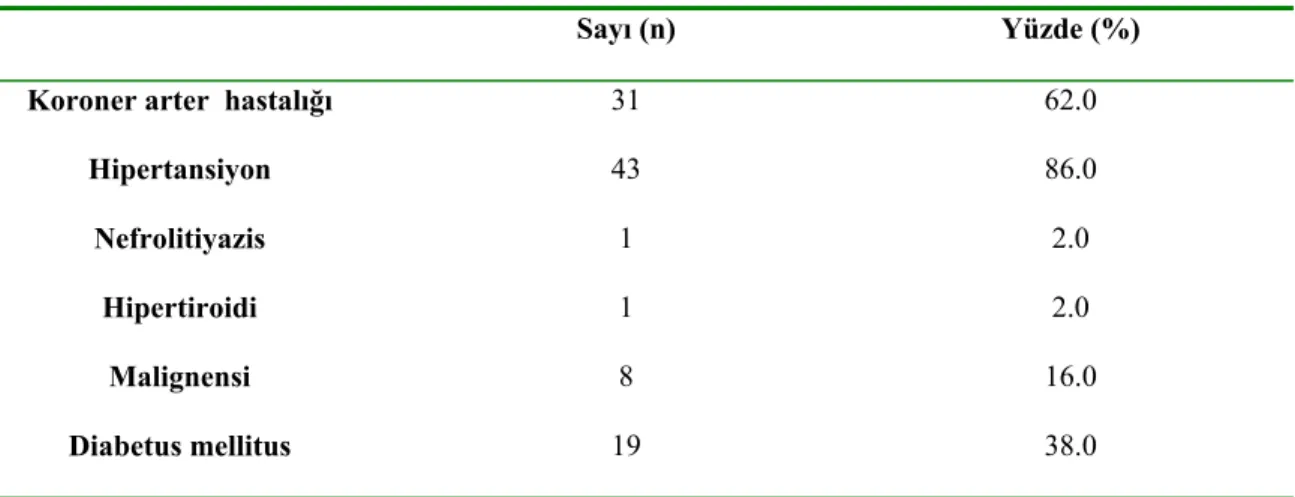
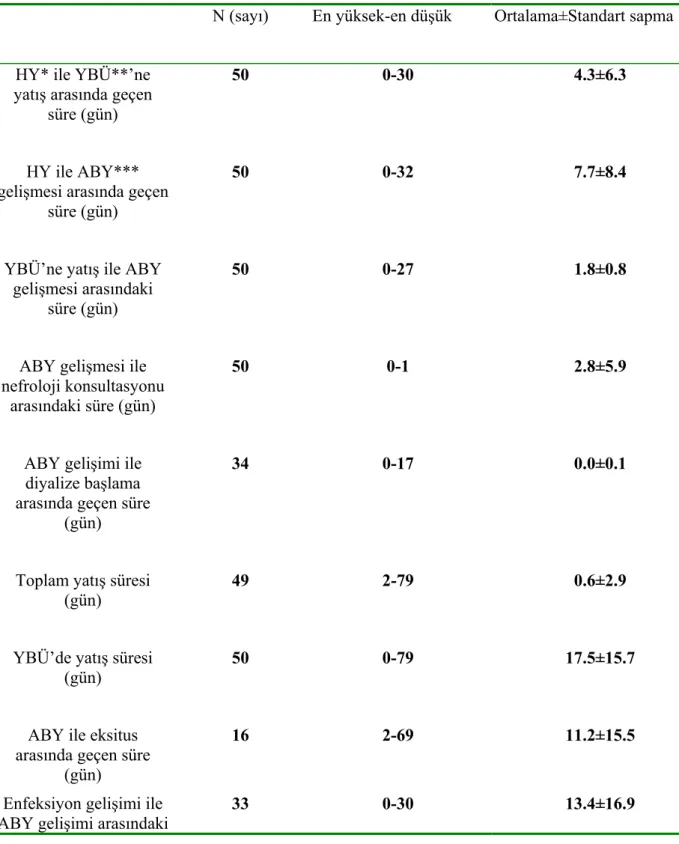

Benzer Belgeler
Karşılaştırma sonucunda, günlük ortalama glukoz, insülin ve insülin direnci (HOMAIR) değerleri eksitus olan grupta istatiksel olarak anlamlı olacak şekilde daha
ABSTRACT Objective: The aim of this study was to identify the frequency of intensive care unit- acquired paresis (ICU-AP) and predisposing factors for muscle weakness in our
Sonuç olarak, kardiyoloji yoğun bakımda yatan hastalarda anksiyete ve depresyonun sık karşılaşılan bir sorun olduğu tespit edilmiş olup hastaların klinisyen
The patients with A.baumannii infections were grouped as “died” and “survived” cases, and the groups were compared according to following factors: age, gender, isolation day
Bu, bütün Balkanlardaki Ortodoks halkları için örnek oldu ve bağımsız hale gelen her Ortodoks devlet Patrikhane’den bağımsız kiliselerini oluşturdu.
Islak, dolu, resimden fırlayacak gibi gözler.. Işık olmuş, göz yaşı olmuş
Summary : Ventricular flutter and fihrilation was diagnosed by means of ECG in a calf ısuffe.ring from diCllrrheıa for tihree days.. The caH ıwas dehydrated,
Sonuç olarak, koyunlarda paratuberkülozisin teşhisinde klinik ve patolojik muayeneler ile birlikte, total protein, albumin, kalsiyum ve magnezyum gibi serum