Trakya Bölgesinde yetişen cirsium creticum ( lam.) D’ urv. subsp. creticum (asteraceae) bitkisinin fitokimyasal incelenmesi ve antioksidan aktivitesinin tayini
Tam metin
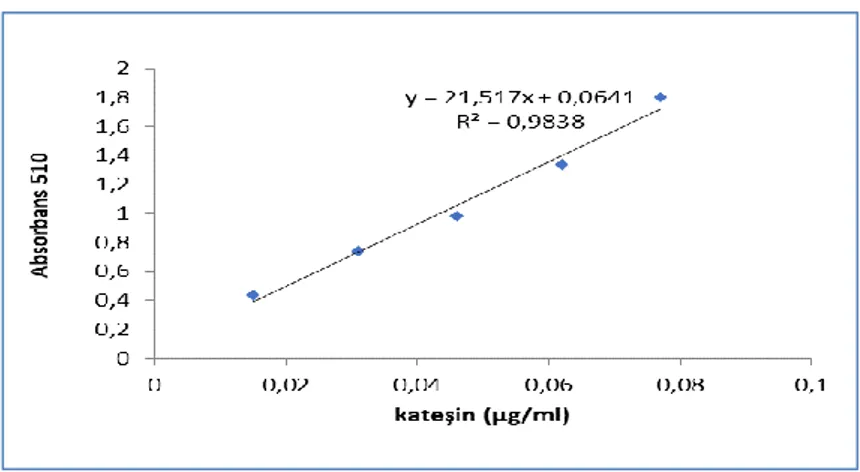
Şekil




Benzer Belgeler
The proposed RB-based method enables the use of existing 2-way GPVS tools that support fixed vertices for solving the oGPVS problem and hence the A -to- A BDO permutation
The rate of missed work due to elbow pain was significantly higher among neurosurgeons who predominately performed spinal surgeries (58.5%), with 65.9% of those who reported
In this present study aimed to determine CAM use and correlates of CAM use in a rural area, the method used to minimize the number of the errors likely to result from disremembering
In vitro degradation studies of homo PCL, PLina-g-PCL and PLina-g-PSt-g-PCL copolymers were carried out enzy- matically in the presence of Pseudomonas lipase according to a
CMV IgG seropo- zitiflik oranlarının sağlıklı kontrol grubunda %48.6 (68/140), şi- zofreni grubunda ise %81.3 (109/134) olarak dağıldığı ve sağ- lıklı kontrol grubu
Bunu kuramsallaştıran adımlardan birisi olan Temsili Bürokrasi de, çeşitli toplumsal kesimlerin yönetim içinde temsil edilmesi veya geniş toplumsal grupların
Bu çalıĢmada flavonoidlerin, insan meme kanseri hücresi MCF-7 hücrelerinin proliferasyonunu doz ve zaman bağımlı olarak inhibe ettiğini gerçek zamanlı hücre
Üçüncü bir alt başlıkta, Modern sanat eleştirisinde imge-anlam ilişkisine, H.Wölfflin' den imgeye bakışla, temel kavramlar alanında çalışmalarına,