Ratlarda karaciğer iskemi reperfüzyon hasarına deksmedetomidinin etkisi
Tam metin
Şekil


Benzer Belgeler
Roth (1992, s.18) tarafından çevre okuryazarlığı; bireyin çevre ve çevresel problemlere yönelik bilgi, çevreye ve çevre sorunlarına yönelik tutum, beceri, çevre
Almanca, Biyoloji, İngilizce, Kimya, PDR, Tarih, Türk Dili ve Edebiyatı ve Türkçe Öğretmenliği bölümlerinde öğrenciler 1 saatten az; Din Kültürü ve Fizik
Sonuç olarak bu bulgular eþliðinde mortaliteyi ve morbiditeyi azaltmadýðý ve çok pahalý bir tedavi olduðu için daha geniþ sayýda çocuk hastanýn alýndýðý
Developmental studies of the duodenum, jejunum and ileum as well as investigations of diet-based structural modifications of the small intestine were carried out in the rats using
Yukarıda mevcut olan genel bilgiler ışığında çalışmamızın amacı görece geniş katılımlı bir prospektif izlem tasarımında GDM’li hastalarda postpartum
Rektum kanserinin lokal rekürrensi sıklıkla inkürabldır. Bununla birlikte hastaların yaşam kalitesini oldukça etkilemektedir. Bu yüzden rektum kanserinde cerrahın
Measurement Of Electromagnetic Radiation Emitted By Dect Phones Used In Office Environments And Evaluation Of The Results In Terms Of Occupational Health And Safety..
Kıyıları karşılıklı veya yan yana olan devletlerin arasındaki münhasır ekonomik bölge sınırlandırılması hakça çözüm bulmak amacıyla UAD
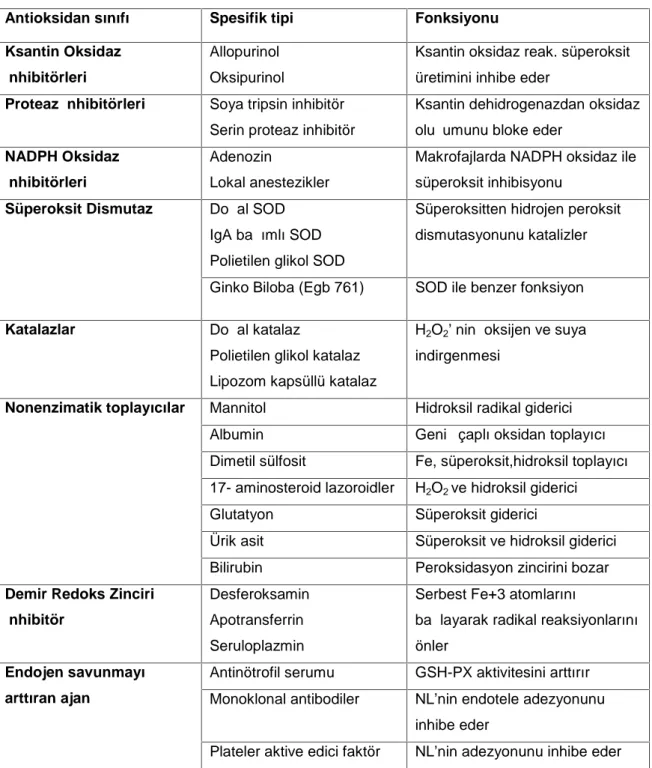
![Tablo 5: Karaciğer dokusunda MDA, SOD, KAT, GSH-Px ve GSH düzeyleri [ortanca (min- (min-maks), ortalama ± SD]](https://thumb-eu.123doks.com/thumbv2/9libnet/2994690.1297/44.892.129.809.557.837/tablo-karaciger-dokusunda-gsh-duzeyleri-ortanca-maks-ortalama.webp)