FEN B MLER ENST TÜSÜ
FAZ TRANSFER KATAL ZÖRÜ OLAB LECEK KAL KSAREN TÜREVLER N SENTEZ VE SEÇ LM
REAKS YONLARDA UYGULAMALARI
Ezgi AKCEYLAN
DOKTORA TEZ Kimya Anabilim Dal
Ocak-2011 KONYA Her Hakk Sakl r
iv
DOKTORA TEZ
FAZ TRANSFER KATAL ZÖRÜ OLAB LECEK KAL KSAREN
TÜREVLER N SENTEZ VE SEÇ LM REAKS YONLARDA
UYGULAMALARI
Ezgi AKCEYLAN
Selçuk Üniversitesi Fen Bilimleri Enstitüsü Kimya Anabilim Dal
Dan man: Prof. Dr. Mustafa YILMAZ 2011, 189 Sayfa
Jüri
Prof. Dr. Mustafa YILMAZ Prof. Dr. Mehmet SEZG N
Prof. Dr. Abdulkadir SIRIT Doç. Dr. Hasalettin DEL GÖZ Doç Dr. Ahmet KOÇAK
Bu çal ma kaliks[4]arenin fenolik birimlerinin p-pozisyonundan ve fenolik-O üzerinden farkl gruplarla fonksiyonland lm türevlerinin sentezi ve bu bile iklerin baz reaksiyonlarda kataliz uygulamalar içermektedir.
Sentez çal malar nda, literatürde belirtilen metoda göre p-terbütilkaliks[4]aren (1) sentezlendikten sonra, tersiyer bütil gruplar dealkilasyonla giderildi. Kaliks[4]aren (2), metil bromoasetat ile uygun ko ullarda etkile tirilerek diester türevine (3) dönü türüldü. Kaliksarenin diester türevi önce karboksilik asit türevine, daha sonra tiyonil klorür ile asitklorür türevine ve daha sonra da farkl aminlerle (N-etilpiperazin, 1,4-dioksa–8-azaspiro[4,5]dekan, 3-morfolin-1-propilamin, diallilamin, dibütilamin ve tersiyerbütilamin) etkile tirilerek amit türevleri (6, 7, 8, 9,10 ve 11) sentezlendi. Di er bir emada ( ekil 3.2) kaliks[4]arenin dibrom bile i ile N-etilpiperazin ve 1,4-dioksa–8-azaspiro[4,5]dekan ile etkile tirilerek amin bile ikleri elde edildi (13, 14). Kaliks[4]arenin fenolik birimlerinin p-pozisyonundan de ik dialkil amin türevlerini sentezlemek amac yla seçimli dealkilleme i lemi yap ld . Elde edilen bu bile ik (17) farkl sekonder aminler kullanarak Mannich reaksiyonuna göre dialkil amin türevli kaliksarenlere (18, 19 ve 20) dönü türüldü. Ba ka bir emada ( ekil 3.4) kaliksarenin fenolik birimlerinin p-pozisyonundan de ik tetra alkil amin türevleri sentezlendi. Bile ik 2 Mannich reaksiyonuna göre p-pozisyonundan tek basamakta de ik sekonder aminler ve formaldehit ile tepkimeye sokularak alkil amino kaliksarenler (21 ve 22) sentezlendi. Sentezlenen bu bile ikler esterle me reaksiyonlar nda faz transfer katalizörü olarak kullan ld .
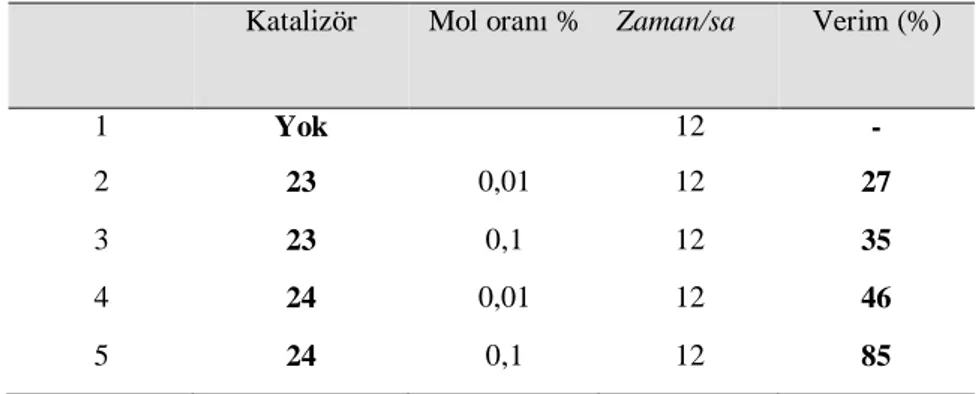
Ayr ca kaliks[4]arenin diamit türevleri (6, 10 ve 11) H2SO4 ortam nda sülfolanarak suda çözünebilen p-sülfonatokaliks[4]arenler (23, 24 ve 25) sentezlendi. 6 ve 9 nolu kaliksarenler CH3I ile etkile tirilerek kuaterner amonyum bile iklerine (26, 27) dönü türüldü. Sentezlenen 23, 24, 26 ve 27 nolu, kaliksaren bile ikleri Mannich-tipi tepkimelerde katalizör olarak kullan ld .
Sentezlenen makrosiklik bile iklerin yap lar spektroskopik teknikler (FTIR, 1H NMR ve 13 C-NMR) ile ayd nlat ld .
Anahtar Kelimeler: Kaliks[4]aren, suda çözünen kaliksarenler, faz transfer reaksiyonu,
v Ph.D THESIS
SYNTHESIS OF CALIXARENE DERIVATES FOR PHASE TRANSFER CATALYSIS AND UTILIZATION OF SELECTED SOME REACTIONS
Ezgi AKCEYLAN
THE GRADUATE SCHOOL OF NATURAL AND APPLIED SCIENCE OF SELÇUK UNIVERSITY
THE DEGREE OF DOCTOR OF PHILOSOPHY IN CHEMISTRY
Advisor: Prof. Dr. Mustafa YILMAZ 2011, 189 Pages
Jury
Prof. Dr. Mustafa YILMAZ Prof. Dr. Mehmet SEZG N
Prof. Dr. Abdulkadir SIRIT
Assoc. Prof. Dr. Hasalettin DEL GÖZ Assoc. Prof. Dr. Ahmet KOÇAK
This study contains synthesis of calix[4]arene derivatives which functionalized from p-position and phenolic-O, and utilization of selected some catalysis reactions.
In the synthetic work, the synthesis of p-ter-butylcalix[4]arene 1 and dealkyllation of this compound were made according to the literature metods. Calix[4]arene (2) was converted to diester derivative (3) with methylbromoacetate in suitable condition. Calix[4]arene diester derivative was firstly converted to carboxylic acid derivative, afterwards acid chloride derivative with thionyl chloride and then treated with various amines (N-ethylpiperazine, 1,4-dioxa–8-azaspiro[4,5]decane, 3-morpholinopropyl amine, diallylamine, dibutylamine and tertiarybutylamine) in order to synthesize amide (6,7,8,9,10 and
11) derivatives. In another schema (Figure 3.2), calixarene dibromide derivative was treated with
N-ethylpiperazine and 1,4-dioxa–8-azaspiro[4,5]decane to obtain amine (13, 14) derivatives. For synthesized different dialkyl amine derivatives on p-position of phenolic unit of calix[4]arene, selective dealkyllation. The compound 17 was treated with various secondary amine for synthesized dialkylamine derivative calixarenes (18, 19 and 20). In another work (Figure 3.4), compound 2 was treated with various secondary amine and formaldehyde in one step according to the Mannich reaction to obtain alkyl amine calixarenes (21, 22). The synthesized compounds were used in esterification reaction as the phase transfer catalyst.
Calix[4]arene diamide derivatives (6, 10 and 11) were reacted with H2SO4 to obtain p-sulfonatocalix[4]arene (23, 24 and 25). Compound 6 and 9 were reacted with CH3I for synthesized quaternary onium compounds (26, 27). The synthesized compounds 23, 24, 26 and 27 were used as catalyst in Mannich-type reactions.
The molecular structures of the synthesized macrocyclic compounds were characterized by spectroscopic techniques (FTIR,1H NMR and13C-NMR).
Keywords: Calix[4]arene, water soluble calixarenes, phase-transfer reaction, catalyst, Mannich
vi
Bu çal ma Selçuk Üniversitesi Fen Fakültesi Kimya Bölümü ö retim üyelerinden Prof. Dr. Mustafa YILMAZ’ n dan manl nda haz rlanarak Selçuk Üniversitesi Fen Bilimleri Enstitüsü’ne doktora tezi olarak sunulmu tur. Bu çal ma ayn zamanda S.Ü. Bilimsel Ara rma Projeleri Koordinatörlü ü taraf ndan 08101023 no’lu proje olarakdesteklenmi tir.
Tez konumun seçiminde, haz rlanmas nda ve yürütülmesinde bana destek veren, beni yönlendirip yard mlar eksik etmeyen sayg de er hocam Say n Prof. Dr. Mustafa
YILMAZ’a te ekkürlerimi sunar m. Ayr ca Tez zleme Komitesi’nin (T K) üyesi hocalar m Say n Prof. Dr. Abdulkadir SIRIT’a ve Say n Doç. Dr. Hasalettin DEL GÖZ’e göstermi olduklar ilgiden dolay te ekkürlerimi sunar m.
Tez çal malar m boyunca bana laboratuvar imkân sa layan Kimya Bölüm Ba kan Say n Prof. Dr. brahim KARATA ’a ve Selçuk Üniversitesi Fen Fakültesi Kimya Bölümü’nde görev yapan çok de erli hocalar ma te ekkür ederim. Ayr ca bu
çal may BAP 08101023 nolu proje ile destekleyen Selçuk Üniversitesi Bilimsel Ara rma Proje Koordinatörlü ü’ne dete ekkürlerimi sunar m.
Çal malar mda bana destek veren ve yard mlar gördü üm, Ar . Gör. Özlem AH N’e, Ar . Gör. Arzu UYANIK’a, Uzman Serkan ERDEM R’e, Ar . Gör. Dr. Begüm TABAKCI’ya, Uzman Selahattin BOZKURT’a, Ar . Gör. Dr. Elif YILMAZ’a, Enise AKÖZ’e, Tuba AKSOY’a, Mustafa ASLAN’a, Kübra ETÇ ’ye, brahim UYANIK’a, Serkan SAYIN’a, Ali Osman KARATAVUK’a ve di er Kimya Bölümü ara rma görevlisi arkada lar m ile yüksek lisans ve doktora ö rencilerine te ekkür ederim.
Ayr ca tez çal mam boyunca ihmal etti im o lum Mustafa Mert AKCEYLAN’a, bana büyük sab r gösteren, yard mlar esirgemeyen hayat arkada m, im Hakan AKCEYLAN’a ve beni yeti tiren, manevi deste ini esirgemeyen babam Münür ALTUNEL ve annem Öznur ALTUNEL’e ve . Nida AH N’e sonsuz te ekkürlerimi sunar m.
Ezgi AKCEYLAN
viii
ÖZET ……. ... iv
ABSTRACT ... v
ÖNSÖZ……... vi
NDEK LER ... viii
1. G ……. ... 1
1.1. Kaliksarenlerin simlendirilmesi ... 4
1.2. Kaliksarenlerin Sentezi ... 5
1.3. Kaliksarenlerin Spektral Özellikleri ... 8
1.3.1. Kaliksarenlerin NMR spektrumlar ve konformasyonlar ... 8
1.3.2. Kaliksarenlerin infrared spektrumlar ... 10
1.3.3. UV spektrumlar : ... 12
1.4. Kaliksarenlerin Baz Fiziksel Özellikleri ... 12
1.5. Suda Çözünen Kaliksarenler ... 12
1.6. Kaliksarenlerin Fonksiyonland lmas ... 15
1.6.1. Kaliksarenlerin fenolik OH üzerinden fonksiyonland lmas ... 15
1.6.2. Kaliksarenlerin p-pozisyonlar ndan fonksiyonland lmas ... 17
1.6.2.1. p-Alkil kaliksarenlerin dealkilasyonu ... 17
1.6.2.2. Elektrofilik sübsitüsyon ... 18 1.6.2.3. p-Clasien Çevrilmesi ... 18 1.6.2.4. p-Klormetilasyon Yolu ... 18 1.6.2.5. p-Kinonmetit Yolu ... 19 1.6.3. pso sübstitüsyon ... 20 1.7. Polimerik Kaliksarenler ... 21
1.8. Kaliksarenlerin Uygulama Alanlar ... 23
1.8.1. Kaliksarenlerin molekül / iyon ta olarak kullan lmas ... 24
1.8.2. Elektrot ve sensör çal malar ... 28
1.8.3. Membran çal malar ... 30
1.8.4. Monolayer çal malar ... 30
1.8.5. Enzim mimik çal malar ... 31
1.8.6. Kromotografi çal malar nda kolon dolgu materyali olarak ... 32
1.8.7. Kiral kaliksarenler ve kiral tan nma çal malar ... 34
2. KAYNAK ARA TIRMASI ... 36
2.1. Katalizörlerin S fland lmas ... 38
2.1.1. Biyokatalizörler ... 38
2.1.2. Homojen katalizörler ... 39
2.1.3. Asit-baz katalizörleri ... 40
2.1.4. Faz transfer katalizörleri ... 41
2.1.4.1. Faz transfer katalizörlerinin genel s fland lmas ... 43
2.1.4.2. Faz transfer katalizörlü reaksiyonlar n mekanizmas ... 45
2.1.4.2.1. S -S reaksiyonlar n mekanizmas ... 46
2.1.4.2.2. Kat -S reaksiyonlar n mekanizmas ... 49
2.1.4.2.3. Üç faz reaksiyonlar ... 50
2.1.4.2.4. Molekülün transferiyle gerçekle en reaksiyonlar ... 51
2.1.4.2.5. Ters faz katalizörleri ... 51
2.1.4.3. Faz Transfer Katalizörlü Reaksiyonlara Etki Eden Faktörler ... 51
2.1.4.4. Endüstride faz transfer katalizörleri ... 53
ix
3.2. Kimyasal Sentezler ve Karakterizasyon ... 65
3.2.1. 5,11,17,23-Tetra-t-bütil-25,26,27,28-tetrahidroksikaliks[4]aren (1) ... 67
3.2.2. p-ter-Bütilkaliks[4]arenin dealkilasyonu (2) ... 67
3.2.3. 25,27-Dimetoksikarbonilmetoksi-26,28- dihidroksikaliks[4]aren (3)... 68
3.2.4. 25,27-dimetoksikarbonilmetoksi-26,28- dihidroksi-kaliks[4]aren (3)’nin hidrolizi (4) ... 69
3.2.5. 25,27-diklorokarbonilmetoksi-26,28-dihidroksi-kaliks[4]aren (5) ... 69
3.2.6. Kaliksaren amit türevlerinin sentezi için genel prosedür ... 70
3.2.7. 25,27-Diklorokarbonilmetoksi-26,28-dihidroksi-kaliks[4]aren (5) ile N-etilpiperazin’in etkile tirilmesi (6) ... 70
3.2.8. 25,27-Diklorokarbonilmetoksi-26,28-dihidroksi-kaliks[4]aren (5) ile (1,4-dioksa-8-azaspiro[4,5]dekan’ n etkile tirilmesi (7)... 70
3.2.9. 25,27-Diklorokarbonilmetoksi-26,28-dihidroksi-kaliks[4]aren (5) ile 3-morfolin 1-propilamin’in etkile tirilmesi (8) ... 71
3.2.10. 25,27-Diklorokarbonilmetoksi-26,28-dihidroksi-kaliks[4]aren (5) ile diallil amin’in etkile tirilmesi (9) ... 72
3.2.11. 25,27-Diklorokarbonilmetoksi-26,28-dihidroksi-kaliks[4]aren (5) ile dibütilamin’in etkile tirilmesi (10) ... 72
3.2.12.25,27-Diklorokarbonilmetoksi-26,28-dihidroksi-kaliks[4]aren(5) ile tersiyerbütilamin’inetkile tirilmesi(11) ... 73
3.2.13. 25,27-Bis(3-bromopropoksi)-26,28dihidroksi kaliks[4]aren ... 75
3.2.14. 25,27-Bis (3-bromopropoksi)-26,28 dihidroksi 5,11,17 tetra(tertbütil) kaliks[4]aren ile N-etilpiperazin’in etkile tirilmesi (13) ... 75
3.2.15. 25,27-Bis(3-bromopropoksi)-26,28dihidroksi 5,11,17tetra(tertbütil) kaliks [4] aren ile 1,4-dioksa–8-azaspiro[4,5]-dekan’ n etkile tirilmesi (14) ... 76
3.2.16. 5,11,17,23-Tetra-t-bütil-26,28-Bis[benzoiloksi]kaliks[4]aren-25,27-diol (15) ... 79
3.2.17. 5,17, Di-t-bütil-26,28-Bis[benzoiloksi]kaliks[4]aren-25,27-diol (16) ... 79
3.2.18. 5,17-Di-ter-bütil-25,26,27,28-tetrahidroksikaliks[4]aren (17)... 80
3.2.19. 17 nolu bile in Mannich reaksiyonuna göre etkile tirilmesi için genel prosedür ... 81
3.2.20. 5,17,Di-ter-bütil-11,23-Bis[(N-etilpiperazino)metil]-25,26,27,28-tetra-hidroksikaliks [4]aren (18). ... 81
3.2.21. 5,17,Di-ter-bütil-11,23-Bis[(diallilamino)metil]-25,26,27,28-tetra -hidroksikaliks [4]aren (19). ... 81
3.2.22. 5,17,Di-ter-bütil-11,23-Bis[(4-benzilpiperidin) metil]-25,26,27,28- tetra-hidroksikaliks [4]aren (20). ... 82
3.2.23. 5,11,17,23-Tetrakis[(N-etilpiperazino)metil]-25,26,27,28-tetrahidroksi kaliks[4]aren ... 84
3.2.24. 5,11,17,23-Tetrakis[(etil-4-piperidinkarboksilto)metil]-25,26,27,28 -tetrahidroksi kaliks [4]aren ... 84
3.2.25. Suda çözünen kaliks[4]arenler için genel prosedür ... 87
3.2.26. Bile ik 23 ... 87
3.2.27. Bile ik 24 ... 87
x
3.2.30. Bile ik 6 ile CH3I’ün etkile tirilmesi ... 90
3.2.31. Bile ik 8 ile CH3I’ün etkile tirilmesi ... 90
3.2.32. 1,3-Difenil-3-fenilamino-propan-1-on (26) ... 91
4. ARA TIRMA SONUÇLARI VE TARTI MA ... 92
4.1. Kaliksaren Bile iklerinin Sentezi ... 92
4.1.1. Kaliksarenin Fenolik OH Üzerinden Fonksiyonland lmas ... 93
4.1.1.1. Amit Türevli Kaliksarenlerin Sentezi... 93
4.1.1.2. Amin türevli kaliksarenlerin sentezi ... 97
4.1.2. Kaliks[4]arenin fenolik birimlerinin para pozisyonundan seçimli fonksiyonland lmas ... 99
4.1.2.1. Suda Çözünen Kaliks[4]aren Türevlerinin Sentezi ... 103
4.1.3. Kaliks[4]aren’in kuaterner amonyum türevlerinin sentezi ... 104
4.2. Faz Transfer Çal malar ... 105
4.2.1. Esterle me Reaksiyonu ... 106
4.2.2. S cakl n p-nitrobenzil bromür ile sodyum bütirat aras ndaki reaksiyona etkisi ... 115
4.3. Mannich Tipi Reaksiyonda Kaliksaren Türevlerinin Kullan lmas ... 119
4.3.1. Asidik Mannich tipi reaksiyon ... 121
4.3.2. Bazik Mannich Tipi Reaksiyon ... 122
5. SONUÇLAR VE ÖNER LER ... 124
6. KAYNAKLAR ... 126
EKLER…….. ... 138
1.
Organik kimya literatüründe yüzlerce s f ve milyonlarca bile ik yeralmaktad r ve her geçen gün bu say h zla artmaktad r. Bu s flardan, supramoleküller son y llarda kimyac lar n dikkatini oldukça çekmi ve önemli bir yere sahiptir. En az dokuz üyeli ve en az üç heteroatomlu halkal bile ikler makrosiklik bile ik olarak kabul edilmektedir. Bunlara örnek taç (crown) eterler (Pedersen 1967, 1988 a,b, zatt 1992), kriptantlar (Lehn 1995, 1988 a,b ), siklofanlar (Vögtle 1993) ve do al siklodekstrinler (Bender 1978, Szejtle 1998) verilebilir. Makrosiklik bile iklerle ilgili en büyük at m, 1967 nda C.J. Pedersen’in taç eterlerle ilgili yapt çal malard r. Pedersen, bu çal malar yla 1987’de Nobel Kimya ödülünü alm r. Son y llarda, taç eterler ve do al bir glikoz oligomeri olan siklodekstrinlerden sonra halkal yap da bir fenol-formaldehit oligomeri olan “KAL KSARENLER” ortaya ç km r. ekil 1.1). Bu bile ikler, di er makrosiklik bile iklerden daha kolay sentezlenip fonksiyonland labilmektedirler. Kaliksarenler supramoleküler kimyada, makrosiklik bile ikler içerisinde son y llardaki en popüler bile ikler s nda kalmay sürdürmektedir.
n O O HO O OH OH O O OH OH HO O O OH OH HO O HO O HO OH O HO O HO OH O OH HO OH O O O O O O O HO OH R R HO OH R R n R = H / alkil
Siklodekstrin Taç (Crown) eter Kaliksaren
ekil 1.1.Siklodekstrin, taç (crown) eter ve kaliks[n]aren'in gösterimi .
Kaliksarenler metasiklofan s ndand r ve ismini ekli vazoya benzedi inden, Yunanca taç, vazo anlam na gelen “Chalice” dan alm r. Kaliksarenlerde ‘calix’ kelimesi ‘vazo, taç’ anlam na gelirken ‘arene’ kelimesi ise aromatik halkalar n varl göstermektedir ( ekil 1.2).
Kaliks(calix) ve aren(arene) aras nda parantez içindeki rakam ise molekül bo lu unu olu turan metilen köprüleriyle birbirine ba fenolik birimlerin say göstermektedir.
ekil 1.2. Metasiklofan ve kaliks[4]arenin moleküler modelinin kupaya benzeyen görünümü
Kaliksarenler ilk olarak 1989 y nda Monographs in Supramolecular Chemistry
de yay nlanm r. O y ldan bu zamana kadar kaliksarenlere ilgi artm ve bu sahada çok zl bir geli me sa lanm r. Kaliksarenler 1989 y nda Gutsche taraf ndan yay nlanmas na ra men kökeni fenolik reçinelerin olu turulmas na yani oldukça eskileri dayanmaktad r. 1872 y nda Alman organik kimyac olan Adolph von Baeyer sulu formaldehit ile fenolü tarak oldukça sert reçinemsi ve kristal olmayan bir ürün elde etmi , fakat o günlerdeki enstrümantal tekniklerinin k tl olmas sebebiyle yap tam olarak ayd nlat lamam , dolay yla bu ürün ticari ve teknik olarak kullan lamam r. 1905–1909 y llar aras nda Leo Hendrick Baekeland fenol-formaldehitten ticari öneme sahip bakalit olarak bilinen plasti i elde etmeyi ba arm r. 20. yüzy ldaki bu ba ar endüstriyel ve akademik ara lar n fenol formaldehit kimyas na ilgisini daha da artt rm r. Zinke ve Ziegler isimli bilim adamlar bakalit prosesi üzerindeki çal malar yo unla rarak para-sübstitüe fenoller ile formaldehitin vermi oldu u kondenzasyon reaksiyonunu ayd nlatmak için p-ter-bütil fenolü, sulu formaldehit ve sodyum hidroksit ile önce 50–55 oC da, daha sonra 110–120 oC da iki saat etkile tirdikten sonra süspansiyon olu turan bu maddeyi bezir ya içerisinde 200 oC ye kadar birkaç saat ld nda erime noktas yakla k olarak 340 oC olan bir madde elde ettiler. p-Kresol,
p-ter-amil fenol gibi farkl fenoller kullan ld nda ise, ayn i lemleri takip etmek suretiyle çok sert, yüksek erime noktas na sahip ürünler elde ettiler. Zinke elde edilen bu ürünlerin p-alkilfenolün sadece iki orto pozisyonu ile formaldehitin reaksiyonu sonucunda olu an lineer bir polimerin halkala mas yla elde edilen siklik tetramer yap da saf bir bile ik oldu unu iddia etti. David Gutsche bu ürünün gerçekte bir tetramer olmay p, tetramer, hekzemer, oktamer ve bir miktar da lineer oligomer kar
oldu unu ispatlad . Daha sonra Gutsche ve arkada lar p-ter-bütilfenol ile formaldehitin kondensasyonu sonucunda siklik tetramer, hekzamer ve oktameri ayr ayr saf olarak yüksek verimle elde etmeyi ba arm r. Profesör Gutsche, çal malar siklik oligomerik bile ikler üzerinde yo unla rd ve bu tür siklik tetramerleri ( ekil 1.3), biyoorganik reaksiyonlar için sentetik enzim mimikleri olarak kullanmay tasarlad (Gutsche, 1989) .
ekil 1.3. p-ter-Bütilkaliks[4]aren'in farkl gösterimleri
Kaliksarenler ile ilgili 1982–2009 y llar aras ndaki yay nlanan makale say na bakt zda ( ekil 1.4) kaliksarenlerdeki büyük geli im görülmektedir. Kaliks[n]arenler, siklodekstrin ve crown eterlerden sonra üçüncü nesil bile ikler olarak bilinmektedir
.
ekil 1.4. 1982–2009 y llar aras nda yay nlanan makale da
p -ter-bütilkaliks[4]aren
R R R R OH OH HO OH HO HO OH O H 4 OH HO HO OH R: t-bütil1.1. Kaliksarenlerin simlendirilmesi
Kaliksarenler, fenolik birimlerin metilen köprüleriyle birbirine ba lanm siklik düzeninden olu an ve siklodekstrinlere benzeyen “[1n]metasiklofanlar” olarak fland r (IUPAC, 1970). Bu kelimenin kullan özellikle tetramer yap ile anla ld . Bu yap , tas veya a geni bir barda a benzer bir konformasyon gösterebilmektedir. ( ekil 1.3) Kaliksarenlerin tetramerik kaliks[4]aren den daha büyük hacimli ve daha esnek oktamerik kaliks[8]arene kadar be bilinen üyesi daha vard r. Bunlardan en yayg n olanlar tetramer, hekzamer ve oktamer üyeleridir ( ekil 1.5).
ekil 1. 5. Kaliks[n]arenlerin gösterimi
Kaliksarenler de ik ara rmac lar taraf ndan farkl isimlendirilmi lerdir. Bu tip bile ikler IUPAC sistemine göre adland lmas çok zor oldu undan Gutsche bu bile ikleri daha pratik bir yoldan isimlendirmi tir. Kaliks ve aren kelimelerinin aras ndaki kö eli parantez içine yaz lan “n” ifadesi ise fenolik birimlerin miktar yani makrosikli in büyüklü ünü gösterir. Onun için bu türden bile iklerin isimlendirilmesinde son y llarda, ya aromatik halka üzerindeki sübstitüentlerin yerlerini ifade eden numaraland rma sistemi kullan r, yada fenolün sübstitue k sm ile fenolik birimin say ifade eden isimlendirme sistemi kullan r. Aromatik halkaya herhangi bir sübstitüent ba oldu u durumlarda bu gruplar n isimleri kaliksaren kelimesinden önce yaz r. Böylece p-alkil fenolden olu an dört üyeli siklik tetramer yap daki bile ik; 5,11,17,23-tetra-ter-alkil–25,26,27,28-tetra hidroksi kaliks[4]aren veya k saca p-alkil-kaliks[4]aren olarak adland lmaktad r. Kaliksarenleri isimlendirirken daha çok basit ismi olan “Kaliks[n]arene” oldu u gibi kullan r ve bütün sübstitüentlerin yerleri ekil 1.6’da gösterildi i gibi numaralarla belirtilir.
OH HO HO OH OH HO OH OH OH HO OH OH HO OH HO OH HO OH p-t er -bütilkaliks[8]aren p-ter-bütilkaliks[6]aren p-t er -bütilkaliks[4]aren
ekil 1.6. Kaliks[n]arenlerin isimlendirilmesi
1.2. Kaliksarenlerin Sentezi
p-ter-Bütilkaliks[4]aren’in sentezini ilk olarak Zinke bir prosedür ile ortaya att .
Orijinal Zinke sentezinde p-alkilfenoller ile formaldehitin kondensasyonunu baz olarak NaOH kullanarak sa lad . Bu sentezde p-ter-bütil fenolden saf ürünler elde edilirken di er fenollerden az verimli, ayr lmas zor kar mlar elde edildi.
a- p-ter-Bütilfenol:
p-t-Bütilfenol’den sentezlenen üç önemli kalik[n]saren u ekilde
sentezlenmektedir;
p-t-Bütilkaliks[4]aren: Fenol ile HCHO ba olarak 0,045 e de er orana kar k gelen miktarda NaOH kar , 2 saat 110-120 oC’de r. Daha sonra bu ürün, 2 saat difenil eterle geri so utucu alt nda kar larak kaynat r.
p-t-Bütilkaliks[6]aren: Fenol ile HCHO ba olarak 0,34 e de er orana kar k gelen miktarda KOH kar , r. Daha sonra bu ürün, 3–4 saat ksilen ile geri so utucu alt nda kar larak kaynat r.
p-t-Bütilkaliks[8]aren: Fenol ile paraformaldehit’in 0,030 e de er orana kar k gelen NaOH ile ksilen ile r.
HO OH HO OH 1 2 3 4 5 6 7 8 11 17 23 25 26 27 28 OHHO HO H O HO OH OH OH HO OH OH HO HO OH 1 2 3 4 5 6 7 8 11 17 23 29 35 37 38 39 40 41 42 12 3 4 5 6 7 8 11 17 23 29 35 41 47 49 50 51 52 53 54 55 56 25,26,27,28-tetrahidroksi-kaliks[4]aren 36,37,38,39,40,41,42-hekzahidroksi-kaliks[6]aren 49,50,51,52,53,54,55,56-oktahidroksi-kaliks[8]aren (Kaliks[4]aren) (Kaliks[8]aren) (Kaliks[6]aren)
ekil 1.7. Kaliks[n]arenlerin sentezi
p-ter-Bütilkaliks[5]aren ilk olarak sadece % 3–5 verimle izole edilmi ti.
Günümüzde ise % 15–20 verimle elde edilebilmektedir. p-ter-Bütilkaliks[7]aren ise ilk olarak % 6 verimle elde edilirken u an baz olarak LiOH kullanarak % 11–17 verimle elde edilmektedir.
Kaliks[4]aren için baz n optimum miktar n kullan lmas gerekir. E er baz konsantrasyonu 0,03 ile 0,04 aras nda e de er miktarda kullan rsa ürün miktar n maksimum oldu u görülür. Yani baz konsantrasyonun etkisi ürün verimi için oldukça önemlidir. Siklik oktamer ve tetramerin eldesi için katalitik miktarda baz kullan tercih edilir. Siklik hekzamer için ise stokiyometrik oranda baz kullan lmal r.
Tetramer, hekzamer ve oktamerin sentezi için farkl alkali metal hidroksitleri kullan lm r ( ekil 1.7). Bir siklik hekzamer olan p-ter-bütilkaliks[6]aren’in RbOH kullan ld nda çok yüksek verimle elde edilmesi “template etki” nin bir sonucudur. Bu kaliksarenler üzerinde bulunan oksijen atomlar aras ndaki mesafenin ölçülmesi ile aç klanmaya çal lm r. Bu mesafe siklik tetramerde 0,8 A, siklik hekzamerde 2,0– 2,9 A, siklik oktamerde ise 4,5 A kadard r. Alkali metal katyonlar n iyon çaplar na
O H HO HO O H OH + HCOH OH HO OH OH O H HO OH OH HO O H HO O H HO OH p-t-bütilkaliks[8]aren p-t -bütilkaliks[6]aren p-t-bütilkaliks[4]aren NaOH KOH NaOH
göre siklik tetramer ve oktamer elde etmek için LiOH, NaOH, siklik hekzamer elde etmek için ise RbOH veya CsOH katyonlar tercih edilir.
b- Di er p-substitue fenoller:
Kaliksarenler, baz katalizli kondenzasyonu ile nitro-, siyano- ve 4-fenoksifenol, 4-hidroksibenzoik asit, 4-hidroksiasetofenon, 4-hidroksibenzil alkol, ve 1,4-dihidroksibenzen’den elde edilememesine ra men baz lar nda ba ar olunmu tur
ekil 1.8). OH OH R R HO OH R R n-3 2 n=4 3 n=5 4 n=6 5 n=7 6 n=8 t-Bu Me Et i-Pr (CH2)10Me a b c d e f g R R OH baz O 10 h i j k l R m n o p O O CH3 R 1
ekil 1. 8. p-Substituefenollerden kaliks[n]arenlerin sentezi
Bunlara örnek verecek olursak; p-kresol’den (1b) % 74 verimle 4b ve % 22 verimle 5b elde edilmi tir. Ayn ekilde, p-etilfenol (1c ) ve p-isopropilfenol’den (1d) 5c (% 27) ve 6d (% 3) elde edilmi tir. p-isopropenilfenolden (1e) kaliks[6]aren 4e ve kaliks[8]aren 6e kar elde edilmi tir. Çözücü olarak etilen glikol, baz olarak Na2B4O7
kullan lm r. Para pozisyonunda uzun alkil zinciri bulunan fenolden (1f) kaliks[6] ve [8] aren türevleri (4f ve 6f) elde edilmi tir. p-Fenilfenol’den de (1g) 4g, 5g ve 6g kar elde edilmi tir. p-Benziloksifenol’den (1h) % 48 verimle 6h elde edilirken yan nda az miktarda 5h ve 2h de elde edilir. p-Benzilfenol’den 1i, 5i (% 33), 4i (% 16) ve 6i (% 12) kar veya 3i ve 5i (% 15–20) kar elde edilmi tir.
Görüldü ü gibi p-ter-bütil fenol d ndaki di er alkil fenollerle yap lan sentezlerde ya çok dü ük verimli kaliksarenler ya da tek ürün yerine kar mlar elde edilmi tir. Bu fenolün kullan lmas n di er önemli bir avantaj ise ter-bütil gruplar n kolayl kla dealkilasyon yap larak kaliksarenden kolayl kla ayr labilmesidir (Gutsche, 1986a,1986b).
1.3. Kaliksarenlerin Spektral Özellikleri
1.3.1. Kaliksarenlerin NMR spektrumlar ve konformasyonlar
Sübstitue olmam kaliksarenler oda s cakl nda ve çözelti içerisinde hareketli bir konformasyona sahiptir. Bu konformasyonlar aril halkalar n a ve yukar yönlenmesinden dolay gerçekle mektedir. Kaliks[4]arenin 4 farkl konformasyonu vard r. Bunlar “koni”, “ smi koni”, “1,2-kar kl ”, “1,3-kar kl ” olarak adland r. Bir kaliks[4]arenin hangi konformasyonda oldu u bu bile in köprü Ar-CH2 –Ar
protonlar n1H-NMR spektrumlar na bak larak ay rt edilebilir. (Çizelge 1.1)
ekil 1. 9. Kaliksarendeki aksiyal ve ekvatoriyal protonlar n gösterimi
Aksiyal protonlar Ha ile gösterilirken, ekvatoriyal protonlar He ile gösterilir ekil 1.9). Aksiyal Ha protonlar dü ük alanda dublet verirken, ekvatoriyal He protonlar yüksek alanda dublet verir. 1,3-kar kl konformasyonundaki kaliksarenin NMR spektrumunda, köprü metilen protonlar tek singlet görülür çünkü Ha ve He de erdir. 1,2-kar kl ve k smi koni NMR’lar birbirine benzemekle beraber aromatik bölge protonlar n farkl klar yla birbirlerinden ayr labilirler.
Kaliksarenlerin konformasyonlar n 13C NMR spektrumlar na bak ld nda, aril gruplar n syn yönlendi i koni konformasyonunda köprü metilen karbonlar 31 ppm de sinyal verirken, aril gruplar n anti yönlendi i 1,3-konformasyonunda köprü metilen gruplar 37 ppm de rezonans sinyali verir ( ekil 1.10).
Çizelge 1. 1. Kaliks[4]aren'in Ar-CH2-Ar protonlar n1H-NMR spektrumlar
Konformasyon Ar-CH2-Ar protonlar Koni Bir çift dublet.
smi Koni ki çift dublet (1:1) veya bir çift dublet ve bir singlet (1:1) 1,2-Kar kl Bir singlet ve iki dublet (1:1)
1,3-Kar kl Bir singlet
OH
HO HO
OH
He Ha
ekil 1. 10. .p-ter-Bütilkaliks[4]aren'in konformasyonlar ve1H NMR,13C NMR ekilleri
Sübstitüe olmam kaliksarenlerin konformasyonel ara dönü ümünün ( ekil 1.11) azalt lmas için ba ca iki yol vard r (Gutsche, 1989).
a) Fenolik-O’den ve p-pozisyonundan büyük hacimli gruplar ba lamak b) Her bir aril halkas na molekül içi köprüler kurmak (Takeshita, 1995).
Konformasyonlar aras ndaki dönü üm h na sübstitüentlerin yan ra çözücüler de etki etmektedir. Kloroform, toluen, brombenzen ve karbondisülfür gibi çözücüler konformasyon dönü üm serbest enerjisini yükseltir. Bu da çözücünün kaliksarenlerle (endokaliks) kompleks olu turdu unu gösterir. Aseton ve asetonitril gibi çözücülerin bilhassa piridinin molekül içi hidrojen ba lar bozmas sebebiyle konformasyon dönü ümüne etkisinin büyük oldu u dü ünülmektedir (Gutsche, 1981).
Koni Ar-CH2-Ar Ar-CH2-Ar smi koni OH HO HO OH OHHOOH HO 3.0 5.0 5. 0 3. 0 Ar-CH2-Ar Ar-CH2-Ar 1,2-Kar l kl 1,3-Kar kl HO OH HO OH OH OH HO HO 3.0 5.0 3 .0 5. 0 30 36 39 33 30 36 39 33 30 36 39 33 30 36 39 33 13 C NMR 1 H NMR
ekil 1.11. Kaliksarenlerin konformasyonel ara dönü ümü
1.3.2. Kaliksarenlerin infrared spektrumlar
Kaliksarenlerin IR spektrumlar na bak ld nda ( ekil 1.12) fenolik –OH gruplar na ait 3150–3300 cm–1 de titre im band gözlenir. Parmak izi bölgesi ise özellikle 1500–900 cm–1 aras nda benzerdir, ancak 500–900 cm–1 bölgesinde farkl klar gözlenmektedir. Kaliks[5]aren için 693–571 cm–1 de, kaliks[6]aren için 762 cm–1 ve kaliks[7]aren de 796 cm–1karakteristik absorbsiyon bantlar görülmektedir. Fonksiyonlu kaliks[4] ve [6]arenlerin alkil eterleri s ras yla 850 cm–1 ve 810 cm–1 de güçlü absorbsiyon bantlar vermektedir.
Koni smi koni
OH HO HO OH OHHOOH HO 1,2-Kar kl 1,3-Kar l kl HO OH HO OH OH OH HO HO
upper rim dönmesi
4000,0 3600 3200 2800 2400 2000 1800 1600 1400 1200 1000 800 650,0 63,9 66 68 70 72 74 76 78 80 82 84 86 88 90 92 94 96 97,2 cm-1 %T 4000,0 3600 3200 2800 2400 2000 1800 1600 1400 1200 1000 800 650,0 53,0 56 58 60 62 64 66 68 70 72 74 76 78 80 82 84 86 88 90 92 94 96,4 cm-1 %T 4000,0 3600 3200 2800 2400 2000 1800 1600 1400 1200 1000 800 650,0 62,3 64 66 68 70 72 74 76 78 80 82 84 86 88 90 92 94 96 98,3 cm-1 %T
ekil 1.12. IR spektrumlar a- bütilkaliks[4]aren, b- bütilkaliks[6]aren, c-
p-ter-bütilkaliks[8]aren
a-
c-1.3.3. UV spektrumlar :
Spektroskopik özelliklerine bak ld zaman 261, 288 ve 318 nm’de kaliks[6]arene ait üç absorpsiyon piki gözlenir (Çizelge 1.2). Aromatik halkaya ait olan bu piklerden 288 nm’deki pik o kadar kuvvetlidir ki 318 nm’ deki piki örter. Kaliks[6]arenin konsantrasyonu art ld zaman spektrumda bir de iklik gözlenmez.
p-ter-butilkaliks[4]aren ve kaliks[4]arenin spektrumlar kaliks[6]arenin
UV-spektrumu ile benzerdir.
Çizelge 1. 2. Kaliks[n]arenlerin absorbsiyon de erleri
Bile ik 280 ± 1 nm 288 ± 1 nm Çözücü
p-ter-bütil kaliks[4]ren 9,800 7,700 CHCl3
p-ter-bütil kaliks[6]ren 15,500 17,040 CHCl3
p-ter-bütil kaliks[7]ren 18,200 20,900 CHCl3
p-ter-bütil kaliks[8]ren 23,100 32,000 CHCl3
1.4. Kaliksarenlerin Baz Fiziksel Özellikleri
Çözünürlükleri: Kaliksarenler kloroform, piridin, karbondisülfür, dimetil formamit ve dimetil sülfoksit gibi çözücülerde çözünürler. Organik çözücülerdeki çözünürlükleri, fonsiyonland larak art labilir. Ester ve eter türevli kaliksarenin organik çözücülerdeki çözünürlükleri fazlad r. Uygun türevlendirmeyle suda çözünen kaliksarenler de elde edilebilir.
1.5. Suda Çözünen Kaliksarenler
1984 y n ba lar nda Ungaro ve arkada lar suda çözünen
p-ter-bütilkaliks[4]aren’nin tetrakarboksimetil eteri sentezlemi lerdir. Suda karboksi kaliksarenlerden daha çok çözünen p-sülfonato kaliks[n]aren’ler 1984 lerin sonlar na do ru Shinkai ve arkada lar taraf ndan sentezlenmi tir. Amino grubu ta yan kaliksarenler de seyreltik asit çözeltisinde çözünmektedir.( ekil 1.13)
n CH2 OH SO3H n = 4, 6 ve 8 n CH2 OH n = 4, 6 ve 8 NR2 n CH2 OH n = 4, 6 ve 8 H2N
ekil 1. 13. Suda çözünen kaliksaren türevleri
Suda çözünen kaliksarenlere ba ka örnek verecek olursak; Consoli ve grubu (2007) fenolik OH’larda dört nükleotid (timin veya adenin) grubu olan suda çözünen kaliksaren türevlerini sentezlemi ler ( ekil 1.14) ve NMR, ESI-MS analizleriyle karakterize etmi lerdir. Sudaki çözünürlüklerinin iyi olmas ndan dolay biomedikal uygulamalarda kullanmay hedeflemi lerdir.
ekil 1.14. Dört nükleotid grubu içeren suda çözünen kaliks[4]aren
lmaz ve grubu (2010) suda çözünen p-sülfonato kaliks[4]aren ve
tetrakarboksilat türevini sentezlemi ler ( ekil 1.15) ve bu bile ikleri quartz kristal mikrobalans tekni inde nem sensörü olarak kullanm lard r. Kaliksarenin nem adsorbsiyonu ve desorbsiyonunun kineti ini incelemi lerdir.
O O O O O O O O P O O O B O HO P O O O B O HO P O O O B O HO P O O O B O HO -N N N N NH2 NH N O O B= B=
OH HO HO OH SO3Na SO3Na NaO3S NaO3S O O O O SO3Na SO3Na NaO3S NaO3S NaO O NaO ONa O O ONa O
ekil 1.15. Nem sensörü olarak kullan lan suda çözünen kaliks[4]arenler
Mourer ve grubu (2010), sülfonat, karboksilat ve fosfonat grubu ta yan antiviral olarak kullan lmak üzere, suda çözünen birçok kaliksaren türevi sentezlemi lerdir ( ekil 1.16.). Bunlardan baz lar n fenolik OH’lar nda 2,2’-bithiazol grubu ba r. Antiviraller virüs enfeksiyonlar na kar kullan lan farmakolojik ajanlard r. Elde ettikleri bu bile ikleri anti-HIV ajan olarak virüslü kan ve hücrelerde kullanm lard r. Bu bile iklerin birço u antiviral özellik göstermi tir.
ekil 1.16. Antiviral özellik gösteren kaliks[4]arenler
OH HO O O O HO OH O S N N S S N N S NaO O NaO O S N N S R R R R R= SO3Na R= CH2POOHONa R= CH2COONa S N N S ONa O ONa O R R R R R= H R= t-bütil R= CH2COONa OH HO HO OH R= SO3Na R= CH2POOHONa R= CH2COONa R R R R
1.6. Kaliksarenlerin Fonksiyonland lmas
Kaliksarenleri, bu kadar önemli hale getiren di er bir etken bunlar n farkl fonksiyonel gruplar kullan larak kolayl kla modifikasyona u rat labilmesidir. Kaliksarenlerin fenolik -OH gruplar n bulundu u dar olan k sm na ‘‘lower rim’’, aril halkalar n para pozisyonunun bulundu u geni olan k sma ise ‘‘upper rim’’ ad verilmi tir ( ekil 1.17). Kaliksarenlere hem upper rim üzerinden hem de lower rim üzerinden kolayl kla de ik fonksiyonel gruplar ba lanabilmektedir.
ekil 1. 17. Kaliks[4]arenin p-konumunun ve fenolik-O bölgesinin ematik gösterimi
1.6.1. Kaliksarenlerin fenolik OH üzerinden fonksiyonland lmas
Kaliksarenlerin fenolik OH gruplar n (lower rim) modifikasyonu eter ve ester gruplar n kolayl kla ba lanmas ile yap lmaktad r. Kaliksarenin eter ve ester türevli ürünleri e er reaksiyon artlar iyi ayarlan rsa mono fonksiyonlu, 1,2 ve 1,3-di, tri ve tetra fonksiyonlu olmak üzere yüksek verimle elde edilirler ( ekil 1.18). Örne in kaliksarenlerin mono eter veya ester türevleri CH3CN çözücü ortam nda K2CO3 veya
DMF çözücü ortam nda CsF gibi zay f bazlar ve uygun reaktifler kullan larak olu turulur (Reinhoudt, 1991) .
OH OH HO OH HO OH HO OH O H HO OH OH OH HO OH HO HO OH
Upper rim
Lower rim
(Fenolik-OH)Kaliksarenlerin 1,2-di-, 1,3-di-, tri- veya tetra-türevlerinin sentezinde de kullan lan baz n ve çözücünün önemi çok fazlad r. Aseton veya asetonitril ortam nda Na2CO3 veya K2CO3 gibi bazlar kullan larak 1,3-difonksiyonlu kaliksarenler,
DMF/THF ortam nda NaH gibi güçlü bazlar kullan larak 1,2-difonksiyonlu kaliksarenler ve DMF ortam nda Ba(OH)2 kullan larak trifonksiyonlu kaliks[4]aren
türevleri sentezlenebilir (Groenen, 1991). Tetra fonksiyonlu kaliksaren türevleri sentezlenirken aseton veya asetonitril ortam nda baz olarak NaOH kullan rsa koni konformasyon, K2CO3 veya CsCO3 kullan rsa k smi koni ve 1,3-kar kl
konformasyonda ürünler elde edilir (Shinkai, 1990).
OH OH O H HO OH O H OH O O OCH3 OH OH OCH3 OCH3 O O O H O O OCH3 O OCH3 O H3CO O O O O m etilb rom as etat K 2CO 3 / A set on me tiliyo dür NaH / D MF -TH F met ilb rom aset at Ba (O H)2 / D MF P rop ili yo dür K 2CO 3 /As et on itril
1.6.2. Kaliksarenlerin p-pozisyonlar ndan fonksiyonland lmas
1.6.2.1. p-Alkil kaliksarenlerin dealkilasyonu
Kaliksarenlerin fenolik OH gruplar n (lower rim) modifikasyonu kolayl kla yap labildi i gibi p-pozisyonuna (upper rim) birçok fonksiyonel grubun ba lanmas da kolayd r. Bunun için öncelikle fenil halkalar na ba p-tert-bütil gruplar n susuz AlCl3/ toluen ortam nda kolayca giderilmesi (dealkilasyonu) gerekir. t-Bütil gruplar n
hepsi giderildi i gibi seçimli olarak dealkilasyonu da mümkündür. Bunun için o-alkilli veya o-açilli kaliksarenlerin ter-bütil gruplar n seçimli olarak giderilmesi ve daha sonra da para pozisyonundan seçimli olarak fonksiyonland lmas r ( ekil 1.19) (See, 1991; Kanamathareddy, 1995; Sharma, 1996). CH2 OH 4 AlCl3 Toluen CH2 OH 4 Toluen AlCl3 ArCOCl HO OHO O 2 O O HO OHO O 4 O O
1.6.2.2. Elektrofilik sübstitüsyon
Kaliksarenin para pozisyonundaki t-bütil gruplar giderildikten sonra amaca uygun olarak nitrolama (Loon, 1992; Verboom, 1992), bromlama (Gutsche, 1985; Hamada, 1990), iyotlama (Arduini, 1990; Timmerman, 1994), sülfolama (Gutsche, 1985; Shinkai, 1986), klor sulfolama, (Morzherin, 1993), diazolama (Shinkai, 1989; Deligöz, 2002) gibi k smi sübstitüsyon reaksiyonlar gerçekle tirilmi tir ( ekil 1.20).
OH HO HO OH HO3S SO3H OH HO HO OH HO3S SO 3H Br Br OH HO HO OH Br Br O2N NO2 OH HO HO OH O2N NO 2
ekil 1.20. Elektrofilik Sübstitüsyon reaksiyonu
1.6.2.3. p-Clasien Çevrilmesi
Kaliksarenlerin türevlendirme yollar ndan biriside p-Clasien çevrilmesidir. Bu metotla kaliks[4]arenin allil eterlerini, fenolik oksijenden p-pozisyonlar na fonksiyonel gruplar n transferinin gerçekle ti i bir metotdur (Gutsche, 1985).
1.6.2.4. p-Klormetilasyon Yolu
Bu metodla sadece belirli pozisyonlar için kontrollu k smi sübstitüsyon yapmak mümkündür. p-klormetilasyon yolunu ilk olarak Parma grubu ortaya ç karm r. Kaliks[4]aren’i oktilklormetileter ve SnCl4 ile reaksiyona sokup % 80 verimle
p-klormetil kaliks[4]aren’i elde etmi ve bundan de ik kaliksaren bile ikleri elde etmi lerdir.
1.6.2.5. p-Kinonmetit Yolu
Kaliksarenlerin p-pozisyonunun nükleofilik reaksiyon verme özelli inden faydalanarak, direk elektrofilik sübstitüsyon reaksiyonlar ndan p-kinonmetit yolu ile birçok fonksiyonlu kaliksareni sentezlenmektedir. Gutsche ve Nam (1988) taraf ndan önerilen bu metot için öncelikle t-bütil gruplar giderilmi kaliksareni formaldehit ve çe itli sekonder aminlerle etkile tirerek Mannich tipi reaksiyonla birçok
p-alkilaminokaliksareni elde etmek mümkündür. Bu bile ikleri quaterner amonyum bile iklerine dönü türdükten sonra nükleofillerle etkile tirildikten sonra istenilen bile ikler elde edilir ( ekil 1.21). p-kinonmetid yolu fonksiyonlu kaliksarenleri elde etmek için k sa yollardan birisidir. Örne in p-tertbütilkaliks[4]aren’den p-(2-amino-etil)kaliks[4]aren’i para Clasien çevrilmesi ile sekiz basamakta elde edilirken kinon metit yolu ile be basamakta elde edilmektedir.
CH2 OH 4 CH2 OH 4 Z CH2 O CH2 4 CHNR2 Z= N R1 R2 H + HCHO R2NH CH3I CH2 4 CH2 O CH2 OH 4 CH2Nü Nü Nü
Nü = CN, OCH3,SEt, CH(CO2Et)2
1.6.3. pso sübstitüsyon
pso sübstitüsyon, elektrofilik aromatik yerde tirme reaksiyonlar n özel bir türüdür. Bu reaksiyonda ayr lan grup hidrojenden farkl bir gruptur. Kaliksarenlerde de ipso fonksiyonland rma yap labilir bunun için kaliksarenin para pozisyonundaki t-bütil gruplar giderilmeden elektrofilik yerde tirme reaksiyonu yap labilir.
Chawla ve grubu (2006), p-ter-bütilkaliks[4]aren’i ipso sübstitüsyonla,
hekzametilentetraamin ve triflorasetik asit ortam nda tersiyer bütil gruplar gidermeden direk aldehit türevine dönü türmü lerdir ( ekil 1.22). Ayn artlarda seçimli dialdehit türevini elde etmek için, p-ter-bütilkaliks[4]aren’in diester ve dipropoksi türevlerini sentezleyerek fenolik OH’ n para pozisyonundan dialdehit türevini elde etmi lerdir. OY YO XO OX OY YO XO OX H H O O N N N N TFA X=Y=H X=Y=H X=H Y=CH2COOC2H5 X=H Y=CH2CH2CH3 X=H Y=CH2COOC2H5 X=H Y=CH2CH2CH3
ekil 1.22. Kaliks[4]arenin ipso sübstitüsyonla di aldehit türevinin elde edilmesi
pso sübstitüsyona ba ka bir örnekte ipso nitrolama, Verboom ve grubu (1992),
p-ter-bütilkaliks[4]aren’in di ve tetra metoksi, propoksi, ve ester türevlerini ipso
sübstitüsyonla para pozisyonundan nitrolam lard r ( ekil 1.23).
OR RO RO OR OR RO OR RO O2N O2N NO 2 NO2 R= CH3 R=CH2COOCH3 R= CH2CH2CH3 R=CH2CH2OCH2CH3 R= CH3 R=CH2COOCH3 R= CH2CH2CH3 R=CH2CH2OCH2CH3 HNO3/ CH3COOH
Coquire ve grubu (2006), kaliks[6]aren’in fenolik birimlerinin p-pozisyonundan seçici fonksiyonland lmas için yeni bir metot geli tirmi lerdir. Kaliksaren türevleri için yeni bir reaksiyon olan ipso- klorsülfolama reaksiyonunu gerçekle tirmi lerdir
ekil 1.24).
ekil 1.24. Kaliks[6]arenin ipso klorsülfolanmas
1.7. Polimerik Kaliksarenler
Memon ve arkada lar (2003), üç yeni polimer destekli kaliks[4]aren türevi sentezlemi ler ( ekil 1.25), metal ve dikromat anyonu s -s ekstraksiyon çal malar nda kullanm lard r. Karboksilik grup içeren polimer bile i 1 A grubu katyonlar ta mazken geçi metallerine kar seçicilik göstermi tir. Monomerik amit türevi ve onun polimeri ise anyon (dikromat) çal malar nda kullan lm ve polimer türevinin monomerine göre seçilen pH larda daha iyi bir ekstraktant oldu u anla lm r. R3 R1 O R2 CH) (H2C (H2C CH) X Y n R1=R2=R3= CH2COOH R1=R3=CH2CONHCH2C6H5 R2=H R1=R2=R3= CH2COOCH3
Shinkai ve ark. 1987 y nda polimerik kaliks[6]aren bile ini sentezlemi ekil 1.26) ve patent çal mas yapm r. Bunun için kaliks[6]areni fenolik gruplar n p-pozisyonundan polimerik iskelete ba lam lar ve bu reçinenin 0,1 gram ak h n 30mL/dk oldu u bir kolondan deniz suyu geçirerek 108 g UO22+ iyonunu seçimli
olarak izole etmi lerdir
OH
O S O
NH
6
n
ekil 1.26. Kaliks[6]aren polietilenamin destekli polimerik yap
Uysal ve ark. (2001) yapt klar bir çal mada kaliks[4]arenin nitril türevini fenolik-O’den farkl polimer iskeletine ba layarak s -s ekstraksiyon çal malar incelemi ler ( ekil 1.27). Sonuçta, her iki polimerin de Hg2+ katyonuna kar seçicilik gösterdiklerini bulmu lard r
OR OR OR O 4 O O HC H2C n OR OR OR O 4 O O HC H2C n HC H2C m X R=CH2CN R=CH2CN X=Ph
lmaz (1999), yapt bir çal mada birden fazla p-ter-bütilkaliks[4]aren triketon biriminin bir arada bulundu u oligomerik yap da bir bile ik ( ekil 1.28) sentezlemi ve bu bile in iyon ta ma özelliklerini inceleyerek Na+, K+, Ag+, Co+2, Ni+2, Cu+2 ve Cd+2 katyonlar varl nda Li+ için bir seçicilik gösterdi ini tespit etmi tir.
ekil 1.28. Polimerik yap daki p-ter-bütilkaliks[4]aren triketon türevi
1.8. Kaliksarenlerin Uygulama Alanlar
Çok say da özelliklere sahip kaliksarenler uygun ekilde fonksiyonland larak siz kullan m alanlar na sahiptirler. Bunlardan baz lar ;
Molekül / iyon ta olarak Elektrot ve sensör çal malar nda Membran çal malar nda
Enzim mimik çal malar nda Kromotografi çal malar nda Monolayer çal malar nda Kiral tan nma çal malar nda
1.8.1. Kaliksarenlerin molekül / iyon ta olarak kullan lmas
Kaliksarenler halkal yap da bile iklerdir ve fenolik birimlerin say na göre bo luk çaplar de mektedir. ekilleri sepet gibi olduklar ndan konuk-konak (host-guest) kimya sahas nda büyük ilgi kayna olmu lard r. Konuk moleküllerin yerle ebilece i bo luklara sahip oldu undan katyon, anyon ve molekül ta olarak yayg n bir ekilde kullan lmaktad r (Asfari ve ark., 2001).
Katyon ta olarak, McKervey ve ark. (1985) kaliksarenlerin ester türevlerini sentezlemi ve özellikle kaliks[4]arenin etil esteri 1 A grubu katyonlar aras ndan Na+ iyonu için seçimli oldu unu tespit etmi lerdir. Bo luk çap kaliks[4]arenden daha büyük olan kaliks[6]arenin metil esteri ise Cs+ kar iyi bir iyonofor olarak kullan lmaktad r
ekil 1.29). OCH3 O O O O O O O OCH3 OCH3 OCH3 OCH3 O CH3 O O O O O
Cs
+ O O O O OC2H5 O C2H5 C2H5O C2H5O O O O O Na+ekil 1.29. p-t-Bütilkaliks[4]arenin tetra estertürevi ile Na+ katyonunun ve p-t-bütilkalik[6]arenin hegzaester türevi ile Cs+ katyonunun kompleksle mesi
Anyon ta olarak, oksi anyonlardan kromat (CrO42), dikromat (Cr2O72)
oldukça toksik olmalar sebebiyle sulardan ve topraktan giderilmesi oldukça önemlidir. Ediz ve ark. (2004) dört tane piridil grubu ta yan kaliks[4]aren türevi sentezlemi lerdir ekil 1.30). Bu dört piridil grubundan iki tanesi lower rim de amit grubu olarak ba , di er iki tanesi ise upper rim de imin tipinde ba r. Bu bile ik dü ük pH’larda suda çözünürken, pH > 2,5 da dikromat (Cr2O72) için iyi bir ekstraktant oldu unu
OH HO O O N N NH+ N + HN HN NH O O N OH -H+ + 2 HCrO7 -HCrO7 -OH HO O O N N N N N HN NH O O N HCrO7
-ekil 1.30.Piridil grubu içeren kaliksaren türevinin dikromat anyonu ile kompleksle me modeli
Bozkurt ve ark.(2005), p-ter-bütilkaliks[4]aren’nin dört tane diamit türevini sentezlemi ler ( ekil 1.31) ve 1H NMR ve 13C NMR’la koni konformasyonunda olduklar ispatlad ktan sonra, dikromat (Cr2O7–2) anyonu ile bu amitlerin
kompleksle melerini incelemi lerdir. Protonlanabilir olanlar n (c ve d) di erlerine (a, b) göre daha iyi ekstraktant olduklar göstermi lerdir.
OHOH O O HN NH O O OHOH O O HN NH O O O O OHOH O O HN NH O O N O N O OHOH O O HN NH O O N N a b c d
ekil 1.31. Kaliksarenin diamit türevleri
Deligöz ve grubu (2008), çal malar nda fenolik-O’ne ba dört asetil, dört metilketon ve üç benzoil grubu bulunduran kromojenik azokaliks[4]aren türevlerini sentezlemi ler ( ekil 1.32) ve bu bile iklerin metal iyonlar için ekstraksiyon çal malar yapm lard r. Hem asetil hem de benzoil türevlerinin geçi metallerinden Ag+2 ve Hg+2 için iyi bir ekstraktant oldu unu göstermi lerdir.
R1 R2 R3 R4 N N R' R1,R2,R3,R4= COCH3 R1,R2,R3,R4= CH2COCH3 R1=H R2,R3,R4= C O L1:R'= C2H5 L4:R'= L7:R'= L10:R'= C4H9 NHCOCH3 N S L2:R'= C2H5 L5:R'= L8:R'= L11:R'= C4H9 NHCOCH3 N S L3:R'= C2H5 L6:R'= L9:R'= L12:R'= C4H9 NHCOCH3 N S
ekil 1.32. Azokaliks[4]aren bile ikleri
Molekül ta olarak, Y lmaz ve grubu (2009), kanserojen azo boyar madde ve aromatik aminlerle sorpsiyon özelliklerini incelemek amac yla kaliks[4]arenin alkil amin türevi ve onun polimerini sentezlediler ( ekil 1.33) ve kat -s ekstraksiyon çal malar yapt lar. Bu çal man n sonucunda kaliks[4]aren kullan lan azo boyalar hemen hemen hiç ta mazken kaliksarenin alkil amin türevi ve onun polimeri önemli derecede sorpsiyon özelli i göstermi tir. Aromatik amin sonuçlar na bakt zda kaliks[4]aren önemli bir adsorban özellik göstermemi tir. Bu bile ik p-dibromoksilen ile etkile tirilerek polimerle tirildi inde daha rijit bir yap olu tu undan monomerine göre daha iyi ekstraktant oldu u gözlenmi tir.
ekil 1.33. Kaliksarenin polimerik alkil amin türevinin kanserojen aromatik amin ve boyalarla
kompleksle me modeli
Son y llarda Y lmaz ve grubu (2009), manyetik özellik gösteren kaliksarenlerin sentezini ilk olarak tasarlam r. Bunun için manyetik Fe3O4manyetik nanoparçac klar
ile aminopropiltrimetoksi silan (APTMS) ile etkile tirmi ve sentezlenen p-ter-bütilkaliks[4]aren diesteri türevi ile etkile tirerek, manyetik özellikteki kaliks[4]aren bile i elde edilmi tir ( ekil 1.34). Sentezlenen bu manyetik nanopartiküller dikromat
-O N O O N N H H H H H O O N O O N O O n O -N O O + Kanserojenik Aromatik am in ve boyalar
anyonunun ekstraksiyon çal mas nda kullan lm r. Bile in pH 2,5–4,5’da iyi bir ekstraktant oldu u gözlenmi tir.
HO HO O O H N N H O O Si O O Si O O Si O Si O O OH OH O O H N N H O O Fe3O4 Cr O O O -O Cr O OHO H Na+ H OH OH O O O O Si Si Si Si O O O O O O O HN Si Si Si Si O O O O O O O N Fe3O4 Fe3O4
ekil 1.34. Manyetik Fe3O4 nanoparçac klar na immobilize edilen kaliks[4]aren
Di er bir çal mada Y lmaz ve grubu (2010), kaliks[4]aren’in N-metil glukamin türevini sentezlemi ler ve daha sonra bu bile i APTMS ile etkile tirilmi olan Fe3O4
manyetik nanoparçac klar na immobilize etmi lerdir ( ekil 1.35) Elde ettikleri bu yeni bile in yap FT-IR, TEM ve TGA analizleriyle ayd nlatm lar. Kat -s ekstraksiyon tekni iyle arsenat ve dikromat iyonlar n sulu çözeltilerden uzakla lmas nda kaliks[4]aren bazl manyetik nanoparçac klar n iyi bir ekstraktant oldu unu anla lm r.
OHOH O O N N HO OH HO OH HO OH OH HO HO OH Si Si Si Si O O O O O O O Fe3O4 OH O Si Si Si Si O O O O O O O HO O OHOH O O N N HO OH HO OH HO OH OH HO HO OH Si Si Si Si O O O O O O O OH O Si Si Si Si O O O O O O O HO O H H HO A A= H2AsO4-/HCr2O7 -Fe3O4 Fe3O4 Fe3O4
ekil 1.35. Manyetik özellik gösteren N-alkil glukamin kaliks[4]aren bile i
1.8.2. Elektrot ve sensör çal malar
lmaz ve arkada lar (2007), p-ter-bütil kaliks[4]arenin diamit türevini ( ekil 1.36) sentezlemi ler ve dikromat anyonu için seçici elektrot olarak kullanm lard r.
ekil 1. 36. Dikromat anyonu için iyonofor özellikteki kaliks[4]aren'in diamit türevi
OHOH O O HN HN O O HN NH N N
Demirel ve ark.(2004), p-ter-bütilkaliks[4]aren azacrown-4 türevini kullanarak hidrojen iyon selektif polivinilmembran (PVC) elektrot çal mas yapm lard r ( ekil 1.37).
O O
OH HO
O O
ekil 1.37. Hidrojen iyon selektif elektron olarak kullan lan kaliks[4]aren azacrown türevi
Kim ve grubu piren grubu içeren kaliksarenin diamit türevini sentezlemi lerdir ekil 1.38.). Bu bile i çe itli anyonlarla (F-, Cl-, Br-, I-, CH3CO2-, HSO4-ve H2PO4-)
kompleksle mesini incelemi ler ve flor ile kompleksinde floresans iddetinin artt gözlemlemi lerdir. O O O O HN NH O O O O O O HN H N O O O O O O H2N N O O F -F -H H + + -
-ekil 1.38. Pren grubu içeren kaliks[4]aren türevinin F- le kompleksle mesi
Ba ka bir çal mada Kim ve ark., floroiyonofor olan, antrasen birimi içeren kaliks[4]azacrown bile ini sentezlemi ler ve Cs+, Rb+ ve K+ iyonlar na kar floresans özelliklerini incelemi lerdir ( ekil 1.39). Yap lan çal mada bile in Cs+ ile kompleksle mesi floresans iddetini art rd ve bu kompleksin Cu+2 iyonlar ilave
edildi inde, Cu+2 azacrown bölgesinden kompleks yaparak Cs+2 floresans iddetini dü ürdü ünü gözlemi lerdir. O O O O O O O O CN O H N O O O O O O O O O CN O H N O O O O O O O O O CN O H N O
Floresans yok Floresans Düsük Floresans
Cs+2 Cs
+2
Cu+2
Cu+2
Cs+2
ekil 1.39. Floresans özellik gösteren antrasen birimi içeren kaliksazacrown bile inin kompleksle me modeli
1.8.3. Membran çal malar
Alpo uz ve ark. (2002) hacimli s membran kullanarak biskaliks[4]aren nitril bile i ( ekil 1.40) ile Hg+2 katyonunun sulu fazdan organik faza transfer özelliklerini incelemi lerdir. OR OR 4 OR O RO RO 4 O RO O R= CH2CN
ekil 1.40. membran olarak kullan lan biskaliks[4]arenin nitril türevi
1.8.4. Monolayer çal malar
Chen ve grubu (2007), kaliksarenin fenolik-O’inde etilester, karboksilik asit ve crown eter grubu olan ve fenolik birimlerin p-pozisyonunda ise tiyol grubu ta yan üç
farkl kaliksaren bile i sentezlemi ler ( ekil 1.41) ve alt n yüzeyine –SH grubundan immobilize ederek baz proteinlerin belirlenmesinde monolayer olarak kullanm lard r.
ekil 1.41. Kaliksaren türevlerinin monolayer olarak kullan lmas
1.8.5. Enzim mimik çal malar
Kaliksarenlere uygun fonksiyonel gruplar ba lanarak enzim mimik özelli i kazand labilir. Burada kaliksaren bo lu u enzimin aktif bölgesini te kil ederek substratlar n katalitik olarak ürünlere dönü mesini sa layabilir.
Dospil ve Schatz (2001), kaliks[4]arenin fenolik gruplar seçimli olarak imidazol ile fonksiyonland rd ktan sonra metal kullan lmaks n p-nitrofenil esterlerinin katalitik hidrolizinde katalizör olarak kullanm lard r ( ekil 1.42).
O O O O S H H S C H3 H3C O O O O O O O S H S H H S H S O O O O H O O H O H H O O O O O S H S H H S H S O O O O E tO O E t O E t E t O Au O O O O S S S S O O O O HO OH OH HO
BSA
ekil 1.42. midazol grubu içeren kaliksaren türevlerinin p-nitrofenil esterlerinin hidrolizinde
kullan lmas
1.8.6. Kromatografi çal malar nda kolon dolgu materyali olarak
Slivka-Kaszynska ve grubu (2010), 1,3-konformasyonunda sabit faz kaliksaren türevlerini sentezlemi lerdir ( ekil 1.43). Bu bile ikleri yüzey alan , hidroskobik seçicilik, aromatik seçicilik, hidrojen ba kapasitesi ve iyon de imi kapasitesi bak ndan karakterize etmi lerdir. Kromatografik özellikleri bak ndan ticari kolonlarla sentezledikleri kolon dolgu maddelerini kar la rm lard r.
ekil 1.43. Silika bazl kaliksaren türevlerinin sentezi ve kolon dolgu maddesi olarak kullan lmas
O O O O R R Si Si - C12H25 -C6H13 R= -C3H7 H2C H2C H2C Cl NO2 O O OCH3 O HN H2C F F F F F O H3C O , , OR RO HO OR N N N N OR RO HO OH N N OH RO HO OR N N N N R=H R=Bz O2N O R O O2N OH R=Ph R=M e N N OR R O H O O H N N + RC OO H
Erdemir ve Y lmaz (2010), sentezledi i 1,3-kar kl kaliks[4]aren türevini -kloropropilsilikajele (CPS) immobilize ederek kolon dolgu maddesi olarak kullanm lard r. ( ekil 1.44) HPLC de bu kolonla baz aromatik hidrokarbonlar, fenolik bile ikler, aromatik aminler ve baz ilaç bile enlerinin ayr lmas nda kullanm lard r.
ekil 1.44. Kloropropilsilikajele immobilize edilmi kaliks[4]aren türevinin kolon dolgu maddesi olarak
kullan lmas
Barc ve Siliwka-Kaszynska (2009), 1,3-kar kl 25,27-bis (pentaflorobenziloksi)- 26,28-bis-(3-propiloksi) kaliks[4]aren ve 25,27-bis(benziloksi)-26,28-bis(3-propiloksi) kaliks[4]aren ba silikajel sabit faz sentezlemi ler ve bu bile ikleri s kromatografisinde flor içeren bile ikler (florobenzen, floro-primidin bazlar ) ve flor içermeyen analitlerin sülfonamitler, non-sterodial anti inflammatory ilaçlar ve polinükleer aromatik hidrokarbonlar n ayr lmas nda kullanm lard r ( ekil 1.45).
ekil 1.45. Flor içeren ve içermeyen bile iklerin ayr lmas nda kullan lan kaliksaren türevlerinin sentezi
O O O O S i S i O O O O O O S i Si O O F F F F F F F F F F KaliksBzF1 Kaliks Bz KaliksBzF10 KaliksBz -kloropropilsilikajel (CPS)
1.8.7. Kiral kaliksarenler ve kiral tan nma çal malar
Farmakolojide pek çok ilac n hammaddesi kiraldir ve istenmeyen enantiyomerler içerir. Enantiomerlerin biyolojik özellikleri ço u zaman birbirinden önemli derecede farkl r. Bu yüzden bile in enantiyomerlerinin ayr bir ekilde elde edilmesi oldukça önemlidir. Çünkü kiral bir maddenin enantiyomerlerinden birisi vücutta fizyolojik olarak de iklik yaparken di er enantiyomeri etkili olmaz veya ciddi fizyolojik zararlar verebilir. Kiral moleküller asimetrik konak (host) moleküller ile kompleks yapabildikleri için kiral gruplar ta yan kaliksaren molekülleri enantiyomerlerin ayr lmas amac yla kullan lmaktad r.
t ve grubu, yeni kiral kaliks[4]azacrown türevlerini sentezlemi ler ve bu bile ikleri enantiyoselektif kiral reseptör olarak UV-vis spektroskopisiyle incelemi lerdir ( ekil 1.46). Kiral kaliks[4]aren türevleri, fenilalanin ve alaninmetilester hidroklorür enantiyomerlerine kar kiral tan nma göstermi lerdir. Kiral reseptör olarak kullan lan furfuril grubu bulunduran kiral kaliks[4]azacrown türevinin , -amino asit esterine kar çok iyi bir enantiyomerik tan ma ay rac oldu unu gözlemlemi lerdir.
OR OR O O O O N OROR O O O O N O R=H, Me R=H, Me
ekil 1.46. Kiral kaliks[4]azacrown türevleri
Durmaz ve ark. kaliksarenin hem fenolik OH’ nda hem de para pozisyonunda kiral sübstütientler içeren yeni Schiff baz türevlerini sentezlemi lerdir ( ekil 1.47). Bu kiral reseptörler -amino asit ester hidroklorürlerine kar iyi kiral tan nma göstermi lerdir. -amino asit esterlerinin moleküler tan nma kabiliyetleri ve enantiyoseçicilikleri termodinamik olarak tart lm r.
OH OH O O O O O O O O O O H N H N CH3 H3C OH OH O O O O O O O O O O H N H N CH3 H3C OH OH O O O O O O O O O O H N H N
ekil 1.47. Kiral sübstütientler içeren Schiff baz türevli kaliksarenler
Bozkurt ve arkada lar (2008), cinchona alkaloidlerden türetilen kaliksaren bazl kiral faz-transfer katalizörü sentezlemi ler ve bu kiral kaliks[4]aren’in katalitik özelli ini, N-(difenilmetilen)glisin etil ester ile benzilbromür aras nda faz-transfer alkilasyonu gerekle tirerek de erlendirmi lerdir ( ekil 1.48). Ayr ca reaksiyonun verimine ve enantiyoseçimlili ine etki eden di er faktörleri de incelemi lerdir.
Ph N O Ph O BnBr, PTC Ph N O Ph O H H3N O O Cl * * OHOH O O N+ +N OH N HO N n n n = 1, 2, 3
2.KAYNAK ARA TIRMASI
Baz tepkimeler vard r, olmas istemeyiz ama olurlar. Bozunma tepkimeleri gibi. Baz lar ise sadece uygun çözücüde ve ortamda kar rmak yeterlidir. Baz tepkimeler ise, endotermiktir, gerektirir, parçalanma tepkimeleri gibi. Kimisi bas nç ister, kimisi hem bas nç hem de ister. Ama kimyada öyle sihirli maddeler vard r ki bunlara katalizör diyoruz birçok i imizi kolayla ran, birçok tepkimenin daha kolay olmas , dü ük s cakl kta gerçekle mesini sa layan maddelerdir. Hiç olmayacak türden tepkimelerin olmas , ya da çok daha k sa sürede, daha dü ük bir s cakl kta gerçekle mesini sa larlar. (Salih, 2008)
Katalizör Yunancada “ = çözülme” anlam na gelir ve kimyasal bir reaksiyonun h artt ran veya yava latan maddelere denir. Katalizör terimi, ilk olarak 1835’te sveçli kimyac Jöns Jakob Berzelius taraf ndan kullan ld . Berzelius, katalizörün reaksiyona giren maddelerin ba lar çözecek ekilde tesir etti ini ve böylece reaksiyonun daha h zl bir ekilde meydana gelmesine yard m etti ini kabul etti. Baz katalizörler reaksiyonun h yava lat r. Bunlara negatif katalizör denir. Buna ra men katalizörlerin ço u reaksiyon h artt r ve reaksiyon h artt ran katalizörlere de pozitif katalizör denir.
lk önceleri, reaksiyon s ras nda katalizörlerin de ikli e u ramad klar dü ünüldü. Daha sonra baz katalizörlerin reaksiyona girdi i, yani bir de ikli e
rad , fakat bunlar n reaksiyon sonunda miktar ve ekil olarak yeniden ilk hallerine döndükleri tespit edildi. Reaksiyonlarda katalizörlerin genelde çok az miktarlar bile etkilidir. Bir katalizör kendinin birkaç bin kat a rl ndaki maddelerin reaksiyonunu katalize edebilir. Katalitik etkimenin gerçek mekanizmas tam olarak bilinmemesine ra men bunun en az ndan baz durumlarda reaksiyona giren maddelerin katalizör yüzeyinin küçük bir k sm üzerinde emildi i (absorbland ) bir yüzeysel olay oldu u dü ünülmektedir. Böyle bir olay, reaksiyonun ba lamas için gerekli olan aktif enerji miktar herhangi bir ekilde azaltabilir. Böylece ilerlemenin daha h zl olmas sa lan r. Negatif katalizörler, zincirleme reaksiyonlardaki bir basama a etki ederek bunu takip eden basamaklar durdururlar. Mesela katalizör, reaksiyon ortam ndaki maddelerden biriyle birle erek reaksiyonun devam na engel olur. Ayn zamanda negatif katalizörler, pozitif katalizörlerle birle erek onun tesirini yok edebilir. Pozitif ve negatif katalizörler baz kirliliklerin etkisine maruz kal r ki o zaman katalizör zehirlenir, yani
katalizörün etkisi ortadan kalkar. Bu ekildeki zehirler, katalizör yüzeyi üzerindeki aktif bölgeleri at l hale getirebilecek ekilde etki edebilirler.
Kimyasal tepkimeler, atomlar n son halkalar ndaki elektronlar n etkile iminden olu ur. Bu durumda molekül ya da atomlar n birbirine çarpmas gerekir. Bu çarp may sa lamak için bir enerji gerekir. te bir reaksiyonu ba latmak için gerekli olan enerjiye aktivasyon enerjisi denir. Her kimyasal tepkimenin kendine özgü bir aktivasyon enerjisi vard r. Bir tepkimenin aktivasyon enerjisinin yüksek olmas , o tepkimenin daha zor ba layaca anlam na gelir. Ayr ca bir katalizör yard yla bir tepkimenin aktivasyon enerjisi dü ürülebilir. Kataliz, aktivasyon enerjisini de tiren tek yöntemdir.
Katalizör reaksiyonun denge konumunu de tirmez ve reaksiyonu sadece katalizlenmemi reaksiyon için gerekli olan Ee 'den daha dü ük bir Ee 'ne sahip bir yoldan yürütür. Yani katalizlenmi ve katalizlenmemi reaksiyonlar farkl iki yoldan yürüyen reaksiyonlard r ( ekil 2.1). Bu bir ki inin bir tepenin di er taraf na en yüksek noktas ndan geçen bir yol yerine yamac ndan giden bir yolla gitmesi gibidir.
2.1. Katalizörlerin S fland lmas
Katalizörleri biyokatalizör, homojen ve heterojen katalizör olmak üzere üç ana gruba ay rabiliriz ( ekil 2.2).
ekil 2. 2. Katalizörlerin s fland lmas
2.1.1. Biyokatalizörler
Enzimler, özel ve karma k tepkimelerin gerçekle mesini sa layan biyokimyasal katalizörlerdir. Biyolojik sistemlerde kimyasal tepkimeleri katalizleyen ve biyokimyasal olaylar n vücutta ya am ile uyumlu bir ekilde gerçekle mesini sa layan katalizörlerdir.
Enzimler biyolojik sistemlerdeki düzenleyicilerdir. Canl sistemlerde gerçekle en hemen her reaksiyon enzimler denetiminde olur. Katalizörlere nispetle daha karma k ve daha yeteneklidirler. Biyolojik katalizör olarak özetlemek mümkün ama yapt klar i leri, çe itliliklerini, özelliklerini özetlemek pek de kolay de il. Asl nda kendileri protein olan enzimler, biyokimyasal tepkimelerin daha h zl gerçekle mesini sa larlar. Birçok biyokimyasal tepkime enzimler varl nda gerçekle ir. Biyokimyasal
Katalizörler
Homojen Katalizörler Biyokatalizörler Geçi Metal Bile ikleri Asit/BazKatalizörleri Faz Transfer
Katalizörleri
Heterojen Katalizörler
tepkimelerdeki stereoseçicili in de ba kayna rlar. Bu nedenle baz enzimler, organik kimyada asimetrik sentez çal malar nda s kl kla kullan r.
Her katalizör gibi enzimler de bir tepkimenin aktivasyon enerjisini (Ea veya
G‡) azaltarak çal r ve böylece tepkime h çarp ekilde art r. Ço u enzim tepkimesi, ona kar k gelen ve katalizlenmeyen tepkimeden milyonlarca kere daha zl r. Di er katalizörler gibi enzimler de katalizledikleri tepkime sonucunda tükenmez ve bu tepkimelerin dengesini de tirmez. Enzimlerin 4000'den fazla biyokimyasal tepkimeyi katalizledi i bilinmektedir.
2.1.2. Homojen katalizörler
Tepkimeye giren maddeler ile katalizör ayn faz içersinde bulunabiliyorsa, bu tür katalizörlere homojen katalizör denir. Bu tan ma göre, homojen bir katalizör, çözelti tepkimelerinde tepkime maddeleri ile kar abilen bir s , gaz tepkimelerinde ise bir gaz olmal r.
Geçi metal bile ikleri, homojen katalizör olarak kullan lmaktad r. 1979 y nda, A. Suzuki ve N. Miyaura 1-alkenilboranlar ile aril halojenürlerin paladyum katalizörü varl nda tepkimeye girmeleri sonucu stereoseçici olarak arillenmi (E)-alkenlerin sentezlendi ini buldular. Suzuki tepkimesi paladyum kataliziyle bir aril boronik asit ile bir arilhalojenürün kenetlenmesidir. Fakat son zamanlardaki bilimsel geli melere paralel olarak bu yöntemin uygulama alan muazzam bir ekilde geni ledi. Bu nedenle “Suzuki Coupling” kavram art k ayn zamanda alkil, alkenil, aril, allil ve alkinil gruplar da içeriyor.
Katalizör, bir metal atomuna (M) de ik ligantlar n ba oldu u bir komplekstir. Ligantlar, nötr (L = PR3, CO, NR3, alken, NHC) veya anyonik (X = Cl, H,
R, Cp) olabilir Organometalik bile iklerin homojen katalizör olarak hem endüstride hem de biyo-organometalik kimyada kullan lmaktad rlar. Suzuki tepkimesine bir örnek verecek olursak,
I + B(OH)2 Pd katalizör
baz
Fenilboronik asit ile fenil iyodürün bazik ortamda Pd katalizörü varl nda bifenil eldesidir. Suzuki çapraz kenetlenme tepkimesinin mekanizmas di er çapraz kenetlenme tepkimelerinin katalitik döngüsüne benzer ve dört belirgin basamaktan olu ur ( ekil 2.3). Bunlar s ras yla yükseltgen kat lma, metatez, transmetalleme ve
indirgen ayr lma basamaklar r. Yükseltgen kat lma basama nda Pd(0) türleri organik halojenür ile Pd(II) olu turacak ekilde yükseltgenir. Bu ayn zamanda reaksiyonun h z belirleyici basama r. Sonra Paladyuma ba anyon eklenen baz n anyonu ile de ir (metatez). Daha sonra Pd(II) ile alkilborat kompleksi aras nda transmetalle me gerçekle ir. Son olarak da C-C sigma ba n indirgen ayr lmas yla yeniden Pd(0) elde edilir. Transmetalleme basama nda kullan lan baz n kesin rolü ve etkisi belirsizli ini korumas kar n, transmetallemenin baz vas tas yla elde edilen ve serbest boronik asitten daha elektrofilik olan dört koordinasyonlu borat anyonu ile kolayla dü ünülmektedir.
ekil 2. 3. Suzuki kenetleme (coupling) reaksiyonu
2.1.3. Asit-baz katalizörleri
Sulu çözelti kimyas nda asit, suya eklendi inde H3O+ konsantrasyonunu art ran
madde olarak tan mlan r. Buna kar k baz, sulu çözeltilerde H3O+ konsantrasyonunu
azaltan maddedir.
Bir kat n asitli i o kat n proton verebilme kapasitesi (Bronsted asitli i) ile ya da elektron alabilme kapasitesi (Lewis asitli i) ile aç klanabilir. Kat larda bazik merkezler katalizör olarak da kullan labilmektedir.
Asit ve bazlar ortama proton vererek veya alarak katalizör olarak kullan labilinir. Petrol hidrokarbonlar n benzine ve benzeri ürünlere dönü türülmesi gibi, sanayide önem ta yan birçok tepkimeden asit katalizörlerden yararlan r. Örne in molekül
![Çizelge 1. 1. Kaliks[4]aren'in Ar-CH 2 -Ar protonlar n 1 H-NMR spektrumlar](https://thumb-eu.123doks.com/thumbv2/9libnet/4713893.89056/18.892.316.574.411.525/çizelge-kaliks-aren-ar-ch-protonlar-nmr-spektrumlar.webp)
![Çizelge 1. 2. Kaliks[n]arenlerin absorbsiyon de erleri](https://thumb-eu.123doks.com/thumbv2/9libnet/4713893.89056/22.892.141.751.382.601/çizelge-kaliks-n-arenlerin-absorbsiyon-de-erleri.webp)
![Çizelge 4. 1.Kaliks[4]arenin amit türevlerinin faz transfer katalizörü olarak kullan ld esterle me ( p- p-nitrofenil n-bütirat) reaksiyon sonuçlar](https://thumb-eu.123doks.com/thumbv2/9libnet/4713893.89056/117.892.140.802.546.1105/çizelge-türevlerinin-transfer-katalizörü-nitrofenil-bütirat-reaksiyon-sonuçlar.webp)
![Çizelge 4. 2. Kaliks[4]arenin amit türevlerinin faz transfer katalizörü olarak kullan ld esterle me (p- (p-nitrofenil n-kaprolat) reaksiyonu sonuçlar](https://thumb-eu.123doks.com/thumbv2/9libnet/4713893.89056/120.892.140.796.190.750/çizelge-türevlerinin-transfer-katalizörü-nitrofenil-kaprolat-reaksiyonu-sonuçlar.webp)

![Çizelge 4. 2.Kaliks[4]aren amin türevlerinin faz transfer katalizörü olarak kullan ld esterle me (p-nitrofenil n-bütirat, p-nitrofenil n-kaprolat ) reaksiyonu sonuçlar](https://thumb-eu.123doks.com/thumbv2/9libnet/4713893.89056/122.892.136.797.668.1029/çizelge-türevlerinin-transfer-katalizörü-nitrofenil-nitrofenil-reaksiyonu-sonuçlar.webp)
![Çizelge 4. 3. Kaliks[4]arenin tetra alkilamin türevlerinin (21-22) faz transfer katalizörü olarak kullan ld esterle me (p-nitrofenil n-bütirat) reaksiyonu sonuçlar](https://thumb-eu.123doks.com/thumbv2/9libnet/4713893.89056/124.892.159.821.198.447/çizelge-alkilamin-türevlerinin-transfer-katalizörü-nitrofenil-reaksiyonu-sonuçlar.webp)
![Çizelge 4. 4. Kaliks[4]aren türevlerinin faz transfer katalizörü olarak kullan ld p-nitrobenzil bromür ile sodyum bütirat n 50 o C deki esterle me reaksiyon sonuçlar](https://thumb-eu.123doks.com/thumbv2/9libnet/4713893.89056/126.892.142.794.158.524/çizelge-türevlerinin-transfer-katalizörü-nitrobenzil-bütirat-reaksiyon-sonuçlar.webp)