TIP FAKÜLTESİ Çocuk Sağlığı ve Hastalıkları Anabilim Dalı
HENOCH - SCHÖNLEİN VASKÜLİTLİ
ÇOCUKLARDA
OKSİDASYON VE ANTİOKSİDAN KAPASİTE
(UZMANLIK TEZİ) Dr. Selvi KELEKÇİ DANIŞMAN
Prof. Dr. Aydın ECE
ÖNSÖZ
Uzmanlık eğitimim süresince bilgi ve tecrübelerinden yararlandığım değerli hocalarım Anabilim Dalı Başkanımız Prof. Dr. Mehmet Ali TAŞ’a, tezimin her aşamasında büyük katkı ve desteği olan Prof. Dr. Aydın ECE’ ye ve diğer hocalarım Prof. Dr. Kenan HASPOLAT, Prof. Dr. Celal DEVECİOĞLU, Prof. Dr. Fuat GÜRKAN, Prof. Dr. Murat SÖKER, Doç. Dr. Mehmet BOŞNAK, Doç. Dr. Bünyamin DİKİCİ, Doç. Dr. Mehmet KERVANCIOĞLU, Doç. Dr. Ahmet YARAMIŞ,Yrd. Doç. Dr. Selahattin KATAR, Yrd. Doç. Dr. Fatma ÇELİK’e teşekkür ederim.
Uzmanlık eğitimimin her aşamasında ve hayatım boyunca maddi ve manevi her konuda desteklerini esirgemeyen aileme ve değerli eşim Murat KELEKÇİ’ ye, tüm doktor, hemşire ve personel çalışma arkadaşlarıma ilgi ve yardımlarından dolayı teşekkür ederim.
İÇİNDEKİLER SAYFA ÖNSÖZ………...1 KISALTMALAR………...2 GİRİŞ………...3 GENEL BİLGİLER………...5 GEREÇ VE YÖNTEM………32 BULGULAR……….34 TARTIŞMA………..42 SONUÇ………..48 ÖZET……….50 İNGİLİZCE ÖZET………..51 KAYNAKLAR……….52
KISALTMALAR
ANA : Anti nükleer antikor
AD : Anlamlı değil
ANCA : Anti nötrofilik sitoplazmik antikor
ASO : Antistreptolizin O
C3 : Kompleman faktör 3
C4 : Kompleman faktör 4
CRP : C reaktif protein
F VIII : Plasma koagülasyon faktör 8 F XIII : Plasma koagülasyon faktör 13
GIS : Gastrointestinal sistem
HSP : Henoch schönlein purpurası
IgA : İmmünglobülin A
MDA : Malondialdehit
OEH : Ortalama eritrosit hacmi
PAN : Poliarteritis nodosa
PNL : Polimorf nüveli lökosit
RF : Romatoid faktör
ROM : Reaktif oksijen molekülü
SOD : Süperoksit dismutaz
TAOA : Total antioksidan aktivite
TBARS : Thiobarbituric asit reacting substance
GİRİŞ
Vaskülitler, dokuların iskemisi ve kan damarlarındaki inflamatuar değişikliklerle karakterize hastalıklardır (1,2). Çocukluk çağında sistemik vaskülit sendromlarına nadir sıklıkta rastlanır.
Vaskülit sınıflandırılmasında klinik, radyolojik ve histolojik özellikler temel alınarak
sınıflama tekrar gözden geçirilmiş ve American Collage of Rheumatology (ACR)1990 sınıflaması, Chappel Hill konsensus konferansı’nda modifiye edilerek bu sınıflamada etkilenen damar çapı esas alınmıştır. Bu sınıflandırmanın klinikte daha kolay uygulanabileceği üzerinde görüş birliği sağlanmıştır. Çocuklarda en sık görülen histopatolojik ve klinik bulgular birlikte değerlendirilerek primer vaskülitler ayrıca sınıflandırılmıştır (1,3, 4,5).
Sistemik tutulum özellikle renal tutulum çocukluk çağında genellikle
Henoch-Schönlein purpurası (HSP), mikroskopik poliarteritis, Wegener granulomatozisi, Kawasaki hastalığı, poliarteritis nodosa (PAN), Churg-Strauss sendromu ve Takayasu arteritinde görülebilmektedir.
Henoch-Schönlein purpurası, çocukluk çağında en sık görülen sistemik vaskülittir.
Hipersensivite vaskülitleri, lökositoklastik vaskülit grubuna dahil olduğundan deri bulguları, özellikle pupura tanı koydurucu en belirgin bulgudur. HSP kan damarlarının inflamasyonu sonucu özellikle böbrek olmak üzere pek çok sistemi etkilemektedir. HSP genellikle kendiliğinden iyleşir. İyi bir prognoza sahip olması yanında, çocukluk yaş grubunda nadiren oluşan ciddi böbrek tutulumu ve hayatı tehdit eden GİS komplikasyonları nedeni ile önem taşımaktadır (1,6,7). Çocukluk çağının en sık karşılaşılan vasküliti olması ve semptomlarının çok çeşitli olması nedeni ile de HSP, kliniğimizde yatırılan hastalıklar için de önemli bir yer tutmaktadır.
HSP patogenezinde immun kompleksler, adezyon molekülleri, anti-nötrofilik
sitoplazmik antikor, anti-endotelyal antikor ve hücresel immünite rol oynar.
Sistemik Vaskülitlerin Sınıflandırılması Küçük damar vasküliti
- Wegener granülomatosiz -Churg-Strauss sendromu -Mikroskopik polanjititis -Henoch-Schönlein purpurası -Esansiyel kriyoglobinemik vaskülit -Kutanöz lökositoklastik vasküli Orta çaplı damar vasküliti
-Poliarteritis nodosa -Kawasaki hastalığı Büyük damar vaskülüti -Dev hücreli (temporal) arterit -Takayasu arteriti
Primer Sistemik Vaskülitlerin Sınıflandirılması:
Poliarterit Dev hücreli arterit
-Poliarterit nodosa -Takayasu arteriti
-Kawasaki hastalığı -Temporal arterit
-Mikroskopik polianjiitis Diğer vaskülitler
-Kutanöz poliarterit -Behçet Sendormu
-Cogan sendromu -Mucha-Habermann hastalığı
Lökositoklastik vaskülit -Henock Schönlein purpurası -Hipersensitivite anjiitisi
-Hipokomplemantemik ürtikeriyal vaskülit -Mikst kriyoglobulinemi
Granülomatöz vaskülit -Churg-Strauss
-Wegener granulomatosiz -Lenfomatoid granulomatosiz -Santral sinir sistemi primer angiitisi
GENEL BİLGİLER
Hastalığın Tanımlanması :
HSP, nontrombositopenik purpura, artrit, artalji, karın ağrısı, gastrointestinal sistem kanaması ve böbrek tutulumu ile karakterize çocukluk çağında en sık görülen lökositoklastik vaskülittir. Primer lezyon, küçük kan damarlarındaki inflamasyondur. Deri lezyonu en belirgin bulgusudur. İç organlardaki lezyonlar daha ciddi olabilir fakat tanınmaları daha zordur. Primer lezyon, küçük kan damarlarındaki inflamasyondur (1,6,8).
Tarihçe:
Johan Schönlein,1837 yılında, tipik döküntüyü ve eklem belirtilerini tarif ederek bunları “Peliosis Rheumatika” diye adlandırılmıştır. 1870’de ise Eduard Henoch gastrointestinal (GİS) ve böbrek bulgularını tanımlamıştır. İlk tanımlanmalarından bu yana hastalık anaflaktoid alerjik ve romatoid purpura, lökositoklastik vaskülit, allerjik vaskülit diye de adlandırılmıştır (1,9).
Epidemiyoloji :
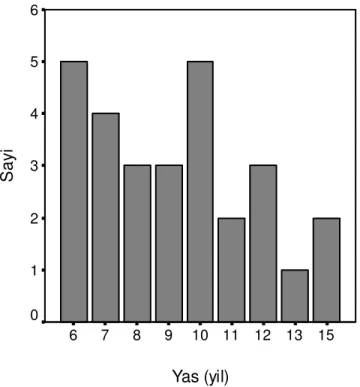
HSP, herhangi bir yaşta görülebilir ancak temelde bir çocukluk çağı hastalığıdır ve en sık çocukluk yaş grubunda görülmektedir. Sıklıkla 5-15 yaş arası görülür, 6 aylık olgularda ve yetişkin yaş grubunda da rastlanılmaktadır (1,9,10). Erkeklerde kızlardan daha sık görülmektedir (1,11,12). Beyaz ırkta zencilere göre daha sık görülür (13). Böbrek ve GİS tutulumu 7 yaş ve üzeri yaştaki hastalarda daha sıktır. Bu nedenle 7 yaş altında hastalık daha selim seyreder (10,12,14,15,16).
Hastalık mevsimsel olarak en sık sonbahar, kış ve ilkbahar aylarında görülür. Hastalık kuzey yarım kürede kış aylarında, Avrupa ve Orta Doğuda ise sonbahar aylarında daha sık görülmektedir (8,16-19).
Etyoloji:
Hastalığın nedeni, tam olarak bilinmemekle beraber, bir çok faktör etyolojik ajan olarak suçlanmaktadır (1,8,9). Çocuklarda enfeksiyonlar ve ilaç kullanımı etyolojide en sık suçlanan sebeplerdir (16,18,20). Sadece deri bulgusunun görüldüğü hastalarda ilaç etyolojisi büyük önem taşımaktadır (21,22).
Enfeksiyonun etyolojideki rolü tartışmalıdır. Hastalığın kış, sonbahar, ilkbahar gibi streptokoksik üst solunum yolu enfenksiyonlarının (ÜSYE) yaygın olduğu mevsimlerde artış göstermesi enfeksiyonun etyolojideki rolünü güçlendirmektedir. Yapılan bir çalışmada HSP’li çocukların üçte ikisinde HSP semptomlarından 2-3 hafta önce enfeksiyon belirtileri bulunmuştur (21). Diğer bir çalışmada HSP’li hastaların %58’inde tetikleyici faktör olarak ÜSYE bulunduğu ve çoğunun sonbahar ve kış aylarında meydana geldiği bildirilmiştir (17). Ayrıca yapılan başka çalışmalarda HSP’li hastaların alınan boğaz kültürlerinde %10-55 arasında A grubu beta hemolitik streptokok üremiştir (16,18,23).
Etyolojide diğer enfeksiyon etkenleri olarak Epstein-Barr virüs, Varicella, Hepatit B, Rubella, Parvovirüs B19, Cytomegalovirüs, M. Pneumonia, C. Enteritis ve Legionella sayılabilir (1,13,24,25). Literatürde hepatit B yüzey antijeni pozitifliğinin HSP ile birlikteliği ve Parvovirüslerin epidemi yaptığı aylarda HSP’nin sık görülmesi bu ajanların etyolojik faktör olduklarını düşündürmektedir (16,23,26,27).
Tifo, paratifo (A,B), kızamık, kolera ve sarı humma aşılarını takiben HSP olgularının tespit edilmesi nedeniyle bu aşılar etyolojik neden olarak düşünülmektedir (23). Böcek
sokması, gıda, ilaç ve soğuk alerjisi (kriyoglobülinlerin rolü olduğu düşünülmekte) de etyolojide suçlanmaktadır (21). Ailesel Akdeniz Ateşi (FMF) ile HSP birlekteliği de yapılan birçok çalışmada gösterilmiştir (28,29).
Yukarıda bahsedilen faktörler dışında gebelikle, malignite (lenfoma, bronş, prostat, kolon kanseri) ve paraproteinemi (monoklonal IgA gammopati) ile birlikte HSP tespit edilmiştir (30,31).
Patoloji ve Patogenez:
Genel olarak tüm sistemik vaskülitlerde olduğu gibi, HSP’de de, kan damarlarının, nekroz ve inflamasyonu ile sonuçlanan immunolojik mekanizmaların primer yada sekonder olarak temel patolojik olayı oluşturduğu düşünülmektedir (1,2,32).
HSP’de spesifik patogenez tam olarak çözülmemekle birlikte IgA’yı kapsayan immunopatogenez ileri sürülmektedir. Bunun sebepleri olarak da; artmış serum IgA konsantrasyonu, dolaşan IgA immun kompleksleri ile IgA romatoid faktör, IgA fibronektin kompleksleri, IgA anti-alfa galaktozil antikorlarının varlığı, artmış IgA taşıyan periferal kan lenfosit oranı ve immunglobulin yapımı ile ilgili immunoregülatuvar anormallikler gösterilmektedir. Mukozal B lenfosit hücreleri genellikle enfekte mukozanın uyarıcı etkisiyle kanda dolaşan dimerik IgA’yı sentezlemek üzere uyarılır. T hücrelerinin immunglobulin sentezi üzerindeki normal kontrol mekanizmaları bozulur. IgA, IgG ve belki de bazı başka
proteinler ile ilişkiye girer ve sonuçta yüksek molekül ağırlıklı makromoleküller oluşturur.Bu makromoleküller kompleman sistemini alternan yoldan aktive eder. IgA fizik özelliklerinden dolayı veya spesifitelerine bağlı olarak yada klirens mekanizmasındaki yetersizlik nedeniyle hedef organlarda depolanır. Depolanan IgA’lar koagülasyon döngüsünü de içeren inflamatuar olayların başlamasına neden olur. Bu ise kanama, fibrin depolanması ve lökositoklastik vaskülit gelişimi ile sonuçlanır (8,32).
HSP’li hastalarda en fazla hastalığın akut dönemlerinde olmak üzere IgA romatoid faktör (IgA-RF) saptanmıştır. IgA-RF, romatoid faktörün bir izotipidir.Yüksek IgA-RF düzeyi ile HSP’deki klinik bulguların ciddiyeti arasında pozitif bir ilişki saptanmıştır.
T hücre supresyonundaki defekt sonucu, IgA yapımında artış olabileceği düşünülmektedir. Bu defektin enfeksiyon ve çevre gibi ekzojen etkenlere mi bağlı olduğu bilinmemektedir. Bununla birlikte bir çok enfeksiyon etkeninin (A grubu streptokok, mycoplasma pneumonia) B hücre aktivatörü oldukları ve bunun sonucunda romatoid faktör üretiminde artış olduğu belirtilmektedir (3,33).
Vaskülit sendromlarında sitokin üretiminin hem kantitatif hem de kalitatif bozuklukları tanımlanmıştır. HSP’de Beşbaş ve arkadaşları tarafından immunohistokimyasal yöntemle deride bazal hücrelerde interlökin-1, interlökin-6 ve TNF-alfa’nın artmış ekspresyonun gösterilmesi ile bu sitokinlerin parakrin yolla vasküler endotel hücrelerine etki ederek, adezyon moleküllerini indükleyip, vasküler zedelenmeye neden olabilecekleri dikkate getirilmiştir (3,8).
Adezyon molekülleri: integrinler, immunoglobulin süper ailesi, selektinler ve kadherinler olarak dört grup altında incelenmektedir. Hücrelerin ekstraselüler matriks proteinlerine ve birbirlerine adezyonu normal immün cevabın gelişiminde kritik bir öneme sahiptir. Dolaşan lökositler ve vasküler endotel üzerindeki adezyon moleküllerindeki değişiklikler, ekstraselüler inflamatuar bölgelere spesifik ve nonspesifik immun cevabın oluşumuna aracılık eden hücrelerin yönlendirilmesinde önemlidir. Normal immun cevaba dahil olan adezyon molekülleri aynı zamanda diğer otoimmun hastalıklar ve vaskülitlerdeki patolojik cevaba da aracılık etmektedir. İntegrinler, ekstraselüler matriks ile hücre arasındaki integrasyonu sağlamada rol oynarlar. Ayrıca integrinler embriyogenez, morfogenez ve yara iyleşmesinde ve ayrıca fibronektin, vitronektin, laminin ve VonWillebrand faktöre adezyonu başlatan trombosit üzerindeki glikoprotein IIb/IIIa için reseptör görevi görürken, lökosit integrinleri ve diğer hücreler ile yabancı partiküllere adezyonda da görev alırlar. İntegrinler her biri ortak bir beta subüniti ile tanımlanan alt gruplara ayrılabilir. Beta 1 ve beta 2 integrinler lökositlerde en fazla eksprese olan ve vaskülit patogenezi ile en fazla ilişkili olan
subgruplardır. İmmunoglobulin süperailesinin üyeleri immunoglobuline yapısal benzerlik gösteren bir yada daha fazla disülfid bağlarının varlığı ile karakterizedir. Bunlar coxachie virüslerin bazı suşlarına ve rihino virüslere reseptör olarak hizmet ederler. Endotel hücreleri, lenfosit, monosit ve eozinofiller üzerine eksprese olarak akut inflamasyondan kronik inflamasyona geçişte inflamasyon bölgesinde mononükleer hücrelerin birikmesine aracılık ederler. Ayrıca endotel üzerinde eozinofil birikimini de sağlar. TNF-alfa, IL-1 gibi proinflamatuar sitokinlerle stimülasyonu takiben immunglobulin süperailesinin endotel hücrelerindeki ekspresyonu belirgin olarak artar. Selektinler inflamasyon bölgesinde lökositlerin endotel hücrelerine bağlanmalarına aracılık eden hücre yüzey karbonhidrat bağlayıcı proteinlerdir. Kadherinler kalsiyuma bağımlı adezyon molekülleridir ve komşu hücreler arasındaki bağlantıyı sağlarlar. Adezyon molekülleri vaskülit için spesifik olmayıp bir çok inflamatuar, malign ve enfeksiyoz hastalıklarda görülebilirler (3,32,34-36). HSP’de oluşan renal patolojide lezyon endokapiler proliferatif glomerulonefrit olup endoteliyal ve mezengiyal hücre artışıyla birliktedir. İnterstisyel alanda belirgin inflamasyon gözlenir. Glomerüllerdeki değişiklikler hafif şekillerden çok ciddi lezyonlara kadar değişkenlik göstermektedir. Işık mikroskopunda çoğu glomerül normal olarak izlenirken, az sayıda glomerülde ise mesengial proliferasyon görülebilmektedir. Hastaların yarısında fokal ve segmental, diğer yarısında ise diffüz (intra veya ekstra kapiler) proliferasyon bulunur. Sıklıkla Bowman kapsülü ve proliferatif glomerül yumağı arasında belirgin bir yarım ay oluşumu vardır. Ciddi lezyonlar diffüz proliferatif olan, PNL infiltrasyonu bulunan, glomerüllerin bir çoğunda belirgin yarım ay oluşumu gözlenen lezyonlardır. Aynı zamanda ciddi olgularda tubuler atrofi ve mononükleer hücrelerin interstisyel infiltrasyonu da bulunabilir. Bazen biyopsilerde tipik membranoproliferatif glomerülonefrit de görülebilmektedir. Elektron mikroskopunda ise en belirgin bulgu mezengiumda, deri kapillerleri ve mezenterik arterlerin çeperlerinde IgA depolanmasıdır. Mezengiumda depolanan IgA’lar özellikle IgA1 sınıfındandır, ancak IgA2’ler bulunduğuna dair çalışmalar da mevcuttur. Mezangil alanlarda genişleme,bazal membranlarda incelme, ayrışma gözlenebilir. İmmunfloresan çalışmalarda, diffüz, granüler, mezangial IgA depolanması en karekteristik bulgudur. Damar duvarlarında diffüz veya segmental olarak IgA birikir. Depolanan subtip IgA1’dir. IgG, IgM, C3 depolanan diğer moleküllerdir. Erken kompleman parçacıkları seyrek saptanır. Alternatif yol komponentleri ve membran atak kompleksi sıklıkla bulunur. Belirgin interstisyel nefrit bulunan olgularda tübüler depolanmalar görülür ve IgA nefritinden ayırımına yardımcı olur. IgA ve C3 papiller dermiste hem purpulalı hem de normal alanlarda damar duvarlarında saptanır. HSP’de oluşan mesangial depolanmalar mesangial hücrelerde proliferasyona neden
olabilmektedir. Glomerüllerin içinde oluşan depolanmaların yerleşim yeri inflamatuar süreçlerin şekillenmesi ve renal histopatolojinin belirlenmesinde önem taşımaktadır. Bazı hastalarda yoğun IgA depolanması olmasına karşın, çok az mesangial proliferasyon mevcuttur. Bunun aksi olarak, bir kısım hastada da yoğun bir proliferasyon görülmektedir. Mezengial depolanmalar, periferik kapiller halkaların subendotelyal alanına doğru yerleştirdiğinde, fokal ve segmental değişiklikler oluşabilir. Subepitelyal depolanmalar da nadiren bulunmakla beraber, bunların yaygın olarak diken formu oluşturma ihtimali çok azdır (1,6,9,37-39).
IgA’nın kompleman ile birlikte depolanmış olması, IgA’nın enflamatuar mekanizmaları harekete geçidiği hipotezini doğrular. Kompleman ve fagositik hücrelerin aktivasyonu, enflamatuar olayların tetiğini çekmektedir. Yapılan çalışmalarda serum polimerik IgA’nın özellikle F(ab)2 bölümünün alternatif yan yolları aktive ederek, kompleman sistemini harekete geçirdiği belirtilmektedir. Ayrıca damar inflamasyonunda TNF-Alfa, IL-1, IL-6 gibi mediyatörlerin rol alabileceği ve von Willebrand faktörün damar enflamasyonunun iyi bir göstergesi olabileceği bildirilmiştir (3,39).
HSP’li hastalarda IgA içeren immun kompleksler, plazmada artmış olarak görülmektedir. Bu kompleksler glomerüllerde ve deri damarlarında da görülebilir. Ayrıca yapılan çalışmalarda GİS tutulumu olan hastalarda IgA’nın GİS tutulumu olmayanlardan yüksek olması, HSP’nin IgA ile düzenlenen, otoimmün bir hipersensitivite reaksiyonu olduğu ve bu hastalıktaki IgA’nın kısmen barsak kaynaklı olduğu hipoteziyle uyumludur. Etkilenen dokularda bulunan IgA depolanmalarının, hastalığa özgü olup olmadığı ve IgA1 ve IgA2 komplekslerinin orjinleri tartışma konusudur. IgA yapımını tetikleyici faktörün, bir enfektif ajan olduğu fikri hala geçerliliğini korumaktadır (6,40,41).
Kompleman aktivasyonunun IgA’nın bileşimine bağlı olduğu, farelerde yapılan monoklonal IgA antikorları ile ilgili çalışmalarda belirlenmiştir. Farelerde yapılan çalışmalarda polimerik IgA ve dimerik IgA’nın güçlü birer kompleman aktivatörü olduğu belirtilmiştir. IgA fagositik hücrelerle etkileşime girerek bunların fagositoz yeteneklerini arttırır, granülositlerden H2O2 salınımını arttırması doku hasarını açıklayabilen bir süreçtir. Ayrıca IgA’nın klirens mekanizması hakkında da çok az şey bilinmektedir. IgA ve immün komplekslerin vücuttan uzaklaştırılmasında Kupffer hücrelerinin ve kompleman önemli bir rol aldığını belirten çalışmalar mevcuttur.
Kupffer hücrelerinde bulunan çeşitli reseptörler yardımı ile büyük IgA immün kompleksleri plazmadan temizlenebilmektedir. Farelerde yapılan bir başka çalışmada, karaciğer endotel hücrelerinin, Kupffer hücrelerinin bulunmadığı durumlarda, IgA
komplekslerini dolaşımdan temizlediği belirlemektedir. Bu bulgular IgA nefropatisi ve HSP ile ilgili bilgilere katkıda bulunmaktadır (42).
HSP’li hastaların kanlarında IgA içeren immün komplekslerin dolaştığı saptanmıştır. Bu kişilerde IgA nefritinde olduğu gibi ya IgA’nın aşırı yapımı yada mononükleer fagositer sistemde immün komplekslerin uzaklaştırılması işleminin eksik yapılmasına bağlı depolanma olabileceği düşünülmektedir (43).
Yapılan çalışmalar IgA’nın hastalığın aktif döneminde daha yüksek seviyeler de olduğunu göstermektedir. Buna rağmen hastalığın süresi ile ilişkili olmayarak akut veya kronik dönemde IgA seviyeleri arasında anlamlı bir fark bulunmadığını bildiren çalışmalarda vardır.
Bununla birlikte IgA birikimlerinin hastalığa spesifik olmadığını bildiren çalışmalarda mevcuttur (44,45). Ayrıca, selektif IgA eksikliği olan bir hastada HSP görüldüğü bildirilmiştir. Bu olguda deride ve glomerüler depositlerde C3, fibrinogen, IgG’ler saptanmış fakat IgA’lar gösterilmemiştir (46)
HSP’de görülen böbrek lezyonlarını, histopatolojik olarak IgA nefropatisinden ayırmak zordur. Yaygın kanı IgA nefropatisi ile ilişkili olduğu yönündedir. Ancak az da olsa farklı antiteler olduğunu idda eden araştırmacılar da vardır (13,37,47).
IgA nefropatisi (Berger Hastalığı), ilk kez 1968 yılında Berger ve Hinglais’in glomerullerde predominant olarak IgA depolanan bir grup hastayı tanımlaması ile tarif edilmiştir. Sistemik veya bir başka renal hastalığın olmaması halinde glomerüllerde IgA’nın dominant birikimi ile karakterizedir. Primer glomerülonefritler içerisinde en sık rastlanan glomerülonefrit formudur ve kronik böbrek yetmezliğine götüren major böbrek kaynaklı nedenlerden biridir. Hastalık özellikle 15-35 yaş grubunda görülür. Erkek/Kadın oranı 2:1 olarak izlenir. Epizodik makrohematüri ve persistan mikrohematüri olguların en az %75’nde saptanır. Makrohematürinin daha sık görüldüğü yaş çocukluk dönemidir.
Proteinürü genelde nefrotik sınırın altındadır. Nadir olarak da nefrotik düzeyde olacak şekilde gelişerek sık görülen klinik bulguyu oluşturur. Hastaların yaklaşık %50 kadarında kanda IgA düzeyi yüksek olup, deri kapillerinde de granüler IgA depozit birikimi mevcuttur. Yapılan renal biopsilerde normal yapı veya oldukça değişik varyasyonlar bulunur. Ekseriyetle diffüz mezengial, fokal veya segmentel proliferasyon mevcuttur. Elektron mikroskopik karakteristiği elektron-dense mezangial depozitlerdir. İmmunofloresan çalışmalarda ise IgA dominant olarak glomerüllerde depolanan immunglobulindir.Ayrıca IgG, IgM, C3 ve %10 gibi bir oranda da C1 ve C4 birikimine rastlanır. Fibrin klasik olarak izlenmez, sadece kresentler içinde depolanır. Fibrin kapillerde depolandığı durumlarda histolojik tablo daha
ağırdır ve bu prognostik önem içerir. HSP’de nefrit bulunan olgularda tubüler depolanmaların görülmesi, IgA nefropatisinden ayrımına yardımcı olur, IgA nefropatisinin genel olarak erişkinlerde görülmesi ve sistemik tutulumun nadir olmasıyla bu iki hastalığın patogenezinin aynı olduğu, ancak immun komplekslerin çocuklarda sistemik tutuluma, erişkinlerde ise böbrek tutulumuna yol açtığı düşündürmektedir (13,37,47-49).
Yapılan bir çok çalışmada HSP’de plazma koagülasyon faktör XIII (F XIII) aktivitesinin hastalığın akut döneminde düştüğü tespit edilmiştir. Ayrıca Kamitsuji ve arkadaşları tarafından HSP nefritinin çeşitli formlarında F XIII’ün glomerüllerde depolandığı gösterilmiştir. F XIII aktivitesinde ki bu düşüş böbrek de fibrin formasyonunun artış ile sonuçlamaktadır. Faktör XIII aktivitesindeki bu düşüşün, HSP’de şiddetli komplikasyonların gelişmesi için önemli bir risk faktörü olabileceğini düşündürmektedir (50-53).
Yine yapılan benzer çalışmalarda HSP’nin aktif dönemlerinde F XIII konsantresinin uygulamasıyla GİS ve eklem semptomlarının hafiflediği, böbrek tutulumu, proteinüri ve hematüriyi azalttığı gösterilmiştir (54,55).
Sonuç olarak: hastalığın etyolojisinin multifaktöryel olması ve durumun bir immünkompleks hastalığı olarak kabul edilmesi nedeniyle spesifik patogenez tam olarak çözülememiştir. Bununla birlikte kesin olan bir şey var ki: hangi nedenle yada etkenle immun sistem harekete geçerse geçsin esas olarak IgA yapımındaki olaylar zinciri başlamaktadır (1,6,8,32,37,47).
KLİNİK BULGULAR Cilt Bulguları :
Hem dağılım hem de lezyonun doğası bakımından HSP döküntüsü farklıdır. Deri döküntüleri, neredeyse hastaların tamamına yakınında görülmektedir. Olguların %90’ında ilk başvuru nedeni döküntüdür. Lezyonlar tipik olarak alt ekstremitelerde ve kalçalarda görülür, fakat üst ekstremiteler, yüz ve gövdeye de yayılabilir. Başlangıçta kol ve bacakların ekstensör yüzlerinde özellikle ayak bileği, dirsek çevresi ve gluteal bölge üzerinde purpuradan ziyade ürtikeryal karakterde başlar. İlerleyen günlerde lezyon daha keskin sınırlı ve makülopapüler bir görünüm alır, zamanla kanın ekstravazasyonuna bağlı olarak purpuraya dönüşürler. Lezyonların dağılımı yer çekimiyle ilgilidir. Sıklıkla çorap ve bel çevresi ve baskıya maruz kalan bölgelerde görülür.Lezyonların bu tipik dağılımıdır ki hastalığı kolaylıkla tanımaya imkan tanır (1,3,6,8,13,16,22,32,56).
Tipik olarak eritamatöz papülü purpura, karın ağrısı, artrit ve nefrit izler. Peteşi ve target lezyon bulunabilir. Tek bir lezyon genellikle 1 cm’den daha küçüktür, ancak birleşerek daha geniş lezyona neden olabilir. Bununla birlikte klasik lezyon ortalama 5 mm çapındaki purpuradır. Bunun yanında ürtikeryal plaklar, peteşiyal lezyonlar, eritematöz makülopapüler veya daha büyük ekimotik görünüşlü lezyonlar da olabilir. Ekimoz nadiren görülmesine rağmen dermal nekroz ve skar ile ilişkili olabilir (purpura nekrotika). Lezyonlar birleşmeye eğilimlidir. Başlangıçta basmakla solarken daha sonra bu özelliğini kaybederler. Lezyonlar kırmızıdan mora dönüşerek, yaklaşık 2 hafta içinde, kahverengi bir iz bırakarak solarlar. Fakat bu süre birkaç günden 3-4 aya kadar uzayabilir. Döküntü geçtikten sonra tekrarlayabilir. %10 olgudan daha azında başlangıç epizodundan aylar hatta yıllar sonra bazen 2-3 kez tekrarlayabilir. İlk ataktan sonraki ataklarda, lezyonlar daha hafif olarak ortaya çıkarlar. Daha çok erişkinlerde görülen eritema multiforme, santral hemorajik ülserasyon ve bül şeklindeki lezyonlar nadiren çocuklarda da görülebilir. Bazı vakalar da hemorajik, nekrotik yada purpura fulminans şeklinde lezyonlara da rastlanmıştır. Döküntülerde nadiren kaşıntı olabilir (1,3,6,8,32,56,57).
Ödem :
HSP’de ödem genellikle lokal tarzdadır ve normal plazma albümini ile birliktedir. Dağılımı periorbital, dudak, perine, skalp, eklemlerin çevresi ile el-ayak sırtı şeklindedir. Bunun yanında yaygın hipoproteinemik ödem, nefrotik sendrom veya protein kaybettiren enteropatinin bir özelliği olarak görülebilir. Ödemin kesin nedeni bilinmemekle beraber vaskülite sekonder gelişen küçük damar permeabilite değişikliği bir neden olabilir. Özellikle 2 yaşın altında sık rastlanan bir bulgudur (1,8,9)
Eklem Bulguları.
Eklem tutulumu artralji veya artrit şeklinde olabilir ve olguların %60-80’inde görülür. Özellikle diz, ayak bileği gibi büyük eklemler etkilenirken, el bileği, dirsek ve parmaklar da etkilenebilir. Karakteristik bulgular şişlik, hassasiyet ve hareket kısıtlılığıdır. Şişlik genellikle ağrıya eşilk eder. Klinik ve radyolojik incelemeler bu şişliğin eklem aralığında efüzyon ve genişleme olmaksızın periartiküler ödeme bağlı olduğunu gösterir. Eklem tutulumu geçicidir ve kalıcı hasar görülmez. Eklem tutulumu birkaç gün ile bir hafta içinde geçer, fakat hastalığın aktif fazında tekrarlayabilir. Olguların %25’inde eklem tutulumu hastalığın ilk bulgusu olabilir (1,8,58,59).
Gastrointestinal Bulgular :
HSP’de döküntüden sonra en sık rastlanan bulgu karın ağrısıdır. Hastaların %65-85’inde görülür. Hastaların %14-20’sinde tipik döküntüden önce karın ağrısının tek başlangıç semptomu olduğu bildirilmiştir. Hastaların yarısında dışkıda gizli kan pozitif olarak saptanır. Bunun yanında melena ve kanlı diyare görülebilir. Bu tabloya sıklıkla kusma, daha nadir olarak da hematemez eklenir. Karın ağrısının nedeni vaskülitle ortaya çıkan submukozal ve subserozal kanama ve ödemdir (1,9,13,16,32,60).
Karın ağrısı sıklıkla şiddetli, kolik tarzında ve ilk bakışta akut karını taklit edebilir. Karın ağrısı göbek çevresinde hissedilmekte ve genellikle batında hassasiyet ve rebound olmamaktadır. Bununla birlikte, yapılan çalışmalarda döküntüden önce, karın ağrısının tek başlangıç semptomu olduğu vakalarda laparatomi uygulandığı ve bunların bazılarına apendektomi yapıldığı bildirilmektedir (1,8,13,16,61).
Karın ağrısı patogenezinde, büyük ihtimalle mezenterik arterlerin vasküliti rol almaktadır. Barsaklardaki vasküler lezyonların, deridekilere benzerlik göstermesi ve yapılan çalışmalarda, gastrointestinal tutulumu olan hastalarda IgA’nın GİS tutulumu olmayanlardan yüksek olması, bu hastalıktaki IgA’nın kısmen barsak kaynaklı olduğunu ve patogenezde vaskülitin rol oynadığı teziyle uyumludur. Barsaklar ileri derecede ödemli ve hemorajiktir. Barsak duvarında subserozal ve submukozal kanama sıktır. Bu durumda sıvı ve kan sızması mukozada lokalize olan ülserasyonlara sebep olmaktadır (6,13,16,40,58).
HSP’de gastrointestinal sistemde en sık olarak jejunum ve ileumda lezyonlar görülmektedir. Endoskopik olarak özafagus, mide, duodenum, sigmoid, kolon ve rektumda da lezyonlar gösterilmiştir (30,45,58).
HSP olgularında gastrointestinal sisteme ait radyolojik bulguları nonspesifiktir. Radyolojik bulgular kanama yapabilen koagülopatiler ve inflamatuar barsak hastalıklarındaki bulgular ile benzerlik göstermektedir. Bu nedenle ayırıcı tanıda klinik bulguların önemi çoktur.
Radyolojik olarak, lokal ödem ve kanamalar psödotümör imajı verebilir. Yapılan çalışmalarda lokal ödem ve submukozal kanamalara bağlı olarak fonksiyonel intestinal obstrüksiyon gelişen olgular bildirilmiştir. İnvajinasyonun tanısı ve diğer komplikasyonların izlenmesinde, baryumlu inceleme her ne kadar lezyonun yaygınlığını gösterip, lezyonun patolojisi ile uygunluk içerisinde olsa da, bazen gözden kaçan durumlar olabilmektedir. Bu nedenle ulturasonografi, hem noninvaziv olması hem de tüm batını değerlendirme olanağı vermesi ve erken teşhisi de olanaklı kılması açısından günümüzde daha fazla uygulama alanı
bulmaktadır. HSP’de görülen GİS’e ait radyolojik bulgular geçicidir ve genellikle 4 hafta gibi bir sürede iz bırakmadan kaybolurlar (58, 61-64).
Gastrointestinal kanama, gaitada gizli kan testinin pozitifliği yanı sıra hayatı tehdit edecek boyutta da olabilir. Kanama GİS tutulumunun en ciddi komplikasyonlarından biridir ve %5 gibi bir oranda görülebilir. Stres ülserleri ve kortikosteroid kullanımına bağlı olarak da oluşabilir. Kanama dışında en ciddi GİS komplikasyonu, barsağın kanamanın başladığı bölgesinde ortaya çıkan, oldukça rijid ve ödemli barsak segmentinin daha hareketli olan barsak segmentinin içine girmesi sonucu oluşan invajinasyon olup, hastaların %3’ünde görülür. Karın ağrısında artma, kanlı, jöle şeklinde gaita, karında palpe edilen bir kitle bulgusu ve hastanın genel durumunun bozulması invajinasyon ihtimalini düşündürmelidir. Pankreatit, intestinal perforasyon, intestinal infarkt ve safra kesesi hidropsu diğer nadir
görülen gastrointestinal komplikasyonlardır. Karın ağrısının şiddetlenmesi bu
komplikasyonları düşündürmelidir. Ayrıca pankreatitli olgularda kan amilaz düzeyi yükselebilmektedir. Safra kesesi hidropsunda ise sağ üst kadranda ağrı ve ele gelen kitle hissi mevcuttur. İleal strüktüre bağlı kronik intestinal obstrüksiyon HSP’nin geç komplikasyonu olarak nadiren görülebilmektedir (1,8,9,13,32,60,64).
HSP olgularında hepatosplenomegali, peritoneal eksuda, mezenterik lenfadenopati hastalığın aktif fazında nadiren görülebilir ve karın ağrısı nedeni olabilirler, bunların tanınması gereksiz laporotomileri önler. Yine ayrıca protein kaybettiren enteropati, steatore, ülseratifkolit gözlenmiştir. Protein kaybettiren enteropati olgularında hipoproteinemi saptanmıştır (1,8,9,13,32).
Böbrek Bulguları :
HSP’li olgularda hastalığın en önemli yönü böbrek tutulumudur. Ancak bazı yayınlarda bu oran %80 ‘e çıkmaktadır (1,6,9,13,15,43,65).
Yapılan çalışmalarda HSP’li çocuklarda renal tutulumun 7 yaş üzerinde daha sık görüldüğü bildirilmektedir. Ayrıca GIS tutulumu, persistan purpura ve FXIII aktivitesi düşüklüğü bulunan HSP ‘li çocuklarda renal tutulum olasılığının daha yüksek olacağı, yapılan çalışmalar sonucunda düşünülmektedir (15,16,65,66).
Bunun yanında yapılan başka çalışmalarda daha büyük çocuklarda renal tutulumun daha sık olduğu vurgulanmıştır (12,14).
Uzak Doğu ve Orta Doğu kaynaklı çalışmalarda renal tutulumun, Avrupa kaynaklı yayınlarda ki renal tutulumdan daha sık olduğu dikkati çekmektedir (18,67).
Çocuklarda renal tutulumun prognozu genellikle iyi olmakla beraber, kalıcı fonksiyon bozukluğu yada nadiren son dönem böbrek yetmezliği de gelişebilmektedir. Bununla birlikte HSP çocuklarda son dönem böbrek yetmezliğinin önemli nedenlerinden biridir. İlk üç ay hastalığın ciddiyetinin belirlenmesi açısından en önemli devredir ve genellikle renal tutulum, döküntünün başlangıcından itibaren üç aylık sürede ortaya çıkar. Bunun yanında bir çok olguda renal tutulum ilk bir ay içinde ortaya çıkabilmektedir. Çok az çocukta yıllar sonra bile tekrarlayan ataklar sonucunda nefrit gelişebilmektedir (1,6,7,9,65,68,69).
Olguların %1’inde, persistan nefropati oluşumu, %1’inden azında ise son dönem böbrek yetmezliği görülebilmektedir. Eğer hastalarda nefritik bulgular varsa %10 ve daha fazla oranda son dönem böbrek yetmezliği gelişebilmektedir. Renal tutulum olmasa da %5’den daha az oranda son dönem böbrek yetmezliği gelişebilir. Yine yapılan araştırmalar da, dialize giren çocukların %2-15’inde, kronik böbrek yetmezliğinin HSP’ye bağlı geliştiği gösterilmiştir (13,23,30,68-70).
HSP’de böbrek histopatolojisi, minimal değişikliklerden ciddi yarım ay oluşumu gösteren glomerülonefrite (kresentik glomerülonefrit) kadar değişebilir. Genellikle histopatolojik lezyon fokal yada diffüz mezenkimal proliferasyondur .Bununla birlikte, tipik immunfloresan bulgusu diffüz mezenkimal IgA depolanmasıdır. HSP’de böbrek hastalığının klinik bulguları geçici izole mikroskopik hematüri ve proteinüriden, silindirüri, oligüri, ödem, bozuk glomerüler filtrasyon hızından nefrotik sendrom, hipertansiyon ve böbrek yetmezliğine kadar değişebilir (1,9,13,37,38,71). Tutulumunun en erken bulgusu genellikle hematüridir. Bazen nefrotik sendrom görülebilir (1,9,32).
İzole mikroskopik hematüri en sık rastlanan bulgu olup renal tutulumu olan olguların %50’sinde mevcuttur. Bununla birlikte mikroskopik hematüri ve birlikte proteinüri görülen olgular daha az sayıdadır. Nefritli olguların 1/3’ünde makroskopik gross hematüri görülürken, yine olguların 1/4’ünde de hafif veya orta derecede proteinüri vardır (6,13,15,32,72).
Nefritik sendrom gelişen olgularda hipertansiyon, azotemi ve oligüri görülebilmektedir. Hipertansiyon çok sık görülmemekle birlikte yapılan çalışmalarda, renal tutulumu olanlarda renal tutulum olmayan olgulardan daha yüksek oranda tespit edilebilen hipertansiyon saptanmıştır. Hipertansiyon oranları değişmekle birlikte, çalışmalarda %10-30 oranında görüldüğü belirtilmektedir (1,9,13,16,73).
Hastalığın akut fazında sadece hematüri veya sadece proteinüri tespit edilen çocuklarda, ileride kronik böbrek hastalığı gelişmezse de, hem proteinüri hem de hematürisi olanlarda %15 oranında renal yetmezlik gelişebileceği belirtilmektedir. On yılın üzerinde
nefritik-nefrotik semptom tablosu gösteren HSP’li olguların %50’sinde, son dönem böbrek yetmezliği oluşmaktadır.
Proteinürinin devam etmesi, renal yetmezliğin en iyi göstergesidir. Belirgin proteinüri, nefrotik sendrom veya bozulmuş renal fonksiyon olsun ya da olmasın kronik renal yetmezlik gelişimi için önemli bir risk faktörüdür. Nefritik veya nefrotik sendrom bulguları olmayan, idrar, kan bulguları normale dönen çocuklarda, son dönem böbrek hastalığı gelişmesi beklenen bir durum değildir. İki yıl içinde iyileşmeyen böbrek bulguları, hastalığın kronikleştiğini göstermektedir (6,13,38,68,70,74-77).
Yapılan çalışmalar patolojik sürecin hastalığın en önemli prognostik göstergesi olduğunu göstermiştir. Son dönem böbrek yetmezliği gelişme riski, renal histopatolojide yarım ay (kresent) oluşumu gösteren glomerüllerin sayısıyla orantılıdır. Yapılan biopsiler de %50’den daha fazla glomerülde yarım ay oluşumu gösteren olguların %55’inde prognozun kötü olduğu ve bunların %36’sında son dönem böbrek yetmezliği geliştiği bildirilmiştir. Nefrotik sendrom ve büyük oranda yarım ay (kresent) oluşumu görülen akut glomerülonefritli olgularda da kötü prognoz saptanmıştır.Yine literatürde yapılan bir çalışmada fibröz yarım ay oluşumu (kresent) gösteren olguların prognozunun, fibroselüler yarım ay oluşumu gösterenlere göre daha kötü olduğu bulunmuştur (38,70,71,74,78). Pozitif idrar bulgusu devam eden veya major böbrek bulguları görülen nefritik olgularda veya nefrotik sendrom olup olmadığına karar verilemeyen olgularda böbrek biyopsisi yapılmalıdır (1,9,13).
HSP’de renal tutulumu olan hastalarda prognoz oldukça değişkendir. HSP’de mortalitenin en önemli nedeni renal tutulumdur ve mortalite oranı %1’in altındadır. Bunun yanında yapılan uzun süreli takiplerde ise morbiditenin %1 civarlarında olduğu belirtilmektedir (1,9,68,71).
HSP’de hastalığın başlangıcında renal tutulumu bulunmasa bile renal tutulum yönünden risk faktörü içeren hastalar sonraki kontrollerinde renal tutulum yönünden dikkatle izlenmelidirler. Ayrıca renal tutulumu bulunan hastaların en az 5 yıl süreyle takibinin önem taşıdığı yapılan çalışmalarda belirtilmektedir (1,6,9,16,38,74,76).
Diğer Üriner Sistem Bulguları ;
HSP, temelde bir vaskülit olduğundan skrotal damarların etkilenmesine bağlı olarak testisler, testis appendiksi, epididim, spermatik kord tutulumu bulunabilmekte ve skrotal duvarda enflamasyon ve kanama da olabilmektedir. Nadiren testis tutulumu cilt bulgularından önce olabilmektedir. Tutulumun %2-38 gibi değişen oranlarda olduğunu belirten çalışmalar mevcuttur (6,13,30,79).
Testis ve epididim tutulumu sonucu oluşan akut skrotal şişme, testis torsiyonunu veya inkarsere ingiunal herniyi taklit edebilir. HSP’de gerçek testis torsiyonu nadir olmakla birlikte, gerçek torsiyon görülen olgular literatürde bildirilmiştir (13,78,79).
Akut skrotal tutulum olan çocuklarda gerçek torsiyon ayrımını yapabilmek için ultrasonografi (USG) ve teknesyum 99 m radionükleit sken kullanılması önerilmektedir. Skrotal ödem nedeniyle USG’de yanlış sonuçlar olabileceğinden, gerçek ayırıcı tanıda nükleer görüntülemenin USG’den daha doğru sonuçlar vereceği bildirilmektedir. Akut cerrahi girişim gerektiren gerçek bir torsiyon olmadıkça skrotal şişme ve ağrı kısa sürede ve tedaviye gerek kalmadan iyileşmektedir (13,78,79).
HSP’de oluşabilecek diğer genitoüriner komplikasyonlar: üreter kalsifikasyonu, mesane duvarı hematomu, üretritis, hemorajik spermatik kord ve hidronefrozdur. Bu bulgular genellikle tedaviye gerek kalmadan, kendiliğinden iyileşmektedir. Steroid tedavisi kullanılmakla beraber yararı tartışmalıdır. Bunların dışında nadiren stenozan üretrit ve ekstrinsik üretral stenosis (retroperitoneal fibrozis) görülen olgular da bildirilmiştir (13,79,80).
Nörolojik Bulgular :
HSP’de hem merkezi sinir sistemi (MSS) hem de periferik sinir sistemi tutulabilir. MSS bulguları; vaskülit, hemorajik diyatez ve bazen de renal tutulum sonucu gelişen hipertansiyon ve metabolik değişikliklere bağlı olarak gelişebilmektedir (6,13,81,82). Genel olarak HSP’de sinir sistemi tutulumu %2-20 arasında değişen oranlar bildirilmiştir (81,82). Baş ağrısı, davranış değişikliği ve konvülsiyon en sık görülen nörolojik bulgulardır. Bazı olgularda baş ağrısı ilk semptom olarak ortaya çıkabilir ve birlikte hipertansiyon olabilir. Baş ağrısının herhangi bir karakteristik özelliği ve tarifi yoktur. Davranış değişikliği, irritabilite, apati, hiperaktivite ve karakter değişikliği şeklinde ortaya çıkabilir.Bu bulgular hastalığın başlangıcında döküntüden önce bile oluşabilmektedir. Konvülsiyonlar; parsiyel, parsiyel ve generalize, parsiyel kompleks, generalize ve status şeklinde olabilmekte ve bazen ilk nörolojik bulgu bir konvülsiyon atağı olabilmektedir. Daha nadir olarak da inflamatuar, iskemik ve hemorajik MSS lezyonlarının varlığı nedeni ile kore, kortikal körlük, afazi, hemiparezi, parapleji, quadripleji, monoparezi ve serebellar disfonksiyon şekillerin de ortaya çıkan fokal nörolojik defisitler de görülebilmektedir (6,13,32,81,83,84).
HSP’li olgularda ortaya çıkan nörolojik bulguların fizyopatolojisine bakıldığında baş ağrısı, ensefalopati ve konvülsiyonların temelinde, diffüz serebral iskemi veya subaraknoid kanama, fokal defisitlerin ve bazı konvülsiyonların temelinde ise daha lokalize serebral
olayların yattığı düşünülmektedir .Serebral ödem oluşumu ise : metabolik bozukluklar, renal tutulum , hipertansiyon ve kortikosteroid tedavisine bağlı olarak gelişebilmektedir. Bununla beraber hipertansiyonun MSS bulgularının ortaya çıkışındaki rolü tartışmalıdır. Hipertansiyon serabral iskemi veya intrakraniyal kanama oluşturarak nörolojik bulgulara neden olabilmektedir. Konvülziyonların temelinde hipertansiyon, elektrolit dengesizlikleri, MSS kanamaları rol alabilmekle beraber nadir olgularda yukarıda söz edilen faktörlerin hiçbirisi olmadan da konvülsiyonlar görülebilmektedir. Burada vaskülite bağlı relatif iskemi sonucu oluşan, nöronal disfonksiyon sorumlu tutulmaktadır (13,81,83).
Mononöropatiler (fasiyal, ulnar, femoral, siyatik, peroneal sinir tutulumu gibi) ve poliradikülopatiler (brakiyal pleksus ve Guillain-Barre sendromu gibi) şeklinde periferik sinir tutulumu da nadir olarak HSP’de görülebilmektedir. Mononöropatilerin fizyopatolojisinde, intranöral hemoraji veya vasa nervosum vasküliti sonucu gelişen iskeminin rol aldığı düşünülmektedir. Bazen bir hematom veya lokalize ödem nedeniyle düşünülen bir fasiyal paralizi olgusu da literatürde bildirilmiştir (1,13,32,81,82,84). Yapılan çalışmalarda,gösterilen anormal EEG bulgularının geçici olduğu saptanmıştır (13,81,83).
Subdural hematom, kortikal kanama, intraparankimal kanama ve infarktlar, subaraknoid kanama veya hipertansif ensefalopatiye bağlı koma HSP’de görülebilen diğer nadir, nörolojik bulgulardır. İntrakraniyal kanamalar ani davranış değişiklikleri ve bilinç kaybı ile ortaya çıkabilirler (13,80,81).
Nörolojik bulgular genellikle geçicidir. Nadiren hemorajik ve iskemik infarktlardan sonra kalıcı defisitler oluşabilir. Konvülsiyonlarda prognoz, konvülsiyonu oluşturan nedenlere bağlıdır. Ciddi intrakraniyal kanama ve renal yetmezlik olmayan durumlarda prognoz iyidir (13,32,81-83).
Hematolojik Bulgular :
HSP’de trombositoz, hipoprotrombinemi, plazma koagülasyon faktör (F VIII ) ve F XIII eksikliği görülebilmekte ve vaskülit ile birlikte hemarojik diyatez bulgularına da saptanabilmektedir (13,15,51,85). Karın ağrısı ve GİS kanaması olan olguların çoğunda trombositoz saptanmaktadır. Trombositozun nedeni tam açıklanmamakla beraber, akut inflamasyonun bir göstergesi olduğu veya GİS kanamasına sekonder olarak ortaya çıktığı ve sedimantasyon hızındaki artış ile ilişkili olduğu belirtilmektedir. Bunun yanında trombositozun GİS kanamasıyla ilişkisinin olmadığını belirten yayınlar da vardır (13,85).
Çalışmalarda F VIII düzeyinin düşüklüğü ile klinik belirtilerin özellikle GİS bulgularının ciddiyeti arasında bağlantı olduğu belirtilmektedir. F VIII düzeyinin normal
değerinin %90’ından daha az olduğunda semptomlar ağırlaşmaktadır. Bununla beraber FXIII düzeyinin hastalığın akut döneminde düştüğü, düşüşle orantılı olarak da GİS semptomlarının arttığı ve renal tutulum gibi önemli komplikasyonların gelişmesi açısından bu durumun önemli bir risk faktörü olabileceği belirtilmektedir. Özellikle F XIII düzeyinin normal değerinin %50’sinin altına düştüğün de komplikasyonların daha hızlı geliştiği ve hastalığın akut döneminde uygulanan F XIII konsantresinin komplikasyon riskini azalttığı yapılan çalışmalarda gösterilmiştir. Bütün bu sözü edilen hematolojik bulgular HSP’de koagülopati oluşturabilmektedir (1,15,51,52,54).
Çok nadir olmakla beraber pulmoner kanama olguları da bildirilmiştir. Pulmoner kanama genellikle öldürücüdür ve yapılan immunokimyasal çalışmalar sonucu alveolar septalarda IgA depositleri saptanmıştır. Yine nadiren subkonjunktival kanamalar, epistaksis ve kas içine kanama görülen olgular da mevcuttur (1,8,9,13,15,86).
Literatürde çok nadir olarak HSP’de göz tutulumu, parotitis, plevral effüzyon, romatoid nodüller, adrenal ve kardiyak tutulum olabileceği bildirilmektedir.Kardiyak tutuluma bağlı ileti bozuklukları ve miyokard infarktüsü olguları da nadir görülen bulgulardandır (1,8,13,15,33,65).
Tanı :
HSP’de tanı öncelikle anamnez ve klinik bulgulara dayanmaktadır. HSP tanısında 1990’da tanımlanan ACR tanı kriterleri kullanılmaktadır (5).
HSP Tanı Kriterleri :
1.Palpabl purpura ( trombositopeni olmadan), 2.Hastalığın başlangıç yaşının 20’den düşük olması,
3.Barsak anjinası; özellikle yemeklerden sonra belirginleşen yaygın karın ağrısı veya genellikle kanlı ishali de içeren barsak vaskülitinin saptanması,
4.Arteriol veya venül duvarlarında granülositleri gösteren histolojik değişiklikler Herhangi iki yada daha fazla kriterin bir arada bulunması HSP’yi %87,1 duyarlılıkla ve %87,7 belirlilikle diğer vaskülitlerden ayırt eder. Çocuklarda HSP tanısı koyabilmek için deri biyopsisi nadiren gereklidir. Fakat yetişkinlerde gerekli olabilmektedir (5).
Ayırıcı Tanı :
HSP genellikle fizik muayene ve anamnezle tanınabilmektedir. Ayırıcı tanı da zorluk sadece bir bulgunun belirgin olduğu veya multisistem tutulumunun bulunmadığı durumlarda
ortaya çıkmaktadır. Bu durumda fizik muayene, laboratuvar testleriyle desteklenmeli ve gerekiyorsa ayırıcı tanı için daha spesifik testler yada görüntüleme yapılmalıdır.
HSP İle Ayırıcı Tanıya Giren Hastalıklar (1,7,9,13,65,87) Meningokok menenjiti yada septisemi
Romatoid artritler Romatizmal ateş
İdyopatik trombositopenik purpura Sistemik lupus eritematosus
Hırpalanmış çocuk İlaç reaksiyonları Bakteriyel endokardit
Kayalık dağlar benekli humması
Laboratuar Bulguları:
Hastalığın tanı koydurucu spesifik laboratuvar bulgusu yoktur. Laboratuvar bulgular sadece tanıya yardımcıdır (1,8,9,13,15).
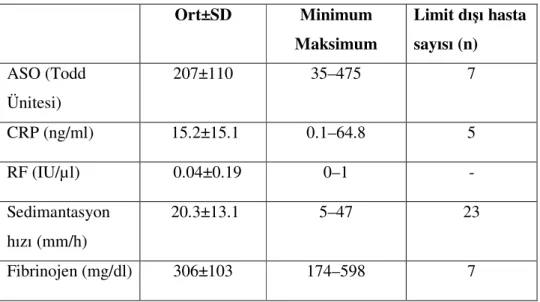
Tam kan sayımında lokösit ve trombosit sayısı sıklıkla orta derecede artmıştır. Eozinofili saptanabilir. Anemi akut kanamalara sekonder olarak gelişebilir. Normokromik anemi gastrointestinal kan kaybı ile ilgili olup, karın ağrısı olan çocukların %80’inde dışkıda gizli kan pozitiftir. Sedimantasyon hızı normal yada enflamasyona bağlı olarak yüksek bulunabilir (1,8,9,13,15).
Bununla birlikte hastalıkta immün kompleksler arttığından, özellikle hastalığın akut fazında çocukların %50’sinde başta serum IgA seviyesi olmak üzere, diğer immunglobin düzeyleri artmıştır. Serum kompleman düzeyi çoğunlukla normal sınırlardadır (1,8,9,10,15,16).
Protrombin zamanı, parsiyel tromboplastin zamanı, kanama ve pıhtılaşma zamanı genellikle normaldir. Hastalığın akut fazında F VIII ve F XIII düzeyleri düşük olabilir ve kanama diyatezi, bu faktörlerdeki düşüklüğe bağlı olarak gelişebilir (1,9,13,54).
Karın ağrısı bulunan hastalarda gaitada gizli kan bakılmalıdır ve %80 olguda pozitiftir. GİS tutulumu bulunan hastalarda serum elektrolit bozuklukları görülebilmektedir (1,8,13).
Böbrek tutulumu sonucu patolojik idrar bulguları görülür. Rutin idrar analizinde hematüriyi saptamak kolaydır. Stickle bakılan idrarda proteinüri pozitif bulunanlarda 24
saatlik protein atılımı, idrar protein/kretain oranı saptanmalı, serum albümin düzeyi bakılmalıdır. Renal tutulum genellikle hastalığın başlangıcından itibaren üç aylık bir sürede çıkabileceğinden, rutin idrar tetkiki bu süre içinde yapılmalıdır. Risk gurubu oluşturan vakalarda bu süre daha da uzun tutulmalıdır. Böbrek bulguları ısrarla devam eden ve majör böbrek bulguları olan olgularda, sböbrek biyopsisi yapılmaktadır. Kan üre ve nitrojeni, kreatinin renal yetmezlik durumlarında artmıştır (1,8,9,13,15).
Komplikasyonları tanımak için yapılan rutin laboratuvar incelemelerine ek olarak, hastalığın seyrine göre tanıya yönelik daha spesifik incelemeler yapılmalıdır. İntraabdominal acil durum şüphesi olan olgularda, ayakta direkt batın grafisi ve USG yapılmalı, hem tanı hem de tedavi açısından baryumlu inceleme planlanmalıdır. Hepatosplenomegalisi ve safra hidropsu bulunan USG ve karaciğere yönelik kan tetkikleri yapılmalıdır. Pankreaittten şüphelenilen olgularda serum amilazı çalışılmalıdır (1,8,9,13).
Ciddi nörolojik bulgular varlığında ileri görüntüleme yapılmalıdır. Skrotal tutulum şüphesinde doppler USG yada sintigrafik görüntüleme planlanmalıdır. Hemoptizi görülen olgularda akciğer grafisi çekilmelidir (1,8,9,13,79,81,82,86).
Etyolojiyi aydınlatmak açısından boğaz kültürü ve serolojik tetkikler yapılabilir. ASO titresinde artış olabilmekle birlikte yapılan çalışmalarda anlamlı fark bulunamamıştır (1,8,9,13,65).
Deri biyopsisinde IgA depolanmaları ve lökositoklastik vaskülit görülebilir (1,6,8,9,13,65).
Bununla birlikte anti-nötrofilik sitoplazmik antikor (ANCA), anti nükleer antikor (ANA), RF genellikle negatif sonuç verirler. Antikardiolipin yada antifosfolipid antikorlar pozitif bulunabilirler ve intravasküler koagülopati oluşumuna katkıda bulunabilirler (1,8,32).
Tedavi :
HSP sıklıkla kendi kendine düzelebilen bir hastalıktır. Çoğu zaman tedaviye gerek duyulmaz. Hastalığın spesifik bir tedavisi yoktur. Esas olan destekleyici tedavidir. Hastalığın akut fazında yatak istirahati ve uygun hidrasyon sağlanmalıdır. Olgularda vital bulgular takip edilmeli, rutin laboratuvar tetkikleri yapılmalı, dışkıda gizli kan bakılmalı ve komplikasyonlar bakımından izlenmelidir. Gereksiz tüm ilaçlar kesilmeli, bilinen allerjen varsa uzaklaştırılmalıdır. Hastada altta yatan bir enfeksiyon varsa uygun antibiyotikle tedavi edilmelidir. Döküntü, eklem tutulumu ve ödem semptomatik olarak tedavi edilmelidir. Nonsteroid antienflamatuarlar ve asetaminofen eklem ve yumuşak doku şikayetlerini azaltmada yararlıdır. Özellikle asetaminofen ateş ve ağrıyı önleme konusunda daha yararlı
olmaktadır. Aktivite kısıtlaması alt ekstremite lokal ödemini azaltmakta ve eğer skrotal ödem var ise skrotum elavasyonu ve lokal soğuk uygulaması rahatlama sağlamaktadır (1,6,8,9,13,65,87).
Kortikosteroidlerin tedavideki yararları hala tartışmalıdır.GİS tutulumu, MSS tutulumu, ağır organ iskemileri ve kanamalarda kullanılmaktadır. Özellikle intestinal komplikasyonlarda (intussusepsiyon, kanama, obstrüksiyon gibi) steriod kullanımı hayat kurtarıcı olabilmektedir. Erken dönemde oral ya da intravenöz kortikosteroidlerle (1-2 mg/kg/gün) tedaviye başlanması ile GİS ve MSS komplikasyonları dramatik biçimde düzelebilmektedir. Bununla birlikte döküntü, eklem şikayetleri veya renal hastalık tek başına mevcut ise kortikosteroid tedavi önerilmemektedir (1,6,8,9,13,16,38).
Erken dönemde steroid kullanımının HSP nefriti gelişimini önlediği konusunda çelişkili sonuçlar bildirilmektedir. Buchanec ve arkadaşlarının çalışmasında hastalığın başlangıcında 1,7 mg/kg prednison başlanan ve 21 gün süreyle tedavi edilen hastalarda nefropati insidansının, kortikosteroid kullanmayan hastalardan altı kat daha az olduğu bulunmuştur (88). Yine Mollica ve arkadaşlarının yaptığı bir çalışmada hastalığın başlangıcında 2 hafta süreyle 1 mg/kg prednison alan hastalarda hiç nefropati gelişmediği ve tedavi edilmeyenlerle karşılaştırıldıklarında iki grup arasında nefropati insidansının anlamlı farklı olduğu bildirilmiştir (89).
Bunların tersine Saulsbury’nin yaptığı çalışmada kortikosteroid tedavinin nefropati gelişimini önlemediği bulunmuştur (90). Bununla birlikte konunun netlik kazanması için daha çok hasta grubu içeren, prospektif ya da kontrollü çalışmalar yapılması gerekli olduğu belirtilmektedir. Ancak ileride erken kortikosteroid kullanımının HSP nefrit gelişimini önlediği kabul görürse, nefrit gelişimi ile ilgili risk faktörleri taşıyan hasta grubuna profilaktik steroid kullanımı düşünülebilir (1,8,15,16,30,65).
Ciddi böbrek tutulumu acil tedavi gerektirir, özellikle nefrotik sendrom veya böbrek biyopsisinde %50’den fazla kresentik glomerül saptanmışsa tedavi hemen başlanmalıdır. Bu durumda intravenöz pulse metilprednisolon başlanır ve üç gün verilir. Yoğun uygulamadan sonra kortikosteroidlerle uygun dozda oral olarak, genellikle üç ay süre devam edilir. Bu süre bir yıla kadar uzayabilir. MSS, pulmoner tutulum gibi hayatı tehdit eden ciddi hastalık tutulumlarında da pulse steroid tedavisi etkilidir. Tedavi pulmoner lezyonların rezolüsyonu, idrar sedimenti bulgularının ve yapılabiliniyorsa tedavi sonrası böbrek biyopsi bulgularının düzelmesi ile değerlendirilir. Pulse steroid etkinliği tartışmalı olmakla birlikte yapılan çalışmalar yararlı olduğu lehinedir (1,9,13,30,32,38,77,86,91).
Bunun yanında kortikosteroid tedavisine yetersiz cevap: beklenmedik şekilde agresiv veya progresif hastalık varlığı, iki aylık yüksek doz steroid tedavisinden sonra steroidin azaltılmaması ve erken steroid komplikasyonları görülmesi gibi durumlarda tedavide immun sistemi baskılayıcı ilaçlar (Siklofosfamid, Azothioprin, Siklosporin, Metotreksat gibi) tek yada steroidler ile birlikte kullanılabilirler. Bu kombinasyon tedavilerinin etkinliği de tartışmalıdır (1,9,13,32,38,85,92,93).
Antitrombositer ilaçlar (Dipridamol, Asetilsalisilik asit gibi) tromboz durumları yada steroid tedavi ile birlikte kullanılabilir (1,8,9,13,93).
Plazmaferezin, özellikle tedaviye dirençli hızla ilerleyen böbrek hastalığında böbrek fonksiyonlarını düzeltmek açısından yararlı olduğu yapılan çalışmalarda belirtilmektedir. Ciddi nörolojik, pulmoner ve GİS tutulumunun var olduğu durumlarda dolaşımda bulunan immün komplekslerin dolaşımdan uzaklaştırmak için de yapılmaktadır. Ancak etkinliği tam olarak ispatlanmamış bir yaklaşımdır (6,13,30,32,39).
Hastalığın akut döneminde F XIII düzeyi düşük olan hastalara F XIII konsantresi verilmesi ile GİS ve eklem semptomlarının düzeldiği, proteinüri ve hematüriyi gerilettiği yapılan çalışmalarda bildirilmiştir .Fakat etkili olmadığını gösteren çalışmalarda mevcuttur (15,54,55).
Nefropati gelişen olgularda sıvı-elektrolit dengesinin sağlanması, tuz alımına dikkat edilmesi, gerekli durumlarda antihipertansiflerin kullanılması gerekmektedir (1,8,9,13,16).
HSP de görülen romatoid nodüllerin, tedavisinde gün aşırı kolşisin kullanılmasıyla tedaviye iyi yanıt alındığı belirtilmektedir (8).
Komplikasyonlar :
Hastalık bir vaskülit olduğundan birçok sistemi tutabilmektedir. Bu nedenle de multi-sistem tutulumunda birden fazla ve değişik komplikasyonlar ortaya çıkabilmektedir. Hastalığın major komplikasyonları böbrek tutulumu ile birlikte nefrotik sendrom gelişmesi ve barsak perforasyonudur. MSS, pulmoner ve skrotal tutulumuma bağlı gelişebilen komplikasyonlar daha nadir ancak ciddi komplikasyonlardır.
HSP ile ilişkili komplikasyonlar şöyle sıralanabilir:
Böbrek yetmezliği, hematüri, proteinüri, GİS kanaması, barsak infarktı, intussusepsiyon, kanama, şok, hepatosplenomegali, miyokard enfarktüsü, pulmoner kanama, plevral effüzyon, nöbetler, mononöropatiler, orşit, testis torsiyonu, gereksiz batın cerrahisi gibi durumlar sıralanabilir (1,6,8,13).
Hastalığın Gidişi ve Prognoz:
Hastalık genellikle selim seyirli ve kendi kendini sınırlayabilen karakterde olduğundan çoğu hasta için prognoz mükemmeldir. Bununla birlikte böbrek ve GİS tutulumu morbidite ve mortaliteyi belirleyicidir. Nadir olarak hastalığın akut fazında barsak infarktı, MSS tutulumu yada böbrek hastalığı sonucunda ölüm olabilmektedir. Daha az olarak pulmoner kanamaya bağlı ölümler bildirilmiştir (1,6,8,9,13,74,86).
Hastalık, genellikle 2-4 haftada semptomatik tedavi sonucunda yada kendiliğinden iyileşmektedir. Bazen iyileşme 6 haftaya kadar uzamaktadır. Hastalık 7 yaş altında daha iyi bir prognoza sahiptir ve daha küçük çocuklarda hastalık daha kısa sürer ve daha az oranda tekrarlar . Hastaların yaklaşık yarısında bir kez tekrarlar ve bu sıklıkla döküntü ve karın ağrısı şeklinde olur. Genellikle tekrar atakları daha hafif ve daha kısa sürelidir. Tekrar atakları spontan olarak veya solunum yolu enfeksiyonlarını takiben ortaya çıkabilmektedir. Tekrarlarda eklem bulguları ve hematüri nadiren olabilmektedir. Hematürinin ilk olarak relapsların birinde izlenmesi daha da nadir bir olasılıktır (1,8,9,13).
Böbrek tutulumu olan hastalarda prognoz oldukça değişken olduğu için böbrek tutulumu olanlarda uzun süreli takip yapılmalıdır. Renal hastalık uzun bir dönem ilerleme göstermeyebileceğinden, renal tutulumu bulunan olguların 5 yıl süreyle izlenmesi gerekli olabilmektedir.
Patolojik süreç hastalığın en önemli prognostik göstergesidir. Son dönem böbrek yetmezliği gelişme riski, renal biyopside ki yarım ay (kresent)oluşumu gösteren glomerüllerin sayısıyla orantılıdır.Yapılan biyopsiler de %50 ya da daha fazla yarım ay oluşumu gösteren glomerül içeren olgular ve nefrotik sendrom ile birlikte büyük oranda yarım ay(kresent) oluşumu görülen akut glomerülonefritli olgular kötü prognoza sahiptir. Fibröz yarım ay oluşumu (kresent) gösteren olguların prognozu, fibroselüler yarım ay oluşumu gösterenlere göre daha kötüdür. Çocuklarda renal tutulumun prognozu genellikle iyi olmakla beraber, kalıcı fonksiyon bozukluğu ve nadiren son dönem böbrek yetmezliği de gelişebilmektedir. Olguların %1’inde persistan nefropati oluşumu, %1’inden azında ise son dönem böbrek yetmezliği gelişebilmektedir. On yılın üzerinde nefritik-nefrotik semptom tablosu gösteren HSP’li olguların %50’sinde son dönem böbrek hastalığı oluşmaktadır. Bunun yanında renal tutulum olsun ya da olmasın son dönem böbrek yetmezliği oranı %5’in altındadır (1,6,9,38,70,71,74,78).
Hastalığın akut fazında sadece hematüri veya sadece proteinüri tespit edilen çocuklarda prognoz mükemmeldir. Belirgin proteinüri, nefrotik sendrom veya bozulmuş renal fonksiyon olsun yada olmasın kronik renal yetmezlik gelişimi için önemli risk bir faktörü olduğundan
bu hastalarda prognoz kötüdür. İki yıl içinde iyileşmeyen böbrek bulguları, hastalığın kronikleştiğini gösterir. İdrar ve kan bulguları normale dönen çocuklar iyi prognoza sahiptir (1,6,8,13,38,68,70,74-77). Nadiren, MSS hasarına bağlı uzun süreli morbidite ve sekeller oluşmaktadır (1,6,8,83).
SERBEST RADİKALLER
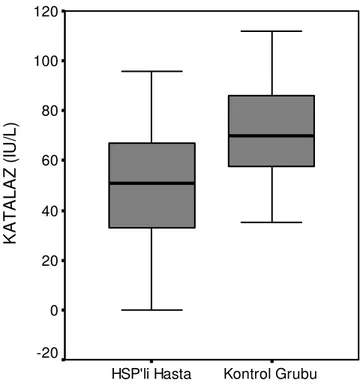
Serbest radikaller en dış yörüngelerinde bir yada daha fazla çiftleşmemiş elektron içeren reaktif moleküllerdir. Oksijen türevi radikaller biyolojik sistemin en iyi bilinen serbest radikalleridir. Canlı hücrelerde normal süreçte fizyolojik miktarlarda üretilir. Aşırı oluştuklarında hücre ve doku hasarına neden olurlar (94,95). Serbest radikaller kararsız moleküllerdir. Etkileri antioksidan yeteneği olan enzim veya moleküller tarafından engellenir (96). Serbest radikal oluşumu ile antioksidan savunma sistemi arasındaki hemostatik denge bozulursa, inaktive edilemeyen serbest radikaller de lipitlerin, proteinlerin, polisakkaritlerin oksidasyonu ve DNA hasarına yol açarlar (97,98,99).
Serbest radikaller, biyolojik sistemde travma, infeksiyon, inflamasyon gibi immun sistemin aktive olduğu durumlarda (100), iskemi –perfüzyon doku hasarında (101), yüksek konsantrasyonda O2 kullanımında (102) aşırı miktarda oluşur. Sepsis, inflamatuar hastalıklar, adült respiratuvar sendromu, diabetes mellitus, kardiovasküler hastalıklar, astım, bronkopulmoner displazi gibi birçok hastalığın patogenezinde serbest radikal hasarı suçlanmıştır (103-109).
Oksidatif stres, serbest radikal oluşumu ile antioksidan sistemler arasındaki hemostatik dengenin bozulması sonucu oluşur.
Oksitatif Stres İle İlgili Terimler ve Açıklamaları
1.Serbest radikal: En dış orbitalarında bir veya birden fazla çiftleşmemiş elektron ihtiva eden, bir çok maddelerle reaksiyona girme yeteneğine sahip yapılardır. Vücutta birçok hücresel hasara yol açabilen reaksiyondan sorumludur.
2.Reaktif Oksijen Türleri: Oksijenin indirgenmesi sonucu oluşan, serbest radikal olabilen atom veya moleküllere denir. En iyi bilinenleri süperoksit, hidrojen peroksit ve hidroksil radikalidir.
3.Oksidasyon: Kimyasal reaksiyonlarda elektron kaybı. 4.Redüksiyon: Kimyasal reaksiyonlarda elektron alımı.
5.Redüksiyon –Oksidasyon: Kimyasal reaksiyonlarda elektronların alışverişini içeren redüksiyon –oksidasyon reaksiyonlarındaki dengedir.
6.Oksidatif Stres: Serbest radikallerin birikimi yada antioksidanların serbest oksijen radikallerin birikimini engelleyememesi, serbest radikal oluşumu ile antioksidanlar arasındaki dengenin bozulması sonucu oluşan durumdur.
7.Antioksidan: Serbest radikalleri ortamdan uzaklaştıran yada onların hücre üzerindeki etkilerini engelleyerek serbest radikallerin birikimini önleyebilen maddelerdir.
Serbest Radikallerin Oluşumu : Serbest radikaller üç yolla oluşabilir:
1.Radikal olmayan bir bileşikteki kovalan bağların koparılmasıyla iki ayrı radikal oluşumu. Bu işlem ultraviyole ışını, ısı, iyonize radyasyon gibi yüksek enerji gerektirir.
2.Normal bir molekülden elektron kaybı. 3.Normal bir moleküle elektron transferi
Serbest radikallerin en dış yörüngesindeki çiftleşmemiş elektron, sonuç olarak oluşan serbest radikalin yükünü değiştirmez. Serbest radikaller elektriksel olarak pozitif yüklü, negatif yüklü ya da nötral olabilir. Elektriksel yük proton ve elekron sayılarıyla ve konumuyla ilişkilidir.
Serbest Radikal Tipleri :
Vücutta bilinen en önemli serbest radikaller Reaktif Oksijen Türleri (ROS) olarak bilinen oksijen kaynaklı serbest radikallerdir.
Süperoksit: Süperoksit serbest radikal anyonu oksijenin en dış yörüngesine elektron transfer edildiğinde oluşur. En önemli kaynak mitokondrilerde bulunan elektron transfer zincirinden kaynaklanan sızıntılardır. Süperoksitin kendisi fazla hasar oluşturmaz fakat birçok zararlı ara ürünlerin oluşumunda rol alır. Önemi, hidrojen peroksit için bir kaynak olması, letal hidroksil radikallerin oluşumunda prekürsör olan geçiş elementleri için redüktan bir madde olmasıdır. Aynı zamanda nötrofillerce hidroklorik asit oluşumunda rol oynar.
Hidrojen peroksit: Serbest radikal değildir. Fakat geçiş metal iyonlarının varlığında hidroksil radikallerinin ana kaynağı olması nedeniyle önemlidir.
Hidrojen peroksit O2’nin iki elektron ile indirgenmesinden oluşur. Kaynağını süperoksit radikalinden alır .İki süperoksit birleşerek hidrojen peroksit ve O2 oluşur.
2 O 2 + 2H → H2O2 +O2 (dismutasyon reaksiyonu)
Yukarda görülen reaksiyonda, reaktanlardan radikal olmayan ürünler oluşur ve bu basamağı SOD (Süperoksit dismutaz) katalizler.
Tekli Oksijen: Radikal olmayan bir reaktif oksijen türüdür. Güçlü oksidan aktivitesi nedeniyle serbest oksijen radikalleriyle ilişkilidir. Oksijenin mutajenik bir formudur ve oluşumu için radyasyon gerekir (110).
Hidroksil Radikali: 1933 ‘de Fritz Haber ve Joseph Weiss ilk defa hidroksil radikalini, süperoksit iyonunun hidrojen peroksit ile etkileşime girdiğinde oluştuğunu buldular. Hidroksil radikali oldukça reaktif bir oksidan radikaldir ve birçok reaksiyonu başlatmada görev alır. Nitrik Oksit: Gaz yapısında en sık görülen serbest radikaldir. Endotelyum kaynaklı gevşetici faktör olarak bilinir. Vasküler endotel nitrik oksit üretir. Nötrofil ve makrofajlar nitrik oksit sentetaz enzimini kullanarak arjininden nitrik oksit oluşturabilirler (111,112). Peroksinitrit: Nitrik oksitin süperoksit ile reaksiyonu sonucu oluşur.
Hipoklorik asit: Klor iyonlarının, hidrojen peroksit varlığında, myeloperoksidaz enzimi etkisiyle etkileşime girmesiyle oluşur. Hipoklorik asit hücre membranlarını geçebilir ve geçiş elementlerin varlığında hidroksil radikali oluştururlar.
Hipoklorik asit lipit peroksidasyonu başlatma yeteneğine sahiptir. Hidrojen peroksitle beraber olduğunda DNA‘ya zarar verebilir, DNA onarım yeteneğini bozabilir, intraselüler ve serbest kalsiyum düzeyini değiştirebilir (113). Hipoklorik asit inflamatuar işlem sırasında doku hasarına katkıda bulunabilir (114).
Serbest Radikal Kaynakları Endojen Kaynaklar:
1.Oto-oksidasyon : Aerobik metabolizmadan kaynaklanan ürünlerdir. Katekolamin, hemoglobin, myoglobin, indirgenmiş sitokrom c ve tiollerin otooksidasyonu sonucu endojen radikaller oluşur. Süperoksit primer oluşan radikaldir. Ferröz demir de bu moleküllerden elektron alarak süperoksit oluşturur ve +3 değerlikli demire dönüşür (115).
2.Enzimatik Oksidasyon: Birçok enzim sistemi serbest radikal oluşturabilir. Lipooksijenaz, aminoasit oksidaz, aldehit oksidaz, ksantin oksidaz, prostoglandin sentaz gibi enzimlerdir. Myeloperoksidaz güçlü bir oksidandır ve hipoklorikasit oluşturmak için hidrojen peroksit ve klor iyonlarını kulanır (116).