BT çekilen hastalarda kontrast madde nefropatisi gelişiminin tesbitinde idrar sitokinleri
Tam metin
Şekil



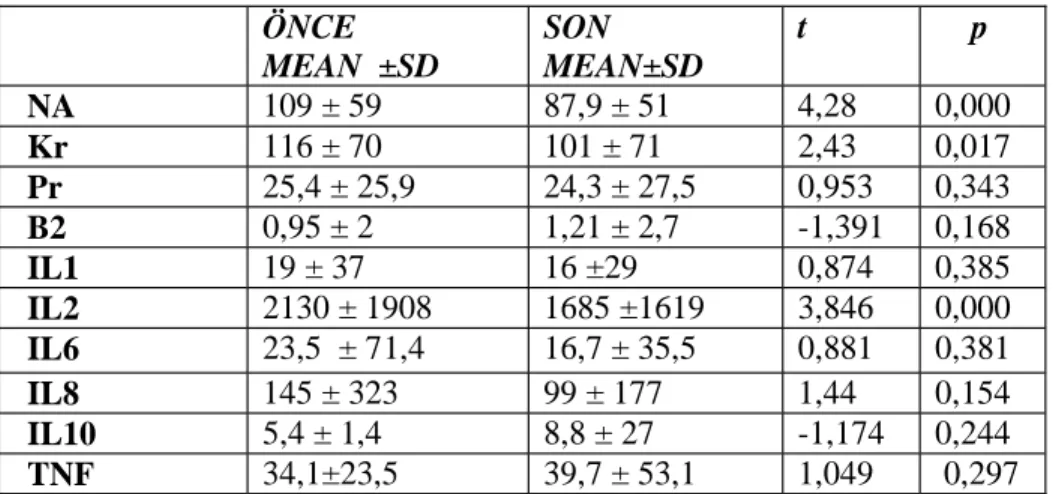
Outline
Benzer Belgeler
17 Mart tarihinde Ara mallar grubu firmalarında kümülatif anormal getiri en düşük seviyesi olan -%13,6’ ya, sermaye malları grubu firmalarında ise -%7’ye ulaşmıştır..
The path tracking effect of an unmanned vehicle is stronger after using this method, according to the above experiments. It is important to study the direction and attitude
ABD’de İse yakın za mana kadar Üniversiteli bir ka dın aynı bölümden biri ile ev lenince ya işinden ayrılmaya, ya da fahri olarak çalışmaya mecbur
Đkinci tanımlamaya göre (bazal kreatinin değerine göre ≥0.5 mg/dl artış) değerlendirildiğinde tüm hastaların 2 tanesinde (% 2,6) KMN gelişti ve bu iki hasta da kontrol
Sonuç olarak yüksek riskli hastalarda, ifllem öncesi ve son- ras› yeterli hidrasyon yap›lmas›, non-ionik izo-ozmolar kontrast madde tercihi, nefroprotektif
Bulgular: Koroner anjiyografi öncesi kaptopril verilen grupta 5 hastada (% 8.3), kontrol grubunda ise 1 has- tada (% 3) kontrast madde nefropatisi geliflti ve bu fark
Kreatinin düzeyi hafif yüksek olan hastalarda koroner anjiyografiden üç saat önce uygulanan oral N-asetilsisteinin kontrast nefropatisini..
Kontrast maddeler, yoğunluğu dokulardan az olan veya çok olan maddeler olup, x – ışınlarını dokulardan daha çok tutar veya daha çok geçirirler.. Bu inceleme ile