T.C.
EGE ÜNİVERSİTESİ
TIP FAKÜLTESİ
İÇ HASTALIKLARI ANABİLİM DALI
Son dönem Kalp yetersizliği olan hastalara uygulanan Sol
ventrikül destek cihazı tekniğinin böbrek fonksiyonları üzerine
kısa ve uzun dönem etkilerinin retrospektif değerlendirilmesi
UZMANLIK TEZİ
Dr. Anar Sadıgov
DANIŞMAN
Doç. Dr. Meltem Seziş Demirci
İZMİR
T.C.
EGE ÜNİVERSİTESİ
TIP FAKÜLTESİ
İÇ HASTALIKLARI ANABİLİM DALI
Son dönem Kalp yetersizliği olan hastalara uygulanan Sol
ventrikül destek cihazı tekniğinin böbrek fonksiyonları üzerine
kısa ve uzun dönem etkilkerinin retrospektif değerlendirilmesi
UZMANLIK TEZİ
Dr. Anar Sadıgov
DANIŞMAN
Doç. Dr. Meltem Seziş Demirci
İZMİR
2018
1
TEŞEKKÜR
Hekimlik mesleğinin öğrenilmesinde önemli kademelerden biri olan asistanlık eğitiminin sonuna gelmiş bulunuyorum. İç Hastalıkları uzmanlık eğitimi boyunca bana emek veren, bilgi, deneyim ve manevi desteklerini benden esirgemeyen başta Anabilim Dalı Başkanımız Prof. Dr. Fehmi Akçiçek olmak üzere her biri çok değerli olan tüm Ege Üniversitesi İç Hastalıkları Ana bilim hocalarıma; Tez çalışmamda bilgi birikim ve görüşleriyle beni yönlendiren tez danışman hocam Doç. Dr. Meltem Seziş Demirci’ye. Tez çalışmam süresince yardımlarını esirgemeyen, Kardiyoloji ABD hocalarımızdan Prof. Dr. Sanem Nalbantgil’e, bilgi ve tecrübesini benimle paylaşan Doç. Dr. Cenk Demirci’ye, Uzm. Dr. Emre Demir’e; Asistanlık sürecinde birlikte çalıştığım saygıdeğer asistan arkadaşım Dr. Alide Aliyeva başta olmakla tüm asistan arkadaşlarıma; Eğitimim süresince birlikte çalıştığımız ve tezim süresince yardımlarını eksik etmeyen tüm hemşire ve personel arkadaşlara teşekkür ederim. Hayatımın her döneminde yanımda olan anne, babam ve kardeşime,
Son olarak; sevgili eşim ve oğluma,
Sonsuz sevgi, saygı ve teşekkürlerimi sunarım.
Dr. Anar Sadıgov İzmir-2018
2
İÇİNDEKİLER
TEŞEKKÜR ... 1 İÇİNDEKİLER ... 2 Özet ... 4 Abstract ... 5 TABLO LİSTESİ ... 7 ŞEKİL LİSTESİ ... 8 KISALTMALAR ... 9 1. GİRİŞ... 11 2. GENEL BİLGİLER ... 13 2.1.KALP YETERSİZLİĞİ ... 13 2.1.1.TANIM VE TERMİNOLOJİ ... 132.1.2. KALP YETERSİZLİĞİNİN EPİDEMİYOLOJİSİ ... 13
2.1.3. KALP YETMEZLİĞİNİN PATOFİZYOLOJİSİ... 13
2.1.4. KALP YETERSİZLİĞİ SINIFLANDIRILMASI ... 14
2.1.5 KALP YETERSİZLİĞİ TANISI ... 15
2.1.5.1 Belirti ve Bulgular ... 15
2.1.5.2 Renin Anjiyotensin Aldosteron Sistemi (RAAS), Natriüretik Peptidler, Elektrokardiyogram, Ekokardiyogram ... 15
2.1.6 KALP YETERSİZLİĞİNİN TEDAVİSİ ... 16
2.1.7 KALP YETMEZLİĞİNDE MEKANİK DESTEK CİHAZI TEDAVİSİ ... 16
2.1.8 Kardiyorenal Sendrom (KRS) ... 20
2.1.9 Kardiyo Renal Sendrom Sınıflaması (KRS) ... 20
2.1.8 AKUT DEKOMPANSE KALP YETMEZLİĞİ TEDAVİSİ ... 22
3. GEREÇ VE YÖNTEM ... 25
3.1 Hastalar ... 25
3.2 Yöntem ... 25
3.3 İstatiksel Analiz ... 25
3
4.1 Bazal Demografik ve laboratuvar Verileri ... 26
4.2 İzlemde GFH değişimleri ve Etkileyen Faktörler ... 29
4.3 Sağkalım ... 31
5. TARTIŞMA ... 38
6. SONUÇ ... 44
4
Özet
Dekompanse kalp yetersizliği tanısı alan ve maksimum medikal tedaviye rağmen istirahatte belirgin kalp yetersizliği semptomları devam eden hastalara girişimsel tedavi yöntemlerinden biri olarak sol ventrikül destek cihazları (LVAD) takılmaktadır. Son dönem kalp yetmezliği hastalarında uç organ perfuzyon bozukluğuna bağlı kardiyorenal sendromun görülme sıklığı yüksektir. Bu çalışmanın amacı son dönem kalp yetmezliği olan hastalara uygulanan LVAD implantasyon tekniğinin böbrek fonksiyonları üzerine kısa ve uzun dönem etkilerinin retrospektif olarak değerlendirilmesidir.
Çalışmamızda son dönem KY tanısı alan 329 LVAD (HeartWare, HeartMate II, HeartMate 3) cihazı takılan hasta alındı. Hastaların LVAD implantasyonu öncesi ve sonrası, 60 ay sürecindeki biyokimyasal parametreleri retrospektif tarandı. Bazal ve izlemdeki GFH (CKD-Epi) değerleri hesaplandı. Tüm istatiksel analizler için “SPSS 22.0” yazılımı kullanıldı. Bazı analizlerde Pearson ve Spearman’ın korelasyon analizi kullanıldı. Sağkalım analizleri için Kaplan-Meier yöntemi uygulandı ve istatistiksel anlamlılık log-rank testi ile değerlendirildi. İzlemde bağımsız mortalite belirleyicilerini saptamak için Cox regresyon analizi yapıldı.
Hastaların yaş ortalaması 50.8±13.2, %86’sı erkek, ortalama bazal GFH’ı 77,6 ± 25,7 ml/dk/1,73m2, %29,5’u DM, %34,1’i HT tanılı idi. LVAD implantasyonu sonrası ilk 1. ayda tüm hastaların ve grupların ortalama GFH değerlerinde bazale göre anlamlı bir artış saptandı (p<0.01). Bazal GFH’ı <60ml/dk olan hasta grubunda imlantasyon sonrası 1, 6, 12, 24. aylarda bazale göre anlamlı artış (p<0.001) mevcut, 36. ayda artış anlamlı değil (p=0.08). Tüm hastaların izlem süresi boyunca; 1 yıllık transplantasyon sansürlü sağkalım %81,9 (n=56), 2 yıllık %70,3 (n=82), 3 yıllık %62,9 (n=93), 4 ve 5 yıllık %55,8 (n=99) idi. Bazal GFH’a göre her 3 grubun sağkalım oranları 1. yıl için baktığımızda 3. grupta (GFH>90) %87,9, grup1 (GFH<60) de %76,2 (p=0,03), grup 2 (GFH 60-90) de ise %81,9 idi. Bazal GFH düşük (<60) olan hastaların %27’sinde postop GFH’da yükselme olmazken, yaklaşık %73’ünün GFH’larının arttığını gördük. Buna karşılık GFH>60’ın üstünde olan hastaların ise yaklaşık %14’ünün postop 1. ayda GFH’ın <60 seyrettiğini saptadık. İlk 1 ayda GFH artan (n=227) (50,4 ± 2,2 ay) ve artmayan hastaları (n=69) (35,7 ± 3,7 ay) 2 grup olarak incelediğimizde; iyileşenlerin 2 yıllık sağ kalımı %73,3 yıllık %65, 4yıllık %58 iken iyileşmeyenlerin ise 2 yıllık %56, 3 yıllık %49, 4 yıllık %38 idi (p<0,01). İzlem boyunca LVAD’la ilişkili komplikasyonlardan en çok serebrovasküler olayların ve pompa trombozu komplikasyonlarının geliştiğini saptadık.
LVAD takılan hastalarda böbrek fonksiyonları açısından kısa ve uzun dönem sonuçları oldukça iyidir. Başlangıçta GFH düşük olsa bile bu hastaların LVAD takılmasından sonra büyük oranda GFH’ında düzelmelerin olduğu ve bu düzelmenin ilk 3 yıla kadar devam ettiğini gözlemledik.
5
Abstract
Left Ventricular Assist Devices (LVAD) are used as an interventional treatment method for patients with decompensated heart failure who have symptoms of heart failure at rest, despite the maximum medical treatment. The incidence of cardiorenal syndrome due to end organ perfusion disorder is increased in patients with end-stage heart failure.The aim of this study is to retrospectively evaluate the short and long-term effects of LVAD implantation technique on renal function in patients with end-stage heart failure (HF).
In our study, 329 patients with LVAD (HeartWare, HeartMate II, HeartMate 3) with end-stage HF were investigated. Biochemical parameters of the patients before and after LVAD implantation were evaluated retrospectively.Basal and follow-up GFR (CKD-Epi) values were calculated.SPSS 22.0 software was used for all statistical analyses. Pearson and Spearman's for correlation analysis, Kaplan-Meier method for survival analysis tests were used, statistical significance was evaluated by log-rank test. Cox regression analysis was performed to determine the independent predictors of mortality.
The mean age of the patients was 50.8 ± 13.2, 86% was male, mean basal GFR was 77.6 ± 25.7 ml/min/1.73m2, 29.5% patients had DM, 34.1% had HT.There was a significant
increase in mean GFR values of all patients and groups in the first month after LVAD implantation (p <0.01). In patients with basal GFR <60ml / min, there was a significant increase (p <0.001) compared to baseline at 1, 6, 12, 24 months after implantation, and the increase at 36 months was not significant (p = 0.08).During the follow-up period of all patients; 1. year transplantation censored survival was 81.9% (n = 56), 70.3% (n = 82) for 2. year, 62.9% (n = 93) for 3. year, 55.8% for 4. and 5. years (n = 99).The survival rates of all 3 groups according to basal GFR were for 1. year was 87.9% in group 3 (GFR> 90), 76.2% (p=0.03) in group 1 (GFR <60) and 81.9% ingroup 2 (GFH 60-90).In 27% of patients with low baseline GFR (<60) there was no increase in postoperative GFR, while approximately in 73% of patients GFR was increased. On the other hand, we found that approximately 14% of patients with GFR> 60 had a GFR of <60 on the postoperative 1. month. While comparing first month GFR increased (n = 227) (50.4 ± 2.2 months) and not increased (n = 69) (35.7 ± 3.7 months) groups; for increased group 2-year survival rate was 73%, 3-year was 65%, 4-year was 58% and for not increased group 2- survival rate was 56%, 3-year was 49% and 4-year was 38% (p <0.01).During the follow-up, we found that the most common complications associated with LVAD were cerebrovascular events and complications of pump thrombosis.
6 In patients with LVAD, short- and long-term results are quite good in terms of renal function. Even though GFR was low before, we observed that there was a significant improvement in GFR after LVAD implantation and this improvement continued for the first 3 years.
7
TABLO LİSTESİ
Tablo 1. Kalp yetersizliği sınıflamasında ACC/AHA ya göre evrelemesi (6). ... 14
Tablo 2. Mekanik Destek Cihazının (MDC) kullanım endikasyonları (8). ... 17
Tablo 3. Sol Ventrikül Destek Cihazı impantasyonu için uygun hasta kriterleri (9). ... 17
Tablo 4. HeartWare destek cihazının parçaları ... 19
Tablo 5. Hastalar bazal GFH değerlerine göre Kronik Böbrek Yetmezliği Tanı sınıflamasına göre sınıflandırılmıştır. ... 26
Tablo 6. LVAD öncesi glomerüler filtrasyon hızı kategorilerine göre bazal karakteristikler .. 27
Tablo 7. Bazal GFH ile Değişkenler arası Korelasyon Analizi. ... 28
Tablo 8. Takip süresince GFH değişmelerini etkileyen faktörle ... 30
Tablo 9. GFH artışını etkileyen faktörlere regresyon analizi ile baktığımızda ... 31
Tablo 10. GFH bazal grup * GFH 1. ay grup Crosstabulation ... 33
Tablo 11. Postoperatif Komplikasyonlar ve Klinik Sonlanım ... 36
Tablo 12. Bazal GFH Gruplarına Göre Klinik Sonlanımlar ... 36
Tablo 13. Ölüm nedenleri ... 37
8
ŞEKİL LİSTESİ
Şekil 1. HeartWare tipi mekanik destek cihazı ... 18
Şekil 2. HeartWare tipi mekanik destek cihazı. ... 18
Grafik 3. Tüm hastaların GFH'nın zamanla olan değişimi ... 29
Grafik 4. Bazal GFH gruplarının GFH'larının zaman içindeki değişimi. ... 29
Grafik 5. Transplantasyon sansürlü sağkalım... 31
Grafik 6. Bazal GFH’lerine göre 3 grubun 3 yıllık sağkalım oranları (p=0,129) ... 32
Grafik 7. Bazal GFH grupların 1 yıllık sağkalımı (p=0,03, Grup 1 ve Grup3) ... 32
Grafik 8. 1. Ay GFH gruplarının transplantasyon sansürlü sağkalımları (log rank p<0,001) .. 34
Grafik 9. İzlemin 1. ayında GFH’ı artanların ve azalan/değişmeyenlerin sağ kalımı (log rank p<0,01) ... 35
9
KISALTMALAR
ACE : Anjiyotensin Dönüştürücü Enzim
ACE-I : Anjiyotensin Dönüştürücü Enzim İnhibitörü AF : Atriyal Fibrilasyon
AHA : Amerikan Kardiyoloji Cemiyeti ANP : Atriyal Natriüretik Peptit
ARB : Anjiyotensin Reseptör Blokeri
ARNİ : Anyitensin Reseptör Neprilisin İnhibitörü AST : Aspartat Amino Transferaz
ALT : Alkalen Trasnferaz
ADKY : Akut Dekompanse Kalp Yetersizliği AT- II : Anjiyotensin II
BB : Beta Bloker
BNP : Beyin Natirüreitk Peptit CNP : C-Natriüretik Peptit DM : Diyabetes Mellitus
ECMO : Ekstrakorporeal Membran Oksijenasyonu ET-1 : Endotelin-1
EF : Ejeksiyon Fraksiyonu EKG : Elektrokardiyografi EKO : Ekokardiyografi
GFH : Glomerüler Filtrasyon Hızı
ICD : İmplante Edilebilir Kardiyoverter Defibrilatör İABP : İntra Aortik Balom Pompası
10 KBY : Kronik Böbrek Hastalığı
KRS : Kardiyorenal Sendrom İKMP :İskemik Kardiyomiyopati KKY : Konjestif Kalp Yetmezliği KY : Kalp Yetmezliği
KAS : Koroner Arter Stenozu LA : Sol Atriyum
LV : Sol Ventirkül
LVAD : Sol Ventrikül Destek Cihazı
LVEF : Sol Ventrikül Ejeksiyon Fraksiyonu MRA : Minerelokortikoid Reseptör Antagonistleri Mİ : Miyokad Enfarktüsü
MDC : Mekanik Destek Cihazı NE : Norepinefirin/ Noradrenalin NP : Natriüretik Peptit
NT-ProBNP : N-Terminal Probnp
RAAS : Renin Anjiyotensin Aldosteron Sistemi RV : Sağ Ventrikül
HT : Hipertansiyon HPL : Hiperlipidemi VKİ : Vücut Kitle İndeksi
SPAP : Sistolik Pulmoner Arteriyel Basınç SVO : Serebro Vasküler Olay
11
1. GİRİŞ
KY patogenezinin temelinde kalp debisinin, doku ve organların oksijen ve metabolik ihtiyaçlarını karşılayamayacak kadar azalmasıdır. En sık rastlanan KY şekli pompa yetersizliği olmakla beraber kalbin gevşeme yetersizliği, damarsal ve hormonal bozuklukları da KY nedenleri arasındadır (1). KY geliştiği sırada birçok mekanizma kardiyak volümü kompanze etmek amaçlı devreye girer. Sistolik disfonksiyon ve azalmış ventriküler output geliştiği taktirde, kalbin atım hacmi ve hızında artmayla kompanze edilmeye çalışılır. Periferik vasküler direnç artışı kompansatuar mekanizma olarak yeterli kan basıncı oluşmasına sebep olur. Kompanzatuar mekanizmalar normal LV dolum basınçlarını ve kardiyak kan atımını sağlayamadığında, hastalık semptomatik hale gelir.
Sol ventrikül ejeksiyon fraksiyonundaki azalma ile sistol ve diyastol sonu hacimlerde artış yapmakla ventrikülün yeniden şekillenmesine (remodeling) sebep olur. Ventrikül dilatasyonu ve remodeling sonucunda atriyoventriküler halka genişler, papiller kaslarda uzama sonucu kapak yetersizliğine neden olur. Mitral ve triküspid kapakta oluşan dilatasyon ve yetmezlik kardiyak atım hacmini daha da azaltır. Sonuç olarak sistol sonu hacim artışı ve ventriküler duvar gerilimi daha da artar. Bu değişiklikler de bir kısır döngü oluşturarak kalbin kaviter alanında artışa sebep olur (1).
Hastaların akut dekompanse kalp yetersizliği ile başvurması sırasında kalbin Ejeksiyon Fraksiyonun azalmasına bağlı uç organ perfüzyonu azalmakta ve renal fonksiyonların azalma olasılığı artmaktadır. KY’de artmış ekstrasellüler sıvı volümüne rağmen, intravasküler sıvı volümü azalmakta ve kompansatuvar olarak Sempatik sistem, RAAS ve Vazopressin aktivasyonu ile sodyum ve su tutulumu arttırılarak renal perfüzyon ve renal filtrasyon fraksiyonunu korunmaya çalışılır. Artmış Anjiotensin II üretimi böbrekte Endotelin-1 (ET-Endotelin-1) ekspresyonunu stimüle eder. ET-Endotelin-1 güçlü bir pro-inflamatuar ve pro-fibrotik vazokonstrüktör peptittir. ET-1 konjestif kalp yetersizliğinde renal kan akımı ve glomerüler filtrasyon hızını azaltarak iskemiye bağlı akut böbrek hasarına neden olmaktadır (2).
Dekompanse kalp yetersizliği tanısı alan ve maksimum medikal tedaviye rağmen istirahatte belirgin kalp yetersizliği semptomları devam eden hastalara girişimsel tedavi yöntemleri uygulanmaktadır. Bu uygulamaya nakil veya mekanik destek cihazı takılması örnek gösterile bilir. Dünyada yıllık 6300 üzerinde hastaya nakil yapılmaktadır. Donör azlığından ve nakil için uygun olmayan hastalar (Tablo 2) için köprü veya Uzun süreli dolaşım desteği sağlamak amaçlı sol ventrikül destek cihazları (LVAD) takılmaktadır. LVAD kalbin iş yükünü ciddi şekilde azaltarak hastayı yatağa bağımlı halden kurtarır, hastaya aktif yaşam kalitesi kazandırır. Bu hastalar transplantasyon olanağı sağlanıncaya kadar aktif yaşamını sürdürmek
12 ve kalp yetersizliğinin organlar ve sistemler üzerindeki bozucu etkilerini düzeltmek amaçlı köprü olarak LVAD’dan faydalanırlar. Nakil için uygun şartlar sağlanamayan hastalar Uzun süreli dolaşım desteğiyle yaşamlarını devam ettirmektedirler. Bizim çalışmamıza 3 nesil mekanik destek cihazı (HeartWare,HeartMate II, HeartMate 3) takılan hastalar alınmıştır.
LVAD implantasyonu sonrası böbrek fonksiyonunu araştıran gözlemsel çalışmaların çoğu retrospektiftir ve sınırlı izlem süresine sahiptir. Bu çalışmaların çoğunda GFH ve serum kreatinin konsantrasyonunun, LVAD takılmasından hemen sonraki aylarda iyileştiği gözlenmektedir. Özellikle ilk ayda belirgin bir iyileşme oluyor daha sonra bu iyileşme belli bir süre azalarak devam etmektedir. Ayrıca, bu iyileşme daha kötü böbrek fonksiyonu olan hastalarda daha belirgin gibi olduğu görülmektedir. Bunun nedenlerinden en önemlisi uç organ perfuzyon bozukluğu olduğu düşünülmektedir. Fakat operasyon sonrası oluşa bilen hemodinamik bozukluklar ve sağ kalp yetersizliği akut böbrek yetmezliği oluşturmaktadır Yapılan çalışmalarda böbrek fonksiyonlardaki bu iyileşmenin ilk birinci ayda yaşam sürecini %84 iyileştirdiği sonuçlarına varılmıştır (3).
Amacımız LVAD sonrası kısa ve uzun vadede böbrek fonksiyonlarını değerlendirmek, bu iyileşmenin yaşam sürecinde etkisini öğrenmektir.
13
2. GENEL BİLGİLER
2.1.KALP YETERSİZLİĞİ
2.1.1.TANIM VE TERMİNOLOJİ
Kalp yetersizliği, kalbin yapısal ve fonksiyonel bozukluğuna bağlı olarak, kalbin dokuların metabolik ihtiyaçlarını karşılayacak miktarda kanı, normal doluş basınçları altında dokulara gönderememesi veya ancak yüksek doluş basınçları altında bunu gerçekleştirebilmesiyle seyreden klinik tablodur. KY miyokardın, perikardın, endokardın, kalp kapakçıklarının, damarsal yapının veya metabolik bozuklukların neden olduğu hastalıklardan kaynaklanabilir (4).
2.1.2. KALP YETERSİZLİĞİNİN EPİDEMİYOLOJİSİ
Günümüzde ABD de 6 milyon, Avrupa’da 15 milyonun üzerinde KY tanısı alan hasta olduğu düşünülmektedir. Ülkemizde yapılan HAPPY prevlans çalışmasında ise kalp yetersizliği tanısı alan ve kalp yetersizliği gelişimi için risk faktörleri olan yaklaşık 4 milyon kişi olduğu saptanıştır. Bu hastaların yaklaşık 1,5 milyonunun ise semptomatik (diyastolik kalp yetmezliği)olduğu tahmin edilmektedir (5).
2.1.3. KALP YETMEZLİĞİNİN PATOFİZYOLOJİSİ
KY patogenezinin temelinde kalp debisinin; doku ve organların oksijen ve metabolik ihtiyaçlarını karşılayamayacak kadar azalmasıdır. En sık rastlanan KY şekli pompa yetersizliği olmakla beraber, kalbin gevşeme yetersizliği, damarsal ve hormonal bozuklukları da KY nedenleri arasındadır. KY geliştiği sırada birçok mekanizmalar kardiyak volümü kompanze etmek amaçlı devreye girer. Sistolik disfonksiyon ve azalmış ventriküler output geliştiği taktirde kalbin atım hacminde ve hızında artmayla kompanze edilmeye çalışılır. Periferik vasküler direnç artışı kompansatuar mekanizma olarak yeterli kan basıncı oluşmasına sebep olur. Kompanzatuar mekanizmalar normal LV dolum basınçlarını ve kardiyak kan atımını sağlayamadığında, hastalık semptomatik hale gelir.
Sol ventrikül ejeksiyon fraksiyonundaki azalma ile sistol ve diyastol sonu hacimlerde artış yapmakla ventrikülün yeniden şekillenmesine (remodeling) sebep olur. Ventrikül dilatasyonu ve remodeling sonucunda atriyoventriküler halka genişler, papiller kaslarda uzama ile kapak yetersizliğine neden olur. Mitral ve triküspid kapakta oluşan dilatasyon ve yetmezlik kardiyak atım hacmini daha da azaltır. Sonuç olarak sistol sonu hacim artışı ve ventriküler duvar
14 gerilimi daha da artar. Bu değişiklikler de bir kısır döngü oluşturarak kalbin kaviter alanında artışa sebep olur (1).
2.1.4. KALP YETERSİZLİĞİ SINIFLANDIRILMASI
Kalp yetersizliği, anatomik olarak sağ ve sol kalp yetersizliği, atım hacmine göre düşük ve yüksek debili kalp yetersizliği, klinik olarak akut ve kronik kalp yetersizliği diye sınıflandırılabilir. Fonksiyonel olarak KY sistolik ve diyastolik KY ne ayrıla bilir. Sistolik KY de ejeksiyon fraksiyonu düşer, diyastolik KY de ise ejeksiyon fraksiyonunun genelde korunduğu görülmektedir.
Tablo 1. Kalp yetersizliği sınıflamasında ACC/AHA ya göre evrelemesi (6).
Evre A KY için yüksek risk mevcuttur, fakat yapısal kalp hastalığı ya da KY semptomları yoktur (HT, DM, KAH)
Evre B Yapısal kalp hastalığı mevcut, fakat KY semptomu yok (asemptomatik kapak hastalığı veya geçirilmiş Mİ ola bilir)
Evre C Yapısal kalp hastalığı mevcut, şimdi veya geçmişte KY semptomları vardır Evre D Maksimum medikal tedaviye rağmen istirahatte belirgin kalp yetersizliği
15
2.1.5 KALP YETERSİZLİĞİ TANISI
2.1.5.1 Belirti ve Bulgular
KY egzersiz intoleransı, çabuk yorulma, ortopne ve ayak bileği şişmesi gibi semptomlarla birlikte, eşlik eden periferik ödem bulguları ve artmış juguler venöz basınç gibi bulgular ile karşımıza çıkmaktadır.
2.1.5.2 Renin Anjiyotensin Aldosteron Sistemi (RAAS), Natriüretik Peptidler, Elektrokardiyogram, Ekokardiyogram
Kan basıncının düzenlenmesinde önemli önemli rol oynayan RAAS, böbreklerden sodyum tutulumunu arttırarak vazokontriksiyona neden olur. Böbreklerin jukstaglomerüler cisimindeki beta-1 adenoreseptörleri kan basıncının düşmesiyle uyarılır ve renin salınımına sebep olur. Plazma renin aktivitesi, orta ve ağır KY hastalarında yüksek NE düzeyine paralel olarak yükselir. Bu nedenle KY’de renin düzeylerinin yüksekliği önemli bir prognostik faktördür [7].
Natriüretik peptitler; atrial natriüretik peptit (ANP), B-tipi natriüretik peptit (BNP), C-tipi natriüretik peptit (CNP), D-C-tipi natriüretik peptit (DNP) nörohormonlarından oluşur. Bu hormonlar kalp, beyin, endotel ve diğer organlardan salınmaktadır. Natriüretik peptitler yaygın etki göstermektedirler. Natriürez, diürez, kan hacmi, kan basıncı, yağ metabolizması, kemik büyümesi ve hücre çoğalmasının engellenmesinin düzenlenmesinde rol oynarlar. Bu biyolojik aksiyonlarını membran guanil siklaz reseptörleri yoluyla düzenlemektedirler. Atrial Natriüretik Peptit (ANP); başlıca sentez yeri atriumdur (en çok sağ atriyum), ancak sol ventrikülde disfonksiyon ya da ventriküler hipertrofi durumunda ventrikül dokusundan da köken alabilmektedir. ANP vazodilatasyonla birlikte aldosteron inhibisyonu yaparak diurezi sağlar. Dolayısıyla RAAS’ne karşı çalışmaktadır [8].
B-Tip Natriüretik Peptit (BNP): en çok ventriküllerden salınır.Peptit önce proBNP olarak salınır,ardından aktif BNP ve inaktif fragman olan NT-proBNP ye ayrışır.BNP plazma yarı ömrü kısa olduğundan tanıda genelde NT-proBNP kullanılmaktadır. BNP ventriküllerin miyokardiyumunda depolanır, ventriküler basınç artışı sonucu miyositlerin gerilmesindeki artış BNP’in daha fazla ve sürekli salınımına sebep olmaktadır. BNP seviyesi özellikle sol ventrikül hipertrofisinde artmaktadır. Hasarlı dokuda BNP’in fazla olması, yerel stres ve onarım mekanizmaları ile ilişkili olabileceğini düşündürmektedir. KY’de artan kan BNP seviyesi miyokard gevşemesini etkilediği gibi, vazokonstriksiyona, Na retansiyonu ve aktiflenmiş RAAS’nin antidiüretik etkisi sonucu ventrikül volümünde oluşan ani artışa karşı düzenleyici rol oynar. Bu nedenle, plazmada BNP düzeyinin yüksek bulunması KY’nin önemli bir tanı kriteridir. Yaşlı hastalarda BNP düzeyi yüksek, obez hastalarda ise düşük olduğu saptanmıştır [9].
16 C-Tip Natriüretik Peptit (CNP): esas olarak damar duvarlarında sentezlenmektedir. Bunun yanında CNP, makrofajlar, nöronlar, osteoblastlarda da sentezlenmektedir. Vazodilatatör olmakla beraber, kardiyak fibroblastlarda kollajen sentezini baskılar. CNP ‘nin natriüretik ve diüretik etkisi olmadığı bilinmektedir.
Natriüretik peptitlerin renal etkileri: ANP glomerüler filtrasyon hızını ve buna bağlı olarak diurezi artırmaktadır. Bunun dışında sodyum, magnezyum, kalsiyum ve potasyum atılımını artırmakta, tersine idrar osmolaritesini ve renin sekresyonunu azaltmaktadır. ANP’nin glomerüler filtrasyon hızını arttırması, glomerüllarda afferent arteriolar direnci azaltırken, efferent arteriolar direnci arttırması sonucu glomerülar kapiller hidrostatik basıncın artmasını sağlar. Proksimal tübüllerde ANP anjiyotensin-II etkili sodyum ve su atılımını inhibe eder. Toplayıcı kanallarda amiloride duyarlı katyon kanalını inhibe ederek sodyum adsorbsiyonunu düşürür. ANP’nin bu transport etkilerinin tümü cGMP bağımlı olarak gerçekleşmektedir [10]. EKG: kardiyoloji pratiğinde hemen hemen her hasta için kullanılan bir yöntemdir.KY de anormal bir EKG tanı koyma olasılığı yüksek olsa da özgüllüğü düşüktür [11].
EKO kalbin duvar kalınlığı, kapak hastalığı, şüpheli aort disseksiyonu, endokardit ve ventrikülün sitolik, diyastolik fonksiyonları hakkında ayrıntılı ve hızlı bilgiler sunan yararlı bir testtir.
2.1.6 KALP YETERSİZLİĞİNİN TEDAVİSİ
Anjiyotensin dönüştürücü enzim inhibitörleri (ACE-İ), beta blokerler (BB), minerolokortikoid reseptör antagonistleri (MRA (Spironolakton ve eplerenon), anjiyotensin reseptör neprilisin inhbitörü (ARNI) sakubitiril/valsartan, ivabradin, diüretikler, hidralazin-isosorbid dinitrathidralazin kombinasyonu ve digoksin düşük ejeksiyon fraksiyonlu kalp yetersizliği tedavisinde etkinlikleri kanıtlanmış ilaçlardır. Bunlar arasında mortalite yararı kanıtlanan ACE-İ, BB, MRA ve ARNI kılavuzlar tarafından sınıf I endikasyon düzeyinde önerilmektedir (7).
2.1.7 KALP YETMEZLİĞİNDE MEKANİK DESTEK CİHAZI TEDAVİSİ
ACC/ AHA kılavuzunda da belirtildiği üzere sözü keçen medikal tedaviye rağmen hastalar evre C ve evre D kriterlerine geldiklerinde, farmakolojik tedavilerin yanı sıra mekanik destek cihazı veya transplantasyon tedavilerinin uygulanması gerekebilir.
17
Tablo 2. Mekanik Destek Cihazının (MDC) kullanım endikasyonları (8).
Transplantasyona Köprü (Bridge to Transplantation:
BTT)
Yüksek ölüm riskli, nakil için donör bekleyen hastalara takılır.
Adaylığa Köprü
Nakile uygun olmayan, tedavi süreci içinde uç organ işlevinin iyileşmesiyle nakile uygun hale getirilmesi planlanan hastalara takılır.
Karar için köprü
İlaca dirençli akut dolaşım kollapsı ve ölüm riski yüksek olan hastalara takılır (tedavisi düzenlenmiş, ek tedavi kararı alınana kadar köprü amaçlı)
İyileşmeye köprü
Kardiyak rezervi kötü olan hastalara iyileşme aşamasına kadar destek cihazı takılmakta (organ fonksiyonelliğini kazandıktan sonra MDC çıkarılır.)
Uzun süreli tedavi (Destination therapy: DT)
Nakil için uygun olmayan ve son dönem kalp yetersizliği olan hastalarda nakile alternatif olarak uzun dönem kullanmak amaçlı takılır.
Tablo 3. Sol Ventrikül Destek Cihazı impantasyonu için uygun hasta kriterleri (9). Optimal ilaç ve cihaz tedavilerine rağmen 2 aydan fazladır ciddi semptomları olan ve aşağıdaki kriterlilerden iki veya daha fazlası olan hastalar:
LVEF <%25, pVO2 <12 mL/kg/dk Son 1 senede >3 hastaneye yatış öyküsü İV inotropik tedaviye bağımlı kalma
Azalmış perfüzyona bağlı karaciğer ve renal fonksiyonlarda progrese olan bozulma Sağ ventrikül işlevlerinde (triküspit yetersizliği olmaksızın) bozulmanın başlaması
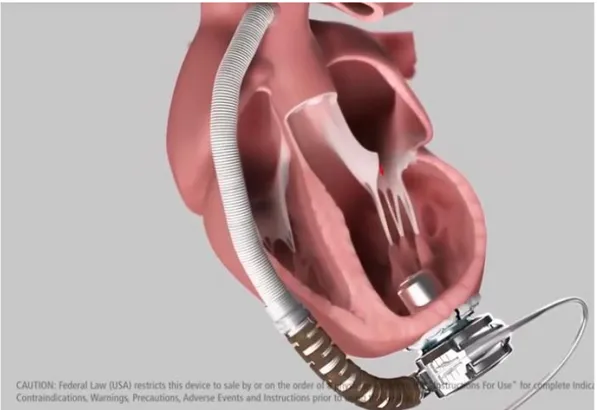
MDC’dan sık kullanılan sol ventrikül destek cihazıdır (LVAD). Cihazın görevi sol ventrikül içine retrograd yerleştirilir, yüksek hızlarda dönen pompa kanı sol ventrikülden alır ve yükselen aortun proksimaline ulaştırır.
18
Şekil 1. HeartWare tipi mekanik destek cihazı
19
Tablo 4. HeartWare destek cihazının parçaları
• Vücut içerisinde bir ventriküle bağlı bir pompa.
• Pompayı izleyen küçük bir bilgisayar olan harici bir kontrol ünitesi.
• Pompayı ve kontrol birimini çalıştıran güç kaynakları,Batarya
HeartWare: Devamlı sentrafüj akımlı yeni nesil bir pompadır. HeartWare’in sadece bir hareketli parçası, çarkı ve hiçbir mekanik yatağı yok. HeartWare pompada yatak bulunmadığından ve daha düşük devirde çalıştığı için, uzun süre dayanıklıdır. Daha önceki cihazlardan çok daha küçüktür ve cerrahi olarak implant yapmak daha kolaydır.
HeartMate 3: Santrifüj akış mekanizmalı pompa, 10 L/dk’ya kadar pompalama kapasitesine sahiptir. Duvarı özel dokuyla kaplı sütun içinde asılı çarkı mevcut ,çarkın temas yüzeyi az olduğundan tromboembolizm riskini azaltır, cihazı dayanıklı kılar (8).
LVAD’ın faydaları:
• Son organ perfüzyonunu arttırır.
• İntrakardiyak dolum basınçlarını azaltır.
• Sol ventrikul hacmi,duvar stresini ve miyokardiyal oksijen tüketimini azaltır.
• Koroner perfüzyonda artış yapar.
Mevcut parametrelerde iyileşme sonucu klinik olarak: • Kardiyojenik şok önlenir.
• Pulmoner konjesyon azalır.
• Miyokardiyal iskemi belirtileri azalır.
• Enfarktüs boyutu azalır.
2007 senesinde REMATCH çalışma grubunun sol ventrikül destek cihazı takılan 68 hastayla, optimal ilaç tedavisi alan 61 hasta randomize edildi. Cihaz grubunda bir yıl hayatta
20 kalma oranları %52’iken, medikal tedavi grubunda %25, ikinci yıldaki oranlar sırasıyla %23 ve %8 olduğu saptandı (10).
Günümüzde LVAD implantasyonu ve beş yıllık takip sürecinde harcanan maliyet 350.000 doları aşmaktadır. LVAD implantasyonu sonrası oluşa bilecek antikoagülasyon gereksinimine bağlı kanamalar, akut ve kronik sağ kalp yetersizliği, tromboembolizm, enfeksiyon, aort yetersizliği, ventriküler aritmiler ve hemoliz gibi komplikasyonlar sağkalımı ciddi azaltmaktadır.
2.1.8 Kardiyorenal Sendrom (KRS)
2007 senesinde Ulusal Kalp, Akciğer ve Kan Enstitüsü tarafından yayınlanan ve tanımlanan Kardiyorenal Sendrom (KRS) kavramı kalp yetersizliği tedavisinin ilerleyici böbrek yetmezliğine bağlı olarak kısıtlandığı tezi üzerine kullanılmıştır (11). Kardiyorenal Sendrom genel olarak kalp veya böbrekten birindeki akut veya kronik bozulmanın diğerinde akut veya kronik disfonksiyona yol açması ile gelişen durumlar olarak tanımlanabilir. Kardiyak hastalıklar böbrek fonksiyonlarını azaltarak, böbrek hastalıklarında progresyona sebep olmaktadır (12).
2.1.9 Kardiyo Renal Sendrom Sınıflaması (KRS)
KRS Tip I: (Akut Kardiyo Renal Sendrom): Akut kardiyak bozulmaya bağlı gelişen böbrek fonksiyonlarında azalma
KRS Tip II: (Kronik Kardiyo Renal Sendrom): Uzun süreli kardiyak fonksiyon bozukluğu sonucunda gelişen böbrek fonksiyonlarında azalma
KRS Tip III: (Akut renokardiyak sendrom): Böbrek fonksiyonlarında akut bozulma sonucu kardiyak disfonksiyon gelişmesi
KRS Tip IV: (Kronik renokardiyak sendrom): Böbrek fonksiyonlarındaki uzun süreli (kronik) bozulukluklar sonucunda kardiyak hastalık gelişmesi
KRS Tip V: (Sekonder Kardiyorenal Sendromlar): Kalp ve böbrekte eş zamanlı olarak disfonksiyona yol açan sistemik durumlar.
Aynı şekilde kronik böbrek hastalığı da kardiyovasküler olaylar ve sonuçlar için bağımsız bir risk faktörüdür (13). Akut dekompanse kalp yetersizliği (ADKY) olan hastalarda serum kreatininde 0,3 mg/dl’den fazla artış, artmış mortalite, uzamış hospitalizasyon ve daha sık hastaneye başvuruya yol açmaktadır (14, 15)
Akut dekompanse kalp yetersizliği tanısıyla hospitalize edilen hastaların %21-45’inde serum kreatininde artış görülmektedir (16). KY tanılı ve eş zamanlı GFH <60 ml/dk olan hastalarda mortalite riski belirgin olarak daha yüksek olduğu saptanmıştır (17).
21 Hastaların akut dekompanse kalp yetersizliği (ADKY) ile başvurması sırasında kalbin Ejeksiyon Fraksiyonun azalmasına bağlı akut böbrek yetmezliği gelişme olasılığı çok daha fazla olup kardiyojenik şokta bu oran %70’in üzerine çıkmaktadır. Artmış ekstrasellüler sıvı volümüne rağmen, intravasküler sıvı volümü azalmakta ve kompansatuvar olarak Sempatik sistem, RAAS ve Vazopressin aktivasyonu ile sodyum ve su tutulumu arttırılarak böbreğin perfüzyon ve filtrasyon fraksiyonunu korunmaya çalışılır. Artmış Anjiotensin II üretimi böbrekte Endotelin-1 (ET-1) ekspresyonunu stimüle eder. ET-1 güçlü bir pro-inflamatuar ve pro-fibrotik vazokonstrüktör peptittir. ET-1 konjestif kalp yetersizliğinde renal kan akımı ve glomerüler filtrasyon hızını azaltarak iskemiye bağlı akut böbrek hasarına neden olmaktadır (2).Azalmış kardiyak output sempatik sinir sistemi, RAAS’ni aktive ederek venöz basıncın yükselmesine, intraabdominal basıncın artmasına ve renal venoz konjesona neden olmakla renal bozulmaya daha fazla katkıda bulunduğu saptanmıştır (18).
Hastaların kronik kalp yetersizliği tanısıyla başvurusunda %30-40 oranında GFH <60ml/dk (Evre 3 ve üzeri KBY) olduğu görülebilmektedir [19]. Patofizyolojisinde RAAS ile birlikte özellikle Aldosteron düzeylerinin kalp, damar yapısı ve böbreklerdeki uç organ hasarında kilit rol oynadığı gösterilmiştirtir [20] RAAS sistemi ile ilişkisi olan Transforming Growth Factor β düzeyinin artması renal fibroz ve glomerülosklerozu tetklemektedir. Klinik olarak kronik kalp yetersizliği hastasında artmış kan basıncı, giderek bozulan GFH, diüretik direnci ve perifer ödemi artan KRS bulgularıdır [21]. Bu hastalarda GİS ödemine bağlı malabsorbsiyon, malnutrisyon, TNF, IL6 artışı ve böbrek yetmezliğine bağlı olarak anemi gelişir.Anemi azalmış sol ventrikül sistol sonu ve diyastolik volümü, artmış sol ventrikül kitle indeksi, bozulmuş sol ventrikül ejeksiyon fraksiyonu, artmış pulmoner kapiller wedge basıncı, sağ ve sol ventrikül basınçlarında artış sonucu kardiyomegaliye sebep olur.
Hastaların Akut Böbrek Yetmezliği (ABY) tanısıyla başvurusunda oluşa bilen Hipervolemi pulmoner ödem KY oluşumunda katkıda bulunmaktadır. Hiperkalemi aritmi ve kardiyak arrest yarabilir. Üremi myokardial depresan faktörlerin birikimi ile kardiyak kontraktiliteyi bozar, perikardit gelişimine yol açabilir. Üremik asidoz ise pulmoner vazokonstrüksiyon yaparak özellikle sağ kalp yetersizliğini tetikler. Asidozun negatif inotropik etkisi ve oluşabilen elektrolit inbalansı aritmiye yol açmaktadır. Renal iskemi, kardiyak apaptoz ve inflamasyonu tetiklemektedir. Örneğin çalışmalarda iskemi sonrası renal hasar görmüş olguların böbreğinde nötrofil, monosit/makrofaj ve lenfosit birikimi ve sistemik TNF-α, IL-1, IL-6 ve IL-8 artışı olduğu gösterilmiştir (19).
Hastaların Kronik böbrek yetmezliği (KBY) tanısıyla başvurusunda oluşabilen koroner aterosklerozis ve sol ventrikül hipertrofisinden dolayı kardiyovasküler hastalık için bağımsız bir risk faktörü olarak kabul görmüştür. Azalmış renal fonksiyonla gelişen olumsuz
22 kardiyak sonuçların bazı üremik toksinlerin direkt etkisi mi yoksa ortak metabolik, sellüler veya hormonal bozuklukların sonucu olup olmadığı hala araştırma konusudur. Olası risk faktörlerlerine anemi, ilerlemiş glikolizasyon son ürünleri, anormal kalsiyum fosfat metabolizması, nutrisyonel faktörler, kronik ekstrasellüler sıvı volüm yükü, kronik inflamasyon, insülin direnci, hiperhomosisteinemi, oksidatif stres ve lipid metabolizma bozukluğu gösterile bilir. Bu süreci üremi, parathormon ve artmış çeşitli pro-inflamatuar sitokinlerin presipite ettiği düşünülmektedir (20).
Hastaların hem kalp hem de böbreği etkileyen patofizyolojik değişikliklerle başvurusunda her iki organda geri dönüşlü veya kalıcı zarar oluşturabiliyorsa bu sekonder kardiyorenal sendrom olarak adlandırılır. Bu süreci oluşturan Diabetes Mellitus, amiloidoz, pulmoner hipertansiyon, Sistemik Lupus Eritematozus ve sepsis gibi hastalıklar örnek gösterile bilir. KRS tanısında çeşitli biyobelirteçler kullanılmaktadır. Akut koroner sendromlarda artmış kardiyak troponin, myosit spesifik kreatin kinaz ve serum BNP düzeyleri kardiyak belirteçler olarak Böbrek biyobelirteçleri ile kıyaslamada ön planda durmaktadır. Çeşitli çalışmalarda BNP’nin kronik böbrek yetmezlikli hastalarda kardiyovasküler mortalite ve renal hastalık progresyonu arasında pozitif bir ilişkisi olduğu bulunmuştur (21-23).
Renal biyobelirteçlerinden ise KIM 1, NGAL, IL-18 ve sistatin C örnek gösterile bilir. Sistatin C’nin yoğun bakımda akut böbrek hasarını kreatinine dayalı kriterden daha erken ve mükemmel bir doğrulukta yakaladığı saptanmıştır (24).
2.1.8 AKUT DEKOMPANSE KALP YETMEZLİĞİ TEDAVİSİ
Akut dekompanse kalp yetersizliği tedavisinde konjestif veya iskemik semptomları azaltmak amaçlanmaktadır. Uygun ilaç kullanımı ve girişimler, hastanın hemodinamisi baz alınarak ayarlanan sıvı tedavisi, tedaviye yanıtın izlenmesi gerekmektedir (25).
Akut dekompanse kalp yetersizliğinde Konjestif veya iskemik semptomları gidermek amaçlı diüretikler, vazodilatatörler ve morfin kullanılmaktadır. Bu ilaçların kullanımıyla kardiyak output veya renal perfüzyon basıncını iyileştirmek, intraabdominal basıncı ve renal konjesyonu düşürmek amaçlanmaktadır. Yıllardır kullanılan diüretikler klinik olarak hızlı düzelme sağlasa da ,sıklıkla böbrek fonksiyonlarında kötüleşme ile komplike olmaktadır (26).
Diüretik kullanımının amacı interstisiyumdakı sıvı volümünün intravasküler alana doluşunu sağlayarak, ekstrasellüler sıvı volümünü azaltmaktır. Diüretikler sıklıkla elektrolit imbalansı oluşturarak, efektif dolaşan volümü azaltır ve istenmeyen nörohormonal yanıtları aktive eder. Tiyazid diüretiklerinin böbrek fonksiyonları azalmış hastalarda etkileri az olduğundan Loop diüretikleri daha çok tercih edilmektedir.
23 RAAS blokajı yapan ilaçlar kalp yetersizliği tedavisinin temelini oluşturmaktadır. GFH <60 ml/dk olan Retrospektif çalışmaya alınan hastalarda RAAS blokajı ile elde edilen etkinlik kronik böbrek yetmezliği olan ve olmayan hastalarda eşit saptanmış(25).RAAS blokajı yapan ilaçların önemli yan etkileri potasyum seviyelerinde yükselme ve böbrek fonksiyonlarını bozmasıdır. Buna rağmen ACE inhibitörleri ve ARB’lerin ileri derecede azalmış böbrek fonksiyonu olan hastalarda bile renoprotektif olduğu yönünde kanıtlar vardır(27).
İki ay gibi zaman zarfında bazal kreatinin düzeyinde %30’a kadar artış olan hastalarda renal fonksiyonların uzun vadede korunduğu 12 randomize kontrollü çalışmada gösterilmiştir. Ancak bu çalışmalar primer böbrek hastalığı olan hastalarla yapılmış olup kalp yetersizliği hastaları ayrıca değerlendirilmemiştir. Sonuç olarak serum kreatinin düzeyinde %30 artış ve potasyum düzeyi >5 mEq/ml olana kadar ACE inhibitörleri ve ARB’lerin kullanımı uygun görülmektedir.
Spironolakton ve Eplerenon EF <%35 olan hastalarda konvansiyonel tedaviyle karşılaştırıldığında mortalite ve morbiditeyi azaltmaktadır. Ancak kalp yetersizliği hastalarında ACE inhibitörü ile verildiğinde hiperkalemi yaptığı çok sık görülmektedir(28).
Βeta blokerler KKY veya iskemik kalp hastalığı olan hastalarda böbrek fonksiyonlarını etkilemeden sempatik sinir sistemi etkisinin azalmasında önemli role sahip olduğu bilinmektedir. Atenolol, nadolol ve sotalol böbreklerden atıldığından böbrek fonksiyonu azalmış hastalarda dikkatli kullanılmalıdır(21).
Akut dekompanse kalp yetmezlikli hastalarında semptomların giderilmesi ve hemodinaminin stabilize edilmesi amaçlı Nitrogliserin (nitrik oksit donörü) kullanılmaktadır.Nitrogliserin düşük dozlarda venülleri dilate ederek kardiyak dolum basıncını azaltır ve miyokardın oksijen ihtiyacını azaltır. Yüksek dozlarda ise ard yükü azaltır, kardiyak debiyi artırır(29).
Sodyum nitroprussid vasküler düz kas hücrelerinde siklik guanozin monofosfat üzerinden arteriel ve venöz vazodilatasyon yapmaktadır. Kan basıncı normal veya artmış hastalarda,ön yük ve ard yükü artmış, pulmoner ve venöz konjesyon bulguları olan hastalarda kullanılmalıdır.Nesiritid ise rekombinan insan B tipi natriüretik peptid olup, ön yük, ard yük ve pulmoner vasküler direnci azaltır, akut dekompanse kalp yetersizliğinde kardiyak output’u artırır, etkin diürezi sağlar, kalp yetersizliğinde dispneyi azaltır(30).
Düşük kardiyak output durumunda Dobutamin veya Fosfodiesteraz inhibitörleri kullanma gereksinimi bulunmaktadır, ancak myokard hasarı ve aritmileri artırabildiklerinden, sonuçları kötüleştirebilir (31).
Levosimendan bir diğer hemodinami ve renal perfüzyonda düzelme sağlayan ajan olarak kullanımı bilinmektedir. Özellikle iskemik kalp hastalığına sekonder KKY de anti-trombotik
24 ilaçlardan Aspirin:siklooksijenaz ve renal prostoglandinler üzerinden glomerül filtrasyon hızını etkilemesine rağmen, düşük dozlarda uzun zamandır böbrek yetmezliği hastalarında güvenle kullanılmaktadır.
Son dönem KY hastalarında uç organ perfüzyon bozukluğuna bağlı kardiyorenal sendromun görülme sıklığı yüksektir. Kronik kardiyolenal sendrom ve KBY gelişen hastalar genellikle LVAD imlantasyonu sonrası düzelir. Yapılan çalışmalarda LVAD sonrası ilk ayda bu iyileşmenin daha ön planda olduğu görülmektedir. Çalışmamız LVAD sonrası takibinde bu iyileşmeği kısa ve uzun vadede analiz etme imkanı sunmaktadır. Çalışmamızda hem hasta sayısı hem de implantasyon sonrası 5 senelik takip süresi baz alındığında, özellikle uzun süreli mekanik destek alan hasta grubunda diğer çalışmalarla mukayesede daha iyi sonuçlar alınacağı düşünülmektedir.
Bu çalışmada son dönem Kalp yetersizliği olan hastalara uygulanan Sol ventrikül destek cihazı implantasyon tekniğinin böbrek fonksiyonları üzerine kısa ve uzun dönem retrospektif etkilerinin değerlendirilmesi amaçlanmıştır.
25
3. GEREÇ VE YÖNTEM
3.1
Hastalar
2011-2018 senelerinde Ege Üniversitesi Tıp Fakültesi hastanesinde sol ventrikül destek cihazı implante edilen 450 hasta retrospektif olarak taranmıştır. 18-76 yaş arası ve LVAD sonrası elektronik dosyada bilgi ve laboratuvar değerleri olan 329 hasta çalışmaya alınmıştır.
3.2
Yöntem
Çalışma olgularına sürekli akım sağlayan HeartWare, HeartMate II, HeartMate3 (HeartWare Inc, Framingmam, MA) cihazı takılmıştır. Hastaların demograik verileri yaş, cinsiyet, boy, kilo, vücut kitle indeksi, vücut yüzey alanı ve yandaş hastalık, komorbid durumlar (diyabet, hipertansiyon, hiperlipidemi, koroner arter hastalığı), operasyon öncesi pulmoner arter basınçları, kardiyak debi, pulmoner kapiller kama basıncı, inotrop tedavi alıp almadığı kayda alındı. İmplantasyon öncesi bazal ve implantasyon sonrası 1, 6, 12, 24, 36, 48, 60 aylar rutin biyokimyasal parametreler (sodyum, potasyum,C-reaktif protein, AST, ALT, albumin, üre, kreatin, GFH) retrospektif olarak tarandı. Bazal ve izlemdeki GFH (CKD-Epi) değerleri hesaplandı.
3.3
İstatiksel Analiz
Tüm istatiksel analizler için “SPSS 22.0” yazılımı (SPSS Inc., Chicago, IL, USA) kullanıldı.Hastalar bazal ve 1.ay GFH düzeylerine göre üç gruba bölündü. Gruplar arasındaki farklılıkların değerlendirilmesinde değişkenlere göre tek yönlü varyans analizi veya ki-kare testi uygulandı. İzlemde anlamlı GFH değişimlerini analiz etmek için paired-t testi, GFH değişimini etkileyen faktörlerin analizi için ise lojistik regresyon testi kullanıldı. Bazal GFH ile numerik veya kategorik değişkenlerin korelasyonunun değerlendirilmesinde Pearson ve Spearman’ın korelasyon analizi kullanıldı. Sağkalım analizleri için transplantasyon sansürlü Kaplan-Meier yöntemi uygulandı ve istatistiksel anlamlılık log-rank testi ile değerlendirildi. İzlemde bağımsız mortalite belirleyicilerini saptamak için Cox regresyon analizi yapıldı. Numerik değişkenler ortalama ± standart sapma, kategorik olanlar ise yüzde değer olarak raporlandı. Tüm analizlerde p <0,05 değeri istatiksel olarak anlamlı kabul edildi.
26
4. BULGULAR
4.1 Bazal Demografik ve laboratuvar Verileri
Çalışmaya alınan 329 hastanın yaş ortalaması 50,8±13,2, %86’sı erkek, vücut kitle indeksi (VKİ) 24,9 ± 4,2 kg/m2, ortalama bazal GFH (Glomerüler Filtrasyon Hızı) 77,6 ± 25,7
ml/dk/1,73m2, 29,5’u diyabetik, %34,1’inde hipertansiyon mevcut idi.
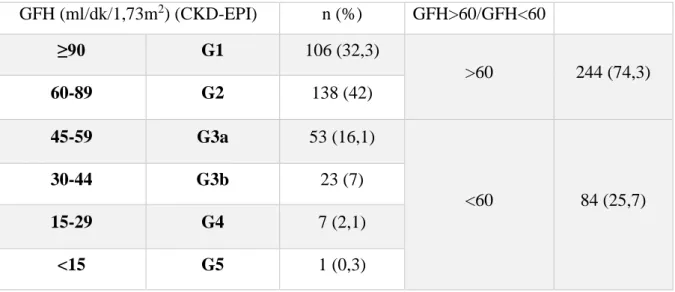
Tablo 5. Hastalar bazal GFH değerlerine göre Kronik Böbrek Yetmezliği Tanı sınıflamasına göre sınıflandırılmıştır. GFH (ml/dk/1,73m2) (CKD-EPI) n (%) GFH>60/GFH<60 ≥90 G1 106 (32,3) >60 244 (74,3) 60-89 G2 138 (42) 45-59 G3a 53 (16,1) <60 84 (25,7) 30-44 G3b 23 (7) 15-29 G4 7 (2,1) <15 G5 1 (0,3)
Hastalar GFH düzeylerine göre üç eşit gruba bölündü (1.grup GFH <60 ml/dk., 2. grup GFH: 60-90 ml/dk., 3. grup GFH >90ml/dk.).
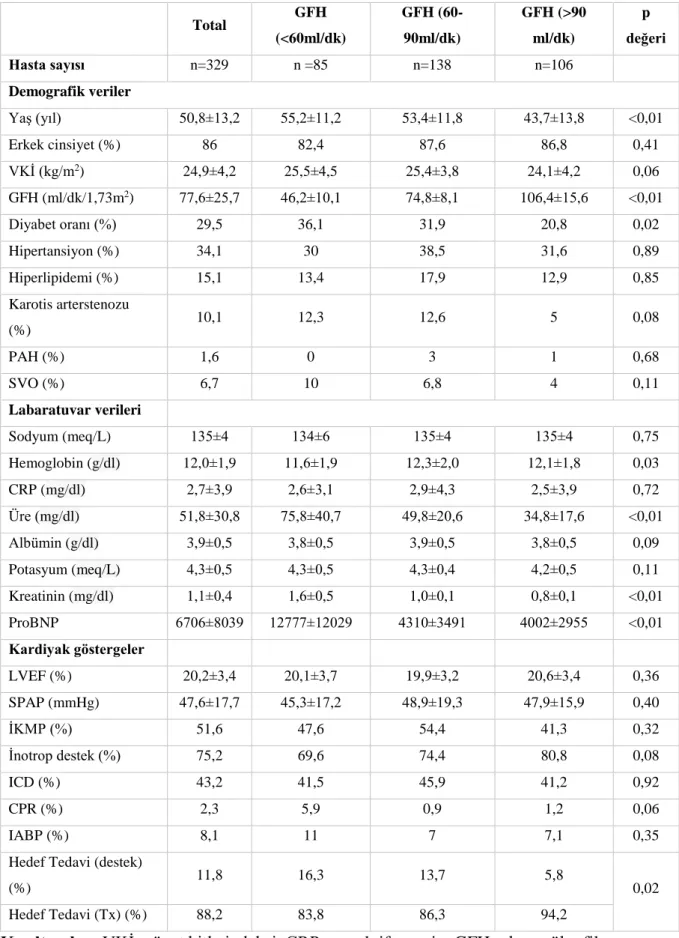
Total ve GFH kategorilerine göre hastaların bazal demografik, laboratuvar verileri ve kardiyak göstergeleri Tablo 6.de özetlenmiştir:
27
Tablo 6. LVAD öncesi glomerüler filtrasyon hızı kategorilerine göre bazal karakteristikler
Total GFH (<60ml/dk) GFH (60-90ml/dk) GFH (>90 ml/dk) p değeri Hasta sayısı n=329 n =85 n=138 n=106 Demografik veriler Yaş (yıl) 50,8±13,2 55,2±11,2 53,4±11,8 43,7±13,8 <0,01 Erkek cinsiyet (%) 86 82,4 87,6 86,8 0,41 VKİ (kg/m2) 24,9±4,2 25,5±4,5 25,4±3,8 24,1±4,2 0,06 GFH (ml/dk/1,73m2) 77,6±25,7 46,2±10,1 74,8±8,1 106,4±15,6 <0,01 Diyabet oranı (%) 29,5 36,1 31,9 20,8 0,02 Hipertansiyon (%) 34,1 30 38,5 31,6 0,89 Hiperlipidemi (%) 15,1 13,4 17,9 12,9 0,85 Karotis arterstenozu (%) 10,1 12,3 12,6 5 0,08 PAH (%) 1,6 0 3 1 0,68 SVO (%) 6,7 10 6,8 4 0,11 Labaratuvar verileri Sodyum (meq/L) 135±4 134±6 135±4 135±4 0,75 Hemoglobin (g/dl) 12,0±1,9 11,6±1,9 12,3±2,0 12,1±1,8 0,03 CRP (mg/dl) 2,7±3,9 2,6±3,1 2,9±4,3 2,5±3,9 0,72 Üre (mg/dl) 51,8±30,8 75,8±40,7 49,8±20,6 34,8±17,6 <0,01 Albümin (g/dl) 3,9±0,5 3,8±0,5 3,9±0,5 3,8±0,5 0,09 Potasyum (meq/L) 4,3±0,5 4,3±0,5 4,3±0,4 4,2±0,5 0,11 Kreatinin (mg/dl) 1,1±0,4 1,6±0,5 1,0±0,1 0,8±0,1 <0,01 ProBNP 6706±8039 12777±12029 4310±3491 4002±2955 <0,01 Kardiyak göstergeler LVEF (%) 20,2±3,4 20,1±3,7 19,9±3,2 20,6±3,4 0,36 SPAP (mmHg) 47,6±17,7 45,3±17,2 48,9±19,3 47,9±15,9 0,40 İKMP (%) 51,6 47,6 54,4 41,3 0,32 İnotrop destek (%) 75,2 69,6 74,4 80,8 0,08 ICD (%) 43,2 41,5 45,9 41,2 0,92 CPR (%) 2,3 5,9 0,9 1,2 0,06 IABP (%) 8,1 11 7 7,1 0,35
Hedef Tedavi (destek)
(%) 11,8 16,3 13,7 5,8 0,02
Hedef Tedavi (Tx) (%) 88,2 83,8 86,3 94,2
Kısaltmalar: VKİ: vücut kitle indeksi, CRP: c-reaktif protein, GFH: glomerüler filtrasyon hızı, SVEF: Sol ventrikül ejeksiyon fraksiyonu, SPAP: Sistolik pulmoner arter basıncı, İKMP: İskemik kardiomiyopati. ICD: İntra-kardiyak defibrilatör.
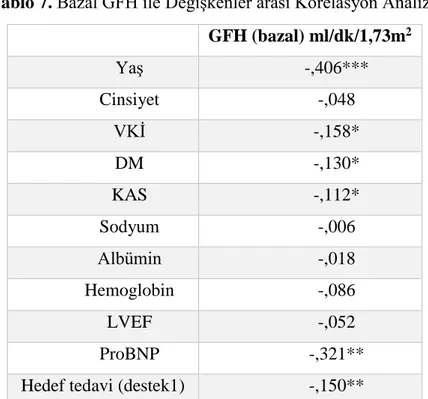
28 Bazal GFH ile bakılan değişkenler arasındaki korelasyon analizi sonucunda; yaşlı, VKİ yüksek, diyabet ve karostis arter stenozu olan hastaların başlangıç GFH’ları anlamlı düşüktü. Ayrıca GFH’ı düşük olanların ProBNP’leri daha yüksek olup hedef tedavi olarak daha çok destek tedavi grubuna dahil olma durumu istatistiksel açıdan anlamlı bulundu (Tablo 7).
Tablo 7. Bazal GFH ile Değişkenler arası Korelasyon Analizi.
GFH (bazal) ml/dk/1,73m2 Yaş -,406*** Cinsiyet -,048 VKİ -,158* DM -,130* KAS -,112* Sodyum -,006 Albümin -,018 Hemoglobin -,086 LVEF -,052 ProBNP -,321**
Hedef tedavi (destek1) -,150**
Kısaltmalar: GFH: glomerüler filtrasyon hızı değişimi, VKİ: vücut kitle indeksi, DM:diyabetis mellitus, KAS:karotis arter stenozu, Hb: hemoglobin, SVEF: sol ventrikül ejeksiyon fraksiyonu. *p<0,05; **p<0,01; ***p<0,001
29
4.2 İzlemde GFH değişimleri ve Etkileyen Faktörler
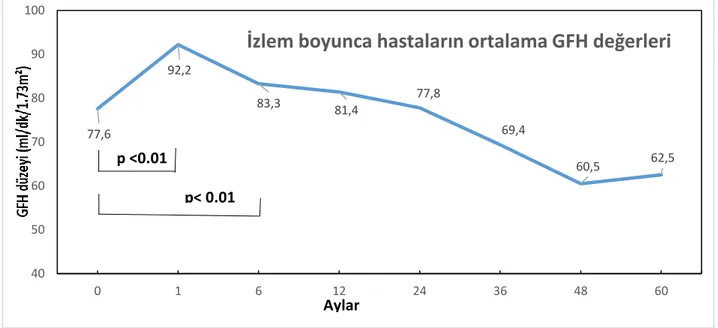
Ortalama izlem süresi 22,6±17,9 (0,2-71,6) ay idi. İzlem süresi boyunca hastaların aylık GFH değerleri hesaplandı. İlk ayda tüm hastaların ve grupların ortalama GFH değerlerinde bazale göre anlamlı bir artış mevcuttu. Hastaların izlemdeki GFH değişimleri ilk 1yıl artıyor 2.yıldan itibaren düşmektedir.
Grafik 3. Tüm hastaların GFH'nın zamanla olan değişimi
Bazal GFH gruplarına göre baktığımızda; 1. ve 2. gruplarda 6. ayda da benzer bir artış gözlendi. Tüm hastalarda ve gruplarda toplam 60 aylık izlem sonuçları grafik 3 ve grafik 4’de gösterilmiştir.
Grafik 4. Bazal GFH gruplarının GFH'larının zaman içindeki değişimi.
77,6 92,2 83,3 81,4 77,8 69,4 60,5 62,5 40 50 60 70 80 90 100 0 1 6 12 24 36 48 60
İzlem boyunca hastaların ortalama GFH değerleri
Aylar p <0.01 p< 0.01 46,2 74,5 65,9 63,3 58,3 51,5 44,9 64,5 74,8 86,7 80,8 77,7 76,8 69,0 67,7 59,4 106,4 113,8 100,7 99,0 90,2 82,4 70,4 64,0 0 20 40 60 80 100 120 0 1 6 12 24 36 48 60
İzlem boyunca gruplarda ortalama GFH değeri
1.grup 2.grup 3.grup
30
1. grup (<60): 1, 6, 12, 24. aylarda bazale göre anlamlı artış (p<0,001), 36. ayda artış anlamlı değil (p=0,08).
2. grup (60-90): 1 ve 6. aylarda bazale göre anlamlı artış (p<0,01 ve p=0,02).
3. grup (>90): Bazale göre sadece 1. ayda artış (p<0,001).
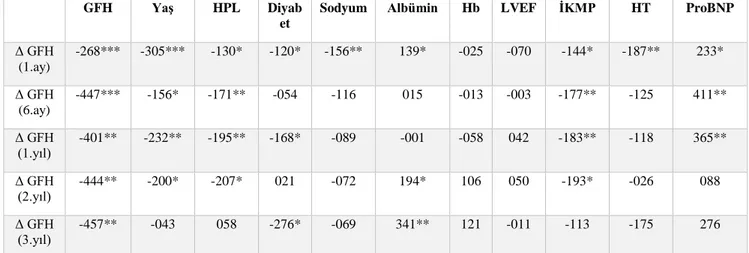
Bu gruplarda ilk 3 yılda gözlenen GFH artışını etkileyen faktörleri araştırmak için korelasyon ve regresyon analizi yaptık (Tablo 8).
Tablo 8. Takip süresince GFH değişmelerini etkileyen faktörle
Kısaltmalar: ΔGFH: glomerüler filtrasyon hızı değişimi (bazalden), VKİ: vücut kitle indeksi, Hb: hemoglobin, LVEF: sol ventrikül ejeksiyon fraksiyonu, İKMP: iskemik kardiomiyopati. *p<0,05, **p<0,01, ***p<0,001
Regresyon analizi ile baktığımızda (Tablo 9)
1. ayda GFH artışını belirleyenler; yaş, bazal GFH, preop Na ve preop albümin idi. 1. yılda GFH artışını; yaş, bazal GFH düşüklüğü ve DM varlığı, yokluğu belirliyor. GFH gruplarını modele koyarsak, 1. grupta olmak 14 kat, 2. grupta ise 5 kat (OR). 2. yılda GFH artışını, yaş ile bazal GFH düşüklüğü ve preop albumin yüksekliği belirliyor. GFH gruplarını modele koyarsak, 1. grupta olmak 19 kat, 2. grupta ise 5 kat (OR) idi.
GFH Yaş HPL Diyab et
Sodyum Albümin Hb LVEF İKMP HT ProBNP
Δ GFH (1.ay) -268*** -305*** -130* -120* -156** 139* -025 -070 -144* -187** 233* Δ GFH (6.ay) -447*** -156* -171** -054 -116 015 -013 -003 -177** -125 411** Δ GFH (1.yıl) -401** -232** -195** -168* -089 -001 -058 042 -183** -118 365** Δ GFH (2.yıl) -444** -200* -207* 021 -072 194* 106 050 -193* -026 088 Δ GFH (3.yıl) -457** -043 058 -276* -069 341** 121 -011 -113 -175 276
31
Tablo 9. GFH artışını etkileyen faktörlere regresyon analizi ile baktığımızda
1.ay 1.yıl 2.yıl
%95 C.I.for EXP(B) %95 C.I.for EXP(B) %95 C.I.for EXP(B)
Sig. Exp(B) Lower Upper Sig. Exp(B) Lower Upper Sig. Exp(B) Lower Upper
Yaş ,000 ,933 ,900 ,968 ,000 ,903 ,866 ,941 ,002 ,942 ,907 ,978 Bazal GFH ,000 ,963 ,946 ,981 ,000 ,943 ,923 ,963 ,000 ,958 ,938 ,978 DM var ,016 ,388 ,180 ,840 PreopNa ,027 ,911 ,838 ,990 PreopAlb ,005 2,769 1,356 5,653 ,050 2,298 1,001 5,276
Modele konanlar; yaş, cinsiyet, VKİ, HT, DM, IKMP, HPL, Preop Na, preop albümin ve GFH bazal
4.3 Sağkalım
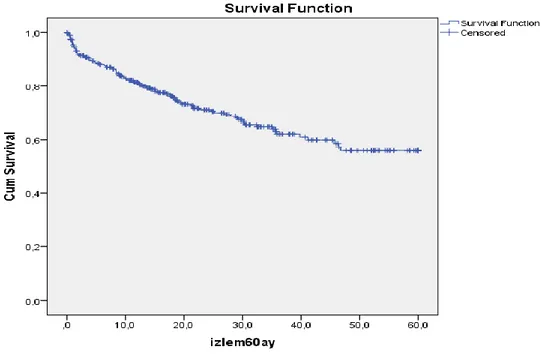
Tüm hastaların izlem süresi boyunca; 1 yıllık transplantasyon sansürlü sağkalım %81,9 (n=56), 2 yıllık %70,3 (n=82), 3 yıllık %62,9 (n=93), 4 ve 5 yıllık %55,8 (n=99) idi (Grafik 5).
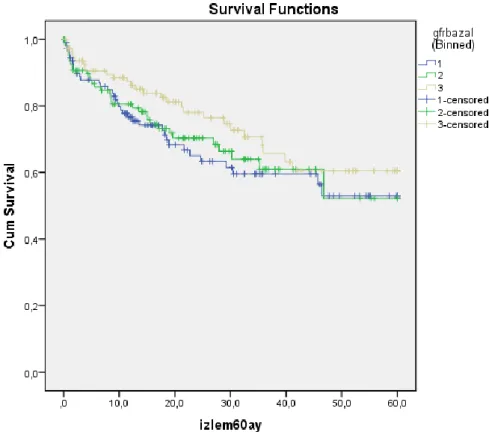
32 a) Bazal GFH’a göre her 3 grubun sağkalım oranlarına baktığımızda; 60 ayda istatistik
anlama ulaşmasa da (Grafik 6) 1. yıl için baktığımızda 3. Grupta (GFH>90) %87,9, Grup1 (GFH<60) de %76,2 olup daha iyi sağkalım mevcuttu (p=0,03) Grup 2 (GFH 60-90) de ise %81,9 idi (Grafik 7).
Grafik 6. Bazal GFH’lerine göre 3 grubun 3 yıllık sağkalım oranları (p=0,129)
33 b) En belirgin GFH artışı 1. ayda olduğu için hastaları 1. ay GFH sonuçlarına göre tekrardan 3 gruba ayırdık ve hastaların bazal ve 1. ay gruplar arası değişimine baktığımızda; bazal GFH grup 1’de olan hastaların %27’si postop Grup 1 şeklinde kalmaya devam ederken yaklaşık %73’ünün GFH’larının arttığını gördük. Buna karşılık GFH>60’ın üstünde olan hastaların ise yaklaşık %14’ünün postop 1. ayda grup 1’e gerilediğini gördük.
Tablo 10. GFH bazal grup * GFH 1. ay grup Crosstabulation
GFH BAZAL (ml/dk/1,73m2) GFH 1ay (ml/dk/1,73m2) Total <60 60-90 >90 <60 N 20 34 20 74 % 27,0 45,9 27,0 100 60-90 N 17 40 72 129 % 13,2 31,0 55,8 100 >90 N 1 9 83 93 % 1,1 9,7 89,2 100 Total N 38 83 175 296 % 12,8 28,0 59,1 100
Bakılan 1. ay GFH gruplarının izlem boyunca olan transplantasyon sansürlü sağ kalım oranlarına baktığımızda 1. grup (<60)’un (n=38) sağ kalım oranı %44,7 (29,7 ± 5,5 ay), 2. grubun (60-90) (n=83) sağ kalım oranı %71,1 (46,3 ± 3,3 ay) ve 3. grubun (>90) (n=175) sağkalım oranı %68,9 (49,8 ± 2,6 ay) olup istatiksel açıdan bazal GHF gruplarının sağkalımına göre anlamlıydı (p<0,01).
34
Grafik 8. 1. Ay GFH gruplarının transplantasyon sansürlü sağkalımları (log rank p<0,001)
c) İlk 1 ayda GFH artan (n=227) (50,4 ± 2,2 ay) ve artmayan hastaları (n=69) (35,7 ± 3,7 ay) 2 grup olarak incelediğimizde; iyileşenlerin 2 yıllık sağ kalımı %73, 3 yıllık %65, 4yıllık %58 iken iyileşmeyenlerin ise 2 yıllık %56, 3 yıllık %49, 4 yıllık %38 idi (p<0,01)(grafik 9).
35
Grafik 9. İzlemin 1. ayında GFH’ı artanların ve azalan/değişmeyenlerin sağ kalımı (log rank p<0,01)
4.3 Postoperatif Komplikasyonlar
İzlem boyunca LVAD’la ilişkili komplikasyonlara baktığımızda hastalarda en çok iskemik ve hemorajik serebrovasküler olayların ve pompa trombozu komplikasyonlarının geliştiğini saptadık (Tablo 11). Zaman içinde kalp nakli olan hasta oranı %15,3, ölüm oranı %30,3 idi İzlemde bazal GFH’ı düşük olanların daha az kalp nakli oldukları gözlendi (Tablo 12). Bakılan ölüm nedenleri içinde ilk sırayı serebrovasküler olaylar, ikinci sırada enfeksiyonlar ve üçüncü en sık neden olarak da kardiyovasküler olaylar görüldü (Tablo 13).
36
Tablo 11. Postoperatif Komplikasyonlar ve Klinik Sonlanım
Toplam Hasta /Olay Yüzde (%)
Postop Sağ Yetmezlik 27/301 7,8
Geçici RVAD (Levitronix veya ECMO)
6/292 2,1
Pnömoni 17/280 6,1
Akut Böbrek yetmezliği (hemodiyaliz ihtiyacı olan)
11/253 4,3
Pompa cep enfeksiyonu 11/346 3,2
Hemoliz 21/254 8,3 GIS Kanama 23/259 8,9 İskemik SVO 39/255 15,3 Pompa trombozu 41/265 15,5 Hemorajik SVO 36/261 13,8 Aritmi 26/244 10,7 Transplantasyon 52/330 15,8 Ölüm 100/330 30,3
İzlemde devam eden 178/330 53,9
Tablo 12. Bazal GFH Gruplarına Göre Klinik Sonlanımlar
İzlem Tx Ex Toplam GFH BAZAL GRUP <60 n 48 8 29 85 % 56,5 %9,4 34,1 100,0 60-90 n 72 22 44 138 % 52,2 15,9 31,9 100,0 >90 n 57 22 27 106 % 53,8 20,8 25,5 100,0 Toplam n 177 52 100 329 % 53,8 15,8 30,4 100,0
37
Tablo 13. Ölüm nedenleri
Toplam Hasta /Olay Yüzde (%)
Serebrovasküler 26/87 29,9 Enfeksiyon 22/87 25,3 Kardiyovasküler 13/87 14,9 Pompa trombozu 9/87 10,3 Diğer 5/87 5,7 Bilinmeyen 12/87 13,8
Mortalite belirleyicilerine Cox regresyon analizi ile baktığımızda; 1.ay GFH ve preop albümin düşüklüğü mortalite belirleyicisidir. Bazal GFH’ından ziyade 1. ay GFH’nın
mortalite için daha belirleyici olduğunu bulduk (Tablo 14). Tablo 14. Mortalite için Cox Regresyon Analizi
Modele; yaş, cinsiyet, VKİ, HT, DM, GFH bazal, GFH 1.ay ve albümin ilave edildi.
B SE Wald df Sig. Exp (B) 95,0% CI for Exp (B) Lower Upper Değişkenler GFH 1ay -,008 ,004 4,304 1 ,038 ,992 ,985 1,000
Preop-Albumin
38
5. TARTIŞMA
KY, yaşam beklentisi ve kalitesinde belirgin azalma ile seyreden klinik bir tablodur. Kalp yetersizliğinin prevelansı tüm dünyada hızla artmaktadır ve ABD'de 6 milyondan fazla insanı ve dünya çapında 30 milyondan fazla kişiyi etkilediği tahmin edilmektedir. Tıbbi ve farmakolojik tedaviye rağmen son evreye giderek artan sayıda hasta ilerlemektedir. Bu hastalar sık hastaneye yatış gerektirir, bir yılda %80’e kadar yüksek bir mortalite oranına sahiptir. Bu nedenle hastaların tedavi ve bakım maliyetleri oldukça yüksek seyretmektedir (32). Dekompanse kalp yetersizliği tanısı alan ve maksimum medikal tedaviye rağmen istirahatte belirgin kalp yetersizliği semptomları devam eden hastalara girişimsel tedavi yöntemleri uygulanmaktadır. Kalp nakil veya mekanik destek cihazı takılması bunlara örnek gösterilebilir. Kalp transplantasyonu, son dönem KY olan tüm yaş gruplarındaki hastalarda, yeterli başarı oranıyla uygulanabilecek en uygun tedavi seçeneğidir.
Transplantasyon adayı hastaların yaklaşık %20-40’ı bekleme sırasında, %20’si naklin ilk yılı içerisinde kaybedilmekte, bu ilk yıldan sonraki her yıl için %5’lik mortalite riski eklenmektedir (33, 34).Donör azlığı nedeniyle henüz nakil olamamış hastalara uygun organ bulunana kadar veya nakil için uygun olmayan hastalara uzun süreli dolaşım desteği sağlamak amaçlı sol ventrikül destek cihazları (LVAD) takılmaktadır. LVAD kalbin iş yükünü ciddi şekilde azaltarak hastayı yatağa bağımlı halden kurtarabilir ve ona aktif yaşam kalitesi kazandırabilir. Bu şekilde hastalar transplantasyon olanağı sağlanıncaya kadar yaşamlarını sürdürmek ve kalp yetersizliğinin organlar ve sistemler üzerindeki bozucu etkilerini düzeltmek amaçlı köprü olarak LVAD ‘dan faydalanırlar. Nakil için uygun olmayan hastalar da cihaz desteğiyle dolaşım sağlanarak uzun süre yaşamlarını devam ettirebilmektedirler. Medikal tedavi ile ileri sistolik kalp yetersizliği olan bireyler (stage D) için bir yıllık sağkalım %25'dir ve 2 yılda <%10'a düşer. Devamlı LVAD uygulaması ile, post-LVAD sağkalım, 1 yılda %85 ve 2 yılda %70'dir ve tıbbi tedaviden daha iyidir.
INTERMACS raporuna göre, daha yüksek serum kreatinin konsantrasyonu ve LVAD implantasyonunda diyaliz alınması ölüm için bağımsız risk faktörleridir (35). Bizim çalışmamızın sonuçları da INTERMACS çalışmasındakine benzer (grafik 10) hatta daha iyi olup 1 yıllık transplantasyon sansürlü sağkalım %81,9, 2 yıllık %70,3, 3 yıllık %62,9, 4 ve 5 yıllık %55,8 idi.
39
Grafik 10. INTERMACS raporu.
LVAD implantasyonundan sonra, özellikle kardiyorenal patofizyoloji mevcutsa, böbrek fonksiyonu kısa vadede iyileşebilir; daha uzun vadedeki, veriler sınırlıdır. LVAD implantasyonu sonrası böbrek fonksiyonunu araştıran gözlemsel çalışmaların çoğu retrospektiftir ve sınırlı izlem süresine sahiptir. Çalışmamızın diğer çalışmalara göre izlem süresinin daha uzun (60 ay) ve hasta sayısının daha çok olması elde ettiğimiz sonuçları güçlü kılmaktadır. Literatürdeki çalışmaların çoğunda GFH ve serum kreatinin konsantrasyonunun, LVAD takılmasından hemen sonraki aylarda iyileştiği gözlenmektedir (36-39). Özellikle ilk ayda belirgin bir iyileşme olmakta daha sonra bu iyileşme belli bir süre azalarak devam etmektedir. Ayrıca, bu iyileşmenin daha kötü böbrek fonksiyonu olan hastalarda daha belirgin olduğu görülmektedir (36-39). Bu durumun en önemli nedeninin uç organ perfüzyon bozukluğunda iyileşme olduğu düşünülmektedir.
Yakın zamanda 184 hastayla yapılan Daimee ve ark.nın çalışmasında, hastalar bazal GFH’a göre üç gruba ayrılmış ve implantasyon sonrası birinci ayda her üç grupta GFH ‘da anlamlı bir iyileşme olduğu saptanmıştır. Düşük GFH (<45ml/dk ) grubunda LVAD sonrası 2 yıllık süreçte GFH değerlerinin bazale göre anlamlı yüksek seyrettiği (p= 0,012), GFH si 45-59 ml/dk olan grupta ise bazal GFH değerlerine indiği görülmüştür. GFH >60 ml/dk üzerindeki hasta grubunda ise artış 1. ay sonrasında bazal GFH değerlerine inmiştir. Sonuç olarak, bu çalışmada GFH düşük ve orta gruplarda implantasyon sonrası GFH iyileşmesinin benzer düzeyde ve hızlı şekilde olduğu, GFH iyi olan gruptaysa genel olarak stabil olduğu
40 görülmektedir (36) Çalışmamızda da benzer şekilde ilk ayda tüm hastaların ve grupların ortalama GFH değerlerinde bazale göre anlamlı bir artış gözlenmiştir (p<0,001, p<0,01, p<0,001). Farklı olarak, GFH <60 ml/dk olan grupta iki yıl sonuna kadar GFH’da bazale göre anlamlı artış (p<0,001) devam etmiş, hatta üçüncü yılda bile istatiksel olarak anlamlılığa yakın bir artış saptanmıştır (p=0,08). GFH 60-90 olan grupta da ilk 6 ay bazal GFH değerlerine göre anlamlı artış görülmüştür (p=0,02). GFH >90 olan grupta ise diğer çalışmalarla benzer şekilde sadece 1.ayda anlamlı artış olmuştur (p<0,001).
Bir diğer 238 LVAD takılan hastada yapılan çalışmada hedef tedavi (Destination Terapi) ve köprü tedavisi (Bridge to Transplantation) alan hastalar olarak 2 grupta analiz edilmiş. Hedef tedavi grubunda bazal GFH ı düşük ve normal olan hastaların LVAD sonrası 18 ay sonuçlarında anlamlı fark saptanmamıştır(p=0,87). 1 sene sonunda hedef tedavi grubunda %43, köprü tedavisi alan grupta ise %57’de GFH >60 ml/dk üzerine çıktığı görülmüştür. Bu çalışmada düşük GFH li hasta grubuna LVAD implantasyonunun herhangi bir engel oluşturmadığı sonucuna varılmıştır (37).
R.Muslem ve arkadaşlarının 241 hastada LVAD sonrası yaş ve renal fonksiyon bozukluğu ilişkisi konusunda yaptıkları çalışmada yaş <45 olanlarda ortalama Bazal GFH 72 ml/dk, yaş >65 olanlarda ise 49 ml/dk olduğu saptanmış. 65 yaş üstü hasta grubunda LVAD sonrası 1. senede GFH anlamlı artmamış (p = 0,73). Yapılan univariate analizinde 1 sene sonunda yaş, iskemik kardiyomiyopati ve bazal GFH düşüklüğünün LVAD sonrası GFH üzerinde etkili olduğu saptandı (39). Bizim çalışmamızda da 1. Yıl GFH’nı belirleyen faktörler arasında yaş, bazal GFH ve diyabet varlığı mevcuttu ki benzer şekilde yaş önemli bir faktördü. Yoshioka D. ark. çalışmasında implantasyon sonrası GFH’ı iyileşen hastaların 6 aylık takibi yapılmıştır, 6 ay sonrasında sadece bazal GFH ı düşük hastaların GFH da iyileşmenin devam ettiği gözlemlenmiştir (40). Bizim çalışmamızda bazal GFH ı düşük olan hastaların operasyon sonrası %27’de GFH ‘da iyileşme olmadığı, %73’de iyileşme olduğu saptandı. Buna karşılık GFH>60’ın üstünde olan hastaların ise yaklaşık %14’ünün operasyon sonrası GFH ‘da iyileşme olmadığı gözlenmiştir. 1 yıl sonunda bazal GFH <60 ml/dk olan hasta grubunda ortalama GFH 63,3 ml/dk olduğu saptandı. Regresyon analizi ile baktığımızda 1.ayda GFH artışını belirleyenler; yaş, bazal GFH, preop Na ve preop albümin idi. 1.yılda GFH artışını; yaş, Bazal GFH düşüklüğü ve DM varlığı, yokluğu belirliyor. 2.yılda GFH artışını, yaş ile bazal GFH düşüklüğü ve preop albumin yüksekliği belirliyor. Bütün bu bulgular LVAD tedavisinin son evre kalp yetmezlikli hastalarda oluşabilen perfüzyon bozukluğunu geri çevirdiğini güçlendirmektedir. Bizim çalışmamızda da alınan verilere göre böbrek fonksiyon bozukluğu LVAD implantasyonu için engel oluşturmadığını güçlendirmektedir.