T.C.
EGE ÜNİVERSİTESİ
TIP FAKÜLTESİ
SPOR HEKİMLİĞİ ANABİLİM DALI
Düzenli Egzersizin Multiple Skleroz Progresyonu Üzerine Etkisi
UZMANLIK TEZİ
Dr. Mehmet AÇIK
TEZ DANIŞMANI
Dr. Öğretim Üyesi Seçkin ŞENIŞIK
T.C.
EGE ÜNİVERSİTESİ
TIP FAKÜLTESİ
SPOR HEKİMLİĞİ ANABİLİM DALI
Düzenli Egzersizin Multiple Skleroz Progresyonu Üzerine Etkisi
UZMANLIK TEZİ
Dr. Mehmet AÇIK
TEZ DANIŞMANI
Dr. Öğretim Üyesi Seçkin ŞENIŞIK
ÖNSÖZ
Uzmanlık eğitimim boyunca, çok değerli bilgileri ve tecrübelerinden faydalandığım, yanında çalışmaktan onur duyduğum, bizlere her zaman yakınlık gösteren, yardımseverliği, iyi niyeti ve hoşgörüsü ile üzerimde hayat boyu kalacak izler bırakan, asistanı olduğum için kendimi çok şanslı addettiğim kıymetli hocam ve tez danışmanım Dr. Öğretim Görevlisi Dr. Seçkin Şenışık’a,
Birlikte çalışmaktan onur duyduğum, bilgisi, deneyimleri ve yönlendirmeleri ile eğitimimize katkıda bulunan bilimsel ortamı bizlere hazırlayan hocalarım Prof. Dr. Cengizhan Özgürbüz, Prof. Dr. Metin Ergün, Prof. Dr. S. Oğuz Karamızrak’a,
Tezim süresince desteklerini esirgemeyen her konuda yardımcı olan kıymetli hocalarım Prof. Dr. Ayşe Nur Yüceyar ve Prof. Dr. Dilek Taşkıran’a,
Spor Bilimleri Fakültesinin tüm imkanlarını sağlayarak çalışmamda bana destek olan Doç. Dr. Tolga Akşit, Öğr. Görevlisi Ramazan Aydınoğlu, Öğr. Görevlisi Dr. Görkem Aybars ve Doktora öğrenimine devam eden Hakan As’a,
Eğitimim boyunca asistanlık sürecinin zorluklarını da keyfini de birlikte paylaştığım Dr. Ogün Köyağasıoğlu, Dr. İhsan Yörük, Dr. Göksu Gökçe ve Dr. Yunus Emre Meydanal’a uzmanlık eğitimini tamamlamış olan Uzm. Dr. Abdülaziz Türksoylu ve Uzm. Dr. Yavuz Lima’ya,
Tezim süresince desteklerini esirgemeyen Ege Üniversitesi Spor Hekimliği Anabilim Dalı personellerinden Sevda Anşen, Serap Tanınmış ve Gülşah Afyoncu’ya,
Dünyanın en yardımsever, gönlü güzelliklerle dolu, hayat tecrübeleri ile hayata bakış açımızı değiştiren, desteğini her an hissettiğim Erol Cem Girgin’e,
Hayatımı birleştirdiğim; sevgisi, iyi niyeti, anlayışı ve güler yüzüyle bana hep güç veren, destek olan ve hayatıma anlam katan eşim Şeyma Açık’a,
Kalpten teşekkür ederim.
Dr. Mehmet AÇIK İZMİR 24.12.2019
i İÇİNDEKİLER
İÇİNDEKİLER ... i
ÖZET ... iv
ABSTRACT ... vi
TABLOLAR LİSTESİ ... viii
ŞEKİLLER LİSTESİ ... ix
KISALTMALAR ... x
1. GİRİŞ ... 1
1.1. Multiple Skleroz ve Fiziksel İnaktivite ... 1
1.2. Nörotrofinler ... 1
1.3. Araştırmanın Önemi ve Amacı ... 2
1.4. Araştırmanın Hipotezleri ... 2 2. GENEL BİLGİLER ... 3 2.1. Multiple Skleroz ... 3 2.1.1. Tanım ... 3 2.1.2. Epidemiyoloji ... 3 2.1.3. Etiyoloji ... 4 2.1.3.1. Otoimmunite ... 4 2.1.3.2. Genetik ... 4 2.1.3.3. Enfeksiyöz ... 4 2.1.3.4. Vitamin D ... 5 2.1.3.5. Sigara ... 5 2.1.4. İmmunpatogenez ... 5
2.1.5. Klinik Semptom ve Bulgular ... 6
2.1.5.1 Motor Semptomlar ... 6
2.1.5.2. Duysal Semptomlar ... 6
2.1.5.3. Beyin Sapı Semptomları... 7
2.1.5.4. Görme ile İlişkili Semptomlar ... 7
2.1.5.5. Kognitif Bozukluk ve Depresyon ... 7
2.1.5.6. Paroksismal Semptomlar ve Epilepsi ... 8
2.1.5.7. Yorgunluk ve Uyku Bozuklukları ... 8
2.1.5.8. Serebellar Semptomlar ... 8
2.1.5.9. Mesane, Barsak Fonksiyon Bozuklukları... 8
2.1.5.10. Cinsel fonksiyon bozuklukları ... 9
2.1.5.11. Baş Ağrısı ... 9
2.1.6. Klinik Tipleri ... 9
ii 2.1.6.2. Relapsing Remitting MS (RRMS) ... 11 2.1.6.3. Sekonder Progresif MS (SPMS) ... 11 2.1.6.4. Primer Progresif MS (PPMS) ... 12 2.1.6.5. Relapsing Progresif MS (RPMS) ... 12 2.1.6.6. Benign MS ... 12 2.1.7. Tanı ... 12 2.1.7.1. Tetkikler ... 14
2.1.7.1.1. Manyetik Rezonans Görüntüleme (MRG) ... 14
2.1.7.1.2. Beyin Omurilik Sıvısı İncelemeleri... 15
2.2. Nörotrofinler ... 15
2.2.1. Sinir Büyüme Faktörü (NGF) ... 16
2.2.1.1. Sentezlendiği hücreler ... 16 2.2.1.2. Etki mekanizması ... 16 2.2.1.3. Fonksiyonu ... 17 2.2.2. Nörotrofin-3 (NT-3) ... 17 2.2.2.1. Sentezlendiği hücreler ... 17 2.2.2.2. Etki mekanizması ... 17 2.2.2.3. Fonksiyonu ... 17 2.2.3. Nörotrofin ve Egzersiz ... 18 2.3. Egzersiz ... 18 2.3.1. Egzersiz Tipleri ... 19 2.3.1.1. Aerobik Egzersiz ... 19 2.3.1.2. Kuvvet Egzersizleri ... 21 2.3.2. MS, Yorgunluk ve Egzersiz ... 23 2.3.2.1. Primer Nedenler ... 23
2.3.2.1.1. Merkezi sinir sistemi hasarı ... 23
2.3.2.1.2. Sitokin artışı ... 24
2.3.2.1.3. Nöroendokrinolojik sistemin etkilenmesi ... 24
2.3.2.2. Sekonder Nedenler ... 25
2.3.2.2.1. Psikolojik sorunlar ve Kognitif bozulma ... 25
2.3.2.2.2. Periferik nedenler ... 25 2.3.2.2.3. Uyku bozuklukları ... 25 2.3.2.2.4. İyatrojenik durumlar ... 26 2.3.2.2.5. Vücut ısısı artışı ... 26 2.3.2.2.5. Kondisyon eksikliği ... 27 2.3.2.3. Egzersizin Etkileri ... 27
iii
2.3.2.3.2. Egzersizin sekonder nedenler üzerine etkileri ... 28
2.3.3. MS, Denge ve Egzersiz ... 30
2.3.3.1. Egzersizin denge üzerine etki mekanizmaları ... 30
3. GEREÇ VE YÖNTEM ... 32
3.1. Katılımcılar ... 32
3.1.1. Çalışmaya Seçilme Kriterleri ... 32
3.1.2. Çalışmadan Dışlanma Kriterleri ... 32
3.2. Deneysel Tasarım ... 33
3.2.1.Cihaz ve Teçhizat ... 34
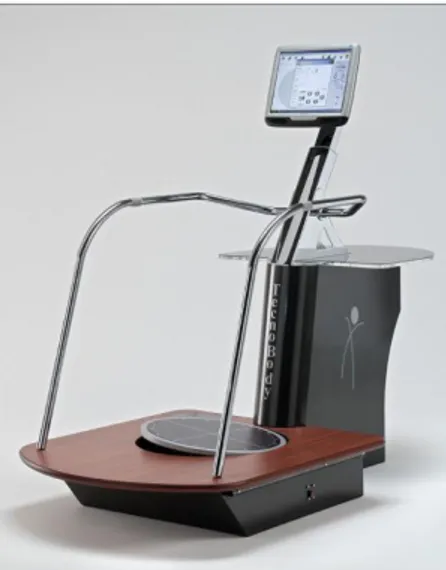
3.2.1.1.Stabilometre (Tecnobody PK-252) ... 34
3.2.1.2.Dinamometre ... 35
3.2.1.3.Bisiklet Ergometresi ... 36
3.2.1.4. Nabız Ölçer Saat ve Göğüs Bandı ... 37
3.2.1.5. Kan Alma Tüpleri ve Santrifüj Cihazı ... 37
3.2.2. Anket ve Ölçekler ... 38
3.2.2.1. BICAMS Bataryası ... 38
3.2.2.1.1. Symbol Digit Modalities Test (SDMT) ... 38
3.2.2.1.2. California Verbal Learning Test II (CVLT II) ... 38
3.2.2.1.3. Brief Visuospatial Memory Test-Revize (BVMTR) ... 38
3.2.2.2. Multipl Skleroz Yaşam Kalitesi (MSQoL)- 54 Enstrümanı... 39
3.2.2.3. Pittsburg Uyku Kalitesi İndeksi (PUKİ): ... 39
3.2.2.4. Yorgunluk Etki Skalası Ölçeği ... 39
3.3. Prosedürler ... 40
3.3.1.Denge Ölçümleri ... 40
3.3.2.Kuvvet Ölçümleri ... 40
3.3.2.1.İzometrik el kavrama gücü testi ... 40
3.3.2.2.İzometrik üst ekstremite-sırt gücü testi ... 41
3.3.2.3.İzometrik bacak gücü testi ... 41
3.3.3.Aerobik Kapasite Ölçümü ... 41
3.3.4. Kan Örnekleri Alımı, Santrifüj İşlemi ve Örneklerin Saklanması ... 42
3.3.5. NGF ve NT-3 düzeylerinin ölçümü ... 43 3.4. İstatistiksel Analiz ... 44 4. BULGULAR ... 45 5. TARTIŞMA ... 61 6. SONUÇ ... 67 7. KAYNAKÇA ... 68
iv ÖZET
Amaç:
Multiple Skleroz hastalarında sedanter bir yaşam tarzının benimsenmesi yaygındır. Bu durum fiziksel performans değerlerini kötüleştirir ve MS bulgularının alevlenme döngüsünü başlatabilir. Düzenli yapılan egzersizin nörotrofinlerin düzeyinde artış sağladığı ve nörotrofinlerin de merkezi sinir sistemi üzerine olumlu etkileri olduğu bilinmektedir. Çalışmamızdaki ilk amacımız düzenli egzersizin MS hastalarında sinir büyüme faktörü (NGF) ve Nörotrofin-3 (NT-3) düzeylerini artırdığını göstermektir. İkinci amacımız ise bu artışın merkezi sinir sistemini olumlu yönde etkileyeceğini ve bilişsel işlevlerde bozulmayı, yorgunluğu, denge bozukluğunu, uyku ve yaşam kalitesini düzelteceğini göstermektir.
Metot:
Ege Üniversitesi Nöroloji Kliniğinde takip edilen EDSS skoru 4 ve 4’ün altında olan 53 Relapsing Remitting MS hastası çalışmaya dahil edildi. Hastalar aerobik egzersiz grubu (AG), kuvvet egzersizi grubu (KG) ve kontrol grubu olmak üzere randomize bir şekilde 3 gruba ayrıldı. Egzersiz gruplarındaki hastalar 3 ay boyunca, haftada 3 gün belirlenen egzersiz programlarını uyguladılar. Tüm hastaların aerobik kapasite ve kuvvet ölçümleri, denge testleri yapıldı, ELISA yöntemi ile NGF ve NT-3 plazma değerleri analiz edildi. MSQoL54 yaşam kalitesi, yorgunluk etki skalası ve PUKİ ölçekleri hastalar tarafından dolduruldu. Kognitif fonksiyonu değerlendirmek için BICAMS ölçeği uygulandı. Egzersizin etkisini gösterebilmek için tüm ölçekler ve analizler çalışma öncesi ve sonrası tekrarlandı.
Bulgular:
Egzersiz gruplarında VO2max (AG: p<0,001, KG: p=0,003) ve kuvvet değerlerinde (sırt kuvveti; AG: p=0,002, KG: p<0,001, bacak kuvveti; AG: p<0,001, KG: p<0,001) istatistiksel olarak anlamlı artış görüldü. Egzersiz ile NGF (AG: p<0,001, KG: p=0,002) ve NT-3 (AG: p=0,08NT-3, KG: p<0,001) plazma düzeylerinde istatistiksel olarak anlamlı artış görüldü. Ancak NT-3’ün aerobik grupta artışı istatistiksel olarak anlamlı değildi. Ayrıca egzersiz gruplarında kognitif fonksiyon, uyku ve yaşam kalitesinde istatistiksel olarak anlamlı düzelme görüldü. Denge değerlerinde aerobik grupta istatistiksel olarak anlamlı düzelme görülürken, kuvvet grubunda ise düzelme olmasına rağmen istatistiksel olarak anlamlı değildi. Yorgunluk etki skalasına göre tüm grupların yorgunluk skorlarında istatistiksel olarak anlamlı azalma görüldü.
v Sonuç:
Çalışmamız, düzenli egzersiz ile MS progresyonunun engellenebileceğini ve hastalığa bağlı gelişebilecek komplikasyonların önüne geçilebileceğini göstermektedir.
vi ABSTRACT
Objective:
The adoption of a sedentary lifestyle is common in MS patients. This deteriorates physical performance values and may initiate the exacerbation cycle of MS symptoms. It is known that regular exercises increase the level of neurotrophins and neurotrophins which have positive effects on the central nervous system. Our first aim in this study is to show that regular exercises increase the levels of nerve growth factor (NGF) and neurotrophin-3 (NT-3) in MS patients. Our second aim is to show that this increase will affect the central nervous system positively and improve cognitive dysfunction, fatigue, balance disorder, sleep and quality of life.
Method:
Fifty-three relapsing remitting MS patients with EDSS scores 4 and below 4 were followed at Ege University Neurology Clinic were included in the study. The patients were randomly divided into three groups as aerobic exercise group (AG), strength exercise group (SG) and control group. The patients in the exercise groups performed the exercise programs determined for 3 months, 3 days per week. Aerobic capacity and strength measurements, balance tests were performed and NGF and NT-3 plasma values were analyzed by ELISA. MSQoL54 quality of life, fatigue effect scale and PSQI scales were filled by patients. BICAMS scale was used to assess cognitive function. All scales and analyzes were repeated before and after the study to show the effect of exercise.
Results:
Statistically significant increases were found in VO2max (AG: p <0.001, SG: p = 0.003) and strength values (back strength; AG: p = 0.002, SG: p <0.001, leg strength; AG: p <0.001, SG: p <0.001) in exercise groups. There were statistically significant increase in NGF (AG: p <0.001, SG: p = 0.002) and NT-3 (AG: p = 0.083, SG: p <0.001) plasma levels via exercise. However, the increase of NT-3 in aerobic group was not statistically significant. In addition, there were statistically significant improvements in cognitive function, sleep and quality of life in exercise groups. Statistically significant improvement was observed in balance values in aerobic group, however the improvement in the strength group was not statistically significant. There was a statistically significant decrease in fatigue scores of all groups according to the fatigue effect scale.
vii Conclusion:
Our study shows that the progression of MS and complications related to the disease can be prevented by regular exercise.
viii TABLOLAR LİSTESİ
Tablo 1. Multiple Skleroz tanı kriterleri ... 13
Tablo 2. Hastaların genel özellikleri ... 45
Tablo 3. VO2max’ın gruplarda zamana bağlı değişimi ... 46
Tablo 4. Kuvvet değerlerinin gruplarda zamana bağlı değişimi ... 46
Tablo 5. NGF değerlerinin gruplarda zamana bağlı değişimi ... 48
Tablo 6. NT-3 değerlerinin gruplarda zamana bağlı değişimi ... 49
Tablo 7. Yorgunluk etki skalası ölçeğinin gruplarda zamana bağlı değişimi ... 50
Tablo 8. PUKİ'nin gruplarda zamana bağlı değişimi ... 51
Tablo 9. BICAMS alt ölçeklerinin gruplarda zamana bağlı değişimi ... 53
Tablo 10. MSQoL54 ölçeğinin gruplarda zamana bağlı değişimi ... 54
Tablo 11. Çift ayak statik zemin denge ölçümünün istatistiksel verileri ve grafikleri ... 56
Tablo 12. Sağ ayak statik zeminde denge ölçümünün istatistiksel verileri ve grafikleri ... 57
Tablo 13. Çift ayak dinamik zeminde denge ölçümlerinin istatistiksel verileri ve grafikleri-1 ... 58
Tablo 14. Çift ayak dinamik zeminde denge ölçümlerinin istatistiksel verileri ve grafikleri-2 ... 59
ix ŞEKİLLER LİSTESİ
Şekil 1. MS modifiye fenotipleri-relapsing form ... 10
Şekil 2. MS modifiye fenotipleri – progresif form ... 10
Şekil 3. Çalışmada kullanılan stabilometre cihazı... 34
Şekil 4. Çalışmada kullanılan el dinamometresi ... 35
Şekil 5. Çalışmada kullanılan Sırt-Bacak Dinamometresi ... 36
Şekil 6. Çalışmada kullanılan bisiklet ergometresi ve dijital ekranı ... 36
Şekil 7. Çalışmada kullanılan nabız ölçer saat ve göğüs bandı ... 37
Şekil 8. Çalışmada kullanılan kan tüpleri ve santrifüj cihazı ... 37
Şekil 9. NGF ve NT-3 düzeylerinin ölçümü için kullanılan ELISA testi ... 43
Şekil 10. VO2 max'ın gruplarda zaman içinde değişiminin göreceli etki grafiği ... 46
Şekil 11. Sırt kuvvetinin gruplarda zaman içinde değişiminin göreceli etki grafiği ... 48
Şekil 12. Bacak kuvvetinin gruplarda zaman içinde değişiminin göreceli etki grafiği ... 48
Şekil 13. NGF'nin gruplarda zaman içinde değişiminin göreceli etki grafiği ... 49
Şekil 14. NT-3'ün gruplarda zaman içinde değişiminin göreceli etki grafiği ... 50
Şekil 15. Yorgunluk etki skalası ölçeğinin gruplarda zaman içinde değişiminin göreceli etki grafiği ... 51
Şekil 16. PUKİ'nin gruplarda zaman içinde değişiminin göreceli etki grafiği ... 52
Şekil 17. BVMT-R'nin gruplarda zaman içinde değişiminin göreceli etki grafiği ... 53
Şekil 18. SDMT'nin gruplarda zaman içinde değişiminin göreceli etki grafiği ... 53
Şekil 19. CVLT-2'nin gruplarda zaman içinde değişiminin göreceli etki grafiği ... 53
Şekil 20. BMS'nin gruplarda zaman içinde değişiminin göreceli etki grafiği ... 55
Şekil 21. BFS'nin gruplarda zaman içinde değişiminin göreceli etki grafiği ... 55
Şekil 22. Çift Ayak Statik ML salınımın gruplarda zaman içinde değişiminin göreceli etki grafiği ... 56
Şekil 23.Çift Ayak Statik Elips Alanının gruplarda zaman içinde değişiminin göreceli etki grafiği ... 56
Şekil 24. Sağ ayak Statik FB salınımın gruplarda zaman içinde değişiminin göreceli etki grafiği ... 57
Şekil 25. Sağ ayak Statik Elips Alanının gruplarda zaman içinde değişiminin göreceli etki grafiği ... 57
Şekil 26. Sağ ayak Statik çevre'nin gruplarda zaman içinde değişiminin göreceli etki grafiği 57 Şekil 27. Çift Ayak Dinamik FB salınımın gruplarda zaman içinde değişimin göreceli etki grafiği ... 58
Şekil 28. Çift Ayak Dinamik ML salınımın gruplarda zaman içinde değişimin göreceli etki grafiği ... 58
Şekil 29. Çift ayak dinamik elips alanının gruplarda zaman içinde değişimin göreceli etki grafiği ... 59
Şekil 30. Çift ayak dinamik çevrenin gruplarda zaman içinde değişimin göreceli etki grafiği 59 Şekil 31. Sol ayak statik zeminde elips alanının gruplarda zaman içinde değişimin göreceli etki grafiği ... 60
x KISALTMALAR
ABD : Amerika Birleşik Devletleri
ACSM : American College of Sports Medicine ACTH : Adrenokortikotropik Hormon
BFS : Bileşik Fiziksel Sağlık
BICAMS : Brief International Cognitive Assessment for MS
BMS : Bileşik Mental Sağlık
BOS : Beyin Omurilik Sıvısı
BVMTR : Brief Vasospatial Memory Test- Revize CVLT II : California Verbal Learning Test II
EBV : Ebstein Barr Virus
EDSS : Expanded Disability Status Scale EHA : Eklem Hareket Açıklığı
FB : Front-Back
HHV-6 : Human Herpes Virüs-6
HLA : Human Lökosit Antijen
HPA : Hipotalamus-Hipofiz-Adrenal
HSV : Herpes Simplex Virus
HTLV- 1 : Human T-Hücre Lenfotropik Virüs-1 IFN-α : İnterferon Alfa
IFN-β : İnterferon Beta
IFN-γ : İnterferon Gama
IL-1 : İnterlökin 1
IL-6 : İnterlökin 6
INO : İnter Nükleer Oftalmopleji
KBB : Kan Beyin Bariyeri
KİS : Klinik İzole Sendrom
MAPK : Mitojen Aktiveli Protein Kinaz
MHC : Majör Histokompaktabilite Kompleksi
ML : Medio-Lateral
MRG : Manyetik Rezonans Görüntüleme MRS : Manyetik Rezonans Spektroskopi
xi MSQoL-54 : Multipl Skleroz Yaşam Kalitesi-54 ölçeği
MSS : Merkezi Sinir Sistemi
MT : Maksimum Tekrar
NGF : Sinir Büyüme Faktörü
NT : Nörotrofin
NT-3 : Nörotrofin-3
NO : Nitrik Oksit
OKB : Oligoklonal Band
ON : Optik Nörit
p75NTR : p75 Nörotrofin Reseptörü PPMS : Primer Progresif MS
PUKİ : Pittsburg Uyku Kalitesi İndeksi RRMS : Relapsing Remitting MS SDMT : Symbol Digit Modalites Test SPMS : Sekonder Progresif MS TNF-α : Tümör Nekroz Faktör Alfa Trk : Tirozin Kinaz reseptör VO2max : Maksimal oksijen tüketimi
1 1. GİRİŞ
1.1. Multiple Skleroz ve Fiziksel İnaktivite
Multiple Skleroz (MS) genç erişkinlerde en sık nörolojik engelliğe neden olan Merkezi Sinir Sisteminin (MSS) demiyelinizan hastalığıdır. Hastalığın etiyolojisinde günümüzde kesin bir neden bulunamamıştır. Histolojik olarak inflamasyon, demiyelinizasyon, aksonal hasar, gliozis ve remiyelinizasyonla giden multifokal ve multifazik bir süreç içerir. Hastalık daha çok ataklar ve remisyonlarla giden formdan zamanla sekonder progresif faza ilerleyip engelliliğe ve kognitif bozulmalara yol açar.
Fiziksel inaktivite ya da sedanter bir yaşam tarzının benimsenmesi, MS hastalarında yaygındır. MS hastaları, sağlıklı kişilerden fiziksel olarak daha az aktiftir ve fiziksel performans değerleri zaman içinde giderek kötüleşmektedir (1,2). Fiziksel inaktivite, MS hastalarında nöral uyarının azalması nedeniyle ilerleyen kas atrofisine yol açar (3). MS semptomlarının bozulma ve kötüleşme döngüsünü başlatabilir, yaşam kalitesinin azalmasına, yorgunluk şikayetlerinde artışa neden olur. MS ayrıca kardiyorespiratuar sistemi etkiler. MS hastalarında
kardiyorespiratuar uygunluk, performans ve sağlık belirteci olan maksimal oksijen tüketimi (VO2max) azalmaktadır (4,5). Hareketsizlik, azalmış kas gücü ve bozulmuş kardiyorespiratuar fonksiyon kombinasyonu kardiyovasküler hastalık riskini de artırmaktadır. Bir arada ele alındığında Multiple Skleroz Uluslararası Fonksiyonellik, Engellilik ve Sağlık Sınıflaması (ICF: The International Classification of Functioning, Disability and Health) modelinin tüm düzeylerine ilişkin bir dizi önemli fonksiyonel ve sağlıkla ilişkili faktörleri etkiler (6).
1.2. Nörotrofinler
Nöronların hayatta kalmasını, hipertrofisini, nörogenezi ve sinaptik plastisiteyi sağlayan büyüme faktör ailesidir. MSS başta olmak üzere periferik sinir sistemi nöronlarında, periferik dokularda birçok hücre tipinden sentezlenmektedir. Nörotrofin (NT) sentezindeki yetersizliğin veya bozukluğun nörodejeneratif hastalıklara karşı yatkınlığı artırabileceğine dair görüşler vardır. Nörodejeneratif hastalıkların tedavisinde NT’ler kullanım alanı bulmaktadır (7). Sinir Büyüme Faktörü (NGF) ve Nörotrofin-3(NT-3) nörotrofin ailesinin ilk tanımlanan üyelerindendir.
2 1.3. Araştırmanın Önemi ve Amacı
Düzenli yapılan egzersizin nörotrofinlerin düzeyinde artış sağladığı bilinmektedir. Nörodejeneratif hastalıklarda nörotrofinlerin olumlu etkileri birçok çalışmada gösterilmiştir. Çalışmamızda düzenli egzersiz ile MS hastalarında nörotrofin düzeylerinin arttığı gösterilmek istenmiş olup bu artış ile MSS’de meydana gelen hasarı ve buna bağlı gelişen kognitif bozulma, yorgunluk, uyku problemleri ve denge bozuklukları gibi yaşam kalitesini bozan patolojileri düzeltmek amaçlandı. Literatürde nörotrofinlerle ilgili yapılan insan çalışmaları kısıtlıdır. Ayrıca çalışmamız MS hastalarında egzersiz, NGF ve NT-3’ün birlikte değerlendirileceği ilk insan çalışması olarak literatüre katkı sağlayacaktır.
1.4. Araştırmanın Hipotezleri
Bu çalışmadaki ilk hipotezimiz MS hastalarının aerobik ve kuvvet egzersizleri yaptıktan sonra VO2max ve kas kuvvetlerindeki artış ile NGF ve NT-3’ün plazma düzeylerinin yükseleceğidir. İkinci hipotezimiz ise MS hastalarında görülen kognitif fonksiyonlarda ve dengede bozulma, yorgunluk artışı, uyku ve yaşam kalitesinde azalma gibi bulguların düzenli egzersiz yaparak düzeleceği ve hastalık progresyonunun yavaşlayacağıdır.
3 2. GENEL BİLGİLER
2.1. Multiple Skleroz
2.1.1. Tanım
MS özelikle beyaz cevher olmak üzere gri cevherin de etkilendiği, inflamasyon, demiyelinizasyon, aksonal hasar ve gliozis ile karakterize, kronik inflamatuar ve nörodejeneratif bir hastalıktır (8).
Hastalığın seyri kişiden kişiye farklılık gösterebilmektedir. MSS’de etkilenen anatomik bölgeye göre farklı nörolojik bulgular görülebilmektedir. Klinik olarak hastalarda ani kötüleşme, kendiliğinden düzelme veya nörolojik bulguların yavaş yavaş ilerlemesi görülebilmektedir (8).
2.1.2. Epidemiyoloji
MS genç erişkinlerde kafa travmasından sonra MSS hastalıkları içinde en sık engelliğe neden olan hastalıktır (9). Kadınlarda 2-3 kat daha sık görülmektedir. Hastalık başlangıcı 20 ile 40 yaşları arasında farklılıklar gösterebilir. Hastalığın prevalansı 10 yaşından önce ve 50 yaşından sonra azalma gösterir. Kadınlarda hastalığın başlangıcı erkeklere göre yaklaşık 5 yıl daha erkendir. Erken başlangıçlı MS 16 yaş öncesi başlangıç gösteren vakaları tanımlar ve bu grup tüm MS hastalarının %5 kadarını oluşturur (10).
Tüm dünyada yaklaşık 2 milyon, Amerika Birleşik Devletleri’nde prevelansı 309,2/100.000’dir (11,12).
Türkiye'de MS prevelansı ile ilgili yapılan çalışma sayısı azdır. İstanbul’da yapılan bir araştırmada MS prevalansı 101.4/100.000 olarak bulunmuştur (13). Güncel verilere göre Orta Karadeniz Bölgesinde 2017 yılında yapılmış olan bir çalışmada MS prevalansı 43.2/100.000’dır (14).
4 2.1.3. Etiyoloji
2.1.3.1. Otoimmunite
MS oluşum mekanizmasında otoimmunite olma ihtimali olsa da hala kesin bir kanıt bulunamamıştır (15).
2.1.3.2. Genetik
Genetik faktörler incelendiğinde yapılan çalışmalar genetik geçişin varlığını göstermiştir (16). Genel popülasyonla kıyaslandığında birinci derece akrabalarında MS hikayesi olanlarda hastalığın gelişme riski 10-25 kat artmaktadır. Bunun yanı sıra cinsiyet, akrabalık derecesi, aile kökeni durumu etkileyen faktörler arasındadır (17). İkiz çalışmalarında tek yumurta ikizlerinde risk %20-39 arasında iken, çift yumurta ikizlerinde risk normal kardeşlerle benzer şekilde %3-5 arasındadır(18). Anne ve babası MS hastası olan çocuklarda %9 oranında hastalığın görüldüğü bildirilmiştir. Hastalık seyri ve şiddeti aile içerisinde etkilenen bireylerde benzerdir (19).
6. Kromozom üzerinde bulunan MHC (Majör Histokompaktabilite Kompleksi), T hücrelerine antijen sunumunda rolü olan HLA (Human Leukocyte Antigens: İnsan Lökosit Antijeni) genlerini kodlamaktadır. Genetik geçişin belirleyicilerinden biri olarak değerlendirilir. Sınıf II polimorfizmleri (DRB1*15:01– DQA1*01:02–DQB1*06:02), DW2 ve DR2 aynı zamanda güçlü bir ilişki göstermektedir (20). MHC sınıfı dışında da MS’e yatkınlık oluşturabilecek gen lokusları bulunmuştur. IL-7 ve IL-2 reseptör bölgeleri güçlü bir şekilde MS’e yatkınlıkta rolü olan bölgelerdir (21).
2.1.3.3. Enfeksiyöz
Enfeksiyöz uyarılar, immun yanıtları uyararak MS gelişimine eğilim oluşturmaktadır (22). Hiçbir virüsün direkt etkisi tanımlanamamaktadır. Hastalık etiyolojisinde rol aldığı düşünülen virüsler Ebstein- Barr Virus (EBV), Human T-Hücre Lenfotropik Virüs-1 (HTLV-1), Parainfluenza, Human Herpes Virüs-6 (HHV-6) ve Herpes Simplex Virus (HSV)’dir. Son dönemde özellikle mononükleozise neden olan EBV üzerinde durulmaktadır. EBV ile mononükleozis enfeksiyonu sonrası hastalık riskinin normal popülasyona göre 2-3 kat arttığı
5 bildirilmiştir (23). Acinetobacter, Pseudomonas aeruginosa ve Chlamydia pneumoniae etiyolojide öne sürülen bakteriyel ajanlardandır (24,25).
2.1.3.4. Vitamin D
Yetersiz D vitamini düzeyleri birçok çalışmada MS gelişme riskinde artış ile ilişkilendirilmiştir. MS için epidemiyolojik çalışmalarda ekvatordan uzaklaşıldıkça insidansın arttığı saptanmıştır. Bu artışın güneş ışınlarına maruz kalma süresi ve D vitamin değerleri ile ilişkili olabileceği düşünülmüştür. D vitamini replasman tedavisi ile bu riskin azaltılabileceğini vurgulayan birçok çalışma yayınlanmıştır (26–28). Son zamanlarda D vitamini eksikliğinin ve yetersizliğinin kesin kanıt düzeyinde risk faktörü olduğu da belirtilmektedir (29).
2.1.3.5. Sigara
Sigara nörotoksiktir ve inflamasyon gelişimini tetikler. Sigara kullanımı olanların, olmayanlara göre hastalıklarının daha ciddi bir seyre sahip olduğuna dair zayıf da olsa kanıtlar bulunmaktadır (30).
2.1.4. İmmunpatogenez
MS’te beyaz cevherde oluşan lezyonlar sonucu kan beyin bariyeri (KBB) hasarı olur. Hasarlı bölgeye immun reaktif hücre göçü olur. İnflamasyonda primer rol alan T lenfositlerdir. Patogenezi başlatan olay otoreaktif Th17 hücrelerinin periferik kandan servikal lenf nodlarına, ardından beyin omurilik sıvısına (BOS) sonrasında da koroid pleksuslar, meninksler ve parankime geçmesidir (31). İlk aşama bu şekildedir. KBB’nin bozulması sonrası ikinci aşamada daha fazla Th17 ve Th1 hücresi parankime gelir. Miyelin kılıfta reaktif T hücreleri tarafından salınan kemokinler nedeniyle inflamasyon artar. T hücreleri ve makrofajların yüzeyinde bulunan adhezyon moleküllerinin ekspresyonundaki farklılıklardan dolayı KBB’nin aşılması kolaylaşır. İnterlökin 1, 12, 17 ve 23’ün de inflamasyonun ilerlemesinde rolü olduğu saptanmıştır (32).
CD8+ T ve CD4+ T hücrelerinin merkezi sinir sistemine göçüyle ikinci aşama başlar. İnflamasyon mikrogialaları aktifleştirir. Bu hücrelerin aktifleşmesi erken dönemdeki dejenerasyonun temel nedenidir. Sonuç olarak MS’te demiyelinizasyon ve aksonal transeksiyon meydana gelir. Aksonal transeksiyon kalıcı engellilik nedenidir. Bazı MS
6 plaklarında erken dönemde aksonal transeksiyon görülmüştür (33). Makrofaj ve CD8 T hücre sayılarının lezyonlarda meydana gelen aksonal transeksiyonun yoğunluğu ile korele olduğu ortaya konmuştur(34). B lenfositler de hastalık aktivitesinde rol alır. T lenfositler B lenfositleri uyarır. İşleyen tüm süreçlerin sonucunda miyelin harabiyeti, oligodendrogliosit dejenerasyonu ve sonraki dönemlerde hücre ve akson kaybı, gliozis meydana gelir (35). Sonuçta, MS immunpatogenezinde hem T hücreler ile ilişkili hücresel immunite hem de B hücreler ile ilişkili humoral immunite bozukluğu yer alır (35,36).
2.1.5. Klinik Semptom ve Bulgular
2.1.5.1 Motor Semptomlar
İlk MS atağında kortikospinal ve kortikobulber yolların etkilenmesi nedeniyle ortaya çıkan motor semptomlar %32-41 oranında görülür. Piramidal yol etkilenmesi durumunda paraparezi, monoparezi, kuadriparezi, hemiparezi ortaya çıkabilir. Üst ekstremite güçsüzlüğünden daha çok paraparezi ve parapleji görülür. Hastalığın başlarında spastisite saptanmayabilir. Fakat ilerleyen zamanlarda MS hastalarının yaklaşık %70’inde spastisite görülmektedir. MS hastalarında kas atrofisi beklenen bulgu olmamasına rağmen hareket kabiliyeti etkilenen hastalarda el ve kalça kaslarında atrofi gözlenebilir (37).
2.1.5.2. Duysal Semptomlar
MS’te en sık duysal semptomlar görülür. Dizestezi, allodini, hipoestezi gibi duyusal semptomlar hastalığın seyri boyunca görülebilir. Hastalar uyuşma, karıncalanma, yanma, batma hislerinden sıklıkla yakınırlar. Spinal kordun posterior kolonunun etkilenmesine bağlı eklem pozisyon hissinde veya vibrasyon hissinde bozukluk MS hastalarında sık görülmektedir. MS hastalarında başın fleksiyonu ile ekstremitelere ve sırta yayılan elektrik çarpma hissi olarak tanımlanan Lhermitte belirtisi oluşabilir. Bu durum MS hastalarının üçte birinde görülür. Diğer servikal patolojilerde de görülebildiğinden MS için tanısal değildir (38). Oppenheim'in kullanılmayan el sendromu spinal kordun posterior kolonunda veya ilgili arka kök girişindeki demiyelinizan plak nedeniyle ortaya çıkan üst ekstremitede motor, serebellar veya dokunma duyu bozukluğu olmadan proprioseptif duyu kaybı ile meydana gelen tablodur. Bu durum MS için patogonomik bir bulgudur.
7 2.1.5.3. Beyin Sapı Semptomları
Beyin sapı etkilendiğinde göz hareketlerinde bozukluklar saptanır. MS’te yaklaşık %40-70 oranında nistagmus görülür (39). Nistagmus genellikle horizontal düzlemde olmakla birlikte diğer düzlemlerde de görülebilir. Beyin sapında Medial Longitidunal Fasikulus tutulumuna bağlı oluşan, ipsilateral gözde içe bakış kısıtlılığı, kontralateral gözde dışa bakış kısıtlılığı ve nistagmusla seyreden tabloya İnter Nükleer Oftalmopleji (İNO) denir. MS’te genellikle başvuru şikayeti diplopidir. MS’te sık görülen bir diğer beyin sapı semptomu dizartridir. Serebellar etkilenme durumunda konuşma sarhoşvari ve patlayıcı tarzda olur. İntansiyonel tremor, dismetri, disdiakokinezi, fasiyal paralizi, yutma güçlüğü, blefarospazm, işitme azalması ya da kaybı, tinnitus, vertigo, inatçı hıçkırık karşımıza çıkabilecek diğer beyin sapı bulgularıdır.
2.1.5.4. Görme ile İlişkili Semptomlar
MS hastalığı sürecinde vizüel yolların etkilenmesi en sık optik nörit (ON) şeklinde olur. MS hastaların %15-20’sinde başlangıç bulgusu olarak görülür(40). Hastalar birkaç gün içinde ortaya çıkan, genellikle tek taraflı görmede azalma ve göz hareketlerinde ağrı ile başvurur. Hastaların %90’ında ON atağından 2 ila 6 ay sonra görme normal haline döner(41).
2.1.5.5. Kognitif Bozukluk ve Depresyon
Hastaların %40-60’ında kognitif fonksiyonlarda bozukluklar gözlenir. Bu bozulmalar Relapsing Remitting MS (RRMS)’de %35-45 oranında iken, progresif formlarda (SPMS-PPMS) %50-60 oranındadır (42). Benign formda bile %20 oranında görüldüğü bildirilmiştir (43). Limbik, kortikal ve subkortikal yolakların etkilenmesine sekonder ortaya çıkar.
Psikiyatrik bulgular, genel popülasyona göre MS hastalarında daha fazla görülür. Bu bulgular hastalığa ve hastalığın neden olduğu engelliliğe sekonder olarak görülebilir.
8 2.1.5.6. Paroksismal Semptomlar ve Epilepsi
MS’te gözlenen paroksismal belirtiler; hemifasiyal spazm, ataksi ve trigeminal nevralji, tonik spazm, dizartri, duyusal ataklardır. MS’te epileptik nöbet prevalansı %2,3’tür. Genel popülasyona oranla nöbet geçirme riski 3-6 kat fazladır. Epileptik nöbetlerin muhtemel anatomik nedeni kortikal/jukstakortikal beyaz maddenin inflamasyonu, ödemi ve lezyonlara sekonder demiyelinizasyon alanları olarak düşünülmektedir(44).
2.1.5.7. Yorgunluk ve Uyku Bozuklukları
MS hastalarının en sık yakındığı şikayetlerdir. Uyku bozuklukları normal populasyona göre 3 kat daha fazla görülür (40). Yorgunluk hastalığa bağlı ya da depresyon, spazm ve noktüriye bağlı uyku düzensizliği yapan sekonder nedenler sonucu gelişebilmektedir (39,45).
2.1.5.8. Serebellar Semptomlar
MS hastalarının yaşam kalitesini en çok düşüren durum serebellar etkilenmedir. MS’te sık görülen serebellar bulgular; tremor, ataksi, nistagmus, dizartri, ataksi ve titubasyondur (45). İleri vakalarda ayakta duramama (astazi), intansiyonel tremor nedeniyle el fonksiyonlarını yerine getirememe ve anlaşılmaz konuşmalar olabilir.
2.1.5.9. Mesane, Barsak Fonksiyon Bozuklukları
Mesane fonksiyon bozuklukları hastaların %75’inde, hastalık süresi 10 yılın üstünde olan hastalarda ise %96’sında saptanmıştır(40). Sıklıkla medulla spinalis etkilenmesine bağlı olmakla birlikte, medial frontal lob ve pontin lezyonlarında idrar depolanması, boşaltılması veya her iki fonksiyonun birlikte bozukluğunun görüldüğü tablolar ortaya çıkabilir. Bağırsak problemleri hastalığın ilk zamanlarında hastaların %45’inde, ilerleyen zamanda ise hastaların %68 inde görülmektedir. Konstipasyon, diyare, fekal inkontinans genellikle görülen bağırsak problemleridir (46).
9 2.1.5.10. Cinsel fonksiyon bozuklukları
Cinsel işlev bozukluğu, MS hastaları tarafından sıklıkla ihmal edilir. Erkekler için erektil disfonksiyon ve libido azalması, kadınlar için de libido azalması ve vajinal sekresyon azalması önemli bir problem olarak görülmektedir (46).
2.1.5.11. Baş Ağrısı
MS hastalarında primer baş ağrısı yaygındır ve hastaların yaklaşık %58’inde görülür (47). İnsidans olarak genel populasyondan yüksektir. Migren benzeri, küme tipi ya da gerilim tipi baş ağrısı olarak bildirilebilir (48).
2.1.6. Klinik Tipleri
MS’in temel fenotipleri relapsing (tekrarlayıcı) ve progresif (ilerleyici) olarak düşünülebilir (49). Klinik tip aktif ve progresif olarak ikiye ayrıldı. Akut relaps, manyetik rezonans görüntüleme (MRG)’de yeni/artan T2 lezyon veya kontrast tutan lezyon varlığı olarak tanımlanmıştır. Buna göre belirli bir zamanda atak geçiren veya çekilen MRG’de yeni lezyon saptanan hastalar aktif RRMS olarak tanımlanmaktadır. Primer Progresif MS (PPMS) ve Sekonder Progresif MS (SPMS) hastaları da belirli bir zaman diliminde progresyon gelişen ve gelişmeyen olarak alt kategorilere ayrılmıştır. Buna göre progresif hastalarda aktif/inaktif ve progresyon gelişen/gelişmeyen olarak adlandırılır (Şekil 1,2) (49). Bu güncellemelerle klinik süreçler daha net tanımlanmaktadır. Eski sınıflamada progresif relapsing MS formunun, yeni revizyonda ayrı bir kategoride değerlendirilmek dışında, hastalık aktivitesinin olduğu aktif progresif tip olduğu düşünülmektedir.
10 Şekil 1. MS modifiye fenotipleri-relapsing form (49)
11 Hekimler arasında hastaların klinik takibinde Kurtzke genişletilmiş engellilik durum ölçeği (Kurtzke expanded disability status scale; EDSS) ortak dil ve standardizasyon sağlamak amacıyla kullanılır. Bu ölçekte normal bulgu 0, MS nedeniyle ölüm 10 olarak numaralandırılmaktadır. EDSS 4’ün üzerinde ise hastalar yürümek için bir desteğe ihtiyaç duyarlar ve ambulasyona göre değerlendirme yapılır.
2.1.6.1. Klinik İzole Sendrom (KİS)
MS tanı kriterlerini karşılamayan ilk atağı tanımlamak için kullanılan tabirdir. MSS tutulum kriterlerini karşılayan MR lezyonları bulunmamaktadır. Hastanın anamnezinde demiyelinizasyon bulguları ile ilgili kanıt yoktur (49). Klinik izole optik nöropati, medulla spinalis tutulumu, beyin sapı sendromu daha az sıklıkla hemisferik tutulum şeklinde ortaya çıkabilir. MS olgularının %85’i KİS ile başvurur (50). Bu olguların %50-70’inin kranial MRG’lerinde beyaz cevher de demiyelinizasyonu düşündüren çoklu asemptomatik beyin lezyonlarına rastlanılmıştır. Beyin MRG’de lezyon saptanan KİS hastaları için uzun dönemde (>7 yıl) MS gelişme riski %60’ın üzerindedir (51,52). MRG lezyonu saptanmayan ortalama 20 yıl takip edilen KİS hastaları için MS gelişme riski %21 bulunmuştur (53).
2.1.6.2. Relapsing Remitting MS (RRMS)
MS’in en fazla görülen klinik tipidir. Başlangıçta hastaların %80-85’inde görülür. Ataklarla karakterize tam ya da kısmi sekelli olarak iyileşen formdur. Ataklar arasında progresyon olmaz. Ataklar sonrası kalan sekellerin birikimi sonucu engellilikte artış olabilir. Ataklar genellikle subakut seyirlidir. Atağın iyileşme zamanı birkaç haftadan birkaç aya kadar uzayabilir. Atak tanısı konulabilmesi için semptomların en az yirmi dört saat sürmesi ve iki atak arasında en az 1 ay olması gerekmektedir (54).
2.1.6.3. Sekonder Progresif MS (SPMS)
SPMS 30-40 yaşları arasında görülür. Kadınlarda 2-3 kat daha sık görülür. %30-50 oranında görülür. RRMS tanısı alan hastaların yaklaşık %50’sinin hastalık formu on yıl içinde SPMS formuna dönüşür. MSS’de sürekli negatif süreç vardır. Nörolojik defisitlerde yavaş yavaş artış görülür. Prognozu kötü seyreder (55).
12 2.1.6.4. Primer Progresif MS (PPMS)
Kırk yaş üzerinde başlar. Hastalığın görülmesinde cinsiyet farkı yoktur. MS olgularının %5-10’unu oluşturur. Genel olarak motor tutulum ve progresyon gösteren paraparezi ile başlar. Hastalığın başlangıcından itibaren engellilik progresif seyir gösterir (55). Bu form diğer MS tiplerinde farklı bir patogeneze sahiptir. Bilinen mevcut tedavilere dirençlidir (56).
2.1.6.5. Relapsing Progresif MS (RPMS)
MS hastalarının %5’ini oluşturur. Hastalığın tanısının konulmasından itibaren Primer Progresif MS’e (PPMS) benzer şekilde progresif olarak kötüleşme görülür. Bundan dolayı ilk atağa kadar PPMS’den ayırt edilemez. Ataklar olguların yarısında ilk 10 yıl içinde başlangıç gösterir. Ataklar sık aralıklarla gelişmez. Ataklar arasında da progresyon mevcuttur (57,58). Ataklar sonrasında tam iyileşme hali görülmez. EDSS skorunun 6’ya ulaşma süresi yaklaşık 8-10 yıldır. En yüksek mortaliteye sahip klinik formdur.
2.1.6.6. Benign MS
Motor belirtilerin ve duyusal bulguların hafif olduğu, ON ile ortaya çıkan ve tam iyileşme görülen, 10-15 yıllık süreçte EDSS skoru 3’ün altındaki hastalar benign MS olarak tanımlanır (59).
2.1.7. Tanı
MS tanısındaki temel görüş, MSS’deki lezyonların ve sebep olduğu kliniğin zamanda ve alanda yayılımının gösterilmesi ve benzer özellik gösteren hastalıkların klinik ve/veya inceleme yöntemleri ile dışlanmasıdır.
Kesin MS tanısı koyduracak patogonomik bir klinik veya laboratuvar bulgusu olmadığından uzun yıllar tanı kriterleri oluşturma çalışmaları yapılmıştır. MS tanısı için ilk olarak Schumacher (1965) ve Poser’in (1983) geliştirdiği tanı kriterleri kullanılmıştır. Günümüzde de geçerli tanı kriterleri olarak McDonald kriterleri kullanılmaktadır. 2001 yılında oluşturulan McDonald kriterleri 2005 ve 2010 yıllarında revize edilmiştir (60–62). Daha sonra yeni verilerin elde edilmesi ve gelişen teknoloji nedeniyle “International Advisory Committee
13 on Clinical Trials in Multiple Sclerosis” 2016 ve 2017’de iki kez toplanmış McDonald 2010 kriterlerinde güncelleme yapmıştır (Tablo 1) (62).
Tablo 1. Multiple Skleroz tanı kriterleri (63)
Revize McDonald tanı kriterleri 2017 (Thompson ve arkadaşları)
Atak Objektif klinik bulgulu lezyon sayısı
MS tanısı için gerekli ek veri
≥2 ≥2 Yok (a)
≥2 1+ öyküde başka bir alanda ki lezyona ait atak (b)
Yok (a)
≥2 atak 1 MSS’de farklı bir alandaki lezyona ait yeni
bir atak veya MRG (c) ile mekanda yayılımın gösterilmesi
1 atak ≥2 Ek bir klinik atak veya MRG (d) ile zamanda
yayılımın gösterilmesi veya BOS-spesifik OKB(e) varlığı
1 atak 1 lezyona ait objektif klinik bulgu
MSS’de farklı bir alandaki lezyona ait yeni bir atak veya MRG (c) ile mekanda yayılımın gösterilmesi ve ek bir klinik atak veya MRG (d) ile zamanda yayılımın gösterilmesi veya BOS-spesifik OKB (e) varlığı
Sinsi progresyon
1 yıl klinik progresyon (retrospektif veya
prospektif, ataktan bağımsız olarak)
Aşağıdakilerin 2’si
•MS tipik alanlarda ≥1 lezyon
(periventriküler, kortikal/jukstakortikal veya infratentoryal)
• Spinal kordda ≥2 lezyon • BOS-spesifik OKB varlığı
a: Mekanda ve zamanda yayılımı göstermek için ek bir teste gerek yoktur. Ancak beyin MRG tüm hastalara yapılmalıdır. Tanıyı destekleyecek yetersiz klinik ve MRG bulguları olanlarda, tipik KİS olmayanlarda, atipik özellikleri olan hastalarda ek olarak spinal kord MRG ve BOS tetkiki yapılmalıdır. Bu tetkikler yapılamadıysa ya da negatifse MS tanısı koymadan önce dikkat edilmeli ve alternatif tanılar göz önünde bulundurulmalıdır.
14 b: Atak için objektif nörolojik bulgular temelinde konulmuş klinik tanı en güvenilirdir. Öyküdeki atağa ait dökümante edilmiş objektif nörolojik bulgular yoksa, öykü
inflamatuar demiyelinizan olaya ait tipik semptom ve klinik gelişim özelliklerini
içermelidir. Ancak en az bir atak objektif bulgularla desteklenmelidir. Objektif kanıtların yokluğunda dikkatli olunmalıdır.
c: MRG’de alanda yayılım; MS tipik (periventriküler, kortikal/jukstakortikal, infratentoryal ve spinal kord) 4 alanın ≥2’sinde ≥1 lezyon olması.
d: MRG’de zamanda yayılım; herhangi bir zamanda çekilen MRG’de kontrast tutan ve tutmayan lezyonların aynı anda bulunması veya takip MRG’sinde ilk MRG (çekildiği zamandan bağımsız olarak) referans alındığında yeni bir T2 hiperintens lezyonun ya da kontrast tutan lezyonun olması.
e: BOS-spesifik OKB varlığı zamanda yayılımı göstermez ama tanıda onun yerine geçer. MS: Multipl skleroz, MSS: Merkezi sinir sistemi, MRG: Manyetik rezonans görüntüleme, BOS: Beyin omurilik sıvısı, OKB: Oligoklonal band
2.1.7.1. Tetkikler
2.1.7.1.1. Manyetik Rezonans Görüntüleme (MRG)
MS ön tanısı olan hastada ilk yapılması gereken tetkiktir (64). MS lezyonlarının yayılımı, eski ve yeni lezyonları saptayarak tedaviye alınan yanıtın izlenmesi için de kullanılır (65). Kraniyal MRG’de genellikle periventriküler, sagittal kesitlerde korpus kallosuma dik, ovoid yapıda, çapı 3 mm’den büyük beyaz cevher lezyonları saptanır. Lezyonlar proton dansitesindeki T2 ağırlıklı görüntülemelerde hiperintens, T1 ağırlıklıda ise hipointens izlenirler. T1 ağırlıklı görüntülemelerdeki hipointens lezyonlar, demiyelinizasyona ek olarak aksonal kaybı gösterir. Kontrast madde tutuluşu olan lezyonlar akut inflamasyonun ve T hücre infiltrasyonu olan bozulmuş KBB’nin patolojik kanıtıdır. Medulla spinalis MRG’sinde sıklıkla servikal ve torakal segmentlerinde yerleşimli, iki vertebra boyundan kısa, daha çok lateral ve posterior kolonunu tutan, belirgin ödem etkisi olmayan simetrik ya da yama tarzında lezyonlar dikkat çeker. Korteksteki lezyonlar ve atrofi MS’de kognitif fonksiyonların bozulmasının öncül belirteci olarak düşünülmektedir. MS’de derin gri maddede atrofi kognitif gerileme ile ilişkilendirilir (66,67). MS’te beyin atrofisinin erken dönemde gelişmesi 5 yıl içinde kognitif fonksiyonlarda kaybın ortaya çıkacağının göstergesidir (68).
15 2.1.7.1.2. Beyin Omurilik Sıvısı İncelemeleri
MS tanısında BOS’ta oligoklonal band (OKB) saptanması ve IgG indeks yüksekliği önemli bir parametredir. BOS OKB pozitifliğinin 2017 McDonald kriterlerinde ikinci klinik atak ya da MRG de ortaya çıkacak yeni bulgu yerine zamanda yayılımı destekler olarak kullanılabileceği belirtilmiştir. OKB pozitifliği ve IgG indeksi intratekal IgG sentezini gösterir (63).
MS için intratekal IgG sentezi karakteristiktir fakat MS’e özgül değildir. IgG indeksi, BOS ve serum IgG düzeylerinin oranının, BOS ve serumdaki albumin düzeyi oranına bölünmesi ile elde edilir. Üst sınırı konusunda hala tartışmalı değerler olsa da genellikle 0.70 üstündeki değerler artmış oranı göstermektedir. OKB, MS’in başlangıcında negatif bulunabilir, ilerleyen dönemlerde pozitifleşebilir ve sonra bir daha kaybolmazlar (63).
OKB’lerin incelenmesinde kabul gören ve önerilen yöntem, BOS ve serumda izoelektrik fokuslamadır. OKB’nin BOS’ta pozitif, serumda negatif olması ya da BOS’da serumdan daha fazla bant gözlenmesi MSS’de immünolojik aktivasyonun olduğunu gösterir. Klinik kesin MS olgularının izoelektrik fokuslama ile %90’nından fazlasında OKB pozitifliği gözlenmektedir (63).
MS tanısına BOS’un rutin tetkiklerinin katkısı yoktur. Fakat diğer hastalıkların ayrıcı tanısında önemlidir. Bundan dolayı mutlaka yapılmalıdır. MS’li hastalarda BOS görünüm olarak berraktır. BOS basıncı, Cl ve şeker düzeyi normaldir. BOS’da hücre sayısı 0-20/mm3 ’dür ve genellikle lenfosittir. 50 /mm3 üzerinde hücre gözlendiğinde diğer hastalıklar için tekrar değerlendirilmelidir (63).
2.2. Nörotrofinler
Nöronların hayatta kalmasını, büyümesini, sayılarının artmasını ve sinapsların stabilizasyonunu sağlayan polipeptid yapılı büyüme faktör ailesidir (69). Etkilerini tirozin kinaz reseptör (Trk) ve p75NTR (p75 nörotrofin reseptörü) ile gösterirler.
MSS başta olmak üzere periferik sinir sistemi nöronlarında, periferik dokularda birçok hücre tipinden sentezlenmektedir. NT sentezindeki eksikliğin ya da bozukluğun nörodejeneratif hastalıkların ortaya çıkma ihtimalini artırabileceğine dair görüşler vardır. Nörotrofinlerin, nörodejeneratif bozuklukların ve sinir hasarının tedavisinde terapötik ajan olarak kullanım alanı bulunmuştur (7).
16 2.2.1. Sinir Büyüme Faktörü (NGF)
NGF, Levi-Montalcini ve Hamburger tarafından 1950’li yılların başında nörotrofin ailesinin ilk tanımlanan üyesidir (70). Sinir dokusunun gelişiminde, hayatta kalmasında ve onarımında merkezi bir rol oynadığı düşünülen hücre kaynaklı bir nörotrofik faktördür (71). NGF’nin beyin dokusunun dışında periferal dokularda da eksprese edildiği bildirilmiştir (72,73).
2.2.1.1. Sentezlendiği hücreler
NGF’nin büyük kısmı MSS’de nöron ve astroglialarda üretilmektedir (74–76). Periferal sinirlerin gelişimi ve rejenerasyonunda Schwann hücreleri NGF ve p75 reseptörü açısından zengin bir kaynaktır (77). İntrauterin 15-16. haftada neokortekste, 23-28. haftalarında hipokampusta NGF ekspresyonu olduğu bildirilmiştir (78). Bunların dışında mast hücreleri, lenfositler, yağ doku hücreleri, pankreatik β hücreleri, kıl folikülleri, düz kas hücreleri, fibrob-lastlarda da sentezlendiği gösterilmiştir (79).
2.2.1.2. Etki mekanizması
NGF etkisini hücre yüzey reseptörlerine bağlanarak gösterir. Bu reseptörler TrkA ve p75NTR’dir (80,81). NGF reseptöre bağlanır ve hücre içi sinyal yolaklarını aktive eder. NGF’nin TrkA ve p75NTR bağlanması ile etkinleşen başlıca hücre içi sinyal yolakları; hücre dışı sinyal-ilişkili kinaz, fosfolipaz C gamma, mitojen-aktiveli protein kinaz (MAPK) ve fosfotidil inozitol 3-kinaz’dır (82,83). TrkA reseptörü, hücrelerin hayatta kalması ve farklılaşması için gerekli olan fosforilasyon kaskadını aktive eder. NGF’nin sadece p75NTR’ye bağlanması ile nüklear faktör-κB yolağı aktifleşir (7,81). Bu yolaklar aracılığıyla hücre yaşam döngüleri ve farklılaşmaları meydana gelir.
17 2.2.1.3. Fonksiyonu
MSS’de bazal ön beyin kolinerjik nöronların bütünlüğünü sağlamak, periferik ganglionlardan nöritlerin büyümesini desteklemek, nöritlerin büyüme hızını ve doğrultusunu düzenlemek ve ganglion hücrelerinin canlılıklarının devamını sağlamaktır (84). Periferik sinir sisteminde sempatik ve duyusal liflerin hayatta kalmasında ve gelişiminde rol alır. NGF periferik dokuda aksonların yenilenmesini destekler (70,85). Sinir sisteminin dışında da NGF’nin biyolojik etkileri vardır. İmmun yanıtlara TrkA reseptörü ile aracılık ettiği ve inflamatuar reaksiyonlarda yer aldığı gösterilmiştir (86,87).
2.2.2. Nörotrofin-3 (NT-3)
NT ailesinin üçüncü üyesidir. NT-3 ‘ün mRNA ekspresyonu, ilk fare hipokampusunda gösterilmiştir (88).
2.2.2.1. Sentezlendiği hücreler
NT-3’ün MSS hücreleri, akciğer, karaciğer, kalp, timus, böbrek, dalak, deride, bağırsak ve iskelet kasında sentezlendiği gösterilmiştir. NT-3 MSS’de korteks, serebellum ve hipokampusta sentezlenir (89).
2.2.2.2. Etki mekanizması
NT-3 yüksek affinite gösterdiği TrkC reseptörüne bağlanarak etkisini ortaya çıkarır. Periferik ve santral sinir sistemindeki nöronların farklılaşmasında ve hayatta kalmasında rol alır (90,91). NT-3 oligodendrositlerde MAPK’ın fosfosforile olmasını sağlar (92).
2.2.2.3. Fonksiyonu
En önemli fonksiyonu, nöral sağ kalımı sağlamaktır (93–95). Embriyonik dönemin erken safhalarında sempatik nöronların sağ kalımında etkisi olduğu bildirilmiştir (90,96). NT-3, oligodendrosit prekürsör hücrelerin proliferasyonunu uyarır. Oligodendrositlerin gelişimine diğer nörotrofik faktörlerle birlikte katkıda bulunur (97). NT-3 eksik olan farelerde
18 proprioseptif ve mekanoreseptif duysal nöron alt grupları görülememiştir (98,99). NT-3’ün intestinal hareketlerin kontrolünde rol alan nöronların fonksiyonları için önemli olduğu bildirilmiştir (100).
2.2.3. Nörotrofin ve Egzersiz
Egzersiz, beyin plastisitesini destekleyen, koruyan moleküleri ve hücresel kaskadları harekete geçiren kolay uygulanabilir ve ucuz yöntemdir. Egzersiz ve beyin sağlığı arasındaki ilişkinin altında yatan çeşitli mekanizmalar ile iligili son kanıtlar nörotrofin reseptör sinyal yolağının önemli bir rol oynayabileceğini göstermektedir. Bu yolağın aktivasyonu yeni nöronların ve sinapsların büyümesine ve farklılaşmasına neden olur, aksonal ve dendritik büyümeyi destekler, sinaptik plastisiteyi ve mevcut nöronların hayatta kalmasını sağlar. Öğrenme ve hafızayla ilişkili beyin bölgesi olan hipokampuste plastisite ile ilişkili genlerin ekspresyonunu indükler.
Nörotrofinlerin sağlıklı ve hasta insanlarda egzersize bağlı biyolojilerini araştıran çalışmaların sayısı son yıllarda sayısal olarak artmıştır. Nörotrofinlerin beyin biyolojisine katkısı ve egzersizin de bilişsel işlev üzerindeki etkisi düşünüldüğünde, egzersizin nörotrofin üretimini teşvik etmek için umut verici bir seçenek olarak kabul edilebileceği hipotezini ortaya koymaktadır.
2.3. Egzersiz
Egzersiz, fiziksel uygunluğun bir veya daha fazla bileşenini geliştirmek ve korumak için yapılan planlı, yapılandırılmış ve tekrarlanan bedensel hareketlerden oluşan bir tür fiziksel aktivitedir (101).
Fiziksel uygunluk, bireylerin fiziksel aktivite gerçekleştirme yetenekleriyle ilgili elde ettiği bir özellik olarak tanımlanmaktadır. Çoğu yetişkin için aerobik, direnç, esneklik ve nöromotor egzersiz eğitimi içeren bir egzersiz programı, fiziksel zindeliği ve sağlığı geliştirmek ve sürdürmek için vazgeçilmezdir.
Egzersiz yapan bireylerde kardiyorespiratuar dayanıklılıkta artış, vücut kompozisyonu olarak kas kitlesi lehine değişim, kas kuvvetinde, esnekliğinde ve dayanıklılığında artış meydana gelir. Ayrıca egzersizle kişilerin çeviklik, koordinasyon becerileri, denge, reaksiyon süresi gibi fiziksel uygunluk bileşenlerinde de gelişmeler meydana gelir.
19 1995 yılında, CDC (U.S. Centers for Disease Control and Prevention) ve ACSM (American College of Sports Medicine) “Her ABD'li yetişkin, haftanın çoğu, tercihen her gün 30 dakika veya daha fazla ılımlı fiziksel aktivite yapmalıdır.” tavsiyesini yayınlamıştır (102). Bir kişinin önerilen hedeflere ulaşmasa bile egzersiz yapması özellikle sedanter yaşam tarzını benimseyen kişilerde faydalı olacaktır.
Düzenli egzersiz programı oluşturulurken kişilerin fiziksel yeteneği, fiziksel uygunluğu, sağlık durumu, fiziksel ve sosyal ortamı dikkate alınmalıdır.
2.3.1. Egzersiz Tipleri
2.3.1.1. Aerobik Egzersiz
Vücudun büyük kas gruplarının dinamik ve ritmik olarak kullanıldığı egzersizlerdir. Endurans (dayanıklılık) uzun süre efor gösterebilme ve bunu devam ettirebilme yeteneğine denir. Aerobik sistem dayanıklılığı etkileyen sistemdir. Aerobik egzersizler kardiyorespiratuar sisteme yüklenerek daha fazla çalışmasını ve uzun dönemde de adaptasyonların gelişmesini sağlar. Yürüyüş, koşu, bisiklet, yüzme, dans gibi aktiviteler VO2max’ı artıran aerobik egzersiz türleridir. Aerobik kapasite, kardiyorespiratuar uygunluk, VO2max anlamlı olarak kullanılmaktadır. Aerobik kapasite, kardiyorespiratuar sistem fonksiyonel kapasitesinin ölçümüdür. VO2max (mLO2×kg-1×dk-1) olarak ifade edilir. VO2max bütün vücut ağırlığının
kilogramı başına, mililitre cinsinden dakikada tüketilen oksijen miktarıdır. Aerobik egzersiz programı:
Kişilerin yaşı, soy geçmişi, sigara kullanımı, sedanter hayat tarzı, obezite, hipertansiyon, lipit metabolizma bozukluğu, diyabet gibi kardiyak risk faktörlerinin varlığının belirlenip değerlendirilmesi gerekir. Spor yapmasına engel herhangi bir problemi olmayan kişilere egzersiz programı düzenlenir. Aerobik egzersiz programı FITT (Frequency, Intensity, Time, Type) prensiplerine göre oluşturulur (103).
20 a. Maksimum kalp hızı yüzdesi (%) yöntemi:
Maksimum kalp hızını hesaplamada kullanılan formül; MKH=220-yaş’tır. Bulunan değer, istenen yoğunluk yüzdesinin (%60-90) alt ve üst limitleri ile çarpılarak egzersiz sırasında sürdürülecek “hedef kalp hızı aralığı” bulunur (103).
b. Kalp hızı rezerv yöntemi (Heart Rate Reserve, Karvonen metodu):
Kalp hızı rezervi maksimum kalp atım hızından istirahat kalp atım hızı çıkarılarak hesaplanır. Egzersizin yaptırılmak istendiği fonksiyonel kapasite yüzde değerleri (%50-90 arası) ile kalp hızı rezervi olarak bulunan değer çarpılır. Egzersizde ulaşılmak istenen kalp hızı aralığını ayarlamak için bulunan değerlerle istirahat kalp hızı toplanır. Böylelikle egzersizin sürdürüleceği kalp hızının alt ve üst sınırı belirlenir (103).
Hedef kalp hızı = (Maksimal kalp atım hızı-İstirahat kalp atım hızı) x yoğunluk % + İstirahat kalp atım hızı
c. Algılanan zorluk derecesi:
Kişilerin egzersiz toleransını değerlendirmede Borg Skalası (Rating of Perceived Exertion) kullanılır. Borg skalası (6-20 puan) kişilerin egzersiz esnasında hissettiği yorgunluğu hiçbir şey (6 puan), çok çok hafif (7-8 puan), çok hafif (9-10 puan), hafif (11-12 puan), biraz zor (13-14 puan), zor (15-16 puan), çok zor (17-18 puan), çok çok zor (19 puan), tükenme (20 puan) olarak tanımlamasına dayanır (103).
Kişin biraz zorlandığı (13-14 puan) seviye maksimal kalp atım hızının %60-70’ ine, zorlandığı seviye (15-16 puan) ise %70-80’ine denk gelmektedir (103). Kişinin bu seviyeleri bulup egzersizi bu tempolarda devam ettirmesi aerobik kapasite gelişimini sağlayacaktır.
2- Egzersiz süresinin belirlenmesi:
ACSM orta şiddetteki egzersizlerin (tempolu yürüyüş, yüzme vb.) günde 30-60 dakika (en az 150 dakika/hafta), yüksek şiddetteki egzersizlerin (koşu, bisiklet vb.) ise günde 20-30 dakika (en az 75 dakika/hafta) yapılmasını önermiştir (103).
21 3- Egzersiz sıklığının belirlenmesi:
Egzersiz, şiddetine göre haftada en az üç gün önerilir. Orta şiddette 30-60 dakika beş gün/hafta veya yüksek şiddette 20-30 dakika üç gün/hafta olarak uygulanır (103).
2.3.1.2. Kuvvet Egzersizleri
Serbest ağırlık, ağırlık makinası, direnç lastiği, makara sistemleri ya da vücut ağırlığı gibi dirence karşı kas kuvvetinin ve dayanıklılığının artırılması için yapılan egzersizlerdir.
Kuvvet egzersizi programı oluşturulurken ve program uygulanırken dikkat edilmesi gereken önemli kurallar vardır (103). Bunlar;
-Egzersiz programı: Kişiye özgü olmalıdır.
-Doğru nefes alıp verme: İntratorasik basınçtaki ani değişimlere bağlı kan basıncında ve kan dolaşımında ani artış ve azalmalar meydana gelir. Konsantrik kas kasılması süresince (kaldırma-yükseltme fazı) nefes verilmeli, eksantrik kas kasılması süresince de (indirme-düşürme fazı) nefes alınmalıdır. Efor esnasında asla nefes tutulmamalıdır.
-Kas dengesi: Antagonist ve agonist kas gruplarının kuvvet oranını koruyarak güçlendirme yapılmalıdır.
-Egzersiz hızı: Yumuşak doku ve eklem yaralanmalarına neden olmamak için hareketler sabit bir hızda yavaş ve kontrollü olarak yapılmalıdır.
-Tam eklem hareket açıklığı (EHA): Egzersizler eklem ve yumuşak doku yaralanmalarına yol açmamak ve istenen kas grubunu çalıştırmak için düzgün postürde ve tüm EHA boyunca yapılmalıdır. Setler arasında en az bir dakika dinlenme süresi verilmelidir.
Kuvvet egzersizi programı:
1-Egzersiz sıklığı:
Haftada en az iki kez kuvvet egzersizi yapılmalı ve iki egzersiz arası en az 24-48 saat süre istirahat edilmelidir (103).
22 2-Egzersiz şiddeti ve süresi:
Her hareket için ilgili eklemin tam hareket açıklığı boyunca, yalnız bir kez direnç uygulayabileceği en yüksek ağırlık olarak tanımlanan bir maksimum tekrar (1 MT) belli periyotlarla değerlendirilmelidir. Bu sayede kişinin her sette 12-15 tekrar yapabileceği uygun direnç (1 MT’nin %60-80’i) belirlenebilir (103).
3-Tekrar/set:
Program 8-10 büyük kas grubunu içeren, her bir hareket için 12-15 tekrarlı, 2-3 set olacak şekilde yapılır (103).
4- Egzersiz eğitiminin ilerlemesi ve idamesi:
Kuvvet kazanımı için kademeli artan yüklenme prensibi geçerlidir. Kas kuvvetinde artış oldukça set sayısı veya direnç artırılmalıdır (103).
23 2.3.2. MS, Yorgunluk ve Egzersiz
Yorgunluk, MS hastaları arasında, depresyon veya engellilikten bağımsız olarak, yaşam kalitesinin bozulmasının ana nedenlerinden biri olarak kabul edilir. MS hastalarının en az %75' inin hastalık seyrinin bir noktasında rapor ettiği semptomlar arasındadır (104). MS’te yorgunluğun oluşmasına yol açan primer nedenler MSS hasarı, proinflamatuar sitokinlerin artışı ve nöroendokrinolojik sistemin etkilenmesidir. Sekonder nedenler ise psikolojik sorunlar, kognitif bozulma, uyku bozuklukları, iyatrojenik durumlar, vücut ısısı artışı, kondisyon eksikliği ve periferik nedenleri içermektedir. Ayrıca MS'te yorgunluk hastalık yükünün birikmesinden dolayı da ortaya çıkabilir. MS'te yorgunluğun tedavisi ilk olarak MS ile ilişkili olmayan nedenlerin, örneğin anemi, hipotiroidizm veya obstrüktif uyku apnesi gibi uyku bozukluklarının dışlanmasını içerir. Bunun dışında hastalık modifiye edici ilaçlardan yorgunluk üzerinde yararlı etkileri olan ilaçlar seçilebilir.
2.3.2.1. Primer Nedenler
2.3.2.1.1. Merkezi sinir sistemi hasarı
MS için yapısal ve fonksiyonel nörogörüntüleme kullanılarak yorgunluğun nedenini araştırmak için birçok çalışma yapılmıştır. MSS'nin belirli alanlarındaki hasarlar MS'teki yorgunluğun kökeninde rol oynayabilir.
İleri MRG yöntemleri parietotemporal ve frontal bölgelerdeki lezyon yükünün ve kortikal, subkortikal yolakları etkileyen bölgesel atrofinin MS yorgunluğuyla korele olduğunu göstermiştir (105–108).
Proton manyetik rezonans spektroskopisinin (MRS) kullanıldığı bir çalışmada yaygın serebral aksonal yaralanmanın MS yorgunluğu ile ilişkisi ortaya koyulmuştur. MSS hasarı nedeniyle herhangi bir rutin görev sırasında kortikal alanların ve sinir yolaklarının aktivasyonunun artmasına neden olarak algılanan eforun şiddetinde artışa yol açar. Sonuç olarak eforla uyumsuz yorgunluk hissi meydana gelir (109). Bir başka MRS çalışmasında çoklu
beyin bölgelerinde N-asetilaspartat / kreatin (NAA / Cr) oranlarında önemli düşüşler olduğu görülmüştür (109).
Longitudinal bir çalışmada 2 yıllık bir süre zarfında yorgunluk şikayetleri artış gösteren hastalarda sonraki 6 yılda progresif beyin atrofisi gelişmiş ve bunun yorgunlukla ilişkili olduğu görülmüştür (110). Genel olarak, MS'te lezyon yükü, beyin atrofisi ve yorgunluk
24
arasında bir ilişki olduğu görülmektedir, ancak kesin mekanizmalar ve nedensellik açık değildir.
MS yorgunluğunun patogenezinde olası bir diğer faktör, kortikal metabolik aktivitenin azalmasıdır (111). Yorgunluk şiddeti skoru yüksek MS hastalarında yapılan bir çalışmada
F-florodeoksiglukoz pozitron emisyon tomografisi kullanılmış, engellilik derecesi ve depresyondan bağımsız olarak frontal kortekste, beyaz cevherde ve bazal ganglionda glukoz metabolizmasında anlamlı bir azalma gösterilmiştir (112). Bu alanların demiyelinizasyonu nedeniyle azalan enerji metabolizması MS yorgunluğunun kortikal ve subkortikal yolakların bozulması ile ilişkili olabileceği fikrini desteklemektedir (112).
2.3.2.1.2. Sitokin artışı
Serum ve beyin omurilik sıvısındaki proinflamatuar ve antiinflamatuar sitokinlerin seviyesi, sağlıklı kontrollerle karşılaştırıldığında MS hastalarında artmış olarak görülmüştür (113).
MS relapslarında interferon-γ (IFN-γ), tümör nekroz faktörü-α (TNF-α), lenfoksin-α, interlökin 1 (IL-1) ve interlökin 6 (IL-6) gibi proinflamatuar sitokinlerin seviyelerinde bir artış meydana gelir (114). Bu durum algılanan yorgunluk seviyesinde artış ile ilişkilendirilmiştir (115). Ayrıca, interferon-α (IFN-α) ve interferon-β (IFN-β) gibi immünomodülatör ilaçların kullanılması sıklıkla yan etki olarak yorgunluğu indükler. Önceki çalışmalar proinflamatuar sitokinler IFN-γ ve TNF-α (ve TNF-α mRNA ekspresyonu) ile MS yorgunluğu arasında önemli ilişkiler olduğunu göstermiştir (116–118).
Yüksek proinflamatuar (TNF-α, IL-1β ve IL-6) sitokin seviyeleri glutamat klirensini bozduğu ve astrogliyal hücreler üzerinde zararlı etkilere neden olduğu için glutamat nörotransmisyonu üzerine zayıflatıcı etkileri vardır (119). Özetle, MS ile ilişkili yorgunluğun etiyolojisinde sitokinler, inflamasyona bağlı olarak MSS nörofizyolojisinde değişikliklere yol açmaktadır.
2.3.2.1.3. Nöroendokrinolojik sistemin etkilenmesi
Endokrin ve bağışıklık sisteminin etkileşimi nedeniyle, hipotalamus-hipofiz-adrenal (HPA) aksının MS yorgunluğu üzerindeki etkisi de araştırılmıştır (120,121). Artmış proinflamatuar sitokin seviyeleri, HPA aksının aktivitesinin artmasına neden olabilir, böylece kortikotropin salgılatıcı faktör ve kortizol seviyesini artırabilir (115). Uyanmadan önce ve
25
uyandıktan sonra kortizol salgılanmasındaki sapmalar, MS yorgunluğunda rol oynamaktadır, ancak nedensel bir faktör olup olmadığı belirsizdir (122).
Yorgunluğun ayrıca düşük serum dehidroepiandrosteron ve dehidroepiandrosteron sülfat düzeyleri ilişkili olduğu düşünülmüştür (123). Yorgunluk şikayeti olan MS hastalarında deksametazonla baskılanmış kortikotropin salgılatıcı hormon testinde anlamlı derecede yüksek adrenokortikotropin seviyeleri gösterilmiştir (120). MS hastalarında yapılan çalışmalarda çelişkili sonuçlar görülse de bu sonuçlar MS' te yorgunluğa olası bir endokrin katkı olduğunu göstermektedir (123).
2.3.2.2. Sekonder Nedenler
2.3.2.2.1. Psikolojik sorunlar ve Kognitif bozulma
MS yorgunluğunun depresyon, anksiyete, stress ve kognitif bozukluk ile ilişkisinin olduğu görülmüştür. Bu ilişkiler açık olmasada psikolojik faktörler ve yorgunluğun altında yatan ortak patofizyolojik mekanizmalar ile açıklanabilir. Dopaminerjik, histaminerjik ve serotonerjik yolların bozulması ve HPA aksının disfonksiyonu depresyon ve MS yorgunluğunun altında yatan mekanizmalardır (124).
Santral işlem hızı ile MS yorgunluğunun ciddiyeti arasında ters bir ilişki olduğu bulunmuş; primer ve sekonder yorgunluğu olan kişiler arasında kognitif bozulmada fark görülmemiştir (125).
2.3.2.2.2. Periferik nedenler
MS hastalarında tibialis anterior kasında azalmış kas lifi boyutu, daha az Tip I lifler ve
daha fazla Tip II lif olduğu görülmüştür. Fakat yapılan çalışmalar MS yorgunluğunun temelinde merkezi bir sorun olduğunu, miyojenik faktörleri içermediği fikrini desteklemektedirler (124).
2.3.2.2.3. Uyku bozuklukları
MS hastalarında sık görülür ve ağrı, spastisite, anksiyete, depresyon, mesane disfonksiyonu ve ilaçlar gibi birçok faktörden kaynaklanabilir (126). MS hastalarındaki en yaygın uyku bozuklukları insomnia, uyku apnesi, huzursuz bacak sendromu, REM fazı bozukluğu ve narkolepsidir (126). Bu patolojiler genel uyku bozukluğu veya gündüz aşırı uyku
26
haline yol açarak MS yorgunluğuna neden olabilir. Uyku apnesi ile artan oksidatif strese sekonder inflamatuar aktivasyonun gelişmesi nörodejenerasyonu şiddetlendirerek MS ile ilişkili yorgunluğu artırabilir (126).
Yakın zamanda yapılan bir çalışmada belirgin uyku bozukluğu olmayan MS hastalarında, uykunun yorgunluğu giderici fonksiyonunda bir değişiklik olduğu ve bununda MS yorgunluğu ile ilişkili olduğu gösterilmiştir (127).
2.3.2.2.4. İyatrojenik durumlar
MS semptomlarını tedavi etmek için kullanılan birçok ilaç, yorgunluğa neden olma potansiyeline sahiptir. Bunlar arasında birkaç ağrı kesici ilaç (opioidler), antispastisite ajanları (baklofen ve tizanidin), antidepresanlar ve yatıştırıcılar, antihistaminikler, antikonvülsanlar ve beta blokerler bulunmaktadır. MS atağında kullanılan kortikosteroidler, immunmodülatör ve immunsupresif tedaviler de yorgunluğa neden olma veya şiddetlendirme potansiyeline sahiptirler (124).
2.3.2.2.5. Vücut ısısı artışı
MS hastalarının ısıya duyarlı olduğu, ısıya maruz kalma veya egzersiz yoluyla vücut sıcaklığındaki artışla yorgunluğun ortaya çıkabileceği veya artabileceği iyi bilinmektedir (128,129).
MS hastalarında istirahatte vücut sıcaklığının yaş ve cinsiyet uyumlu sağlıklı kontrollere göre daha yüksek olduğunu ve bunun algılanan yorgunlukla ilişkili olduğunu göstermiştir (130).
Vücut sıcaklığındaki küçük bir artış ile merkezi aktivasyonda azalmaya neden olan MSS'deki demiyelinize lezyonlar, merkezi motor iletim süresini yavaşlatırlar ve kortikal uyarılabilirliği bozarlar (129). Bu durum ısıya bağlı mekanizmaların merkezi sinir sistemi düzeyinde etkili olduğunu gösterir.
MS hastalarında vücut soğuması sonrası yorgunlukta azalmanın meydana gelmesi lökositler tarafından üretilen nitrik oksit (NO)’in azalması ile ilişkilendirilmiştir (128). Ayrıca vücudun egzersiz öncesi soğutulmasının, aktivite süresini ve performansı artırdığı da gösterilmiştir (128).