T.C.
EGE ÜNİVERSİTESİ TIP FAKÜLTESİ
GÖĞÜS HASTALIKLARI ANABİLİM DALI
GEÇ DÖNEMDE HASTANEDE GELİŞEN
PNÖMONİ ETKENLERİNİN HIZLI
MOLEKÜLER YÖNTEMLER İLE SAPTANMASI
UZMANLIK TEZİ
Dr. Ahmet UYSAL
TEZ DANIŞMANI
Doç. Dr. Mehmet Sezai TAŞBAKAN
II
Proje ile ilgili yayınımız yoktur.
III
TEŞEKKÜR
Hekimlik mesleğinin öğrenilmesinde ara kademelerden biri olan asistanlık
eğitiminin sonuna gelmiş bulunuyorum.
Göğüs hastalıkları eğitimim süresince bilgi ve tecrübelerini esirgemeyen,
birlikte çalışmaktan onur duyduğum Ege Üniversitesi Göğüs Hastalıkları Anabilim
Dalı Ailesinde yer alan değerli hocalarıma emeklerinden dolayı teşekkür ederim.
Tez çalışması sürecinde gece gündüz yardımlarıyla ve hoşgörüsüyle hep
yanımda olan danışman hocam Doç. Dr. Mehmet Sezai TAŞBAKAN’a,
emeklerinden dolayı Prof. Dr. Feza BACAKOĞLU’na, Prof. Dr. Hüsnü
PULLUKÇU’ya (Enfeksiyon Hastalıkları ve Klinik Mikrobiyoloji A.D.) Prof. Dr.
Şöhret AYDEMİR’e (Klinik Mikrobiyoloji A.D.), Prof. Dr. Timur KÖSE’ye
(Biyoistatistik ve Tıbbi Bilişim A.D.) ve Prof. Dr. Mehmet UYAR’a (Anestezi ve
Reanimasyon A.D.) teşekkürlerimi sunarım.
Asistanlık süresinde tecrübelerinden faydalandığım kıdemlim Uzm. Dr.
Tarık ŞİMŞEK’e ve birlikte çalışmaktan zevk aldığım klinik arkadaşlarım Dr. Dilek
ERASLAN’a, Dr. İmren NESİL’e ve Dr. T. Asena ARISOY AYDIN’a teşekkür
ederim.
Doğumumdan itibaren maddi ve manevi desteğini esirgemeyen aileme; her
zaman yanımda olan sevgili eşime, iş hayatımdaki yorgunluğumu unutturan oğluma
ve kızıma teşekkür ederim. Sizleri seviyorum, iyi ki varsınız.
Ege Üniversitesi Rektörlüğü Bilimsel Araştırma Projeleri Komisyonuna ve
Ege Üniversitesi Tıp Fakültesi Bilimsel Araştırma Projeleri Alt komisyonuna
projemize verdikleri destek nedeniyle teşekkür ederim.
Ahmet UYSAL
İzmir - 2017
IV
İÇİNDEKİLER
TEŞEKKÜR ... III
ÖZET ... VI
ABSTRACT ... VIII
KISALTMALAR ... X
ŞEKİLLER LİSTESİ ... XI
TABLOLAR LİSTESİ ... XI
1
GİRİŞ ve AMAÇ ... 1
2
GENEL BİLGİLER ... 2
2.1 TANIMLAR ... 2 2.1.1 Pnömoni ... 22.1.2 Toplumda Gelişen Pnömoni ... 2
2.1.3 Hastanede Gelişen Pnömoni ... 2
2.1.4 Ventilatör İlişkili Pnömoni ... 3
2.1.5 Sağlık Bakımı İlişkili Pnömoni... 3
2.1.6 Aspirasyon Pnömonisi ... 3
2.2 HGP Epidemiyolojisi ... 4
2.3 HGP Patogenezi ... 4
2.4 HGP Etiyolojisi ... 5
2.5 HGP Risk Faktörleri ... 7
2.5.1 HGP Gelişimine Yol Açan Risk Faktörleri ... 7
2.5.2 HGP’de Mortaliteyi Artıran Risk Faktörleri ... 9
2.6 HGP Prognozu ... 9
2.7 Klinik Yaklaşım ve Tanı Yöntemleri... 10
2.8 Tedavi ... 13
2.9 Korunma ... 17
2.9.1 HGP/VİP Riskinin Olduğu Süreyi Kısaltmak ... 17
2.9.2 Endotrakeal Tüp Kolonizasyonu ve Kontamine Mikroaspirastları Azaltmak 18 2.9.3 Kolonizasyonun Önlenmesi ... 19
3
GEREÇ ve YÖNTEM ... 20
3.1 Hastalar ... 20
3.2 Çalışmaya Alınma Ölçütleri ... 20
3.3 Gönüllüleri Dışlama Kriterleri ... 20
V 4.1 Mikrobiyolojik İnceleme ... 21
5
BULGULAR ... 24
6
TARTIŞMA ... 33
7
KAYNAKLAR ... 38
8
EKLER ... 43
EK1: Bilgilendirilmiş gönüllü onam formu ... 43
VI
ÖZET
Giriş ve Amaç: Hastaneye yatışı takip eden 5. günden sonra ortaya çıkan
geç dönemde hastanede gelişen pnömonilere (HGP) genellikle çok ilaca dirençli
bakteriler neden olmaktadır. Etkenlerin geç saptanması, uygun antibiyotiğin
zamanında başlanamaması HGP prognozunu olumsuz olarak etkilemektedir. Son
yıllarda enfeksiyon etkeni mikroorganizmaların hızlı moleküler yöntemlerle kısa
sürede izole edilmesi, tedavinin daha erken ve etkin olarak başlanmasını
sağlamaktadır. Bu durumun prognozu olumlu yönde etkileyeceği düşünülmektedir.
Bu çalışmada, HGP’de etkenlerin hızlı moleküler yöntemlerle saptanması ve
sonuçların konvansiyonel yöntemlerle karşılaştırılması amaçlanmıştır.
Gereç-Yöntem: Ocak 2014 ile Ocak 2016 tarihleri arasında Ege Üniversitesi
Tıp Fakültesi Göğüs Hastalıkları ile Anestezi ve Reanimasyon yoğun bakım
ünitelerinde izlenen ve 2005 yılında yayınlanan ATS-IDSA kriterlerine göre HGP
tanısı alan 62 hasta çalışmaya alınmıştır. HGP tanısı konulduğu anda hastalardan
bronkoskopik (BAL, BASP) ve nonbronkoskopik (mini-BAL) yöntemlerle alt
solunum yolu örnekleri alınmıştır. Alınan örnekler hem konvansiyonel yöntemler ve
hem de hızlı moleküler yöntemlerle bakteriyolojik etkenler açısından incelenmiştir.
Bulgular: Hasanede gelişen pnömoni tanısı alan 62 hasta (42 erkek, yaş
ortalaması 69.7±15.6) alınmıştır. Hastaların %95.2'sinde ek hastalık olup, 33
hastaya invaziv mekanik vetilasyon (İMV), 28 hastaya İMV + noninvaziv mekanik
ventilasyon (NİV) uygulanmıştır. Hastanede gelişen pnömoni tanısı anında 59
hastanın 39'inin akciğer grafisinde tek taraflı infiltrasyon, 20'sinde çift taraflı
infiltrasyon saptanmıştır. Üç hastanın akciğer grafisinde ise tek taraflı infiltrasyon
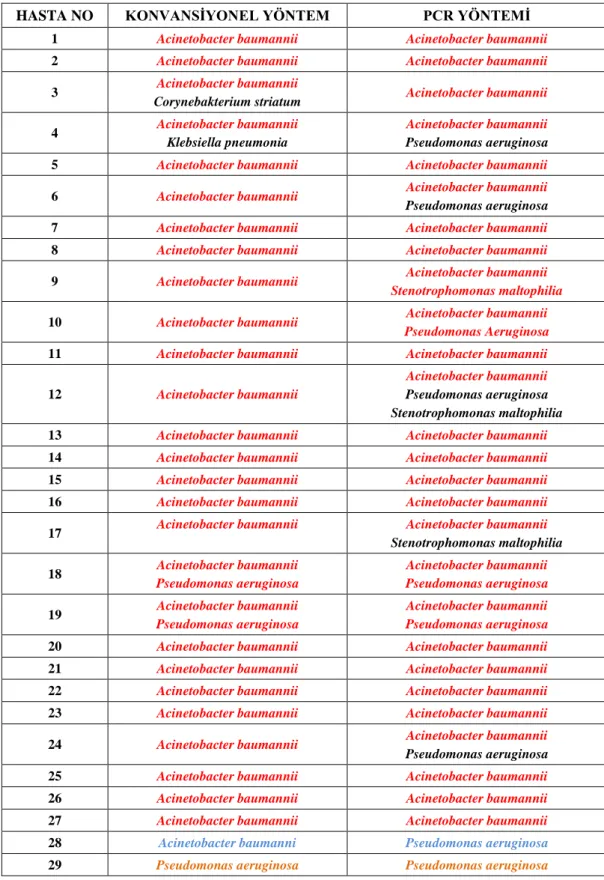
yanısıra plevral efüzyon uyumlu dansite artışı izlenmiştir. Konvansiyonel yöntem
ile 62 hastanın 40’ında (%64.5) bakteriyel etken saptanırken, polimeraz zincir
reaksiyon (PCR) ile 62 hastanın 57’sinde (%91.9) bakteriyel etken izole edilmiştir.
Etken saptanması açısından konvansiyonel yöntem ile PCR yönteminin birbiriyle
uyumlu olduğu gözlenmiştir (kappa:0.797). Ayrıca, PCR ile etken saptanma
oranının anlamlı olarak yüksek olduğu görülmüştür (p=0.0004). Her iki yöntem ile
en sık Acinetobacter baumannii saptanmıştır. İzlemde 62 hastanın 45’inde (% 72.6)
mortalite izlenmiştir.
VII
Sonuç: Geç dönemde ortaya çıkan HGP etkenlerinin saptanmasında
konvansiyonel yöntemler ile PCR arasında uyumun iyi olduğu ve PCR ile daha
fazla hastada etken saptanabileceği bu çalışmada gösterilmiştir. Bakteriyel
etkenlerin hızlı moleküler yöntemlerle saptanmaya başlanmasının, hastanede gelişen
pnömoni etkenlerinin hızla belirlenmesi sonucu, etkin bir şekilde tedavi edilmesinin
yolunu açabileceği düşünülmüştür.
Anahtar Kelimeler: Hastanede gelişen pnömoni, bakteriyel etkenler, hızlı
moleküler yöntemler
VIII
ABSTRACT
Introduction and Purpose: Patients with late-onset hospital-acquired
pneumonia pneumonia (HAP) that develop after the fifth day following admission
to the hospital are usually caused by multi-drug resistant bacteria. Late detection of
the pathogens and inability to start appropriate antibiotic on time have negative
effect on HAP prognosis. The isolation of infectious microorganisms in a short term
by fast molecular methods in the last years ensure that treatment can be started
earlier and more effectively and this situation is thought to affect prognosis
positively. In this study, it was aimed to determine the factors in HAP with rapid
molecular methods and to compare the results with conventional methods.
Material-Method: Total 62 patients, with HAP diagnosis according to the
criteria of ATS/IDSA published in 2005, who were followed-up in the intensive
care units of Anesthesia and Reanimation Department and Chest Disease
Departments of Ege University Faculty of Medicine between January 2014 and
January 2016, were taken into the study. Lower respiratory tract samples were
obtained from patients after HAP diagnosis with bronchoscopic (BAL, BASP) and
non-bronchoscopic (mini-BAL) methods. The samples were examined in terms of
bacteriological agents with conventional methods and fast molecular methods.
Results: 62 patients (42 males, mean age: 69.7 ± 15.6), diagnosed with
hospital-acquired pneumonia, were included. 95.2% of the patients had comorbid
disease. Invasive mechanical ventilation (IMV) was applied to 33 patients and IMV
- non-invasive mechanical ventilation (NIV) was applied to 28 patients. At the time
of hospital-acquired diagnosis; 39 of 59 patients had unilateral infiltration and 20
had bilateral infiltration on chest x-ray. Chest x-ray of three patients showed pleural
effusion and increased density consistent with unilateral infiltration. Bacterial agent
was detected in 40 (64.5%) of 62 patients with conventional method, whereas
bacterial agent was isolated in 57 of 62 patients (91.9%) with polymerase chain
reaction (PCR). It has been observed that the conventional method and the PCR
method are compatible with each other in terms of detecting the agent
(kappa:0.797). Besides, PCR was found to have a significantly higher rate of agent
detection (p=0.0004). Acinetobacter baumannii was detected most frequently with
both methods. In the follow-up, mortality was observed in 45 (72.6%) of 62
patients.
IX
Conclusion: It has been shown in this study that there is a good agreement
between conventional methods and PCR in the detection of late-onset HAP agents
and that agents can be detected by PCR in more patients. Detection of bacterial
agents by rapid molecular methods is thought to lead to the effective treatment of
hospital-acquired pneumonia by rapid identification of the causative agents.
Key Words: Hospital-acquired pneumonia, bacterial agents, rapid molecular
methods
X
KISALTMALAR
APACHE II : Acute Physiological and Chronic Health Evaluation II
ARDS
: Acute Respiratuvary Distress Syndrome
ATS/IDSA
: American Thoracic Society/Infectious Diseases Society of
America
BAL
: Bronkoalveoler Lavaj
BASP
: Bronkoskopik Aspirasyon
CDC
: Centers for Disease Control
CFU
: Colony-forming units
CPIS
: Clinical Pulmonary Infection Score
CRP
: C-Reaktif Protein
ÇİD
: Çok İlaca Dirençli
DM
: Diyabetes Mellitus
HGP
: Hastanede Gelişen Pnömoni
HT
: Hipertansiyon
İMV
: İnvaziv Mekanik Ventilasyon
KOAH
: Kronik Obstruktif Akciğer Hastalığı
Konv.
: Konvansiyonel
MODS
: Multiple Organ Disease Syndrome
MRSA
:
Methicillin-resistant Staphylococcus aureus
MSSA
: Methicillin-sensitive Staphylococcus aureus
NİV
: Noninvaziv Mekanik Ventilasyon
OUAS
: Obstruktif Uyku Apne Sendromu
PCR
: Polymerase Chain Reaction
PCT
: Procalcitonin
PTE
: Pulmoner Tromboemboli
ssp
: Species plural (türleri anlamına gelir)
SAPS
: Simplified Acute Physiology Score
VİO
: Ventilatör İlişkili Olay
VİP
: Ventilatör İlişkili Pnömoni
XI
ŞEKİLLER LİSTESİ
Şekil 1: Konvansiyonel yöntem ve PCR ile etkenlerin saptanma oranları ... 26
Şekil 2: Konvansiyonel yöntemler ve PCR ile saptanan mikroorganizmalara göre mortalite oranları ... 32
TABLOLAR LİSTESİ
Tablo 1: Hastanede gelişen pnömoni etkenleri ... 6Tablo 2: Klinik pulmoner enfeksiyon skoru (CPIS) ... 11
Tablo 3: Ventilatörle İlişkili Pnömoni Tanı Algoritması ... 12
Tablo 4: Ventilatör ilişkili pnömonide çok ilaca dirençli etken risk faktörleri ... 15
Tablo 5: ATS/IDSA 2016 yılı rehberinde çok ilaca dirençli patojenler için risk faktörleri ... 16
Tablo 6: Ampirik ventilatör ilişkili pnömoni tedavisi için güncel kılavuzlar ... 16
Tablo 7: Ventilatör ilişkili pnömonide metisilin dirençli S. aureus ve ikili antipsödomonal/gram(-) etkili tedavinin uygun olduğu ünitelerdeki ampirik tedavi seçenekleri* ... 17
Tablo 8: Hastaların başvuru anındaki demografik özellikleri, yatış tanıları, ek hastalıkları ve laboratuvar bulguları ... 24
Tablo 9: Hastanede gelişen pnömoni tanı anında enfeksiyon belirteçleri ve radyolojik bulguları ... 25
Tablo 10:Konvansiyonel ve PCR yöntemleri ile saptanan etkenler ... 28
Tablo 11: Hastalarda hastanede yattığı sürede kullanılan antibiyotikler ... 30
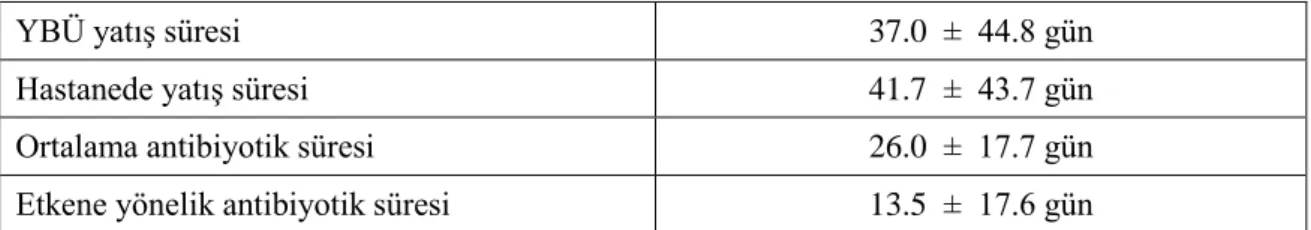
Tablo 12: Hastanede ve YBÜ'nde ve hastanede yatış süresi, antibiyotik süresi ... 30
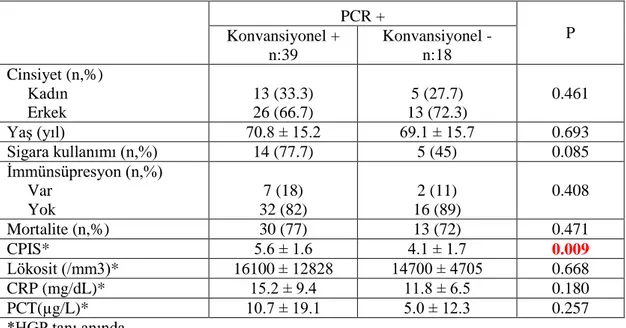
Tablo 13: PCR ile etken saptanıp konvansiyonel yöntemlerle etken saptanan ve saptanmayan hastaların karşılaştırılması ... 31
Tablo 14: Klinik özelliklerin ve örnek alındığı günkü laboratuvar bulgularının mortalite ile ilişkisi ... 31
1
1
GİRİŞ ve AMAÇ
Yeni tanı yöntemlerine, geniş spektrumlu antibiyotiklere, destekleyici tedavilere
ve koruyucu önlemlere rağmen hastanede gelişen pnömoni (HGP)’ler günümüzde hala
önemli bir sağlık sorunudur. Ülkemizde HGP’ler hastane enfeksiyonları arasında 2.
veya 3. sırayı almaktadır. Yapılan çalışmalarda, dünyada hastane enfeksiyonları
içindeki HGP oranı %15 düzeyinde bildirilmiştir. Ülkemizdeki verilere bakıldığında ise,
HGP’nin tüm hastanede gelişen enfeksiyonlar arasında % 11-30 oranında (ortalama
%19) olduğunu gösterilmiştir (1,2). Hastanın hastanede bulunduğu kliniğe göre de HGP
sıklığı değişebilmektedir. Yoğun bakım birimlerinde tedavi edilen hastalarda HGP
görülme sıklığı 5-10 kat fazla olup, ülkemizde yapılan bir çalışmada bu sıklığın 20 kata
ulaştığı gösterilmiştir (3). HGP, hastanede gelişen enfeksiyonlar arasında en sık
mortalite nedenini oluşturmaktadır. Ülkemizde HGP saptanan olgularda mortalite oranı
%30-87 arasında değişmektedir (4-6). Pnömoniye bağlı mortalite oranları; bakteriyemi
gelişen hastalarda, Acinetobacter spp., Pseudomonas aeruginosa gibi çoklu ilaç direnci
olan bakterilerle oluşan pnömonilerde, yaşlı hastalarda (>60 yaş), uygunsuz antibiyotik
kullananlarda ve ventilatör ilişkili pnömoni (VİP)’lerde daha fazladır (7-11). Tanı
zorlukları, gereksiz ve uzun süre antibiyotik kullanımı, antibiyotiklere dirençli yeni
bakteriyel enfeksiyon gelişme riski ve ilaç toksisiteleri, HGP’de tedavi maliyetinde
artışa neden olmaktadır (12,13). Etkenlerin geç saptanması, uygun antibiyotiğin
zamanında başlanamaması HGP prognozunu olumsuz olarak etkilemektedir. Son
yıllarda enfeksiyon etkeni olan mikroorganizmaların, hızlı moleküler yöntemlerle kısa
sürede izole edilmesi, tedavinin daha erken ve etkin olarak başlanmasını sağlamaktadır.
HGP etkenlerinin hızlı saptanması ve tedavinin bir an önce başlanmasının prognozu
olumlu yönde etkileyeceği düşünülmektedir.
Bu çalışmada, HGP etkeni olan mikroorganizmaların hızlı moleküler yöntemlerle
araştırılması ve bu sonuçlar ile konvansiyonel kültür sonuçlarının karşılaştırılması
amaçlanmıştır.
2
2
GENEL BİLGİLER
2.1 TANIMLAR
2.1.1 Pnömoni
Terminal bronşiyollerin distalindeki akciğer parankiminin enfeksiyonudur.
2.1.2 Toplumda Gelişen Pnömoni
Toplumda günlük yaşam sırasında ortaya çıkan, akciğer parankiminin akut
enfeksiyonudur.
2.1.2.1 Tipik Pnömoni
Ani başlayan, üşüme titreme ile 39-40˚C'ye yükselen ateş yüksekliği, öksürük,
pürülan balgam çıkarma, plöretik tipte yan ağrısı gibi semptomlarla genellikle akut ve
gürültülü bir şekilde başlayan, radyolojik olarak sıklıkla lober konsolidasyon gözlenen,
oskültasyonda inspiryum sonu raller ve/veya bronşiyal ses duyulan, laboratuvar
bulgularında ise lökositozla karakterize bakteriyel pnömonidir.
2.1.2.2 Atipik Pnömoni
Başlangıcı gürültülü olmayan, prodromal dönemin ardından kliniğin
belirginleştiği, daha çok gençlerde ortaya çıkan pnömonidir.
2.1.3 Hastanede Gelişen Pnömoni
Hastaneye yatıştan sonra 48 saat sonra gelişen ve hastanın yatışında enkübasyon
döneminde olmadığı bilinen pnömoni olguları ile, hastaneden taburcu olduktan sonraki
48 saat içinde ortaya çıkan pnömoni olarak tanımlanır (14).
3
2.1.3.1 Erken Dönemde Hastanede Gelişen Pnömoni
Hastaneye yatıştan sonra ilk 4 gün içinde gelişen pnömonidir. Temel etkenler
Streptococcus pneumoniae,
Haemophilus
influenzae
ve
metisiline
duyarlı
Staphylococcus aureus’tur (14).
2.1.3.2 Geç Dönemde Hastanede Gelişen Pnömoni
Hastaneye yatıştan sonra 5. ve daha sonraki günlerde gelişen pnömonidir. Geç
dönemde HGP’lerde, Pseudomonas aeruginosa, Acinetobacter spp., Enterobacter spp.,
Klebsiella spp. gibi Gram negatif etkenler yer alırken, Gram pozitif koklar da etken
olarak saptanmaktadır (14).
2.1.4 Ventilatör İlişkili Pnömoni
Entübasyon esnasında olmayan, invaziv mekanik ventilatör desteğindeki hastada
entübasyondan 48 saat sonra gelişen pnömonidir (14).
2.1.5 Sağlık Bakımı İlişkili Pnömoni
Aşağıdaki özelliklerden birine sahip kişilerde gelişen pnömonidir (14).
Son 90 gün içinde iki gün veya daha uzun hastanede yatmak
Sağlık bakımı için uzun süreli bakım evinde kalmak
Evde infüzyon tedavisi almak
Evde bası yarası bakımı yapılması
Son 30 gün içerisinde hemodiyaliz merkezine tedavi amaçlı devam etmek
Aile bireylerinde çok ilaca dirençli bakteri enfeksiyonu varlığı
2.1.6 Aspirasyon Pnömonisi
Solunum yolunun savunma mekanizmasının çeşitli nedenlerle etkisiz kalması
halinde ağız içi sekresyonların, mide asit içeriğinin ve besinlerin alt solunum yollarına
aspire edilmesi ile ortaya çıkan pnömonidir (15).
4
2.2 HGP Epidemiyolojisi
HGP'ler, genellikle bakteriyel kaynaklıdır. ABD'de ikinci en sık görülen hastane
enfeksiyonu olup; yüksek mortalite ve morbidite ile ilişkilidir (7). Ülkemizde de hastane
enfeksiyonları arasında sıklık açısından 2. veya 3. sırayı almaktadır (14). Hastaneye
yatan hastalar arasında %0.5-2 oranında görülmektedir. Dünyada hastane
enfeksiyonları içindeki HGP oranı %15 düzeyinde bildirilirken, ülkemizdeki veriler %
11-30 arasında (ortalama %19) olduğunu göstermektedir (1,2). Türkiye'de yapılan geniş
kapsamlı (43 farklı merkez, 133 yoğun bakım ünitesi, 1030 hasta) bir nokta prevalans
çalışmasında yoğun bakım ünitesinde (YBÜ) kazanılmış enfeksiyon prevalansı %21
olarak belirlenmiş ve en sık görülen enfeksiyon olarak HGP (%45.5) olduğu
görülmüştür (16). Tüm YBÜ’nde kullanılan antibiyotiklerin %50'den fazlasını HGP’ye
yönelik tedaviler oluşturmaktadır (13).
HGP, hastanede gelişen enfeksiyonlar arasında en sık mortalite nedenidir (16).
Çevik ve arkadaşlarının yaptığı bir çalışmada pnömoni gelişmesinin YBÜ hastalarında
mortaliteyi 3 kat artırdığı gösterilmiştir (17).
HGP tanısını koymak ve neden olan etkeni saptamak her zaman mümkün değildir.
Tanı zorlukları, gereksiz ve uzun süre antibiyotik kullanımı, antibiyotiklere dirençli
bakteri enfeksiyonu gelişme riski ve toksisite tedavi maliyetinde artışa neden olmaktadır
(12,13).
2.3 HGP Patogenezi
Alt solunum yolu enfeksiyonunun gelişebilmesi için konakçı savunmasının
bozulması ile birlikte yeterli miktarda virülan mikroorganizmanın alt solunum yollarına
ulaşması gerekmektedir. HGP’de ise; genellikle hastaneye yatışın ilk 48 saatinde,
hastanın normal üst solunum yolları florasının hastanedeki dirençli mikroorganizmalar
ile yer değiştirmesi ve bu mikroorganizmaların alt solunum yollarına aspirasyonu söz
konusudur.
HGP oluşumunda mikroorganizmalar alt solunum yollarına başlıca üç yoldan
ulaşmaktadır (14):
5
1. Orofarinkste kolonize mikroorganizmaların aspirasyonu
2. İnhalasyon yolu
3. Hematojen yol
Hastanın bilinç düzeyindeki olumsuz değişiklikler, solunum sistemine
uygulanan invaziv girişimler, mekanik ventilasyon uygulaması, gastrointestinal sistemin
invaziv girişimleri ve cerrahi girişimler bu süreci kolaylaştırmaktadır. Ayrıca bakıma
muhtaç hastalarda ve yoğun bakım hastalarında hastanın kendisi veya sağlık personeli
aracılığıyla rekto-pulmoner kontaminasyon, kolonizasyon ve sonuçta HGP olma
olasılığı vardır.
Kontamine solunum cihazlarından, entübasyon tüplerinden ve nebulizasyon
cihazlarından kaynaklanan 5 μm’den küçük ve mikroorganizmalar içeren partiküllerin
inhalasyon yolu ile alt solunum yollarına ulaşması sonucu da HGP gelişebilmektedir.
Hematojen yolla HGP oluşması nadirdir. Buna karşın, flebit, endokardit gibi
başka bir enfeksiyon odağından bakteriyemi ile etkenler alt solunum yollarına ulaşıp
HGP oluşturabilmektedir. İmmunsüpresyonda, kanser varlığında ve geniş yanıklarda
gastrointestinal sistemdeki bakterilerin translokasyonu ile bakteriyemi sonucunda HGP
gelişimine yol açabilir (11).
2.4 HGP Etiyolojisi
HGP etkeni mikroorganizmaların sıklığı; hastane, hasta popülasyonu ve
kullanılan tanısal yönteme göre değişiklik gösterebilmektedir. Etken mikroorganizmalar
çoğunlukla bakteriler olduğu için, pek çok hastanede virüs, anaerop ve fungal patojen
izolasyonuna yönelik kültür yöntemlerinin kullanılmadığı da bir gerçektir.
Erken başlangıçlı pnömonilerde temel etkenler; Streptococcus pneumoniae,
Haemophilus
influenzae ve
metisiline duyarlı Staphylococcus aureus’tur. Bu
mikroorganizmaların etken olmasında hastanın henüz herhangi bir antibiyotik tedavisi
almamış olması ve çok ilaca dirençli mikroorganizmaların kolonizasyonu için yeterli
sure geçmemiş olması etkili olabilir. Gram-pozitif koklar ve H. influenza, pnömoni
gelişme süresinden bağımsız olarak antibiyotik almamış hastalarda gelişen
pnömonilerin 3/4’ünde etken olarak saptanmıştır (18).
6
Geç dönemde gelişen pnömonilerde en sık izole edilen etkenler olarak,
Pseudomonas aeruginosa, Acinetobacter spp., Enterobacter spp., Klebsiella spp. gibi
gram-negatif etkenler ve metisiline dirençli S. aureus (MRSA) tanımlanmaktadır
(7,14,19). Yapılan bazı çalışmalarda HGP’nin polimikrobiyal etkenlere bağlı olarak da
gelişebileceği ve bu oranın VİP olgularında %40-59’a çıkabileceği bildirilmiştir (20,21).
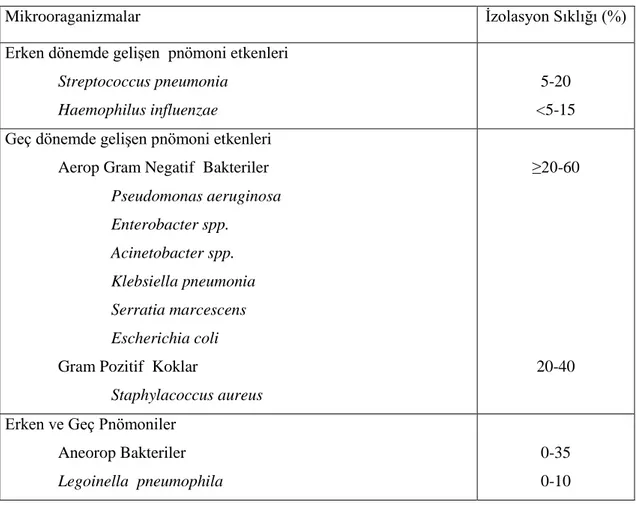
HGP’ye yol açan etkenler tablo 1’de gösterilmiştir (22).
Tablo 1: Hastanede gelişen pnömoni etkenleri
Mikrooraganizmalar İzolasyon Sıklığı (%)
Erken dönemde gelişen pnömoni etkenleri
Streptococcus pneumonia Haemophilus influenzae
5-20 <5-15 Geç dönemde gelişen pnömoni etkenleri
Aerop Gram Negatif Bakteriler
Pseudomonas aeruginosa Enterobacter spp. Acinetobacter spp. Klebsiella pneumonia Serratia marcescens Escherichia coli
Gram Pozitif Koklar
Staphylacoccus aureus
≥20-60
20-40 Erken ve Geç Pnömoniler
Aneorop Bakteriler
Legoinella pneumophila
0-35 0-10
Ülkemizde elde edilen sürveyans verilerine göre yoğun bakım enfeksiyonlarının
yaklaşık %5-10’unda etken olarak S. aureus izole edilmiş ve bu suşların %60-95’ini
metisiline dirençli suşların oluşturduğu saptanmıştır (14). Acinetobacter türleri
ülkemizde yoğun bakım infeksiyonlarında, özellikle VİP’e sebep olan bakterilerdendir
(23).
7
2.5 HGP Risk Faktörleri
HGP’de rol oynayan risk faktörlerini 3 ana grupta ele alabiliriz (14);
1-HGP gelişimine yol açan risk faktörleri
2-HGP’de mortaliteyi artıran risk faktörleri
3-HGP’de çok ilaca dirençli mikroorganizmalarla etken olarak karşılaşılmasında
rol oynayan risk faktörleri
2.5.1 HGP Gelişimine Yol Açan Risk Faktörleri
2.5.1.1 Hastaya Bağlı Risk Faktörleri
a- Konak savunma mekanizmalarının zayıflaması: Koma, malnütrisyon, uzun
süre hastanede kalma, hipotansiyon, metabolik asidoz, sigara, kronik obstrüktif akciğer
hastalığı (KOAH), akut sıkıntılı solunum sendromu (ARDS), hipoalbüminemi, kistik
fibroz, bronşektazi, diyabetes mellitus, alkolizm, solunum yetmezliği, kronik böbrek
yetmezliği/diyaliz uygulaması, nöromüsküler hastalıklar, hava yolu reflekslerinin
azalması, santral sinir sistemi patolojileri, APACHE II >16, travma, kafa travması,
sinüzit, erkek cinsiyet, sonbahar- kış mevsimi, aspirasyon, organ yetersizlik indeksi ≥3
olması.
b- İleri yaş ( >60 yaş)
2.5.1.2 İnfeksiyon Kontrolü İle İlişkili Faktörler
a. Hastane infeksiyonu kontrolüne yönelik genel kurallara uyulmaması
Hastane personelinin elleri ile kontaminasyon
Kontamine solunumsal tedavi araçlarının kullanımı
Entübe hastanın transportu
8
2.5.1.3 Girişimlere Bağlı Faktörler
a-
Medikal tedaviye bağlı risk faktörleri
Sedatifler
Kortikosteroid
Sitostatik ajanlar
Antiasidler ve H
2reseptör blokerleri
Önceden antibiyotik kullanımı
Total parenteral beslenme
b- İnvaziv girişimlere bağlı risk faktörleri
Torako-abdominal cerrahi (uzamış ve komplike girişimler)
Entübasyon
Acil entübasyon, reentübasyon,
Uzamış mekanik ventilasyon,
Trakeostomi
Bronkoskopi
İntrakraniyal basınç monitorizasyonu
Nazogastrik sonda ile enteral beslenme uygulanması ve bu
uygulamaların sırtüstü pozisyonda yapılması
Ventilatör devrelerinin 48 saatten önce değiştirilmesi
Tüp torakostomi
Subglottik sekresyonların aspire edilmemesi,
Endotrakeal balon basıncının gereğinden düşük olması,
Kardiyopulmoner resüsitasyon
2.5.1.4 Etkene Ait Faktörler
Çok ilaca dirençli bakteri
9
2.5.2 HGP’de Mortaliteyi Artıran Risk Faktörleri
HGP’nin uygun olmayan antibiyotikle tedavisi
Önceden antibiyotik kullanımı
Pnömoni gelişmeden önce hastanede yattığı süre veya yoğun bakımda kalma
süresi
Uzamış mekanik ventilasyon
Yüksek riskli patojenlerle infeksiyon P. aeruginosa - Acinetobacter spp
Stenotrophomonas maltophilia, MRSA
Multilober ve/veya bilateral pulmoner infiltratlar
Altta yatan hastalığın ağırlığı; APACHE II, SAPS
Ağır sepsis/septik şok, multiorgan disfonksiyon sendromu (MODS)
İleri yaş (>60)
Solunum yetersizliğinin ağırlaşması (PaO
2/FiO
2<240)
2.6 HGP Prognozu
Ülkemizde HGP saptanan hastalarda mortalite oranı %30-87 arasında
değişmektedir (4,5,6). Yapılan bir çalışmada pnömoni gelişmesinin yoğun bakım
hastalarında mortaliteyi 2 kat artırdığı gösterilmiştir (16).
Yoğun bakım ünitelerinde gelişen VİP, önemli bir morbidite ve mortalite
nedenidir. Son yıllarda yapılan çalışmalarda, YBÜ’nde yatan ve VİP gelişen hastalarda
mortalite oranlarını 1.73 ve 1.94 kat artırdığı saptanmıştır. Ayrıca VİP gelişimin
hastanede kalış süresini ve hastane maliyetlerini arttırdığı gösterilmiştir (25,26).
Son zamanlarda, HGP antimikrobiyal tedavisinde “hedefe yönelik” tedavi
yaklaşımı öne çıkmaktadır. Hedefe yönelik tedavi yaklaşımı infeksiyona yol açan
etkenin saptanmasıyla tedavinin tekrar düzenlenmesini veya etken üretilememesi
durumunda da antimikrobiyal tedavinin kesilmesini kapsamaktadır (27). Bu konuda
yapılan ve 740 VİP hastasının dahil olduğu bir çalışmada; hedefe yönelik tedavi alan
hastalar hedefe yönelik tedavi almayan hastalarla karşılaştırılmıştır. Hedefe yönelik
tedavi alanların sağkalım süresinin daha uzun olduğu, daha kısa süre geniş spektrumlu
antibiyotik tedavisi aldığı, daha az süreli mekanik ventilatör ihtiyacı olduğu
gösterilmiştir. Buna karşın, mortalite oranının her iki grupta da benzer olduğu
görülmüştür (28). Yapılan başka bir çalışmanın çok değişkenli analizinde, tedaviye
10
rağmen, PaO
2/FiO
2oranında ve organ yetmezliği ölçüm skorunda düzelmenin olmaması
mortalite ile ilişkili bulunmuştur (29).
Yüksek mortalite oranları göz önünde bulundurulduğunda, HGP tanısının erken
konması ve etkene yönelik tedavinin kısa sürede başlanması büyük önem taşımaktadır.
2.7 Klinik Yaklaşım ve Tanı Yöntemleri
HGP veya VİP tanısını koymada altın standart bir yöntem yoktur. Tanı
genellikle klinik olarak şüphelenme sonucunda konulmaktadır. Yapılan çalışmalarda
klinik olarak VİP tanısı konulan hastaların %50’sinde VİP bulunmazken, buna karşın
VİP’i olan hastaların yaklaşık olarak 1/3’üne tanı konulamadığı görülmüştür (30).
1972 yılında Johanson ve arkadaşları VİP tanısı için; 38˚C üzerinde ateş
yüksekliği, lökosit değerinin <4000 ya da >12000 /mm
3olması, pürülan sekresyonun
varlığı ve akciğer grafisinde yeni ya da progresif infiltrasyon izlenmesi durumlarından
en az ikisinin olması gerekliliğini vurglamıştır (31).
Son yıllarda, VİP hastalarının daha iyi tanımlanması için yeni klinik kriterler
oluşturulmuştur. 2005 yılında yayınlanan ATS/IDSA rehberine göre entübasyondan 48
saat sonra çekilen akciğer grafisinde yeni ya da ilerleyici infiltrasyon saptanan hastada
aşağıdakilerden iki veya daha fazlası varsa VİP tanısı konulmaktadır.
- >38˚C ateş
- Lökositoz (>12000 hücre/mm
3) ya da lökopeni (<4000 hücre/mm
3)
- Pürülan sekresyon
- Oksijenizasyonda azalma
Yukarıda VİP tanısı için kullanılan bu dört ölçüt birlikte bulunduğu zaman
özgüllük yüksektir; ancak duyarlılık klinik olarak kabul edilemeyecek sınırların
(%50’nin) altına düşebilmektedir. Ayrıca VİP hastalarında enfeksiyon dışı etiyolojiler
söz konusu olabilmekte, bu nedenle de ek tanı yöntemlerine gereksinim duyulmaktadır.
Özellikle VİP düşünülen hastalarda klinik pulmoner enfeksiyon skorunun (CPIS)
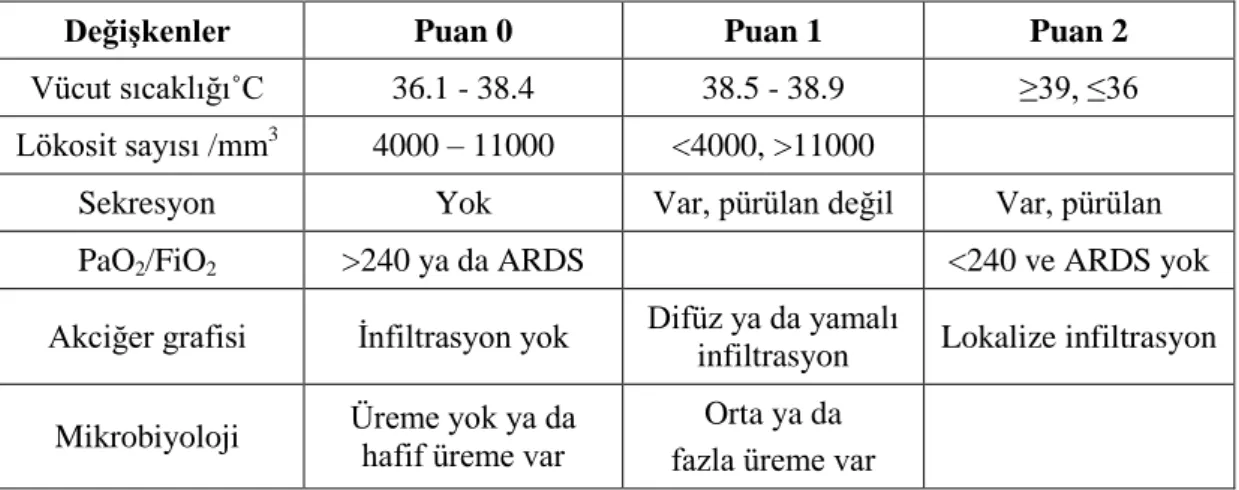
kullanımı da tanı için katkı sağlamaktadır. Klinik pulmoner enfeksiyon skoru tablo 2’de
özetlenmiştir. Otuz üç çalışmanın değerlendirildiği bir metaanalizde CPIS’ın VİP
tanısında orta derecede bir katkısının olduğu saptanmıştır. Bununla birlikte, hasta
11
başında hızlı ve kolay bir şekilde hesaplanabilmesi CPIS’ın bir kullanım avantajı olarak
gösterilmektedir (32). Bu grup hastalarda CPIS’ın 6’nın üzerinde bulunması pnömoni
olasılığını güçlendirmektedir. Ancak CPIS’ın asıl kullanım alanı tedavinin
değerlendirilmesi ve yönlendirilmesi aşamasındadır.
Tablo 2: Klinik pulmoner enfeksiyon skoru (CPIS)
Değişkenler Puan 0 Puan 1 Puan 2
Vücut sıcaklığı˚C 36.1 - 38.4 38.5 - 38.9 ≥39, ≤36 Lökosit sayısı /mm3
4000 – 11000 <4000, >11000
Sekresyon Yok Var, pürülan değil Var, pürülan PaO2/FiO2 >240 ya da ARDS <240 ve ARDS yok Akciğer grafisi İnfiltrasyon yok Difüz ya da yamalı
infiltrasyon Lokalize infiltrasyon Mikrobiyoloji Üreme yok ya da hafif üreme var Orta ya da
fazla üreme var
Son olarak Centers for Disease Control (CDC) tarafından VİP tanı kriterleri
2011 yılında güncellenmiştir. CDC tarafından oluşturulan çalışma grubu, yaklaşık 2
yıllık çalışmanın ardından yeni VİP tanı algoritmasını geliştirmiştir (33). Yeni CDC
VİP tanımları tablo 3’de gösterilmiştir. Yeni geliştirilen bu yaklaşıma göre; mekanik
ventilatöre bağlı hastalarda gelişen pnömoni, ARDS, atelektazi ve pulmoner ödem gibi
önlenebilir komplikasyonların tamamı ventilatör ilişkili olay (VİO) tanımı altında
toplanmıştır. VİP tanısının ortaya konmasında akciğer grafisinin yeterli olmadığına dair
kanıtların artması, radyografi tekniği ile ilgili merkezler arasındaki değişkenlik ve
bulguların değerlendirilmesindeki görecelilik nedeniyle akciğer grafisi VİP tanı
kriterlerinden çıkarılmıştır. Buna karşın tanımlarda oksijenizasyona ayrı bir önem
verilmiş, klinik ve mikrobiyolojik kriterler tekrar ve daha açık olarak tanımlanmıştır.
12
Tablo 3: Ventilatörle İlişkili Pnömoni Tanı Algoritması
Bazal iyilik hali: Ventilatöre bağlı hasta, FiO2 ve PEEP düzeyleri bozulmaya başladığı günden hemen önce en az iki gündür stabil seyrediyor veya minimum günlük FiO2 ve PEEP değerleri açısından düzelme seyri gösteriyor olmalı
Bazal iyilik halinden sonra oksijenlenmenin bozulduğunu gösteren alttaki bulguların en az biri bulunmalı:
1. Günlük minimum FiO2 düzeyinde ≥0.20 (20 puan) artış olması ve bu artışın en az 2 gün devam etmesi
2. Günlük minimum PEEP düzeyinde ≥3 cmH2O artış olması ve bu artışın en az 2 gün devam etmesi
Ventilatörle İlişkili Pnömoni (VİP)
Mekanik ventilasyonun 3. Günü ve daha sonrasında geçerli olmak koşuluyla oksijenlenmenin bozulduğu gün (veya 2 gün içinde) alttaki 2 kriter birlikte karşılanmalı
1. Ateş>380C veya <360C veya lökosit >12000 hücre/mm3 veya <4000 hücre/mm3
2. Yeni bir antimikrobiyal tedavi başlanmış ve en az 4 gün devam edilmiş olması Enfeksiyona Bağlı Ventilatörle İlişkili Komplikasyon
Mekanik ventilasyonun 3. günü ve daha sonrası için geçerli olmak koşuluyla, oksijenlenmenin bozulduğu gün (veya 2 gün içinde) alttaki karşılanmalı:
1. Pürülan sekresyon:
Akciğer, bronşlar veya trakeadan gelen, mikroskobun küçük büyütmesinde ≥25 nötrofil ve <10 epitel hücresi (Ipf x100) içeren alt solunum örneği
Yarı-kantitatif sonuç veren laboratuvar için, yukarıdaki kalite ölçütlerine denk gelen ir sonuç vermiş olmalı
2. Kültür pozitifliği:
Balgam, DTA, BAL veya PSB kalitatif, yarı veya kanitatif kültüründe anlamlı üreme olması. Oral veya solunum yolu flora bakterileri, Kuagulaz Negatif Stafilokolar, Candida türleri veya tiplendirilmemiş mayalar, enterokok türleri izole edildiğinde kültür sonucu anlamlı kabul edilemez. Akciğer doku örneğinin kültüründe ise her üreme anlamlı kabul edilir
Olası Ventilatörle İlişkili Pnömoni
Mekanik ventilasyonun 3. Günü ve daha sonrası için geçerli olması koşuluyla; oksijenlenmenin bozulduğu gün (veya 2 gün içinde) alttaki kriterlerden biri karşılanmalı:
1. Pürülan solunum sekresyonu (olası VİP’te tanımlandığı şekilde) ve alttaki kriterlerden birinin bulunması:
DTA kültürü pozitifliği, ≥ 105
cfu/ml BAL kültürü pozitifliği, ≥ 104
cfu/ml Akciğer dokusu kültürü pozitifliği, ≥ 104
cfu/ml PSB kültürü pozitifliği, ≥103
cfu/ml
2. Alttaki kriterlerden birinin varlığı (Pürülan sekresyon yoksa) Plevral sıvı kültürü pozitifliği
Akciğer dokusunda histopatolojik bulguların varlığı Legionella spp. İçin tanısal testlerde pozitiflik
Solunum sekresyonlarında; İnfluenza virüs, RSV, Adenovirus, Parainfluenza virüs, Human metapnömovirus, Coronovirus pozitifliği
13
Son yıllarda bakteriyel etkenlerin 2-6 saat içinde antibiyotik duyarlılık paternleri
ile birlikte belirlenmesine olanak sağlayan hızlı moleküler yöntemlerin kullanımları
gündeme gelmiştir (36). Ancak, bu moleküler yöntemlerin BAL sıvısında ve trakeal
aspirasyon örneklerinde kullanımı ile igili henüz yeterli kanıt bulunmamaktadır.
Son yıllarda BAL sıvısı ve kanda bazı biyobelirteçlerin tanısal değerileri
araştırılmaktır. C-reaktif proteinin yoğun bakım ünitesinde duyarlılığının düşük olduğu
gösterilmiştir. Copeptin, adrenomedullin ve midregional atrial natriüretik faktör gibi
biyobelirteçlerin de tanısal değerden çok prognostik değeri olduğu saptanmıştır.
Prokalsitoninin ise VİP tanısı alan hastaların antibiyotik tedavi sürelerinin
belirlenmesinde kullanılabileceği ileri sürülmüştür (37).
2.8 Tedavi
Rehberler geç başlangıçlı VİP ya da ÇİD etkenler için risk faktörleri (tablo 4)
olan hastalarda antipsödomonal kombinasyon tedavileri önermektedirler (7).
Yenilenen
2016 yılı ATS/ IDSA rehberinde ÇİD etkenler için risk faktörlerinde bazı değişiklikler
yapılmıştır (Tablo 5). Erken ve uygun ampirik antibiyotik tedavisinin başlanması
VİP’in prognozunu belirleyen en önemli faktörlerden biridir. Ampirik antibiyotik
tedavisi ile olası etken patojenleri en iyi şekilde kapsayacak rehberler oluşturulmuştur
(Tablo 6)
(7,19). Yeni rehberde MRSA riski olan hastalarda vankomisin veya linezolid,
dirençli gram (-) bakteri için risk faktörü varlığında iki anti-pseudomonal antibiyotikle
tedavi önerilmiştir (Tablo 7) (24).
.MRSA ve dirençli gram (-) bakteri riski olmayan
durumlarda monoterapi uygun bulunmuştur. Önerilen tedavi piperasilin/tazobaktam,
sefepim, levofloksasin, imipenem veya meropenemden biridir. Kanıtlanmış MSSA
varlığında tercih edilen ajanlar oksasilin, nafsilin veya sefazolindir, fakat ampirik
tedavide yukarıdaki seçeneklerden biri kullanılmışsa gerek duyulmayacağı belirtilmiştir
(24).
Tedavinin 2-3. günü, ampirik antibiyotik tedavisi hastanın klinik, laboratuvar ve
bakteriyolojik sonuçları ile tekrar değerlendirilmelidir. Solunum örneklerinde etken
patojenler ve duyarlılık paterni belirlenmişse, antibiyotik tedavisi sonuçlara göre tekrar
düzenlenmelidir (7,24).
Uygun tedavi verildiğinde genellikle ilk altı günde klinik parametrelerde anlamlı
düzelme elde edilmektedir. Tedaviye yanıtı değerlendirmede lökosit sayımı, CRP,
Mekanik ventilasyonun 3. Günü ve daha sonrası için geçerli olması koşuluyla; oksijenlenmenin bozulduğu gün (veya 2 gün içinde) alttaki kriterlerden biri karşılanmalı:
1. Pürülan solunum sekresyonu (olası VİP’te tanımlandığı şekilde) ve alttaki kriterlerden birinin bulunması: DTA kültürü pozitifliği, ≥ 105
cfu/ml BAL kültürü pozitifliği, ≥ 104 cfu/ml
Akciğer dokusu kültürü pozitifliği, ≥ 104 cfu/ml PSB kültürü pozitifliği, ≥103 cfu/ml
2. Alttaki kriterlerden birinin varlığı (Pürülan sekresyon yoksa) Plevral sıvı kültürü pozitifliği
Akciğer dokusunda histopatolojik bulguların varlığı Legionella spp. İçin tanısal testlerde pozitiflik
Solunum sekresyonlarında; İnfluenza virüs, RSV, Adenovirus, Parainfluenza virüs, Human metapnömovirus, Coronovirus pozitifliği
14
prokalsitonin, oksijenasyon (PaO
2/FiO
2), akciğer grafisi, ateş, sekresyonların miktarının
ve pürülansının takibi önemlidir. VİP’de optimal tedavi süresi 10-14 gündür (19).
Ancak, ATS /IDSA (American Thoracic Society/Infectious Diseases Society of
America) 2016 yılı rehberinde VİP’li hastalarda 7 günlük tedavi önerisi de yapılmış,
klinik, radyolojik ve laboratuvar bulgularındaki iyileşmeye göre, daha kısa veya uzun
süreli tedavilerin de gerekebileceği belirtilmiştir (24). Ağır pnömonilerde, altta yatan
immünsüpresyon varlığında, klinik yanıtın yetersiz olması durumunda ve etken olan
mikroorganizmanın Ventilatör ilişkili pnömoni tanısı için klinik özellikler tek başına
yeterli olmadığı için, etken patojenlerin izole edilmesi ve izole edilen patojenlere
yönelik uygun tedavinin bir an önce başlanması çok önemlidir. Etken patojenlerin
izolasyonu için uygun solunum örnekleri, antibiyotik tedavisi başlanmadan ya da var
olan antibiyotik tedavisine klinik yanıt yok ise antibiyotik değiştirilmeden alınmalıdır.
Alt solunum yollarından örnek almak için bronkoskopik yöntemler (BAL,
korumalı örnek fırçalama) ve nonbronkoskopik yöntemler (endotrakeal aspirasyon ve
mini-BAL) kullanılmaktadır. Bronkoskopik yöntemlerle alınan alt solunum yolu
örneğinde havayolu kontaminasyonu daha az olmaktadır. Ancak nonbronkoskopik
yöntemler yerine bronkoskopik yöntemlerin kullanılmasının VİP prognozuna olumlu
katkısının olmadığı da gösterilmiştir (34).
Alınan alt solunum yolu örnekleri gram boyama ve mikroskobik inceleme için
en kısa sürede laboratuvara gönderilmelidir. Polimorf nüveli lökosit, solunum epiteli ve
bakteri morfolojileri açısından gönderilen örnek bakteriyologlar tarafından
değerlendirilmelidir. Mikroskopik incelemenin yanısıra alınan tüm alt solunum yolu
örneklerine kantitatif ve yarı kantitatif kültür yöntemleri uygulanmalıdır. Kantitatif
kültür yöntemi bronkoskopik ve nonbronkoskopik örneklere uygulanabilir. Alınan
örnekte üreyen patojen bakteri sayısı eşik değerin üzerinde saptanırsa VİP açısından
anlamlı kabul edilmelidir. Eşik değer endotrakeal aspirasyon için 10
6, BAL için 10
4,
korumalı örnek fırçalama için 10
3cfu/mL’dir.
Yarı kantitatif kültür yöntemleri de hem bronkoskopik hem de non bronkoskopik
alt solunum yolu örneklerine uygulanabilmektedir. Kantitatif kültüre göre, yarı
kantitatif kültür yöntemlerinin havayolu kolonizasyonunu enfeksiyondan ayırdedici
özellikleri daha azdır. Ancak, kantitatif ve yarı kantitatif kültür sonuçlarının
karşılaştırıldığı bir çalışmada VİP prognozuna etkileri açısından fark saptanmamıştır
15
(35). Yenilenen ATS/IDSA HGP/VİP rehberinde; VİP’in mikrobiyolojik tanısında
endotrakeal aspirasyon örneğinin semikantitatif kültürü önerilen yöntem olmuştur (24).
Konvansiyonel bakteriyolojik yöntemleri kullandığımızda, VİP etkenlerinin
izolasyonu ve antibiyotik duyarlılık paterninin belirlenmesi için 48-72 saatlik bir süre
gerekmektedir. Bu nedenle yaygın ilaç direnci gösterdiği durumlarda tedavi süresi daha
da uzun tutulmalıdır
(19).
ÇİD etkenlerin olası olduğu VİP olgularında, spektrumu geniş tutmak için
kombinasyon tedavisi gerekli olmaktadır. Buna karşın, mikrobiyolojik kültür sonuçları
ile kanıtlanmış gram(+) bakteri (MSSA, MRSA) kökenli VİP’lerde ve hafif VİP
olgularında monoterapi ile tedavi denenebilir (7).
Kolistin, ÇİD gram(-) bakterilerin neden olduğu VİP olgularında diğer bir tedavi
alternatifidir (38). Nefrotoksisite kolistinin en önemli doz kısıtlayıcı yan etkisidir (39).
Sistemik kullanımının yanı sıra inhale kullanıma uygun formu da bulunmaktadır. Çok
ilaca dirençli A. baumannii’nin ve MRSA’nın etken olduğu VİP tedavisinde tigesiklin
de son yıllarda kullanılmaktadır. Ülkemizden yapılan bir çalışmada, ÇİD A.
baumannii’nin etken olduğu HGP ve VİP olgularında, tigesiklin tedavisi ile olguların %
65.3’ünde bakteriyel eradikasyon saptanmıştır (39).
Tablo 4: Ventilatör ilişkili pnömonide çok ilaca dirençli etken risk faktörleri
-5 gün ve daha uzun süreli hastanede yatıyor olmak
-Son 90 günde antibiyotik tedavi öyküsü
-Ünitede antibiyotik direncinin olması
-İmmünosupressif hastalık ya da tedavi öyküsü
-Sağlık bakımı ilişkili pnömoni risk faktörlerinin olması
Son 90 günde 2 ve daha fazla gün hastanede yatma öyküsü Sağlık bakım ünitesinden gelme öyküsü Antibiyotik dahil evde infüzyon tedavisi alma öyküsü Son 30 gün içinde diyaliz programında olma öyküsü Evde bası yarası bakımı öyküsü
16
Tablo 5: ATS/IDSA 2016 yılı rehberinde çok ilaca dirençli patojenler için risk
faktörleri (24)
ÇİD VİP için risk faktörleri
Son 90 gün içinde intravenöz antibiyotik kullanımı VİP sırasında septik şok
VİP öncesinde ARDS varlığı
VİP gelişimi öncesinde 5 gün veya daha uzun süre hastanede yatıyor olmak VİP başlangıcı öncesi diyaliz tedavisi
ÇİD HGP için risk faktörleri
Son 90 gün içerisinde antibiyotik kullanımı MRSA VİP/HGP’si için risk faktörleri
Son 90 gün içerisinde antibiyotik kullanımı ÇİD Pseudomonas VİP/HGP’si için risk faktörleri
Son 90 gün içerisinde antibiyotik kullanımı
Tablo 6: Ampirik ventilatör ilişkili pnömoni tedavisi için güncel kılavuzlar
ÇİD patojen riski olmayan erken VİP
ÇİD patojen riski olan ya da geç VİP Olası etkenler MSSA S. pneumonia Haemophilus spp. Enterobacteriaceae MRSA P.aeruginosa Enterobacteriacae A. baumannii Stenotrophomonas maltophilia
American Thoracic Society/ Infectious Diseases Society
of America (2005) Seftriakson ya da Levofloksasin, moksifloksasin, Siprofloksasin ya da Ampisilin/sulbaktam ya da Ertapenem Sefepime ya da seftazidim ya da İmipenem/meropenem ya da Piperasilin/tazobaktam ve Siprofloksasin, Levofloksasin ya da
Amikasin, gentamisin, Tobramisin Vankomisin
ya da Linezolid
(MRSA risk faktörü varsa) European Respiratory
Society/European Society of Clinical Microbiology and Infectious Diseases/European
Society of Intensive Care Medicine (2009) Ampisilin/sulbaktam ya da Amoksisilin/klavunat ya da Sefuroksim ya da Seftriakson ya da Levofloksasin, moksifloksasin Seftazidim ya da İmipenem/Meropenem ya da Piperasilin/tazobaktam ve Siprofloksasin, Levofloksasin Vankomisin ya da Linezolid
17
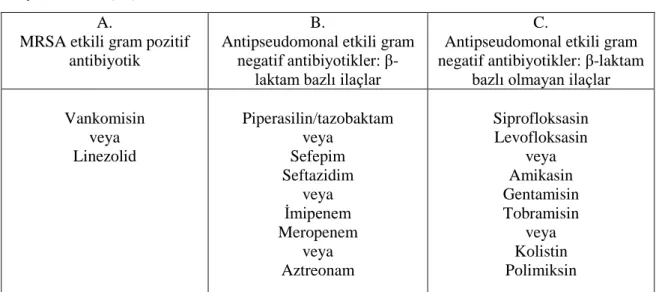
Tablo 7: Ventilatör ilişkili pnömonide metisilin dirençli S. aureus ve ikili
antipsödomonal/gram(-) etkili tedavinin uygun olduğu ünitelerdeki ampirik tedavi
seçenekleri* (24)
A.
MRSA etkili gram pozitif antibiyotik
B.
Antipseudomonal etkili gram negatif antibiyotikler:
β-laktam bazlı ilaçlar
C.
Antipseudomonal etkili gram negatif antibiyotikler: β-laktam
bazlı olmayan ilaçlar Vankomisin veya Linezolid Piperasilin/tazobaktam veya Sefepim Seftazidim veya İmipenem Meropenem veya Aztreonam Siprofloksasin Levofloksasin veya Amikasin Gentamisin Tobramisin veya Kolistin Polimiksin
*A kolonundan bir gram pozitif etkili, B kolonundan bir gram negatif etkili ve C kolonundan bir gram negatif etkili ilaç seçilir.
VİP etyolojisinde MRSA düşünüldüğünde (koma, kafa travması, merkezi sinir
sistemi cerrahisi, diabetes mellitus, renal yetersizlik gibi risk faktörlerinin varlığı) ya da
MRSA izole edildiğinde tedavide vankomisin ya da linezolid önerilmektedir. Linezolid,
vankomisine göre daha yüksek klinik başarı, daha düşük renal hasar yapma
potansiyeline sahiptir. Ancak her iki antibiyotik grubunda 60 günlük mortalite oranları
açısından fark bulunamamıştır (40).
2.9 Korunma
2.9.1 HGP/VİP Riskinin Olduğu Süreyi Kısaltmak
Hastanede kalış süresi ve entübasyon süresi arttıkça HGP/VİP gelişme olasılığı
artmaktadır. Bu nedenle öncelikle entübasyona alternatif noninvaziv mekanik
ventilasyon gibi yöntemler mutlaka her hasta için değerlendirilmelidir. Entübe olan
hastalarda günlük olarak sedasyona ara verilmesi ve ‘weaning’ için hastanın hazır olup
olmadığının değerlendirmesi, entübasyon süresini kısaltmaktadır. Ancak bu amaçla
yapılan bir çalışmada, VİP gelişme riskinin azaldığı gösterilememiştir (41). Entübasyon
18
süresinin azaltılmasına yönelik bir diğer yaklaşım trakeostominin erken açılmasıdır.
Ancak yapılan çalışmalarda trakeostominin erken açılmasının (7 günden önce)
hastanede kalış süresini, VİP gelişme oranlarını ve mortaliteyi etkilemediği
gösterilmiştir (42).
2.9.2 Endotrakeal Tüp Kolonizasyonu ve Kontamine Mikroaspirastları
Azaltmak
Biyofilm; endotrakeal tüpün iç yüzeyinde saptanan, bakteri kolonizasyonuna
olanak sağlayan bir oluşumdur. Aspirasyon ve bronkoskopi sırasında bu oluşumdaki
patojenlerin alt solunum yollarına doğru hareket etmesi ve VİP’e neden olması söz
konusudur. Gümüş kaplı endotrakeal tüpün biyofilm formasyonu oluşumunu ve
dolayısıyla VİP oluşumunu azalttığı gösterilmiştir (43).
Entübasyon tüpünün kafı üstünde biriken kontamine içeriğin alt solunum
yollarına aspirasyonu VİP riskini arttırmaktadır. Subglottik sekresyonların sürekli
aspirasyonunu sağlayan entübasyon tüplerinin kullanımı VİP riskini azaltabilmekteir. 13
randomize kontrollü çalışmanın dahil edildiği bir meta analizde, sürekli subglottik
sekresyonların aspirasyonunu sağlayan entübasyon tüplerinin kullanılmasının VİP
gelişimini, mekanik ventilasyon ve hastanede kalış süresini azalttığı belirlenmiştir (44).
Entübasyon tüpünün kaf basıncının 20-30 cmH
2O basınç aralığında tutulması
kontamine orofarengeal sekteryonların ve mide içeriğinin alt havayollarına aspire
edilmesine engel olabilmektedir. Yapılan çalışmalarda entübasyon tüpünün kaf
basıncının sürekli kontrol edilmesinin VİP gelişim oranlarını azalttığı gösterilmiştir
(45).
Entübe olarak yoğun bakımda izlenen hastaların yataklarının başlarının yüksek
olması mide içeriğinin üst havayollarına ve oradan da alt havayollarına ulaşarak VİP
oluşturmasına engel olabilmektedir. Yapılan çalışmalarda entübe yoğun bakım
hastalarının yatak başlarının özellikle enteral beslenirken 10 ile 30 derece arasında
kaldırılmasının VİP gelişimini azalttığı saptanmıştır (46).
19
2.9.3 Kolonizasyonun Önlenmesi
Üst solunum yollarında ve gastrointestinal sistemde mikroorganizmaların
kolonizasyonunu
engelleyici
yaklaşımlar,
alt
solunum
yollarına
patojen
mikroorganizmaların ulaşmasını önleyebilir. Antiseptik bir ajan olan klorheksidin ile
oral dekontaminasyon yapılmasının VİP gelişimini azalttığı gösterilmiştir (47).
Buna
karşın oral ve parenteral antibiyotikler ile yapılan orogastrik dekontaminasyon
çalışmaları beklenen başarıyı gösterememiş ek olarak bakteriyel direnç gelişimi
sonucunu da beraberinde getirmiştir.
İnsan kaynaklı canlı mikrobiyal ajan olan Lactobacillus rhamnosus’un
probiyotik olarak oral ve gastrik kullanımının VİP gelişme riskini azalttığı
gösterilmiştir. YBÜ’lerinde etkili enfeksiyon kontrolü için çalışanların eğitimi ve
birtakım önlem paketlerinin alınması VİP gelişim oranlarını azaltmaktadır. Bu amaçla
yapılabilecek en etkili yöntemlerinden biri el hijyenine dikkat etmektir. El hijyeni; su ve
antimikrobiyal olmayan sabun ile el yıkama, antiseptik veya dezenfektan ile el
temizliği, dezenfektan ile el ovuşturma (susuz el yıkama) ve cerrahi el antisepsisi
şeklinde yapılabilir.
20
3
GEREÇ ve YÖNTEM
3.1 Hastalar
Ocak 2014-Aralık 2016 tarihleri arasında Ege Üniversitesi Tıp Fakültesi Göğüs
Hastalıkları ile Anestezi ve Reanimasyon Yoğun Bakım Ünitesinde izlenen ve 2005
yılında yayınlanan ATS/IDSA kriterlerine göre HGP tanısı alan 62 hasta çalışmaya
alınmıştır. HGP tanısı konulduğu anda hastalarda bronkoskopik (BAL, BASP) ve
nonbronkoskopik (mini-BAL) yöntemlerle alt solunum yolu örnekleri alınmıştır. Alınan
örnekler konvansiyonel yöntemler ve hızlı moleküler yöntemlerle incelenmek üzere
ikiye bölünmüştür.
3.2 Çalışmaya Alınma Ölçütleri
a. Hastaneye yatışından veya entübasyondan 48 saat sonra gelişen, akciğer
grafisinde yeni ya da ilerleyici infiltrasyon saptanan hastalarda, aşağıdakilerden iki veya
daha fazlasının olması;
- >38˚C ateş
- Lökositoz (>12000 hücre/mm
3) ya da lökopeni (<4000 hücre/mm
3)
- Pürülan sekresyon
- Oksijenizasyonda azalma
b. 18 yaşından büyük olmak
c. Bilgilendirilmiş gönüllü onam almak (Hasta veremiyorsa yakınından)
d. Hastadan alt solunum yolu örneği (BAL, mini-BAL) almaya engel bir durumun
olmaması
3.3 Gönüllüleri Dışlama Kriterleri
1. HGP tanısı olan hastanın bilgilendirilmiş gönüllü onam formu vermemesi
2. Hastadan alt solunum yolu örneği (BAL, BASP, mini-BAL) almaya engel bir
21
4
Örneklerin Toplanması
BAL işleminde, entübasyon tüpü yoluyla fleksibl bronkoskop (Olympus CLE-10
USA) kullanılmıştır. Hastanın radyolojik bulgularına göre pnömoninin düşünülen
akciğer anatomik birimine bronkoskop tamamen ilerletilmiş, bronkoskop ucu
ulaşabileceği en distal havayolunda sabitlenmiştir. Bu işlemden sonra, bronkoskop
aspirasyon sisteminden ayrılarak, bronkoskopun aspirasyon kanalı yoluyla, %0.9 NaCl
20 ml fraksiyonlar halinde enjektörle verilmiş ve yine aynı enjektörle verilen sıvı aspire
edilmiştir. Verilen toplam 120 – 150 cc sıvının %60’nın geri alınması hedeflenmiştir.
BASP işleminde, entübasyon tüpü yoluyla fleksbıl bronkoskop (Olympus
CLE-10 USA) kullanılmıştır. Hastanın radyolojik bulgularına göre pnömoni düşünülen
akciğer anatomik birimine bronkoskop ilerletilmiş, bu alana bronkoskop aracılığı ile
verilen 50 ml %0.9 NaCl verilmiş ve verilen sıvı bronkoskopun aspirasyon sisteminden
geri alınmıştır.
Mini-BAL işleminde, lavaj kateteri (combicath TM; plastimed, Saint-Leu-La
Forêt, France) entübasyon tüpü yoluyla alt hava yollarına ilerletilmiştir. İlerletme
işlemi tamamlandıktan sonra kateter ucundaki koruyucu kılıf çıkarılıp kateterin bronş
ağacı içerisinde biraz daha ilerlemesi sağlanmıştır. Son olarak 20 cc %0.9 NaCl kateter
yolu ile verilip tekrar aynı enjektör ile aspire edilmiştir.
4.1 Mikrobiyolojik İnceleme
Alınan örnekler hem konvansiyonel yöntemlerle hem de hızlı moleküler
yöntemlerle incelenmiştir. Konvansiyonel yöntemler için ayrılan örnekler aynı gün
incelemeye alınırken; hızlı moleküler yöntemler için alınanlar ise toplu olarak
çalışılmak üzere çalışma gününe kadar -80˚C'de saklanmıştır.
Konvansiyonel incelemede, kantitatif kültür yöntemleri kullanılıp BAL için 10
4CFU/ml, mini-BAL için 10
5CFU/ml üreme anlamlı olarak kabul edilmiştir.
Bakteriyel etkenlerin identifikasyonu için Maldi-TOF MS (VITEK MS,
BioMerieux, Fransa) ve antibiyotik duyarlılık testleri için otomatik sistem (VIṪ EK2,
BioMerieux, Fransa) kullanılmıştır.
Moleküler incelemede, dört temel bakteriyi (Staphylococcus aureus,
22
saptamak amacıyla Real Time PCR kiti geliştirilmiştir. Her bir suştan elde edilen
DNA’lar 1/10 dilusyonlar yapılarak PCR etkinlik değerleri ve ideal PCR sıcaklık döngü
koşulları tespit edilmiştir (Tüm patojenler için PCR etkinlik değerleri E: 1,85-2,1
arasında bulunmuştur). Belirtilen gen bölgeleri hedef alınarak primer probe setleri
hazırlanmıştır.
Staphylococcus aureus için phospholipase gen bölgesi (150 bp)
Primer forward: AGTGTTAGCG GCTACAATGTTTG
Primer reverse: CCTGACTGCATTTGATGTGACG
Probe: 5’--CalRed610 TCGCGTTCCCTTGTTCTCCCGGTT BHQ2—3’
Pseudomonas aeruginosa için oprL gen bölgesi (161 bp)
Primer forward: CTGAACTGACGGTCGCCAAC
Primer reverse: CACCTTCACCGGAAGCATCG
Probe: 5’-- Quasar670 AGGAGCAACCCACAGCCACA GCCA—BHQ2—3’
Acinetobacter baumannii için 16S RNA gen bölgesi (145 bp)
Primer forward: GGAACTTTAAGGATACTGCCAGTG
Primer reverse: GGTCGTAAGG GCCATGATGAC
Probe:5’—FAM- CGTCGTCCCCGCCTTCCTCCAGT--BHQ1 —3’
Stenotrophmonas maltophilia için 16S RNA gen bölgesi (134 bp)
Primer forward: GATCCTGGCTCAGAGTGAACG
Primer reverse: CCCACGACAGAGTAGATTCCG
Probe:5’—VIC- -CACCCGTCCGCCACTCGCCAC--BHQ1—3’
-80˚C'de saklanan örneklerden “GenAll DNA/RNA Extraction Kit” (GenAll,
Güney Kore) kullanılarak kit içeriğinde önerildiği şekilde DNA ekstraksiyonu
gerçekleştirilmiştir. Elde edilen 200 µl nükleik asit solüsyonunun 5 µl’si amplifikasyona
alınmıştır. Amplifikasyon için, 2 X Realtime Multiplex Mix with UDG (Genmark
Sağlık Ürünleri, Türkiye) kullanılmış, amplifikasyon, saptama ve veri analizi Realtime
PCR cihazında (CFX96-IVD Biorad, ABD) çalışılmıştır.
23
Örnekte flöresan sinyali alınmış ise, internal kontrolde “melting peak”
gözlenmiş ise ve ekstraksiyon ve amplifikasyon için pozitif kontroller pozitif, negatif
kontroller negatif sonuçlanmış ise test sonucu pozitif kabul edilmiştir
Örnekte flöresans sinyali yokken internal kontrolde “melting peak” gözlenmiş
ise ve ekstraksiyon ve amplifikasyon için pozitif kontroller pozitif, negatif kontroller
negatif sonuçlanmış ise test sonucu negatif kabul edilmiştir.
Negatif kontroller negatif ve pozitif kontroller pozitif olarak sonuçlanmamış ise
veya örnekler negatif olduğu durumda internal kontrolde floresans gözlenmemiş ise test
geçersiz kabul edilmiş ve tekrarlanmıştır.
Çalışma için Ege Üniversitesi Tıp Fakültesi Araştırma Etik Kurulu'ndan onay
alınmıştır. Bilgilendirilmiş gönüllü onam formu, hasta ve hasta yakını bilgilendirildikten
sonra hasta veya birinci derece yakınları tarafından doldurulup imzalanmıştır.
Çalışmaya alınan her hasta için; hastaneye yatış ve HGP tanısı anında akciğer grafisi
buguları, laboratuvar değerleri (lökosit, CRP, prokalsitonin, PaO
2/FiO
2oranı), klinik
pulmoner enfeksiyon skoru (CPIS), demografik verileri, altta yatan hastalıkları,
immunsupresyon varlığı ve hastaneye yatış tanıları kaydedilmiştir.
24
5
BULGULAR
Çalışmamıza Ege Üniversitesi Tıp Fakültesi Göğüs Hastalıkları Anabilim Dalı
Kliniği ile Anestezi ve Reanimasyon Anabilim Dalı Yoğun Bakım Ünitesinde takip
edilen toplam 62 (42 erkek, ortalama yaş 69.7 ± 15.6) hasta alınmıştır. Hastaların 46
(%74)’sı Göğüs Hastalıkları kliniğinde izlenirken, 16 (%26)’sı Anestezi ve
Reanimasyon kliniğinde izlenmiştir.
Hastaneye yatış anında, KOAH (16 hasta), hipertansiyon (16 hasta), diyabet (15
hasta), nörolojik hastalıklar (14 hasta) başta olmak üzere, hastaların %95.2'sinde ek
hastalık saptanmıştır. Tablo 6'da ek hastalıkların dağılımı ve hastaların demografik
verileri gösterilmiştir (Tablo 8).
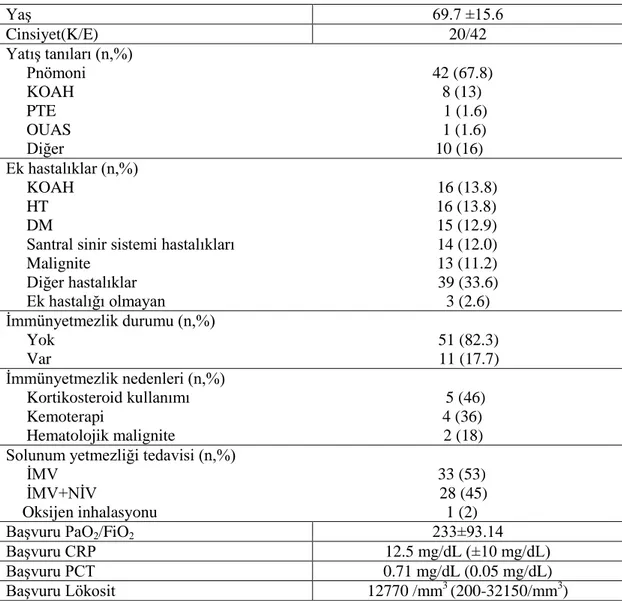
Tablo 8: Hastaların başvuru anındaki demografik özellikleri, yatış tanıları, ek
hastalıkları ve laboratuvar bulguları
Yaş 69.7 ±15.6 Cinsiyet(K/E) 20/42 Yatış tanıları (n,%) Pnömoni 42 (67.8) KOAH 8 (13) PTE 1 (1.6) OUAS 1 (1.6) Diğer 10 (16) Ek hastalıklar (n,%) KOAH 16 (13.8) HT 16 (13.8) DM 15 (12.9) Santral sinir sistemi hastalıkları 14 (12.0) Malignite 13 (11.2) Diğer hastalıklar 39 (33.6) Ek hastalığı olmayan 3 (2.6) İmmünyetmezlik durumu (n,%) Yok 51 (82.3) Var 11 (17.7) İmmünyetmezlik nedenleri (n,%) Kortikosteroid kullanımı 5 (46) Kemoterapi 4 (36) Hematolojik malignite 2 (18) Solunum yetmezliği tedavisi (n,%)
İMV 33 (53) İMV+NİV 28 (45) Oksijen inhalasyonu 1 (2)
Başvuru PaO2/FiO2 233±93.14
Başvuru CRP 12.5 mg/dL (±10 mg/dL)
Başvuru PCT 0.71 mg/dL (0.05 mg/dL)
25
En sık hastaneye yatış nedeni olarak, pnömoni (42 hasta) ve KAOH alevlenme
(8 hasta) olarak belirlenmiştir. Tüm hastalarda solunum yetmezliği saptanmıştır. 33
hastaya İMV, 28 hastaya İMV ve NİV uygulanırken (İMV öncesi NİV uygulaması ya
da İMV sonrası NİV uygulaması), 1 hasta ise oksijen inhalasyonu ile izlenmiştir.
İzlem süresince 58 hastaya endotrakeal entübasyon işlemi yapılmıştır. Ortalama
entübasyon süresi 12.8 ± 10.0 gün olarak bulunmuştur. Üç hasta hastaneye
trakeostomili olarak kabul edilmiş, toplam 19 hastaya izlem süresince trakeostomi
açılmıştır. Bir hasta ise sadece oksijen inhalasyonu ile izlenmiştir.
Başvuru anındaki akciğer grafisi değerlendirildiğinde; 48 hastada parankimal
infiltrasyon, 5 hastada plevral efüzyon ve 1 hastada da atelektazi ile uyumlu dansite
bulguları izlenmiştir.
Hastaneye yatışlarının 48. saatinden sonraki izleminde hastanede gelişen
pnömoni tanısı alan hastalar çalışmaya alınmıştır. Hastanede gelişen pnömoni tanısı
konulduğu anda bakteriyolojik inceleme için 51 hastadan mini-BAL, 7 hastadan BAL
ve 4 hastadan ise BASP alınmıştır.
Hastanede gelişen pnömoni tanısı anında saptanan lökosit, CRP, prokalsitonin,
CPIS ve PaO
2/FiO
2değerleri
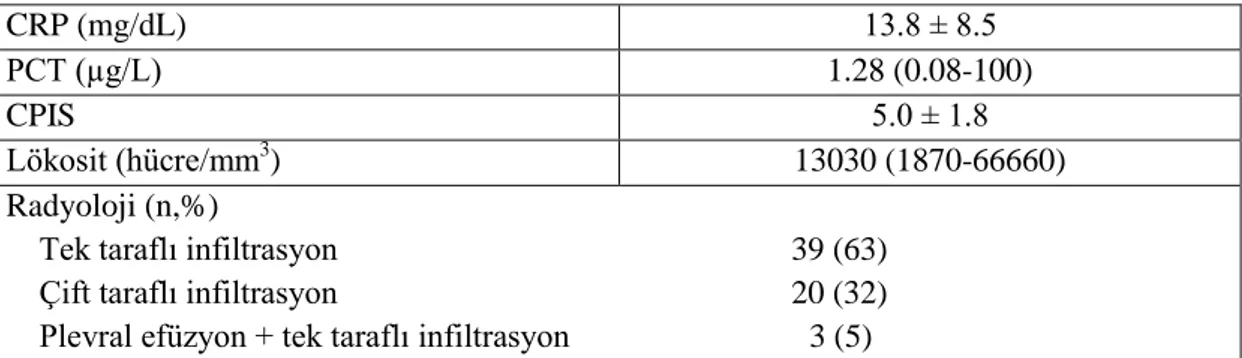
tablo 9’da verilmiştir. Hastanede gelişen pnömoni tanısı
anında 59 hastanın 39'inin akciğer grafisinde tek taraflı infiltrasyon, 20'sinde çift taraflı
infiltrasyon saptanmıştır. Üç hastanın akciğer grafisinde ise plevral efüzyonla birlikte
tek taraflı infiltrasyonla uyumlu dansite artışı izlenmiştir.
Tablo 9: Hastanede gelişen pnömoni tanı anında enfeksiyon belirteçleri ve radyolojik
bulguları
CRP (mg/dL) 13.8 ± 8.5 PCT (µg/L) 1.28 (0.08-100) CPIS 5.0 ± 1.8 Lökosit (hücre/mm3 ) 13030 (1870-66660) Radyoloji (n,%)Tek taraflı infiltrasyon 39 (63) Çift taraflı infiltrasyon 20 (32) Plevral efüzyon + tek taraflı infiltrasyon 3 (5)