FEN BĐLĐMLERĐ ENSTĐTÜSÜ
MANDALĐNA KABUKLARINDAN NANO-GÖZENEKLĐ AKTĐF KARBON ÜRETĐLMESĐ VE SULU FAZDAN BAZI TOKSĐK BOYARMADDE VE KARIŞIMLARI ĐÇĐN ADSORPLAMA YETENEĞĐNĐN ĐNCELENMESĐ
Filiz KOYUNCU
YÜKSEK LĐSANS TEZĐ
KĐMYA ANABĐLĐM DALI
Tez Danışmanı: Prof. Dr. Fuat GÜZEL
DĐYARBAKIR TEMMUZ - 2016
DicLE
LNivERsirpsi
ppN
niriıtrEni
gNsrirüsü
ıaüounrtıĞi;
niyeRnarıR
Fil iz KOYUNCU tarafind an y apıIarı " Man d alin a Ka b u k l arı n dqn N an o - G ö ze n e k l
i
Aktif Kurbon Üretilmesi ve SuIu Fazdan Bazı Toksik Boyarmadde ve Karışımları İçin
AdsorPlama Yeteneğ.inin İncelenmest'konulu bu çalışma, jiirimiz tarafindan Kimya Aıabilim Dalında
yüxsnr
rısaNs
tezi olarakkabul edilmiştirJüri Üyesinin
Unvanr Adı Soyadı
Başkan: Prof. Dr. Fuat GÜZEL (Danışman)
Uye: Prof. Dr. Haluk
AYDIN
Üye: Yrd. Doç. Dr. Hasan
SAYĞILI
,,,.] ,/
,-fff
,fr-Tez Savunma SınavrTarihi:
1210712016I
ve hoşgörüsüyle bilgi ve birikimini benden esirgemeyen değerli hocam tez danışmanım sayın Prof.Dr. Fuat GÜZEL'e,
Tez çalışmaların gerçekleştirilmesinde yardım ve katkılarından dolayı sayın Yrd.
Doç. Dr. Hasan SAYĞILI'ya,
Yüksek Lisans Öğrenimim sırasında destek ve bilgilerini benden esirgemeyen sayın Arş. Gör. Dr. Gülbahar AKKAYA SAYĞILI 'ya
Hayatımın her aşamasında, daima yanımda olan ve her zaman yanımda olacaklarını bildiğim, bugünlere gelmemde büyük emek sahibi olan canım aileme ve
Songül KOYUNCU'ya,
Numunelerimin analizinde yardımlarından dolayı Dicle Üniversitesi Bilim ve
Teknoloji Uygulama ve Araştırma Merkezi personellerine,
Bu tez çalışmasını DÜBAP: ZGEF-15-004 no'lu projeyle maddi olarak destekleyen Dicle Üniversitesi Bilimsel Araştırma Projeleri Koordinatörlüğü'ne teşekkürlerimi sunarım.
II Sayfa TEŞEKKÜR... I ĐÇĐNDEKĐLER... II ÖZET... V ABSTRACT... VI ÇĐZELGE LĐSTESĐ... VII ŞEKĐL LĐSTESĐ... VIII KISALTMA VE SĐMGELER... X
1. GĐRĐŞ... 1
1.1 Adsorpsiyon Hakkında Genel Bilgiler... 2
1.1.1. Gaz Adsorpsiyon Đzotermleri... 2
1.1.2 Gaz Adsorpsiyon-Desorpsiyon Đzoterm ve Histerezis Tiplerinin Sınıflandırılması... 4
1.2 Çözeltiden Adsorpsiyon... 7
1.2.1 Çözeltiden Adsorpsiyonda Kinetik Modelleme... 9
1.2.2. Çözeltiden Adsorpsiyonda Đzoterm Modelleme... 9
1.2.3 Çözeltiden Adsorpsiyon Termodinamiği... 10
1.3. Adsorplayıcılar... 12
1.3.1. Aktif Karbon Hakkında Bilgiler... 12
1.4. Çalışmada Aktif Karbon üretiminde Kullanılan Hammadde ve Adsorplananlar Hakkında Genel Bilgiler... 17
1.4.1 Mandanila Kabukları... 17
1.4.2. Adsorplananlar... 17
1.4.2.1. Metilen Mavisi... 17
III
3.1. Kullanılan Kimyasallar... 23
3.2. Kullanılan Cihazlar... 24
3.3. Mandalina Kabuklarından Optimal Nano-Gözenekli Aktif Karbonun Hazırlanması... 24
3.4. Mandalina Kabuklarının ve Optimal Nano-Gözenekli Aktif Karbonun Karakterizasyonu... 26
3.5. Çözeltiden Adsorpsiyon Çalışmaları... 27
3.5.1. Kalibrasyon ve Ölçüm Yöntemleri... 27
3.5.2. Sulu Çözeltiden Kullanılan Boyarmaddelerin Adsorpsiyon Koşullarının Optimize Edilmesi Çalışmaları... 28
3.5.2.1 pH Etkisi... 28
3.5.2.2. Doz Etkisi... 28
3.5.2.3 Başlangıç Derişimi/Denge Temas Süresi Etkisi ve Kinetik Modelleme Çalışmaları... 29
3.5.2.4 Sıcaklık Etkisi ve Đzoterm Modelleme Çalışmaları... 29
3.5.3 MM ve MS'nin Sulu Çözeltideki Karışımından MM ve MS Adsorpsiyonlarının Đncelenmesi... 30
4. BULGULAR VE TARTIŞMA... 31
4.1 Mandalina Kabuğunun Bileşen ve Termal Analiz Sonuçlarının Değerlendirilmesi... 31
4.2. Aktif Karbonların Hazırlama Koşullarının Etkisine Đlişkin Değerlendirilmeler.. 32
4.2.1. H3PO4 Emdirme Oranının Etkisi... 32
4.2.2 Karbonizasyon/aktivasyon Sıcaklığı Etkisi... 33
4.2.3. Karbonizasyon Süresi Etkisi... 34
IV
Değerlendirilmesi... 38
4.3.1. Proksimate Analiz Sonuçlarının Değerlendirilmesi... 38
4.3.2. SEM Analiz Sonuçlarının Değerlendirilmesi... 38
4.3.3 Yüzey Fonksiyonel Gruplarının Nitel ve Nicel Analiz Sonuçlarının Değerlendirilmesi... 39
4.3.4. Optimal Nano-Gözenekli Aktif Karbona Đlişkin Gözenek Karakterizasyonu Sonuçlarının Değerlendirilmesi... 41
4.4. Metilen Mavisi ve Metanil Sarısı Adsorpsiyonlarına Đlişkin Deneysel Sonuçların Değerlendirilmesi... 43
4.4.1. Metilen Mavisi ve Metanil Sarısı Adsorpsiyonlarının Optimizasyonuna Đlişkin Deneysel Sonuçlarının Değerlendirilmesi... 43
4.4.1.1. pH Etkisi... 43
4.4.1.2 Doz Etkisi... 45
4.4.1.3. Başlangıç Derişimi ve Denge Süresi Etkileri-Kinetik Modelleme... 46
4.4.1.4. Sıcaklık Etkisi - Đzoterm Modelleme ve Termodinamik Analiz... 51
4.4.1.5. Metilen Mavisi ve Metanil Sarısı Yüklü MNK'ın FT-IR Analizlerinin Değerlendirilmesi... 58
4.4.1.6. Metilen Mavisi ve Metanil Sarısı Yüklü MNK'ın SEM Analizlerinin Değerlendirilmesi... 59
4.5 Metilen Mavisi ve Metanil Sarısının Đkili Karışımından Adsorpsiyonlarına Đlişkin Deneysel Sonuçların Değerlendirilmesi... 59
5. SONUÇ VE ÖNERĐLER... 65
6. KAYNAKLAR... 67
V
VE SULU FAZDAN BAZI TOKSĐK BOYARMADDE VE KARIŞIMLARI ĐÇĐN ADSORPLAMA YETENEĞĐNĐN ĐNCELENMESĐ
YÜKSEK LĐSANS TEZĐ Filiz KOYUNCU DĐCLE ÜNĐVERSĐTESĐ FEN BĐLĐMLERĐ ENSTĐTÜSÜ
KĐMYA ANABĐLĐM DALI 2016
Aktif karbon yüksek yüzey alanı, gözeneklilik ve yüksek adsorplama kapasitesinden dolayı yaygın bir şekilde kullanılan adsorplayıcılardan biridir. Aktif karbon atık miktarı fazla bitkisel hammaddelerden kolaylıkla elde edilebilmektedir.
Bu yüksek lisans tezi kapsamında atık miktarı fazla olan mandalina kabuğu kullanılarak ilk kez mikrodalga ön işlemi uygulanarak nano-gözenekli aktif karbon hazırlama koşularının optimizasyonu hedeflendi. Bu amaçla, mandalina kabuğunun aktif karbon hazırlama uygunluğunu tespit etmek için bileşen, proksimate ve termogravimetrik analizleri yapılmıştır. Aktif karbonun hazırlanmasında kimyasal aktivatör olarak H3PO4 tercih edilmiştir. Aktif karbon hazırlama koşulları için 40 saniye 900 W mikrodalga ön işleminden sonra azot ortamında aktivatör emdirme oranı, karbonizasyon/aktivasyon sıcaklığı ve süre etkisi incelenmiştir. Üretim optimizasyon koşulları 40 saniye 900 W mikrodalga ön işlemi, 2:1 gH3PO4/gkabuk emdirme oranı, 500
o
C karbonizasyon/aktivasyon sıcaklığı ve 1 saat karbonizasyon/aktivasyon süresi olarak belirlenmiştir. Belirlenen bu koşullarda hazırlanan aktif karbonun yüzey alanı ve gözenek boyu dağılımları, SEM, FT-IR, proksimate analiz, sıfır yük pH'sı ile Boehm titrasyonu gibi çeşitli fizikokimyasal yöntemlerle karakterize edilmiştir. Ayrıca sulu çözeltiden adsorplama kapasitelerini tespit etmek için metilen mavisi ve metanil sarısı adsorplanan olarak kullanılmıştır. Adsorplama kapasitesini optimize etmek için çözelti pH'ı, adsorplayıcı dozu, adsorplanan başlangıç derişimi, denge süresi ve sıcaklık etkileri gibi çeşitli parametrelerin etkileri incelenmiştir. Belirlenen optimum adsorpsiyon koşullarında kinetik ve izoterm çalışmaları gerçekleştirildi. Yapılan kinetik ve izoterm çalışmalarından, adsorpsiyonlarının kısa sürede, yüksek derişimlerde ve yüksek sıcaklıklarda gerçekleştiği gözlenmiştir.
Bu çalışma sonucunda atık değeri yüksek olan mandalina kabuğundan üretilen optimal nano-gözenekli aktif karbonun gözenek karakteristiği ve çözeltiden adsorpsiyon kapasitesi göz önüne alındığında mandalina kabuğunun ticari aktif karbon üretiminde kullanılabileceği gözlenmiştir.
Anahtar kelimeler: Mandalina kabuğu, Aktif karbon Metilen mavisi, Metanil sarısı, kinetik, izoterm,
VI
THE PRODUCTION OF NANO-POROUS ACTIVARED CARBON FROM TANGERINE SHELLS AND INVESTIGATION OF ADSORPTION CAPABILITY FOR
SOME TOXIC DYESTUFF AND DYESTUFF MIXTURE FROM AQOUES PHASE MSc THESIS
Filiz KOYUNCU DĐCLE UNIVERSITY
INSTITUTE OF NATURAL AND APPLIED SCIENCES DEPARTMENT OF CHEMISTRY
2016
Activated carbon surface area is one of the widely used adsorptions due to its porosity and adsorptance capacity. Activated carbon waste amount can be easily obtained from surplus raw materials.
Within the scope of this master/s thesis, it is aimed to optimize the conditions of preparing nano-porous activated carbon by applying microwave pre-operation for the first time through the use of tangerine shell which has a great waste amount. For this purpose, proximate and thermogravitmetric analyses were carried out to determine the convenience of tangerine shell to activated carbon. H3PO4 was preferred as the chemical activator in the process of preparing activated carbon. After applying 40 seconds 900 W microwave pre-operation for the conditions of preparing activated carbon, the effects of activator impregnation ratio in the nitrogen phase, carbonization/activation temperature and time were investigated. As a result, the conditions of optimization of production were determined as: 40 seconds 900 W microwave pre-operation, 2:1 gH3PO4/gshell impregnation rate, 500
o
C carbonization/activation temperature and 1 hour of carbonization/activation time. Active carbon surface area prepared under these conditions and pore size distributions were characterised with such physicochemical methods as SEM, FT-IR, proksimate analyses, point of zero charge and Boehm titration measurements. Besides, methylene blue and metanil yellow was used as adsorptance to identify adsorption capacity in aqueous solution. To optimize adsorption capacity, the effects of such parametres as the pH of solution, adsorption dose, adsorpted starting concentration, balance time, and temperature impact were investigated. Kinetical and isotherm studies were carried out under determined optimal adsorption conditions. As a consequence of kinetical and isotherm studies, it was observed that their adsorptions occured in high concentrations and high temperatures in a short time.
At the end of this study, it was observed that tangerine shell can be used in the production of commercial activeated carbon considering optimal nano-porous activated carbon pore characteristics and solution adsorption capacity produced from tangerine shell whose waste value is high.
Keywords: Tangerine shell, Activated carbon, Methylene blue, Metanil yellow, kinetic, isotherm
VII
Çizelge No Sayfa
Çizelge 1.1.
Aktif Karbonun Gaz ve Sıvı Faz Uygulamaları... 16 Çizelge 3.1. Metilen Mavisi ve Metanil Sarısının Genel Özellikleri... 23 Çizelge 4.1. Mandalina Kabuğunun Bileşen Analiz Sonuçları... 31 Çizelge 4.2. Mandalina Kabuklarından Çeşitli Koşullarda Hazırlanan Aktif karbonların
Gözenek Karakteristiklerine Hazırlama Koşullarının Etkisi... 37 Çizelge 4.3. Mandalina Kabuğu ile Ondan Üretilen Optimal Nano-Gözenekli Aktif
Karbonun Proksimate Analiz Sonuçları... 38 Çizelge 4.4. MNK'ın Yüzey nicel Analiz Sonuçları... 40 Çizelge 4.5. Hazırlanan Optimal Aktif Karbonlara Đlişkin Gözenek Karakteristikleri
[Mikrodalga ön işlem süresi:40 sn; Emdirme Oranı(gH3PO4/gMK): 2:1; Karbonizasyon/Aktivasyon Sıcaklığı: 600 oC;Karbonizasyon/Aktivasyon Süresi:1 saat]... 42 Çizelge 4.6. MNK Üzerinde MM ve MS'nin Değişik Başlangıç Derişimlerinde Yapılan
Adsorpsiyonlarına Đlişkin Kinetik Parametreler... 51 Çizelge 4.7. MNK Üzerinde Değişik Sıcaklıklarda MM ve MS Adsorpsiyonlarına
Đlişkin Đzoterm Parametreleri... 57 Çizelge 4.8. MNK Üzerinde MM ve MS Adsorpsiyonlarına Đlişkin Termodinamik
Parametreler... 58 Çizelge 4.9 MNK Üzerinde MM ve MS Đkili Karışımından Adsorpsiyonlarına Đlişkin
Đzoterm Parametreleri... 63 Çizelge 5.1. MNK ile Bazı Bitkisel Kökenli Hammaddelerden Hazırlanan ve Ticari
Aktif Karbonların Bazı Gözenek Karakteristiklerinin Karşılaştırılması... 64 Çizelge 5.2. MNK ile Bazı Bitkisel atıklardan Hazırlanan Aktif Karbonlar ve Ticari
Aktif Karbonların MM ve MS Adsorplama Kapasitelerinin Karşılaştırılması... 65
VIII
Şekil No Sayfa
Şekil 1.1. Adsorpsiyon ve Desorpsiyon Đzotermlerinin IUPAC Sınıflandırılması... 5
Şekil 1.2. IUPAC'ın Histerezis Sınıflandırması... 6
Şekil 1.3. Çözeltiden Adsorpsiyonda Giles Đzoterm Sınıflandırılması... 7
Şekil 1.4. Aktif Karbonunun Yüzeyinde Yer Alan Fonksiyonel Gruplar... 14
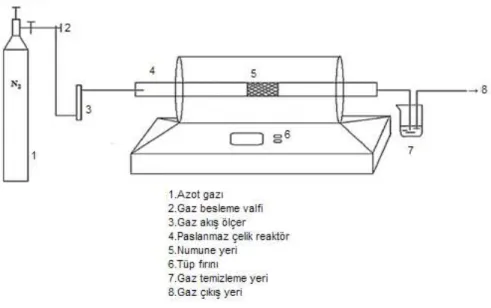
Şekil 3.1. Aktif Karbonların Hazırlanmasında Kullanılan Tüp Fırın Düzeneği... 26
Şekil 4.1. Mandalina Kabuğuna Đlişkin Termal Analiz (TG/DTA) Eğrileri... 32
Şekil 4.2. Mandalina Kabuğundan Değişik Emdirme Oranlarında Üretilen Aktif Karbonların Azot Adsorpsiyon-Desorpsiyon Đzoterm izotermleri... 33
Şekil 4.3. Mandalina Kabuğundan Değişik Karbonizasyon/Aktivasyon Sıcaklıklarında Üretilen Aktif Karbonların Azot Adsorpsiyon-Desorpsiyon Đzotermleri... 34
Şekil 4.4. Mandalina Kabuğundan Değişik Karbonizasyon/aktivasyon Sürelerinde Üretilen Aktif Karbonların Azot Adsorpsiyon-Desorpsiyon Đzotermleri... 35
Şekil 4.5. SEM Analiz Görüntüleri: MK(a) ve MNK(b)... 39
Şekil 4.6. MNK, MM ve MS Đlişkin FTIR Spektrumu... 39
Şekil 4.7. MNK'a Đlişkin pHYSY Çizimi... 40
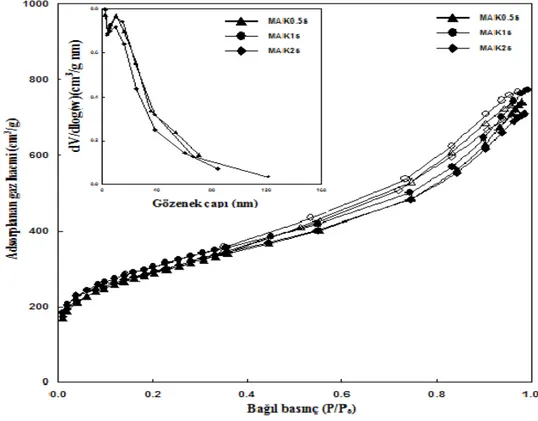
Şekil 4.8. MNK'a Đlişkin Azot Adsorpsiyon-Desorpsiyon Đzotermleri ve Gözenek Boyut Dağılımı Analiz Çizimleri (iç kısımda)... 42
Şekil 4.9. MNKÜzerinde MM ve MS Adsorpsiyonlarına pH Etkisi Çizimleri... 45
Şekil 4.10. MNKÜzerinde MM ve MS Adsorpsiyonlarına Doz Etkisi Çizimleri... 46
Şekil 4.11. MNK Üzerinde MM (a) ve MS (b) Adsorpsiyonuna Đlişkin Başlangıç Derişimi ve Denge Süresi Etkisi Çizimleri... 48
Şekil 4.12 MNK Üzerinde Değişik MM ve MS Derişimlerindeki Adsorpsiyonlarına Đlişkin Çizgisel Kinetik Çizimleri: Lagergren (a-b) ve Ho-McKay (c-d)... 50
Şekil 4.13. Değişik Sıcaklıklarda MNKÜzerinde MM (a) ve MS (b) Adsorpsiyonlarına Đlişkin Đzoterm Çizimleri... 54
Şekil 4.14. Değişik Sıcaklıklarda MNKÜzerinde MM ve MS Adsorpsiyonuna Đlişkin Çizgisel Freundlich (a-b) ve Langmuir (c-d) Çizgisel Đzoterm Çizimleri... 56
IX
Görüntüleri: MNK-MM (a) ve MNK-MS (b)... 59 Şekil 4.17. MNK Üzerinde MM (a) ve MS (b) Đkili Karışımından Adsorpsiyonlarına
Đlişkin Đzoterm Çizimleri... 60 Şekil 4.18. MNK Üzerinde MM ve MS Đkili Karışımından Adsorpsiyonlarına Đlişkin
Çizgisel Freundlich (a-b) ve Langmuir (c-d) Çizgisel Đzoterm Çizimleri... 62
X AK :Aktif Karbon
MNK :Optimal Nano-Gözenekli Aktif Karbon B.E.T :Brunauer-Emmett-Teller
B.J.H :Barret-Joyner-Halenda
b :Adsorpsiyon Enerjisi veya Adsorplananın Adsorplanma Eğilimi ile Đlgili Langmuir Đzoterm Sabiti (L/mg)
c :Adsorpsiyon Isısının, Yoğunlaşma Isısını Aşan Miktarının Ölçüsü Olan B.E.T. Đzoterm Sabiti
Ce :Adsorplananın Denge Derişimi (mg/L)
Co :Adsorplananın Başlangıç Derişimi (mg/L)
DFT :Density Functional Theory Dp :Ortalama Gözenek Yarıçapı (nm)
V :Adsorplayıcının Birim Kütlesi Başına Adsorplanan Gaz Hacmi (mL/g) FT-IR :Fourier Transform Infrared
h :Ho-McKay Başlangıc Adsorpsiyon Hızı (g/mgdk) IUPAC :Uluslararası Temel ve Uygulamalı Kimya Birliği k1 :Lagergren Adsorpsiyon Hız Sabiti (1/dk)
k2 :Ho-McKay Adsorpsiyon Hız Sabiti (g/mgdk)
KF :Adsorplayıcının Adsorplama Eğilimi ile Đlgili Freundlich Đzoterm Sabiti
[(mg/g)(mg/L)-1/n]
KL :Adsorpsiyon Denge Sabiti (qmb)
ko :Adsorpsiyon Hız Sabiti (g/moldk)
m :Adsorplayıcı Miktarı (g) MM :Metilen Mavisi
MS :Metanil Sarısı
n :Adsorplananın Adsorplanma Eğilimi ile Đlgili Freundlich Đzoterm Sabiti P :Adsorpsiyon Sonrası Sistemdeki Denge Buhar Basıncı (atm)
pHb :Başlangıç pH'sı
pHs :Son pH'sı
pHYSY :Yüzey Sıfır Yük pH'sı
XI
qe,d :Deneysel Olarak Denge Anında Birim Adsorplayıcı Miktarı Tarafından
Adsorplanan Miktar (mg/g)
qe :Denge Durumunda Adsorplayıcı Miktarı Tarafından Adsorplanan
Miktar (mg/g)
qm :Tek Tabaka Adsorpsiyon veya Adsorplayıcının Adsorplama Kapasitesi
ile Đlgili Langmuir Đzoterm Sabiti (mg/g)
qt :t Anında Birim Adsorplayıcı Miktarı Tarafından Adsorplanan Miktar
(mg/g)
R :Evrensel Gaz Sabiti (8.314 J/mol K) R2 :Korelâsyon Katsayısı
RL :Ayırma Faktörü
rpm :Dakikadaki Devir Sayısı SBET :B.E.T Yüzey Alanı (m2/g)
SEM :Scanning Electron Microscopy SM :Mezogözenek Yüzey Alanı (m2/g)
Sm :Mikrogözenek Yüzey Alanı (m2/g)
T :Çözelti Sıcaklığı (K) t :Denge Temas Süresi (dk) TG :Termal Gravimetrik Analiz UV-vis :Ultraviole-visible
Vads :Adsorplayıcının Birim Kütlesi Başına Adsorplanan Gaz Hacmi (mL/g)
Vm :Adsorplayıcının Tek Tabaka Örtünmesi veya Adsorplayıcının
Adsorplama Kapasitesi ile Đlgili Langmuir Đzoterm Sabiti (mL/g) VM :Mezogözenek Hacmi (cm3/g)
Vm :Mikrogözenek Hacmi (cm3/g)
VT :Toplam Gözenek Hacmi (cm3/g)
∆Go :Gibbs Serbest Enerji Değişimi (kJ/mol) ∆Ho :Entalpi Değişimi (kJ/mol)
∆So :Entropi Değişimi (kJ/mol K) λmax :Maksimum Dalga Boyu (nm)
1 1.GĐRĐŞ
Günümüzde gelişen teknoloji, sanayileşme ve artan nüfusla birlikte insanoğlunun çeşitli ihtiyacı da artmaktadır. Đhtiyaçların karşılanması için elektronik, endüstri, gıda, tekstil, maden, makine, kimya sanayi ve daha birçok sanayi kolu gelişmiştir. Gelişen sanayi ile çok büyük ve geri dönüşü zor olan çevre kirliliğini beraberinde getirmektedir. Gittikçe artan çevre kirliliği insanların sağlığı üzerinde birçok olumsuz etkiler bırakmaktadır. Đnsanoğlu bu olumsuz yöntemleri ortadan kaldırmak için birçok yöntem geliştirmiştir. Bu yöntemlerden biri adsorpsiyondur. Katı ya da sıvı yüzeylerine değmekte olan gazlar ya da çözünen maddelerin bu yüzeyde tutunması olayına adsorpsiyon denir. Adsorpsiyon olayında, maddeleri yüzeyinde tutan faza adsorplayıcı, adsorpsiyona uğrayan maddeye ise adsorplanan denir (Güzel 1991). Yaygın olarak kullanılan endüstriyel amaçlı adsorplayıcılar arasında çevre kirliliğini kontrol altına almak için şu anda kullanılan adsorplayıcılar arasında en önemlisi aktif karbondur.
Aktif karbon (AK) yüksek yüzey alanı, gözeneklilik ve yüksek adsorplama kapasitesinden dolayı yaygın bir şekilde kullanılan adsorplayıcılardan biridir. Bu özelliklerinden dolayı AK geçmişten bugüne kullanımı artmakla birlikte AK'a olan ihtiyaçlarda artmaktadır. Son yıllarda AK üretiminde karbon içeriği yüksek bitkisel atıklardan, fabrika atıklarından ve birçok hammadde kullanılmaktadır.
Bu yüksek lisans tezi kapsamında atık miktarı fazla olan mandalina kabuğu kullanılarak ilk kez tarafımızdan mikrodalga ön işlemi uygulanarak nano-gözenekli aktif karbon üretildi. Bununla birlikte kabukların karbonizasyon/aktivasyon koşullarını optimize etmek için sırasıyla kimyasal aktivatör emdirme oranı, karbonizasyon/aktivasyon sıcaklığı ve süre etkileri incelendi. Kullanılan kabuklardan üretilen AK'ların üretim koşullarının optimize edilmesi; BET (Brunauer-Emmett-Teller) yüzey alanı, toplam gözenek hacmi, mikrogözeneklilik, mezogözeneklilik ve ortalama gözenek çapı gibi gözenek özellikleri dikkate alınarak gerçekleştirildi.
Üretim koşulları optizimize edildikten sonra AK'ların adsorpsiyon uygulamalarında kullanılabilirliğini test etmek için metilen mavisi(MM) (katyonik) ve metanil sarısı(MS) (anyonik) adsorpsiyon çalışmaları yapıldı. Adsorpsiyon koşullarını optimize etmek üzere pH, adsorplayıcı dozu ve başlangıç boyarmadde derişiminin
2
etkileri incelendi. Belirlenen optimum koşullarda, sırasıyla farklı derişimlerde kinetik ve farklı sıcaklıklarda izoterm çalışmaları yapılarak hazırlanan AKopt-boyarmadde adsorpsiyon sistemleri için bazı fizikokimyasal parametreler belirlenerek karakterize edildi.
1.1. Adsorpsiyon Hakkında Genel Bilgiler
Katı ya da sıvı yüzeylerine değmekte olan gazlar ya da çözünen maddelerin bu yüzeyde tutunması olayına adsorpsiyon denir. Adsorpsiyon olayında, maddeleri yüzeyinde tutan faza adsorplayıcı, adsorpsiyona uğrayan maddeye ise adsorplanan denir. Tutunan taneciklerin yüzeyden ayrılmasına desorpsiyon denir (Güzel 1991).
Adsorpsiyon olayında adsorlanan ile adsorplayıcı yüzeyi arasında etkili olan kuvvetler incelendiğinde kimyasal, fiziksel ve iyonik adsorpsiyon olmak üzere üç şekilde gerçekleşebilmektedir. Kimyasal adsorpsiyon tanecikler ile yüzey arasında bir kimyasal bağ ve genellikle de kovalent bağ oluşumuyla meydana gelen adsorpsiyon türüdür. Fiziksel adsorpsiyon atom, molekül ya da iyon şeklinde olabilen adsorplanan tanecikler ile katı yüzeyi arasında uzun mesafeli fakat zayıf olan van der waals çekim kuvvetlerinin etkili olduğu adsorpsiyon türüdür (Sarıkaya 2005). Đyonik adsorpsiyon seçimli olarak bir iyonun katı yüzeyine tutulması elektrostatik çekim kuvvetlerinin etken olması ile açıklanır (Savcı 2005; Kabak 2008).
1.1.1. Gaz Adsorpsiyon Đzotermleri
Adsorpsiyon izotermleri, sabit sıcaklıkta adsorplayıcı tarafından adsorplanan madde miktarı ile denge derişimi arasındaki (gaz adsorpsiyonu durumunda denge basıncı) bağıntıya denir. Adsorpsiyon izotermleri genellikle; adsorplayıcı kapasitesi, adsorpsiyon enerjisi ve adsorpsiyonun ne türde olduğu gibi önemli bilgilerin elde edilmesini sağlar (Kertmen 2006). Langmuir, Freundlich, Brunauer-Emmett-Teller (BET) adsorpsiyon izoterm verilerini değerlendirmek içi kullanılan en yaygın izoterm modelleridir.
Langmuir Đzoterm Modeli: Langmuir tarafından 1916 yılında kimyasal adsorpsiyon için basit bir izoterm denklemi türetilmiştir. Tek tabakalı fiziksel adsorpsiyon ve çözeltiden adsorpsiyon için de geçerli olan bu eşitliğe Langmuir denklemi denir. Langmuir izoterm modeline göre katı yüzeyindeki bütün noktalar aynı
3
adsorpsiyon aktivitesine sahiptir. Yüzey homojen enerjiye sahiptir. Adsorplanan moleküller birbirleri ile etkileşim halinde değillerdir. Bu nedenle birim yüzeyde adsorplanmış madde miktarının adsorpsiyon hızına herhangi bir etkisi yoktur. Adsorpsiyon işlemi aynı mekanizmaya göre oluşur ve adsorplanmış kompleksler aynı yapıya sahiptir. Tek tabaka ile sınırlı olan adsorpsiyon sadece yüzeydeki aktif adsorpsiyon bölgelerinde gerçekleştiğinden, adsorpsiyon süreci monomüleküler yapıdadır. Maksimum adsorpsiyon, adsorplayıcı yüzeyine bağlanan moleküllerin doygun bir tabaka oluşturduğu andaki adsorpsiyondur. Desorpsiyon hızı sadece yüzeyde adsorplanmış madde miktarına bağlıdır (Savcı 2005). Langmuir denklemi, katı-gaz sistemleri için çizgisel hali Denk. 1.1'de gösterildiği şekilde ifade edilmektedir:
m m V P b V V P + = 1 (1.1)
Denk. 1.1'e göre P'ye karşı P/V olarak çizilen Langmuir çizgisel grafiğinde Vm ve
b değerleri, sırasıyla eğim ve kayma değerlerinden belirlenir.
Freundlich Đzoterm Modeli: Bu model heterojen yüzeylerdeki adsorpsiyonu ifade eder ve Langmuir modeline göre daha gerçekçidir. Langmuir modeli geliştirilirken, adsorplayıcıların tek tabakaya bağlandığı ve tüm aktif merkezlerin adsorplayıcılara karşı eşit ilgiye sahip oldukları gibi kabuller yapılırken, Freundlich modelinde bu kabullere yer verilmemiş ve denklem deneysel sonuçlardan türetilmiştir. Ancak, bunların dışında Langmuir modeli için yapılan diğer tüm kabuller Freundlich modeli için de geçerlidir (Weber 1972; Yener ve Aksu 1999). Freundlich denkleminin çizgisel şekli Denk. 1.2'de gösterildiği gibi ifade edilmektedir.
P n K V F ln 1 ln ln = + (1.2)
Denk. 1.2'e göre, lnP'ye karşı lnV grafiğinin eğim ve kayma değerlerinden
sırasıyla 1/n ve ܭி değerleri belirlenir. 1/n değerinin 0-1 arasında yer alması adsorpsiyon olayının istemli olduğunu ifade eder. Öte yandan, bu değer sıfıra yaklaştıkça adsorplayıcı yüzeyinin heterojenliğinin artması anlamına gelmektedir. Ayrıca, 1/n değerinin 1'e çok yakın olması Langmuir izoterm modeline de uyumlu olduğunu gösterir (Honga ve ark. 2009).
4
Brunauer-Emmett-Teller (BET) Đzoterm Modeli: Bir adsorplayıcının karakterizasyonunda kullanılan en önemli parametrelerden biri adsorplayıcının yüzey alanı olup Brunauer, Emmett ve Teller tarafından geliştirilen B.E.T izoterm modeli (Brunauer ve ark. 1938) gözenekli katıların özgül yüzey alanlarını belirlemede kullanılır. Bu model, çok tabakalı fiziksel adsorpsiyon için uygulanmakta olup B.E.T. izoterminin çizgisel hali Denk. 1.3'de verilmiştir.
0 0 ) 1 ( 1 ) ( V cP P c c V P P V P m m − + = − (1.3)
Denk. 1.3'e göre P/Po'a karşı P/V(Po-P) grafiğinin eğim ve kayma değerleri
sırasıyla Vm ve c belirlenir.
1.1.2. Gaz Adsorpsiyon-Desorpsiyon Đzoterm ve Histerezis Tiplerinin Sınıflandırılması
Sabit sıcaklıkta adsorplayıcı tarafından adsorplanan madde miktarı ile denge basıncı arasında bağıntıya adsorpsiyon izotermi denir. Adsorplanan gaz miktarı genellikle standart (0 oC, 1 atm) koşullardaki hacim ile basınç ise ölçüm sıcaklığındaki bağıl basınç (P/Po) ile ifade edilir. Bağıl basınca karşı ölçülen adsorplanan desorplanan
gaz hacmi değerleri grafiğe geçirildiğinde adsorpsiyon desorpsiyon izotermleri elde edilir. Bu ölçümler genellikle sıvı azotun kaynama sıcaklığında (77 K) gerçekleştirilir (Sayğılı 2015).
Gaz-katı dengesi için adsorpsiyon izotermleri ilk olarak 5 tip olarak sınıflandırılmıştır. B.D.D.T sınıflandırması (Brunauer ve ark. 1940; Brunauer 1943) olarak bilinen bu sınıflandırmaya daha sonra Sing tarafından bir izoterm tipi daha dahil edilmiştir. Böylece IUPAC sınıflandırması 6 tip adsorpsiyon izotermi tanımlanmıştır (Gregg ve Sing 1982; IUPAC 1985; IUPAC 1994; Webb ve Orr 1997). Bu izotermler tipleri Şekil 1.1'de verilmiştir.
5
Şekil 1.1. Adsorpsiyon ve Desorpsiyon Đzotermlerinin IUPAC Sınıflandırılması
Tip I: Genellikle Langmuir izoterm tipi olarak bilinir. Çok ince gözenekli yapıda olan bir katıdaki fiziksel ve kimyasal adsorpsiyon izotermlerin yaklaşık biçimidir.
Tip II: Gözeneksiz veya makrogözeneklere sahip katılara özgü izoterm tipidir. Çok tabakalı adsorpsiyonu belirtir. B.E.T.izotermleri tip II biçimindedir.
Tip III: Bu izoterm tipi, adsorpsiyon ısısının yoğunlaşma ısısına eşit ya da daha küçük olduğu durumlarda görülür. Diğer izoterm türleriyle karşılaştırıldığında daha az rastlanır.
Tip IV: Đzotermin başlangıç kısmında gözeneksiz bir katı için Tip II izotermi gibi aynı yolu izler. Doygunluk basıncına yakın bir bölgede ise basınç eksenine paralel seyreder.
Tip V: Diğer izoterm tipleri arasında yorumlanması en zor olan izoterm tipidir. Tip III izotermi gibi adsorplayıcı- adsorplanan ilgisi zayıftır.
Tip VI: Düzgün bir katı yüzeyi üzerinde basamaklı çok tabakalı adsorpsiyonun biçimidir (Güzel 1991).
Fiziksel adsorpsiyon izotermlerinin çok tabakalı olduğu aralıkta görülen histerezis, genellikle mezogözenekli yapılardaki kapiler yoğunlaşma ile ilgilidir. Histerezis eğrisi ve mezogözenekli adsorplayıcıların doğası (ör: gözenek boyut dağılımı ve gözenek geometrisi vb.) arasında bir ilişkinin var olduğu yaygın olarak kabul
6
görmektedir. Histerezis ilmekleri çeşitli şekillerde olabilmektedir. Histerezis ilmekleri, IUPAC tarafından H1, H2, H3 ve H4 olarak verildiği gibi sınıflandırılmıştır (Şekil. 1.2).
Şekil 1.2. IUPAC’ın Histerezis Sınıflandırması
Bu sınıflamada H1 ve H4 ilmekleri iki uç tip olmaktadır. H1 tipinde adsorpsiyon ve desorpsiyon kolları hemen hemen düşeyken, H4 tipinde ise kollar yataydır ve geniş P/Po aralığı boyunca paraleldir. Bazı açılardan H2 ve H3 tipi ilmekler, bu iki uç
arasındaki ara durumu göstermektedir. Daha düşük kapanma noktasına yol açan desorpsiyon kolu üzerinde dik bir bölgenin bulunması, pek çok histerezis ilmeği için geçerli olan ortak bir özelliktir. Bu durum gözenekli adsorplayıcının doğasından bağımsız olup büyük ölçüde adsorplananın doğasına bağlıdır. H1 tipi, iyi tanımlanmış silindir biçimli gözenek kanalları ya da yaklaşık olarak tekdüze olan kürelerin yoğun bir dağılımını içeren ve bu nedenle dar gözenek boyut dağılımına sahip gözenekli malzemelerle ilişkilidir. H2 tipi histerezis veren inorganik oksit jeller ve gözenekli camlar gibi pek çok gözenekli adsorplayıcı, çoğunlukla düzensiz bir yapıya sahip olup gözenek şekli ve boyut dağılımı iyi derecede tanımlanmamıştır. H3 tipi histerezis veren izotermler, dar ve uzun biçimli gözeneklerden sorumlu olan levhaya benzer parçacıkların gevşek olan kümelenmesi durumunda gözlenir ve yüksek P/Po'da herhangi
bir limit adsorpsiyon göstermemektedir. H3 tipi histerezisin desorpsiyon kolu histerezis ergisinin kapanışı ile ilgili olarak dikey bir bölgeye sahiptir. Bu olay 77 K'de ve 0.40-0.45 bağıl basınç aralığında azot deneylerinde gözlemlenmektedir. Benzer şekilde, H4
7
tipi eğriler dar ve uzun biçimli gözeneklerle ilişkilidir. Ancak burada mikrogözenek bölgesindeki gözenekleri de içermektedir.
Aktif karbon üzerine azot adsorpsiyonu H4 tipi histerezis göstermektedir. Histerezis eğrilerinde kesikli çizgilerle gösterilen bölgeler, düşük bağıl basınçlarda gözlenebilen histerezisi göstermektedir. Düşük basınçlı histerezis, esnek gözeneklerin şişmesi veya adsorplananın boyutuyla aynı genişliğe sahip gözenekler içerisinde tersinir olmayan tutma nedeniyle adsorplayıcının hacmindeki değişim ile ilgili olabilmektedir. Düşük basınçlı histerezis gösteren adsorpsiyon izotermlerinin yorumlanması oldukça zordur ve hassas bir gözenek boyut dağılımı mümkün olmamaktadır (Sing ve ark. 1985; Lowell ve ark. 2006).
1.2. Çözeltiden Adsorpsiyon
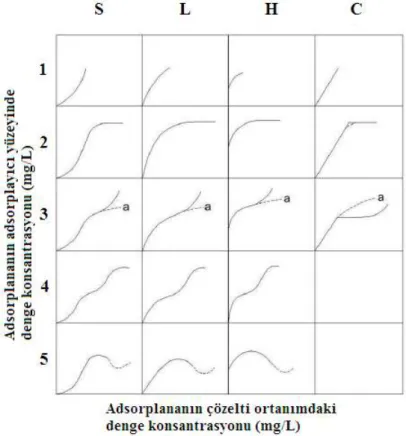
Çeşitli adsorpsiyon izotermlerini inceleyen Giles ve arkadaşları (Giles ve ark. 1974), izoterm eğrisinin başlangıç eğimine dayanan bir sınıflandırma oluşturmuştur. Giles sınıflandırmasında 4 tip izoterm mevcuttur ve bunlar S, L, H ve C tipi izotermlerdir. Her bir izoterm tipi de kendi içinde alt sınıflara ayrılmaktadır (Şekil 1.3).
8
S Tipi: Adsorpsiyonda adsorplanan molekülleri arasındaki çekim kuvvetleri, adsorplanan ve adsorplayıcı arasındaki çekim kuvvetine neredeyse eşittir. Bu halde, birbirine bağlanarak bir yapı oluşturan adsorplanan moleküllerinin yüzeydeki adsorpsiyonu, tek başına bir adsorplanan molekülünün adsorpsiyonundan kararlıdır. Adsorpsiyonda adsorplanan molekülünün tutulduğu yüzey alanları arttığından, izotermin başlangıç eğimi derişimle artmaktadır. S tipi bir izoterm oluşabilmesi için adsorplanan molekülleri arasındaki çekim kuvvetli olmalı, çözücü kuvvetle adsorbe ediliyor olmalı ve adsorplanan molekülü mono fonksiyonel olmalıdır.
L Tipi: Adsorplanan ve adsorplayıcı arasında oldukça güçlü bir çekme kuvveti varken adsorplanan moleküllerinin arasında çok zayıf bir çekme kuvveti vardır. Adsorplanan moleküllerin adsorplayıcı yüzeyine yüksek ilgisi söz konusudur. Artan derişimle birlikte adsorplanan moleküllerin adsorplayıcı yüzeyinde boş alanlar bulması zorlaştığından başlangıç eğimi çözeltideki madde derişimi ile sabit bir azalma gösterir.
H-Tipi: L tipinin özel bir şeklidir. Adsorplanan ve adsorplayıcının çok seyreltik çözeltilerde bile birbirlerine yüksek ilgisi söz konusudur. Bu nedenle izotermin başlangıç kısmı dikeydir. Adsorplanan türler iyonik miseller ya da polimerik moleküller gibi genelde büyük birimlerdir. Fakat bazen bu adsorplanmış türlerin yüzeye çok daha düşük ilgi gösteren diğer türler ile değişilen tek iyonlar olduğu da görülür.
C Tipi: Eğri orijinden geçer. Çözeltide ortamında kalan bileşiğin derişimi ve adsorplanan miktar arasında sabit bir oran söz konusudur.
Giles izotermlerinde; 1 numaralı alt grup, adsorplanan tek tabakasının henüz tamamlanmadığını, 2 ve 2'nin üzerindeki alt gruplardaki dönüm noktasının sonundaki düzlük, adsorplanan tek tabakasının tamamlandığını belirtir. Bunu takiben meydana gelen artış ikinci bir adsorplanan tabakasının oluştuğunu (alt grup 3), ikinci tabakadan sonra oluşan düzlük ise bu tabakanın da tamamlandığını (alt grup 4) gösterir. Adsorpsiyon sırasında, üçüncü ya da üçten fazla adsorplanan tabakaların oluşup tamamlanmasıyla 5 numaralı alt grup izotermi uygunluk olmakta ancak pratikte böyle durumlara sık rastlanmaktadır. Đkinci adsorplanan tabakası, adsorplanan moleküllerin, adsorplayıcı yüzeyinde kalan boşluklara diğer adsorplanan moleküllerinin etkisiyle çekilmeleriyle oluşmaktadır (Özgen 2004).
9
Çözeltiden adsorpsiyona etki eden başlıca parametreler; ortam pH'sı, adsorplayıcı ve adsorplanan maddelerin özellikleri, adsorplayıcı dozu, adsorplananın başlangıç derişimi, yabancı iyon, temas süresi ve sıcaklık olarak sıralanabilir. Bu parametreler, adsorpsiyon hız ve dengesi üzerinde önemli rol oynarlar.
1.2.1. Çözeltiden Adsorpsiyonda Kinetik Modelleme
Kinetik çalışma, adsorplananın uzaklaştırılma hızını, uzaklaştırılma için kalan süreyi ve adsorplanma mekanizmasını belirleyen önemli bir adsorpsiyon işlemidir (Güzel ve ark. 2014). Adsorpsiyon kinetiği, adsorplananın adsorplayıcı yüzeyine adsorpsiyonu sırasında ne tür bir mekanizmanın etkin olduğunu belirlemek için kullanılmaktadır. Ayrıca, adsorpsiyon hızı, adsorplayıcı seçiminde önemli bir faktördür (Akkaya ve Güzel 2014). Bu amaçla çeşitli kinetik modelleri ileri sürülmüştür. Bu modellerden en yaygın olarak kullanılanlar; Lagergren (Yalancı Birinci Mertebe) (Lagergren 1898) ve Ho-Mckay (Yalancı Đkinci Mertebe) (Ho ve McKay 1999) kinetik modelleridir. Bu kinetik modellerin, çizgisel şekilleri sırasıyla Denk. 1.4 ve 1.5'de verilmiştir. Lagergren: qe qt qe k t 303 . 2 log ) log( 1 − = − (1.4) Ho-McKay: t q q k q t e e t 1 1 2 2 + = (1.5)
Denk.1.4 ve Denk.1.5'e göre çizilen çizimlerden sırasıyla k1 ve qe ile k2 ve qe
belirlenmektedir.
Kinetik modelleme genellikle yüksek korelasyon katsayısı (R2) ile dengede hesapla belirlenen adsorplanan miktar (qe,h) ve deneysel olarak belirlenen adsorplanan
miktar (qe,d) değerlerinin uyumluluğuna göre belirlenmektedir.
1.2.2. Çözeltiden Adsorpsiyonda Đzoterm Modelleme
Adsorpsiyon izotermi, adsorplanan bir maddenin adsorplanan miktarı ile onun denge derişimi arasındaki ilişkiyi yansıtması yanı sıra, adsorplayıcı ve adsorplanan arasındaki ilişki hakkında önemli bilgiler vermektedir (Ahmed ve Theydan 2013). Çözeltiden adsorpsiyonda izoterm verilerinin, gaz adsorpsiyonu için sıkça kullanılan Langmuir ve Freundlich çözeltiden adsorpsiyona uyarlanmasıyla elde edilen Denk. 1.6
10
ve Denk. 1.7'deki çizgisel izoterm denklemlerinde değerlendirilip, elde edilen R2 değerlerinden, söz konusu adsorplayıcı-adsorplanan sistemine ilişkin uygun izoterm model tespiti yapılır.
Langmuir: m e m e e q C b q q C + = 1 (1.6) Freundlich: e F Ce n K q ln 1ln ln = + (1.7)
Çözeltiden adsorpsiyonda, adsorplayıcı-adsorplanan sisteminin uygunluğu, sisteme ilişkin Langmuir çizgisel izoterminden belirlenen b sabitinden yararlanarak hesaplanan boyutsuz ayırma faktörü RL parametresi (Denk. 1.8) aracılığıyla da tespit
edilmektedir. o L bC R + = 1 1 (1.8)
RL değerinin 1'den büyük çıkması durumunda adsorpsiyonun elverişsiz, 1'e eşit
olması durumunda doğrusal, 0 ile 1 arasında bir değer olması durumunda istemli (kendiliğinden gerçekleşen) ve 0 olması durumunda ise tersinmez olmaktadır (Annadurai ve ark. 2008).
1.2.3. Çözeltiden Adsorpsiyon Termodinamiği
Çözeltiden adsorpsiyonda, ∆Go, ∆Ho ve ∆So termodinamik parametreler süreci anlamak için önemli bilgiler vermektedir. Literatürlerde adsorpsiyonun gerçekleşebilmesi için gerekli olan enerjilerin farklı iki yolla hesaplanabildiği ifade edilmektedir:
1. Adsorpsiyonda, adsorplanan madde birikimi ile daha düzenli hale geçildiği için entropi azalmaktadır. Adsorpsiyonun kendiliğinden gerçekleşebilmesi için aşağıdaki temel termodinamik eşitliğine göre adsorpsiyon olayının ekzotermik olması gerekmektedir (Singh ve Pant 2003; Nollet ve ark. 2003).
L o K RT G =− ln ∆ (1.9)
11 RT H R S K o o L ∆ − ∆ = ln (1.10)
Burada ܭ = ݍܾ'dir. ∆Go ile ∆Ho ve ∆So termodinamik parametreleri sırasıyla
Denk. 1.9 ve Denk. 1.10'den belirlenir.
2. Adsorplanan maddenin adsorpsiyon davranışı Langmuir adsorpsiyon izoterminden de hesaplanabilmektedir. ∆Go, ∆Ho ve ∆So aşağıdaki şu denklemlerden hesaplanabilmektedir (Liu ve ark. 2001):
RT H b b o ∆ − =ln ' ln (1.11) RT G b o ∆ − = ' ln (1.12) T G H S o o o ∆ −∆ = ∆ (1.13) R S b o ∆ = (1.14)
Adsorpsiyonun endotermik olduğu bir durumda ∆Ho pozitif, ekzotermik olduğu bir durumda ∆Ho negatif bir değer alır. ∆Go'nin negatif değerleri adsorpsiyonun kendiliğinden gerçekleştiğinin bir göstergesidir. ∆So'in negatif değeri çözünen-çözelti ve adsorplayıcı-çözünen faz ara yüzeylerindeki adsorplanan derişiminde azalmayı göstermekte olup, aynı zamanda katı faz üzerinde adsorplanan derişimin arttığını belirtmektedir. ∆So'in pozitif değeri ise katı-çözelti ara yüzeyindeki rastlantısallığın artığını göstermektedir (Goswami ve Ghosh 2005). Ayrıca ∆Ho ve ∆Go termodinamik parametreleri, adsorpsiyon mekanizması hakkında da bilgi vermektedir. Literatürlerde,
∆Ho değeri 84 kJ/mol'den küçükse olay fiziksel adsorpsiyon; 84 kJ/mol'den büyükse olayın kimyasal adsorpsiyon mekanizması üzerinden yürüdüğü ifade edilmektedir (Faust ve Alg 1987). ∆Go değerlerinin ise -20 ve 0 kJ/mol arasında olması, adsorplanan birimler ile adsorplayıcıdaki aktif merkezler arasındaki elektrostatik etkileşime dayanan fiziksel adsorpsiyon olduğunu ifade eder. -80 ve -400 kJ/mol arasında olması, adsorplanan birimler ile adsorplayıcı yüzeyindeki aktif merkezler arasında yük paylaşımı veya transferi sonucu oluşan kimyasal bağlanmaya dayanan kimyasal adsorpsiyon olduğunu ifade edilmektedir (Jaycock ve Parfitt 1981).
12 1.3. Adsorplayıcılar
Adsorplayıcılar, mineral, organik ya da biyolojik temelli olabilmektedir. Aktif karbonlar, zeolitler, killer, silika yataklar, tarımsal atıklar, endüstriyel yan ürünler, bioyokütleler, polimerik materyaller (organik polimerik reçineler ve makroporoz çapraz bağlı polimerler) yaygın olarak kullanılan adsorplayıcılardır (Crini 2005).
1.3.1. Aktif Karbon Hakkında Genel Bilgiler
Yüksek karbon içeriğine sahip maddelere uygulanan aktivasyon işlemi ile iç yüzey alanı ve gözenek hacmi oldukça geliştirilmiş yapılar aktif karbon (AK) olarak adlandırılır. Bu yapıları ifade eden herhangi bir kimyasal formül bulunmamaktadır. AK'nun genişletilmiş yüzey alanı, mikrogözenekli yapısı, yüksek adsorpsiyon kapasitesi ve yüzey reaktivitesi eşsiz bir adsorplayıcı olarak kullanılmasını sağlar. Organik esaslı AK; bileşim olarak % 87-97 oranlarında karbon içermekte olup geri kalan oranlarda ise hidrojen, oksijen, kükürt ve azot içerebilir. Ayrıca kullanılan hammaddeye ve işleme katılan diğer kimyasal maddelerin içeriğine bağlı olarak farklı element içerebilmektedir (Akyıldız 2007).
AK'nun adsorplayıcı özelliği ilk çağdan beri bilinmektedir. Hippocrates kötü kokuların giderimi için odun kömürü tozu kullanılabileceğini ileri sürmüştür. Đsveçli Kimyager Karl Wilhelm Scheele tarafından endüstriyel amaçlı aktif karbon kullanımı 18.yy sonlarında gazların odun kömürü kullanılarak adsorpsiyonu ile başlatılmıştır. Daha sonra ise Rus akademisyen Lovits'in organik madde içeren tartarik asit çözeltisinin rengini gidermek için odun kömürü kullandığı görülmektedir. Sanayi uygulaması 1794 yılında Đngiltere’de şeker sanayisinde renk giderici olarak kullanılması ile başlanmıştır (Küçükgül 2004).
AK'lar kullanım alanlarına göre farklı şekillerde üretilmektedir. Bunlar toz; sıvı faz uygulamalarında ve baca gazı arıtımında, granül; sıvı ve gaz adsorpsiyon uygulamalarında, pellet aktif karbon; gaz fazı uygulamalarında, bunların dışında fibröz ve küresel olarak üretilebilmektedir.
AK hammaddesi olarak kullanılacak maddelerin karbon içeriğinin yüksek olması, ucuz olması ve safsızlık içermemesi önem arz eden parametreleridir. Bu nedenle, AK üretiminde birçok madde kullanılmaktadır. Bunlar arasında mısır
koçanı-13
mısır sapı, içki imalathanesi atığı, hindistan cevizi kabuğu, kemik, pirinç kabuğu, kösele atığı, fındık kabuğu, deniz yosunu, şeker kamışı, talaş, kömür, tahıl kabukları, meyve kabukları, meyve çekirdekleri, odun, linyit, lignin ve daha birçok madde bulunmaktadır.
AK'un en önemli fiziksel özelliği yüksek iç yüzey alanı ve hacme sahip olmasıdır. Aktif karbonun yüzey alanı BET yöntemi ile belirlenir. Bu yöntemde adsorplanan madde olarak genellikle azot ya da helyum gazları kullanılır. BET, gazların katı malzemelerin yüzeylerine fiziksel adsorpsiyon karakteristiğini kullanarak yüzey alanı hakkında bilgi veren bir yöntem olup, gazın bir katı yüzeyinde tek tabakalı fiziksel adsorpsiyonunu temel alır. Farklı basınçlarda katı numune yüzeyine adsorbe olan gaz karışımı miktarlarından sonuca gidilir. BET cihazından numunenin gözenek hacmi, gözenekliliği ve aktif yüzey alanı hakkında detaylı bilgiler elde edilebilmektedir. Tipik ticari ürünler 500-2000 m2/g aralığında yüzey alanına sahiptir. Bununla beraber 3500-5000 m2/g yüzey alanlı ve sentetik orijinli AK'lar ise yüksek adsorpsiyon kapasiteleri nedeniyle özel amaçlı kullanılmaktadır (Kroschwitz 1992; Gündoğdu 2010).
AK'un diğer önemli bir özelliği ise gözenek yapısıdır. Girinti çıkıntılar, kanallar, boşluklar veya yarıklar içeren herhangi bir katı materyal gözenekli kabul edilir. AK oluşumu sırasında; karbonizasyon sıcaklığını artması ile öncelikle H2O, CO2, CH4,
CH3OH gibi küçük moleküller uzaklaşmaktadır. Bu sırada çıkan küçük moleküller
yerine mikrogözenekler oluşmaktadır. Gaz halinde uzaklaşan maddeler ise katı faz içinde artan basınçları sebebiyle mikro kanallar açarlar. Bu esnada çapraz bağlı selülozik ana yapı asla bozulmamaktadır. IUPAC (The International Union of Pure and Applied Chemistry) tarafından, adsorblayıcılar için gözenek büyüklüğünü yarıçaplarına göre üçe ayırmıştır (Sing ve ark. 1985).
1) Makro gözenekler ( r > 50 nm ) 2) Mezo gözenekler ( 2 < r < 50 nm ) 3) Mikro gözenekler ( r < 2 nm )
a) Süper- mikro gözenekler ( 1 < r < 2 nm ) b) Ultra- mikro gözenekler ( r < 0.5 nm )
14
AK'un adsorplama kapasitesi sadece gözenek yapısı ile değil, ayrıca yüzeyin kimyasal doğasıyla da ilgilidir. AK'un yapısında tek atomlar veya fonksiyonel gruplar halinde birçok heteroatom (oksijen, hidrojen, azot ve diğerleri) bulunur. Oksijen, karbon matriksindeki en baskın heteroatomdur (El-Hendawy 2005). Karbon-oksijen yüzey bileşikleri, aktif karbonun yüzey reaksiyonlarını ile yüzey davranışlarını etkileyen en önemli merkezlerdir. Sulu çözeltide karbon taneciklerinin yüzey yükü, yüzey fonksiyonel grupların doğası tarafından kontrol edilir. Yani, AK'un adsorpsiyon özellikleri yüzey gruplarının modifikasyonuyla kontrol edilebilir. AK'un yapısındaki grafit kristalitlerinin kenar bölgelerine oksijen içerikli doymamış karbon grupları bağlıdır. Aktif karbonda bulunan başlıca fonksiyonel gruplar Şekilde 1.4. gösterilmiştir. Bu gruplar hem önemli reaksiyon merkezleri görevi yapmakta ve hem de aktif karbonun polaritesini artırmaktadır. Bu yüzey oksitleri arasında en sık rastlananlar; karboksil grupları, fenolik gruplar, lakton halkaları, kinon türünden yapı taşları, siklik peroksitler ve karboksilik asit anhidritleridir (Strelko ve ark. 2002). AK'un IR temelli spektroskopik yöntemle hem asidik hem de bazik özellikler sergilediği çok uzun yıllardır bilinmektedir. Asidik özellikler, fenolik ve karboksilik asit gruplarının varlığı ile açıklanabilir. Fakat bazik karakteri açıklamak çok daha zordur (Rouquerol ve ark. 1999).
15
Değişik karakterli AK'ların elde edilmesi, üretimi sırasında uygulanan aktivasyon yöntemine ve kullanılan hammaddenin fiziksel ve kimyasal yapısına bağlıdır (Lua ve Yang 2004). AK üretiminde, fiziksel ve kimyasal aktivasyon olmak üzere, iki temel yöntem kullanılmaktadır. Fiziksel aktivasyonda hammadde, yüksek sıcaklıklarda karbonize edilir ve hazırlanan su buharı ya da karbondioksit (CO2) ile aktive edilir.
Karbonizasyon işlemi sırasında uçucu maddelerin uzaklaşması ile gözenekli bir yapı elde edilir. Bu gözenekli yapı aktivasyon işlemi esnasında su buharı ya da CO2
reaksiyona girerek aktif karbon oluşur. Kimyasal aktivasyonda ise kullanılacak hammadde aktivasyon kimyasalı ile emdirme işlemine tabi tutulur inert bir atmosferde yüksek sıcaklıklara kadar ısıtılır. Bu yöntemde karbonizasyon ve aktivasyon basamakları aynı anda gerçekleşir. Su uzaklaştırma ve kimyasalların yükseltgenme tepkimeleriyle gözenekler oluşur. AK üretimi için H3PO4, H2SO4 gibi asitler ile NaCl,
ZnCl2, CuCl2, CaCl2, FeCl2, AlCl3, MgCl2, NH4Cl gibi metal ve ametal klorürler, KOH,
NaOH gibi metal hidroksitler ve K2CO3, Na2CO3 gibi metal karbonat bileşikleri gibi
çok çeşitli aktivasyon kimyasalları kullanılabilir (Hayashi ve ark. 2002).
AK çok sayıda mikro gözenek ve geniş yüzey alanına sahip olduğundan adsorplama yeteneği çok yüksektir. Gaz ve sıvı adsorpsiyon uygulamalarında çok önemli bir yere sahiptir. Bu nedenle gazların sıvılaştırılmasında, koku giderilmesinde, tıbbı uygulamalarda, farmakolojide, gıda sanayinde ve daha birçok yerde kullanılmaktadır.
AK'lar, sulu çözeltilerden fenollerin, ağır metallerin, boyaların ve metal iyonlarının uzaklaştırılmasında kullanılmaktadır. Fenolik bileşikler çevre kirliliğinde etkili olan maddelerdendir. Bu bileşiklerin çok düşük derişimde bile, su kullanımı için engel oluşturmaktadır. Fenoller içme suyunda hoş olmayan tat ve kokuya neden olurlar. Fenolik bileşikler, plastikler, yapıştırıcılar, kompozit malzemeler gibi birçok maddenin üretiminde kullanılırlar. Bu maddelerin bozunması ile fenoller ve türevleri çevreye yayılır ve çevre kirliliğine neden olurlar. Çevre kirliliğine neden olan maddeler aktif karbon ile uzaklaştırılabilir (Ioannidou ve Zabaniotou 2007). Daha geniş kullanım alanları Çizelge. 1'de verilmiştir (Hassler 1967; Bansal ve ark. 1988).
16
Çizelge 1.1. Aktif Karbonun Gaz ve Sıvı Faz Uygulamaları Endüstri
Tanımı Tipik kullanımı
Gaz Fazı Uygulamaları Çözücü geri kazanımı Đşlemin ekonomisini optimize
etmek ve buhar emisyonlarının kontrolü için organik çözeltilerin geri kazanımı
Asetat fiberler (aseton), eczacılıkla ilgili uygulamalar (metilen klor), film kaplama ve boya (etil asetal), manyetik bant Karbondioksit Fermantasyon işlemlerinde
karbondioksit saflaştırılması
Aminlerin, merkaptanların ve alkollerin adsorpsiyonu
Endüstriyel havalandırma Organik buharların adsorpsiyonu Atık imha Evsel, kimyasal ve klinik
atıkların yüksek sıcaklıkta yakarak imhası
Baca gazlarından dioksinlerin ve ağır metallerin uzaklaştırılması Sigara Ağızlıkta toz ve tanecikli filtreler Tadı ve kokusunun kontrolü veya
sigara dumanındaki zararlı elementlerin bazılarının ekstraksiyonu (özütlemesi) Şartlandırma Isıtma ve havalandırma Havaalanları, ofisler Kompozit fiberler Köpük / lifli bileşenler içinde toz
aktif karbonun emprenyesi
Gaz maskeleri, suyun işlenmesi, ayakkabı içi koku gidericileri Koku gidericisi Đstenmeyen kokuların giderilmesi Filtre birimleri
Sıvı Faz Uygulamaları Đçilebilir su işlemleri Tanecikli aktif karbon filtreleri
kullanımı
Organik bileşiklerin uzaklaştırılması, kötü koku ve tadın giderilmesi
Alkolsüz içecekler Đçilebilir su işlemleri, klor ile sterilizasyon
Organik bileşiklerin uzaklaştırılması ve klorun giderilmesi
Altının geri kazanımı Cevher özütleme işlemleri Sodyum siyanürde çözünmüş altının geri kazanımı
Petrokimya Kullanılan buharın temizlenmesi Yağ ve hidrokarbonların uzaklaştırılması
Yer altı suları Yeraltı sularındaki istenmeyen maddelerin uzaklaştırılması
Kloroform, tetrakloroetilen ve trikloretan içeren adsorplanabilir organik halojenlerin ve toplam organik halojenlerin azaltılması Endüstriyel atık sular Çıkan suların çevre için uygun
hale getirilmesi
Biyolojik oksijen içeriğinin, kimyasaloksijen içeriğinin ve toplam organik halojenlerin azaltılması
Yüzme havuzları Organik içeriklerin
uzaklaştırılması için ozon enjektesi
Halojenlerin azaltılması, yüzme havuzları, organik içeriklerin uzaklaştırılması için ozon enjektesi, kloramin seviyesinin
17
kontrolü ve kalan ozonun uzaklaştırılması
Yarı iletkenler Kloramin seviyesinin kontrolü ve kalan ozonun uzaklaştırılması, yarı iletkenler, yüksek saflıkta su
Toplam organik karbonun azaltılması
Alkoller Đçilebilir su işlemleri Fenol ve trihalometanların uzaklaştırılması
1.4. Çalışmada Aktif Karbon üretiminde Kullanılan Hammadde ve Adsorplananlar Hakkında Genel Bilgiler
1.4.1. Mandalina Kabukları
Mandalina (Citrus reticulata), ılıman iklimde yetişmekte olan turunçgiller
(Rutaceae) familyasına ait bir meyve türüdür (tr.wikipedia.org/wiki/Mandalina). Ilıman
iklime sahip bütün ülkelerde çeşitli kültür şekilleri yetiştirilen, yaprak dökmeyen küçük ağaçlara sahip, yaprak ve kabuk gibi kısımlarında uçucu yağ içeren turunçgillerden bir meyve türüdür. Gıda ve Tarım Örgütü'nün 2012 yılı verilerine göre Dünya'da 21 milyon ton mandalina üretilmektedir. En çok mandalina üreten ülkeler Çin, Đspanya, Brezilya, Türkiye, Đtalya, Mısır, Japonya ve Güney Kore'dir. Türkiye yaklaşık 872 bin ton üretimiyle dünya mandalina üretiminde %4'lük pay ile dördüncü sıradadır.Mandalina turunçgil üretimimizin % 25'ini oluşturmaktadır. Mandalina kabuğu soyulduktan sonra yenebildiği gibi suyu sıkılarak da içilebilir. Meyve suyu fabrikalarında kullanıldığında, ağırlığının yaklaşık %48'ü posa olarak çevreye atılmaktadır. Bu atıklar, genellikle gübre, hayvan yemi ve katı yakıt olarak kullanılmaktadır (FAO 2012).
1.4.2. Adsorplananlar 1.4.2.1. Metilen Mavisi
Metilen mavisi (MM), kimyasal formülü, C16H18ClN3S.3H2O
(3,7-bis(dimetilamino)-fenazotiyonyum klorür) olan, suda (4 g/L), etanolde ve kloroformda kolay çözünen, suyu kuvvetle tutma özelliği olan koyu mavi renkte bir boyarmaddedir. MM boyarmadde olarak difteri bakteri hücrelerini ve sinir dokusunu boyamak için kullanılabildiği gibi, pamuğu saf mavi tona boyamak için de kullanılabilir. MM zayıf bir antiseptiktir, fakat diğer antiseptik karışımlarıyla birlikte çok etkilidir. MM'nin redoks indikatörü olarak kullanımı oldukça yaygındır. Süt analizlerinde redoks indikatoru olarak ve Au, B, Bi, Ce, Cu, Ga, Ge, Hg, In, Sb, Se, Sn, Tl, U, Zn, Pb, Fe,
18
Cr, Ti,V, Mo, Sn ve çözünmüş O2 belirlenmesinde titrant veya indikator olarak
kullanılmaktadır. Özellikle tekstil sektöründe ve yukarıda bahsedilen alanlardaki kullanımı nedeniyle atıksularda metilen mavisine sıkça rastlanmaktadır (Yaşar ve Özcan 2004). MM'ne maruz kalındığında gözde yanmalar meydana gelebilir, yutulduğunda gastrointestinal sisteme (mide-bağırsak sistemi) ishal ve bulantı oluşumuna sebep olacak şekilde zarar verir. Dahası uzun süreli solunduğunda, methemoglobinemi, siyanoz (morarma hastalığı), konvülsiyon (kasılma hastalığı), dispnesi (nefes darlığı) gibi hastalıklara neden olmaktadır (Tan ve ark. 2008).
1.6.2.2. Metanil Sarısı
Metanil sarısı (MS) , kimyasal formülü C18H14N3NaO3S olan yaygın olarak ipek,
kağıt, deri, boyanması kullanılan asidik bir boyar madde boyar maddedir.Bu nedenle, bir çok sanayi atıksularda bulunabilir ve çevreye çok tehlikeli olabilir. MS insan vücudunda tümör, bağrısak ve enzimatik rahatsızlıklara neden olabilir(Ramachandani ve ark. 1997).
19 2. ÖNCEKĐ ÇALIŞMALARI
Lafi, meşe palamudu ve zeytin küspesi kullanarak %85'lik H3PO4 ile 2 gün
impregnasyondan sonra ve 400-800 oC'de 1 saat karbonizasyon sonucu Metilen mavisi adsorpsiyon kapasitelerini sırasıyla 127.5 ve 112 mg/g olarak bulmuştur (Lafi 2001).
Srinivasakannan ve Bakar, %60'lık H3PO4 ile Kauçuk ağacı atıkları emdirmeden
sonra, 950 oC de karbonizasyon işlemi ile 1492 m2/g yüzey alanına sahip aktif karbon hazırlamışlardır (Srinivasakannan ve Bakar 2004).
Diaz ve çalışma arkadaşları, kestane, ceviz ve sedir ağacının hammadde olarak kullanarak, H3PO4 ile 5 oC/dk ısıtma hızı, 450 oC'de 4 saat süre ile N2 atmosferinde
aktivasyon işlemi gerçekleştirmişlerdir. Bunun sonucunda, düşük (%36) emdirme oranı ile gerçekleştirilen deneylerden elde edilen aktif karbon numunelerinde daha yüksek yüzey alan ve mikrogözenek yapının elde edildiğini belirlemişlerdir. % 85'lik H3PO4
gerçekleştirilen emdirme işleminde ise heterojen bir gözenek boyut dağılımı belirlemişlerdir. Bunun nedeni olarak geniş boyutlu gözenek yapısını oluşturma yeteneğine sahip polifosforik asitlerin varlığını gösterilmişlerdir (Diaz ve ark. 2004).
Serrano ve arkadaşları, kestane ağacı kullanarak H3PO4 derişimi, impregnasyon
süresinin yüzey özellikleri ve farklı aktivasyon sıcaklığı gözenek boyut dağılımına etkisini incelemişlerdir. Yapılan çalışma sonucunda, 500 oC'ye kadar BET yüzey alan artar iken 735-783 m2/g 600 oC'de BET yüzey alan 551- 658 m2/g azalmıştır (Serrano ve ark. 2005).
Attita ve arkadaşları, şeftali çekirdeğinden H3PO4 kullanarak kimyasal
aktivasyon metoduyla çeşitli H3PO4 derişimlerinde (%30-70) 500 oC'de aktif karbon
üretmişlerdir. Elde edilen aktif karbonlarda emdirme oranının artmasıyla yüzey alanının arttığı ve en yüksek yüzey alanının 1400 m2/g, gözenek hacminin 0.83 mL/g olduğu tespit edilmişlerdir. Genellikle üretilen karbonların mikrogözenekliliğe sahip olduğu görülmüştür. Artan derişimlerle elde edilen aktif karbonlarda göre gözenek boyutunun attığı, toplam yüzey alanının azaldığı görülmüştür. Aynı zamanda elde edilen aktif karbonlar metilen mavisi adsropsiyon çalışmalarında değerlendirilmiştir. Emdirme oranın artmasıyla adsorpsiyon kapasitesinin (198-412 mg/g) arttığı belirtilmiştir (Attita ve ark. 2006).
20
Corcho-Corral ve arkadaşları, asma sürgünleri hammadde olarak kullanarak %60'lık H3PO4 ile 25, 50 ve 85 oC'de 2 saat emdirme ile 150-5500 oC'de karbonizasyon
koşullarında 804-1666 m2/g elde etmişler (Corcho-Corral ve ark. 2006).
Duman ve arkadaşları, çam kozalağından H3PO4 ve ZnCl2 kullanarak kimyasal
aktivasyonla aktif karbon üretmişler ve karakterize ettikten sonra adsorpsiyon performanslarını sulu çözeltiden fenol, metilen mavisi ve Cr(VI)'nın uzaklaştırılmasını incelemişlerdir. Aktif karbonların yüzey özelliklerinin kimyasal aktivatör miktarının artmasıyla geliştiği tespit etmişlerdir. H3PO4 ve ZnCl2 aktivasyonu ile sırasıyla 1597
m2/g ve 1823 m2/g BET yüzey alanlı aktif karbonlar elde etmişler. ZnCl2 ile elde edilen
aktif karbonun sulu çözeltiden fenol, metilen mavisi ve Cr(VI) için adsorpsiyon kapasitelerini de sırasıyla 117.65, 370.37 ve 66.87 mg/g olarak bulmuşlar (Duman ve ark. 2009).
Li ve arkadaşları, pamuk sapı hammadde olarak kullanılarak H3PO4 ile üretilen
aktif karbonların Pb(II) adsorpsiyonuna uygunluğu araştırılmıştır. Aktif karbonların yüzey özelliklerine emdirme oranı (1:1, 1:2, 3:2, 2:1), ısıtma hızı (2, 5, 10, 15 oC/dk), aktivasyon sıcaklığı (350, 400, 500, 600 oC) ve aktivasyon süresinin (30, 60, 90, 120 dk) etkilerini araştırmışlardır. En yüksek yüzey alanına sahip aktif karbonun (1570 m2/g) 3:2 emdirme oranında, 500 oC'de ve 60 dk aktivasyon süresinde elde edildiğini belirlemiştirler. Aynı çalışmada optimum koşullarda elde edilen aktif karbonun Pb(II) adsorpsiyonu etkinliği araştırılmıştır. pH'ın 4.4'e kadar artmasıyla adsorpsiyon kapasitesinin arttığı, pH artışının adsorpsiyon miktarını düşürdüğü belirlenmiştir (Li ve ark. 2010).
Sun ve arkadaşları, mısır sapından kimyasal aktivasyon metoduyla aktif karbon üretiminde sıcaklığın yüzey alanı üzerine etkisini ve gaz adsorpsiyonuna uygunluğunu araştırmışlardır. Azot atmosferinde H3PO4 aktivasyonu ile elde edilen aktif karbonların,
sıcaklığının artışıyla yüzey alanının, gözenek hacminin arttığı ve en yüksek yüzey alanı ve gözenek hacminin sırasıyla 820 m2/g 0.8 cm3/g olarak 500 oC'de elde edildiğini tespit etmişlerdir. Sıcaklığın artışıyla H3PO4'ün ham maddenin iskelet yapısını sıktığı, bu
nedenle yüzey alanında ve gözenek genişliğinde daralma olduğunu gözlemlemişlerdir (Sun ve ark. 2011).
21
Benadjemia ve arkadaşları enginar yapraklarını kullanarak H3PO4 kimyasal
aktivasyonla 500 oC'de aktif karbon elde etmişlerdir. En yüksek yüzey alanına 2:1 emdirme oranında 500 °C'de 2038 m2/g olarak elde edildiği belirtilmiştir. Karakterizasyondan sonra üretilen aktif karbonlar metilen mavisi gideriminde kullanılmıştır. En yüksek adsorpsiyon kapasitesinin 2:1 emdirme oranında pH 9'da 780 mg/g olarak elde edildiği belirtilmiştir (Benadjemia ve ark 2011).
Momcilovic ve arkadaşları, H3PO4 kullanarak kimyasal aktivasyon ile
kozalaktan aktif karbon üretmiş ve Pb(II) adsorpsiyonuna pH'ın etkisini araştırmışlardır. pH'ın artmasıyla aktif karbonların Pb(II) adsorpsiyon kapasitelerinin arttığı görülmüştür. Ancak pH değerinin 6'dan büyük olması durumunda Pb(II) iyonlarının Pb(OH)2 olarak
çöktüğü belirtilmiştir. Bu durumda pH'ın 7, 8, 9 ve 10 olduğu çözeltilerde Pb(II) iyonlarının çözeltiden uzaklaşmasının adsorpsiyon mekanizmasıyla olmadığı saptanmıştır (Momcilovic ve ark. 2011).
Idriss ve arkadaşları, zeytin ağacı kabuğunu hammadde olarak kullanarak H3PO4
kimyasal aktivasyonu sonucunda sıcaklığın gözenek yapısına etkisini araştırmışlardır. Aktif karbonlarda 3.5:1 emdirme oranı kullanılmış ve sıcaklık 350 ile 550 oC arasında değiştirilerek sıcaklığın etkisi incelenmiştir. Sıcaklık artışıyla birlikte aktif karbon veriminin %29.2'den %21.7'ye düştüğü, yüzey alanlarının ve gözenek hacimlerinin arttığı tespit etmişlerdir. En yüksek yüzey alanı 550 °C'de 904 m2/g, gözenek hacmi 0.328 cm3/g olarak belirlenmiştir (Idriss ve ark. 2011).
Xua ve arkadaşları, sazlık çim yapraklarından H3PO4 aktivasyonu ile azot
ortamında değişik aktivasyon sıcaklıklarında ve sürelerinde AK'lar elde etmişler. Elde ettikleri AK'ların yüzey alanı ve iyot sayısı değerlerine göre belirlemiş oldukları optimal koşullarda (500 oC ve 2 saat) 1474 m2/g yüzey alanlı AK elde etmişler (Xua ve ark. 2014).
Qin ve arkadaşları, Marigold samanından azot ortamında H3PO4 aktivasyonu ile
iyot adsorpsiyon değerlerine bağlı olarak belirledikleri optimal hazırlama koşullarında (Emdirme oranı: 2:1; aktivasyon sıcaklığı: 400 oC; Aktivasyon süresi: 2 saat) 1344.23 m2/g yüzey alanlı AK elde etmişler (Qin ve ark. 2014)
22
Shamsuddin ve arkadaşları, kenaf çekirdeğinden H3PO4 aktivasyonu ile azot
ortamında 299.02 m2/g yüzey alan ve 0.12 cm3/g mikrogözenek hacmine sahip AK elde etmişler (Shamsuddin ve ark. 2016)
Demiral ve Güngör, üzüm küspesinden azot ortamında H3PO4 aktivasyonu ile
değişik emdirme oranları ve aktivasyon sıcaklıklarının etkileri incelenerek optimal hazırlama koşulları belirlemişler. Belirledikleri optimal hazırlama koşularında (Emdirme oranı:1/5; aktivasyon sıcaklığı: 500 oC) 1455 m2/g yüzey alanlı ve 0.88 cm3/g toplam gözenek hacimli AK elde etmişler (Demiral ve Güngör 2016)
23 3. MATERYAL ve METOT
3.1. Kullanılan Kimyasallar
Bu çalışmada, yapılan karbonizasyon/aktivasyon işlemlerinde Diyarbakır MSG Medikal Sanayi Gazlar firmasından temin edilen yüksek saflıktaki azot gazı kullanıldı. Bu tez çalışmasında, fosforik asit (H3PO4), metilen mavisi (MM), metanil sarısı (MS),
sodyum hidroksit (NaOH), sodyum bikarbonat (NaHCO3), sodyum karbonat (Na2CO3),
hidroklorik asit (HCl), etil alkol (C2H5OH), sodyum klorür (NaCl), benzen (C6H6),
sülfürik asit (H2SO4), baryum klorür (BaCl2), fenolftalein ve metil oranj kimyasalları
kullanıldı. Kullanılan kimyasallar; Sigma-Aldrich, Merck ve Fluka firmalarından temin edildi. Adsorplanan olarak seçilen MM ve MS boyarmaddelerinin genel özellikleri
Çizelge 3.1'de verilmiştir.
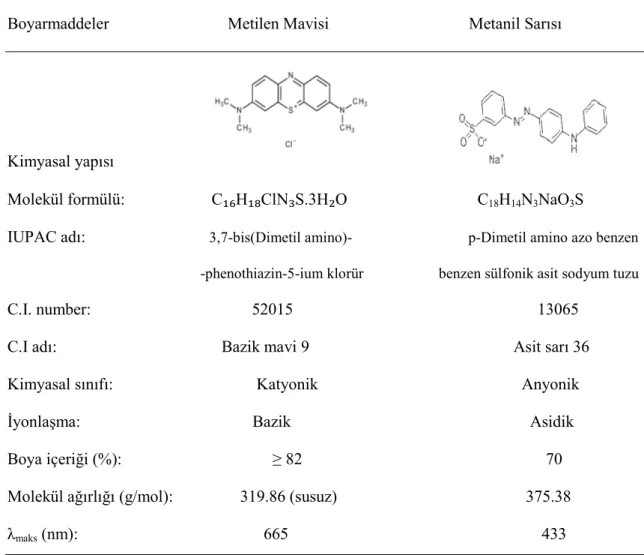
Çizelge 3.1. Metilen Mavisi ve Metanil Sarısının Genel Özellikleri
Boyarmaddeler Metilen Mavisi Metanil Sarısı
Kimyasal yapısı
Molekül formülü: C₁₆H₁₈ClN₃S.3H₂O C18H14N3NaO3S
IUPAC adı: 3,7-bis(Dimetil amino)- p-Dimetil amino azo benzen -phenothiazin-5-ium klorür benzen sülfonik asit sodyum tuzu
C.I. number: 52015 13065 C.I adı: Bazik mavi 9 Asit sarı 36 Kimyasal sınıfı: Katyonik Anyonik Đyonlaşma: Bazik Asidik Boya içeriği (%): ≥ 82 70 Molekül ağırlığı (g/mol): 319.86 (susuz) 375.38 λmaks (nm): 665 433
24 3.2. Kullanılan Cihazlar
Kullanılan kabukların belirli bir boyuta getirilmesinde bitki öğütücü (IKA 20); termal davranışları gözlemlemek için simultane termal analiz cihazı (TG/DTA) (Shimadzu); AK'ların hazırlanmasında mikrodalga ön işlemi için (Bosch HMT84G451) tüp fırın (Protherm PZF12/105/750); Mandalina kabuğu (MK) kül içeriğinin belirlenmesinde kül fırını (Protherm PLF 110/8); gözeneklerdeki değişimleri incelemek için SEM görüntülerinin alımında taramalı elektron mikroskobu (FEI QUANTA 250 FEG) cihazı; gözenek karakterizasyonu için yüzey alanı ve gözenek analiz (Micromeritics, TriStar II Plus) cihazı; yüzey kimyasal yapısını oluşturan fonksiyonel grupların nitel olarak analizinde FT-IR spektrofotometre (Perkin Elmer Spectrum 100) cihazı; sulu çözeltiden adsorplama özelliğinin karakterizasyonu için yapılan çözeltiden adsorpsiyon çalışmalarında ortam homojenizasyonunu sağlamada çalkalama özellikli ve sıcaklık ayarlı su banyosu (Wisebath-WIS 30); pH ölçümleri için pH metre (Microprocessor HI9321); adsorplananların adsorpsiyon öncesi ve sonrası derişim ölçümleri için UV-vis spektrofotometre (Perkin Elmer Lamda 25) kullanıldı.
3.3. Mandalina Kabuklarından Optimal Nano-Gözenekli Karbonun Hazırlanması
Adsorplayıcı olarak kullanılan AKopt'un hazırlanmasında hammadde olarak evsel tüketilen mandalinaların kabukları kullanıldı. Bunlar, kirlilikleri giderilene kadar çeşme suyu ile defalarca yıkandı. Daha sonra, ultra saf su ile yıkanıp etüvde 105 oC sıcaklıkta 24 saat bekletilerek kurutuldu. AK'ların hazırlanmasında, kimyasal aktivatör olarak H3PO4 kullanıldı. Optimum AK hazırlama koşulları, kimyasal aktivatör emdirme
oranı (gH3PO4/gMK), karbonizasyon/aktivasyon sıcaklığı ve süresinin hazırlanan AK'ların gözenek karakteristiklerine etkileri incelendi. Bu etkilerin optimizasyonu, her bir koşul için 77 K'de belirlenen azot gazı adsorsiyon-desorpsiyon izotermleri ve gözenek boyut dağılımı eğrilerinden belirlenen SBET, VT, Vm, VM, %Vm, %VM ve Dp değerlerine bağlı
olarak gerçekleştirildi. AKopt'un hazırlanması aşağıda belirtilen koşullarda gerçekleştirildi:
1. Kimyasal aktivatör emdirme oranı etkisini incelemek için, H3PO4 ile kabuklar
ağırlıkça (gH3PO4/gMK) 2:1, 3:1, 4:1 ve 4.5:1 oranlarında karıştırılarak çamurumsu hale getirildi ve ilk kez tarafımızdan kimyasal etkileşmenin kısa sürede tamamlanması için