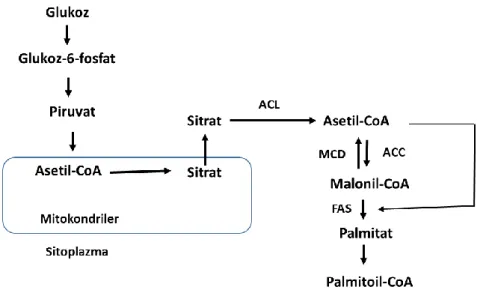
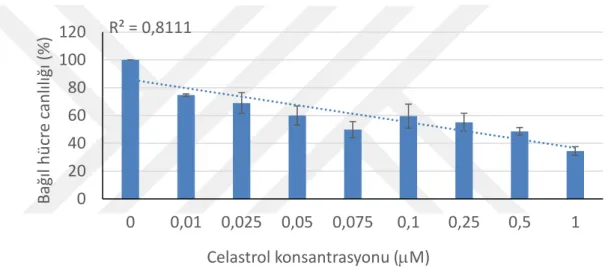
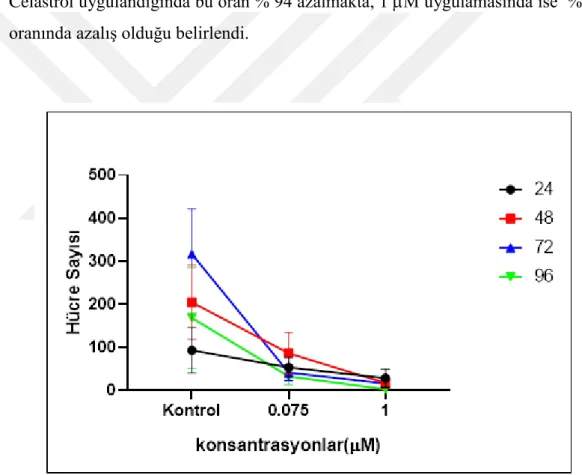
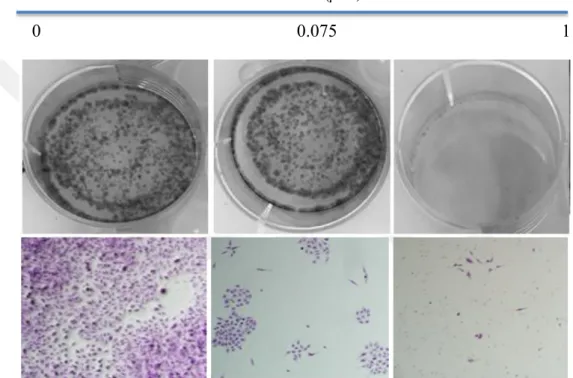
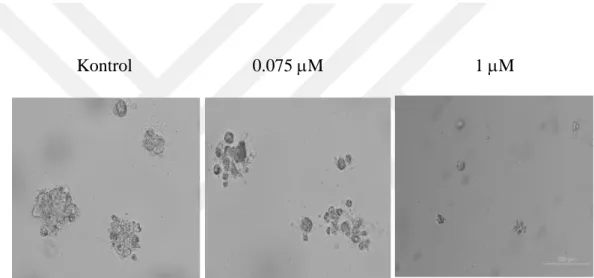
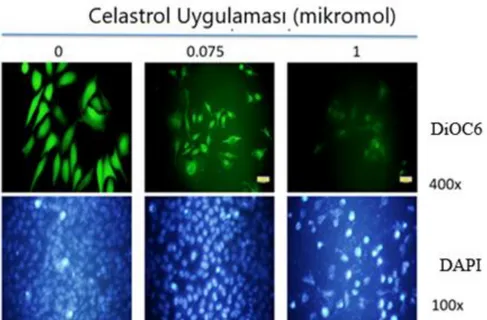
Celastrol'ün yağ asiti sentaz yolağı üzerindeki etkilerinin hela servikal kanser hücrelerinde tanımlanması
Tam metin
Şekil
Benzer Belgeler
A) Aşağıdaki testleri cevaplayınız (4x20=80 puan) Demokrasi nin uygulandığ ı en iyi yönetim biçimidir. Devletin dini kurallara dayanarak yönetilmes idir
[r]
brakiterapiyi takiben yüksek doz external pelvik radyasyon ile tedavi edilir.Ancak durumu uygun olan hastalarda radikal cerrahi de önerilmektedir... • Servikal kanser tedavisi
Tüm Yaş Gruplarındaki Erkeklerde En Sık Görülen Bazı Kanserlerin Bu Grup İçindeki Yüzde Dağılımları (Türkiye Birleşik Veri Tabanı, 2014)... Tüm Yaş
Results: Results showed that low-dose celastrol (20 and 50 nM) treatment significantly increased cell viability and decreased LDH and CK-MB activity in the condition of H/R,
2~ Teknik lise ve endüstri meslek liselerinin elektrik, elektronik ve telekomünikasyon bölümlerinin birinden mezun olmaları veya yüksek okul elektrohik elektrik
Bu bilgiler doğrultusunda çalışmamızda taksan grubu anti-neoplastik b ajan olan dosetaksel bileşiği ile EF24’ün farklı konsantrasyonlarda tek başlarına veya
hayat zamanda iz bırakmaz bir boşluğa düşersin bir boşluktan birikip yeniden sıçramak için. elde var