T.C.
DİCLE ÜNİVERSİTESİ
TIP FAKÜLTESİ KALP VE DAMAR CERRAHİSİ ANABİLİM DALI
TAVUK EMBRİYOSU KORİYOALLANTOYİK MEMBRAN
MODELİNDE PENTOKSİFİLİNİN ANJİYOGENEZ ÜZERİNE
ETKİLERİ
DR. EMRE DEMİR BENLİ TIPTA UZMANLIK TEZİ
T.C.
DİCLE ÜNİVERSİTESİ
TIP FAKÜLTESİ KALP VE DAMAR CERRAHİSİ ANABİLİM DALI
TAVUK EMBRİYOSU KORİYOALLANTOYİK MEMBRAN
MODELİNDE PENTOKSİFİLİNİN ANJİYOGENEZ ÜZERİNE
ETKİLERİ
DR. EMRE DEMİR BENLİ
TIPTA UZMANLIK TEZİDANIŞMAN: DOÇ. DR. AŞKIN ENDER TOPAL
ÖNSÖZ
Uzmanlık eğitimim boyunca teknik ve bilimsel açıdan her türlü desteklerini esirgemeyen ve yaptığım çalışmaların, mesleğim açısından ne kadar önemli olduğunu öğreten değerli hocalarım; Prof. Dr. M. Nesimi Eren, Prof. Dr. Binali Mavitaş, Yrd. Doç. Dr. İsmail Başyiğit, Yrd. Doç. Dr. Celal Yavuz, Yrd. Doç. Dr. Sinan Demirtaş, Yrd. Doç. Dr. Ahmet Çalışkan, Uzm. Dr. Oğuz Karahan, Uzm. Dr. Süleyman Yazıcı, Uzm. Dr. Orkut Güçlü’ye, tez çalışmamda bana yol gösteren danışman hocam, Sayın Doç. Dr. Aşkın Ender Topal’a, çalışma arkadaşlarıma teşekkürlerimi sunarım.
Ayrıca benden desteğini,sabrını,sevgisini eksik etmeyen hayat arkadaşım Pınar’a ve aileme sonsuz teşekkürler…
ÖZET
Embriyolojik büyüme ve yara iyileşmesi gibi birçok fizyolojik süreçte önemli rol oynayan anjiyogenez, proanjiyogenik ve antianjiyogenik faktörlerce etkin bir biçimde sınırlandırılır ve dengede tutulur. Bu kontrol mekanizmalarının bozulması, kardiyovasküler hastalıklar, kanser, diyabetik retinopati ve romatoid artrit gibi problemlerin etyopatogenezinde etkin bir rol oynar. Koriyoallantoyik membran modeli ilaçların antianjiyogenik etkilerinin araştırılmasında değerli bir yöntem olarak kabul görmektedir. . Bu çalışmanın amacı periferik arter hastalığında sıkça kullanılan pentoksifilinin antianjiyogenik etkilerinin koriyoallantoyik membran modelinde araştırılmasıdır. Çalışmada pentoksifilinin antianjiyogenik etkisi, ilaç eklenmemiş parafin ile muamele edilen negatif kontrol grubu ve bu modelde daha önce antianjiyogenik etkiniliği net olarak gösterilmiş olan, vasküler endoteliyal büyüme faktörü inhibitörü bevasizumab eklenmiş pozitif kontrol grubu ile karşılaştırıldı. Çalışmada bu ilaçların 10-2, 10-3, 10-4 ve 10-5 molar (M) konsantrasyonları uygulandı. İlaç uygulamaları sonrasında
ilaçların anjiyogenez üzerine olan etkilerini değerlendirmek için tavuk embriyosu koriyoallantoyik membranı üzerindeki damar yapıları stereoskopik mikroskop altında değerlendirildi. Pentoksifilin in 10-2, 10-3 M konsantrasyonlarının antianjiyogenik etki puanları 10-4 ve 10-5 konsantrasyonlarından
zayıf düzeyde yüksek bulundu. Bevasizumab'ın ise 10-2, 10-3, 10-4 konsantrasyonlarının
antianjiyogenik etki puanları 10-5 konsantrasyonundan anlamlı düzeyde yüksek bulundu. Hastanın
vasküler devamlılığının önem arz ettiği bu tip hastalıklarda antianjiyogenik etkinin ortaya konmasıyla daha çok fayda sağlanabilir.
SUMMARY
Angiogenesis which plays significant roles in a variety of physiological processes such as embryonic growth and wound healing, is strictly may fail and result in formation of a pathologic capillary network during the development of many diseases including cardiovascular disorders, cancer, diabetic retinopathy and rheumatoid arthritis. The chorioallantoic membrane model is considered to be a valuable method for investigation of antiangiogenic effects of drugs. The purpose of this study is to investigate the antiangiogenic effects of the Pentoxifylline which is frequently used as anti-arrhythmic, in the chorioallantoic membrane model. In this study, the antiangiogenic effect of Pentoxifylline was compared with negative control group that dealed pure paraffine and vascular endothelial growth factor inhibitor Bevacizumab added positive control group which which has been shown as clearly antiangiogenic activity in this model previously. The
concentrations of 10-2, 10-3, 10-4 ve 10-5 molar (M) of each drugs were aministered. For the purpose of
determinining the antiangiogenic effects of the drugs, blood vessels of the chorioallantoic membranes were evaluated using a stereoscopic microscope. The antiangiogenic effect scores of Pentoxifylline at the dose of 10-2, 10-3 M molar (M) weak levels were higher than those of 10-4 and 10-5. The
antiangiogenic effect scores of Bevacizumab at the concentration of 10-2, 10-3, 10-4 were significantly
higher than those of 10-5. The optimum benefit can be achieved with the revealing of antiangiogenic
effect in such these diseases.
İÇİNDEKİER
Sayfalar
ÖNSÖZ ……….. i
ÖZET ………. ii
İNGİLİZCE ÖZET (SUMMARY) ……… iii
İÇİNDEKİLER ……….. iv SİMGELER VE KISALTMALAR ………... v 1.GİRİŞ ……….. 1 2.GENEL BİLGİLER ……… 3 2.1. Anjiyogenez ………. 3 2.1.1. Anjiyogenez mekanizması ………. 4
2.1.2. Anjiyogenez ve kardiyovasküler sistem ……… 7
2.1.3. Fizyolojik ve patolojik süreçlerde anjiyogenez ……… 10
2.2. Anti anjiyogenik yaklaşımlar ………11
2.3. Koriyoallantoyik membran modeli ………... 12
2.4. Pentoksifilin ……….. 15 2.5. Bevasizumab ………. 16 3. GEREÇ VE YÖNTEM ………... 20 3.1. Pelletlerin hazırlanması ……… 20 3.2. KAM deneyi ……… 20 3.3. İstatistiksel değerlendirme ……… 25 4. BULGULAR ………... 26 5. TARTIŞMA ………. 30 6. SONUÇ VE ÖNERİLER ………. 33 7. KAYNAKLAR ……… 35
SİMGELER ve KISALTMALAR
M; Molar
bFGF; Basic fibroblast growth factor, Temel fibroblast büyüme faktörü BM; Basal membrane, Bazal membran
ESM; Extracellular matrix, Ekstraselüler matriks
HER-2; Human epidermal growth factor receptor 2, İnsan epidermal büyüme faktörü reseptörü 2 HIF-1; Hypoxia-inducible transcription factor-1, Hipoksiyle indüklenebilir transkripsiyon faktörü-1 IGF-1; Insulin-like growth factor-1, İnsülin benzeri büyüme faktörü-1
IL-1; lnterleukin-1, İnterlökin-1
IL-1P; lnterleukin-1 beta, İnterlökin 1 beta IL-6; lnterleukin-6, İnterlökin-6
IL-10; lnterleukin-10, İnterlökin-10 IL-13; lnterleukin-13, İnterlökin-13 CAM; Chorioallantoic membrane KAM; Koriyoallantoyik membran
MMP; Matrix metalloproteinase, Matriks metalloproteinaz NO; Nitric oxide, Nitrik oksit
PDGF; Platelet derived growth factor, Platelet kökenli büyüme faktörü
PDGFR; Platelet derived growth factor receptor, Platelet kökenli büyüme faktörü reseptörü PIGF-1; Placenta growth factor 1, Plasenta büyüme faktörü 1
TGF-a; Transforming growth factor alpha, Transforme edici büyüme faktörü alfa
TGF-ß; Transforming growth factor beta, Transforme edici büyüme faktörü beta TNFa; Tumor necrosis factor alpha, Tümör nekroz faktör alfa tPA; Tissue plasminogen activator, Doku plazminojen aktivatörü uPA; Urokinase type plasminogen activator, Ürokinaz tip plazminojen aktivatörü
VEGF; Vascular endothelial growth factor, Vasküler endoteliyal büyüme faktörü VEGFR-1; Vascular endothelial growth factor receptor1, Vasküler endoteliyal büyüme faktörü reseptörü1 VEGFR-2; Vascular endothelial growth factor receptor 2, Vasküler endoteliyal büyüme faktörü reseptörü 2
VEGFR-3; Vascular endothelial growth factor receptor3, Vasküler endoteliyal büyüme faktörü reseptörü 3
1. GİRİŞ
Anjiyogenez ve vaskülogenez, hayatın hem doğum öncesi hem de doğum sonrası dönemlerde gerçekleşen olaylardır. İntrauterin yaşamda kök hücrelerden gelişen öncü hücrelerin bir alt tipi olan farklılaşmamış mezenşimal hücreler dönüştükleri anjiogenetik hücre toplulukları aracılığıyla embriyonal dokularda ilk anjiyogenetik alanları oluşturular. Bu yapılardan vaskülogenezin ilk aşamasını temsil eden ilkel damar tüpçükleri meydana gelir. Böylece, embriyonal dokuda başlayan anjiyogenetik süreç vaskülogenetik aşama ile devam eder. Vaskülogenez bir yandan sürerken, diğer yandan yeni anjiyogenetik odaklar da oluşmaya başlar. Böylece farklılaşmamış bir hücre grubundan damar oluşumu gerçekleşir. Postnatal hayatta ise var olan damar endotelinin çoğalması ile yeni endotel hücreleri ortaya çıkar ve anjiyogenez gerçekleşir (1 -3).
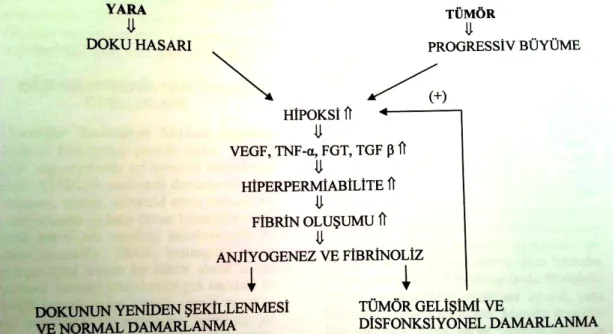
Embriyogenez dışında, yetişkinlerde anjiyogenez yaralanma sonrası doku yenilenmesi ve menstürel siklusta endometriyal proliferasyon ve sekresyon gibi çok sınırlı olaylarda görülmektedir. Anjiyogenezde proanjiyogenik ve anti anjiyogenik faktörler arasındaki denge bozulduğunda anjiyogenez kontrol edilemez. İnflamatuvar hastalıklarda (artrit,kronik inflamasyon, inflamatuvar barsak hastalığı, psöriazis), çeşitli kanserlerde (meme, mesane, akciğer, kolon, nöroblastom, melanom, böbrek, pankreas, uterus, serviks, glioblastom) ve göz hastalıklarında (yaşla ilişkili maküler dejenerasyon, proliferatif retinopati) anjiyogenez patolojik olarak ortaya çıkmaktadır (Şekil 1). Periferik arter hastalıklarında ve gecikmiş yara iyileşmesinde ise anjiyogenezin yetersizliği söz konusu olmakla birlikte, antianjiyogenetik stratejiler, aterosklerotik lezyonun içinde fibromusküler çoğalmanın önlenerek açıklığın korunması için önem oluşturmaktadır. Kardiyovasküler olaylarda ise anjiyogenez vasküler devamlılığın ve gerekli kollateral dolaşımın sağlanması için ciddi önem arz eder. Bu nedenle anjiyogenez konusu günümüzde üzerinde sık çalışılan bir konudur (1-3).
Anjiyogenez bir çok hücre tipinin, çok sayıda molekülün katılıdığı karmaşık ve çok basamaklı bir süreçtir. İn vitro modeller bu süreçte ilgili önemli bilgiler sunmakla birlikte, in vivo süreci tam olarak yansıtamaz. Anjiyogenez araştırmalarında çok yaygın olarak kullanılan bir in vivo model, tavuk embriyosu koriyoallantoyik membran (KAM) modelidir. Bu model, ilaçların antianjiyogenetik potansiyellerini araştırmak için duyarlı, kolay uygulanabilir ve ucuz bir in vivo testtir.
Şekil 1. Normal doku uyarımı ve tümörlerde anjiyogenezi uyaran ortak yollar. (Cerrahpaşa
2.GENEL BİLGİLER
Anjiyogenez; vasküler sistemin devamlılığı, geçirilmiş veya yeni meydana gelecek hastalığın organizma da oluşturacağı etkinin belirlenmesi açısından büyük bir öneme sahiptir. Özellikle, dolaşım sisteminde yeni oluşan kollaterallerin, ana damarların açıklığının kesintiye uğraması durumunda, hayati önem taşıdığının görülmesi daha fazla araştırmacıyı bu konuya yöneltmiştir. Yeni geliştirilen ilaçların anjiyogenez üzerine etkileri önce tavuk embriyosu KAM modeli gibi temel bilim deneyleri ile değerlendirilmektedir.
Bu tez araştırmasında tavuk embriyosu KAM modelinde çeşitli araştırmalarda doğrudan veya dolaylı olarak antianjiyogenetik özellikleri gösterilmiş olan bevasizumab ve non selektif fosfodiesteraz inhibitörü olan ve vasküler sistem üzerine önemli etkiler sağlayabileceği öngörülen pentoksifilinin anjiyogenez üzerine olan etkileri incelendi. Araştırma yönteminin ve bulguların daha iyi anlaşılabilmesi için anjiyogenez, tavuk embriyosu KAM modeli ve araştırma ilaçlarının farmakolojik özellikleri konusunda güncel literatür eşliğinde bilgi sunuldu.
2.1. Anjiyogenez
Anjiyogenez daha önceden var olan vasküler sistemden yeni kan damarı oluşumu sürecidir. Yeni kan damarı gelişimi, embriyogenez süresince esas olarak vaskülogenez ve anjiyogenez ile meydana gelir (1). Vaskülogenez terimi, anjiyoblast olarak adlandırılan kök hücrelerden kaynaklanan endotelial hücrelerin primer kapiller pleksusu oluşturmak üzere farklılaşıp bir araya gelmesini tanımlar. Bu primitif ağ oluşumunun tomurcuklanma, dallanma ve iç çe geçen büyüme şeklindeki farklılaşmasına anjiyogenez denir. Böylelikle mevcut kapiller damarlardan yeni kapiller damarlar meydana gelir. Anjiyogenez bu damar tomurcuklarının sonraki dönemde damar duvarının diğer elemanları ile birlikte stabilizasyonunu ve geniş kan damarlarının oluşumunu ifade eder.
Erişkinlerde anjiyogenez yara iyileşmesi, doku beslenmesi ve tamiri ve menstrüel siklus gibi birçok fizyolojik süreçte ortaya çıkar. Patolojik anjiyogenez ise başta tümörler olmak üzere kollajen doku hastalıkları, retinopatiler ve psöriasis gibi hastalıklarda meydana gelir (2). Aterosklerotik kardiyovasküler hastalıkların etkin tedavisinde anjiyogenetik sinyallere müdahaleler güncel araştırmalarda sıkça ele alınmaktadır. Pozitif proangiogenitic stratejiler, iskemik bölgelere kollateral dolaşımının sağlanması için gerekliyken, negatif
antianjiyogenetik stratejiler, aterosklerotik lezyonun içinde fibromusküler çoğalmanın önlenerek açıklığın korunması için önem oluşturmaktadır (3).
2 .1 .1 . Anjiyogenez Mekanizması
Anjiyogenez süreci pozitif ve negatif etkili moleküller arasındaki denge ile kontrol edilir. Pozitif etkili proanjiyogenetik moleküller, eğer baskın hale gelirlerse anjiyogenez süreci tetiklenir ve yeni damar oluşumu meydana gelir. Bu kavram , ‘anjiyogenetik anahtar (switch)’ olarak adlandırılır (4) .
Anjiyogenez bir dizi olayı içeren çok basamaklı bir süreçtir. Anjiyogenez, temel fibroblast büyüme faktörü (bFGF), tümör nekröz faktör alfa (TNF - α) ve VEGF gibi anjiyogenetik faktörlerin endotel aktivasyonu yapmak üzere çevre dokudan salınımı ile başlar (5). Bazal membranın proteolitik enzimler tarafından yıkılması bu basamaklardan ilkidir. Endotel hücreleri yayılma etkisi göstermeyen tek bir tabaka halinde bulunurlar. Anjiyogenez sürecinde göç etmek ve çoğalmak üzere uyarıldıklarında membran ve hücreler arasında bir bölünme meydana gelir ve sayıları giderek artmaya başlar. Endotel hücrelerinden salınan anjiyogenetik büyüme faktörü komşu dokulara difüzyon yolu ile geçerler. Bu büyüme faktörleri çevre kan damarlarındaki endotel hücrelerinde bulunan özgün reseptörlere bağlanırlar. Hücre içi anjiyogenez uyarısının başlamasıyla bazal membran ve ekstrasellüler matriks hasarına yol açan serin proteazlar ve matriks metalloproteinazlar gibi proteolitik enzimlerin salınımı gerçekleşir. Endotel hücrelerinin damar duvarı dışına kaçışı başlar. Ürokinaz tip (uPA) ve doku tip (tPA) plazminojen aktivatörleri plazminojeni plazmine çeviren serin protezları grubuna aittirler (6) . Endotel hücrelerinin invazyon ve göç süreçleri, plazminojen aktivatör (PA) ve matriks metalloproteinaz (MMP) sisteminin işbirliği içinde aktive olmasının gerektirir. Endotel hücre aktivasyonu, proliferasyonu ve göçü ikinci basamak olarak değerlendirilir. Bu yeni immatür damarlar endotelial hücrelerin migrasyonu ve büyümesini sağlamak için endoteliyum üzerinde boşluklar içerirler (7). Anjiyogenetik uyarı, proteolitik yıkımı takiben endotel hücreleri aktive eder. Bu süreçte en etkili anjiyogenetik faktör VEGF‘ dür (8). Kapiller oluşumu ve damar olgunlaşması anjiogenezin üçüncü basamağıdır. Prolifere olan endotel hücreleri integrinlerin yardımıyla çevre matrikse göç ederler ve komşu damar tomucuğunu oluştururlar (9). Kapiller filizlenmenin ucunda yeni oluşmuş ekstraselüler matrikste yıkılmaya ortaya çıkar. Böylece yayılımın devam etmesi sağlanır. Endotel hücre çoğalmasından sonra ekstrasellüler matriks bileşenlerinin depolanması ve bir araya getirilmesi için ekstraselüler proteoliz mutlaka lokal olarak inhibe edilmelidir. Endotel hücrelerinin
çoğalması ve ilerlemesi sırasında hücre içi ve hücreler arası boşluklar oluşmaya başlar. Hücreler anjiyogenez alanına göç ettikçe damar tomucuğu tüp şeklini alır ve sonrasında damar lümenini oluşturur (5). Böylece, ekstraselüler matriks proteolizinin birbirini sırayla izleyen aktivasyon ve inhibisyonları sonucunda kapillerler oluşur (Şekil 2.1).
Proteolitik yıkılma ve endotel hücresi göçünden sonra yeni oluşan kapillerler bazal membranı oluştururlar. Endotel hücrelerinin yeni kapiller yapılar oluşturabilmeleri için birbirlerine ve ekstraselüler matrikse tutunmaları gerekir. Yeni matriks oluşumu için ekstraselüler matriks proteinleri olan fibronektin, laminin ve kollojen üretilir (10). Yeni damar yapımı tamamlandıktan sonra anjiogenetik faktörlerde azalma görülürken, anjiyogenez inhibitörlerinde artış gözlenir. Endotel hücreleri tekrar stabil haldedirler ve damarlar kan akımını başlatmaya hazır hale gelmiş olurlar. Yeni damarların tam olarak oluşmaları yaklaşık yedi gün sürer (11). Henüz tüm anjiyogenik etkileşimlerin niteliği açıklığa kavuşmamıştır. En büyük olasılık anjiyogenik uyarıcılar ve anjiyogenez inhibitörleri arasındaki dengenin, normalde damarsal bileşenlerin sessiz halde kalmalarını sağlıyor olmasıdır. Anjiyogenik uyaranların artışı ve anjiyogenez inhibitörlerinin azalışı anjiyogenezisi başlatmaktadır. Anjiyogenik ve antianjiyogenik faktörler Tablo 2.1. de gösterilmektedir (12).
Endotelial hücreler lenf damarlarının oluşumuna da katkıda bulunurlar. Lenfatik damarlanma embriyogenez esnasında kan damarları gelişiminden kısa süre sonra gelişir ve kan damarları ile aynı kökene sahip olduğu düşünülür (13, 14). Venöz endotelial hücrelerin lenfatik uyarılara duyarlı hale geldiği ve diferansiye olarak lenfatik tomurcukları oluşturduğu
Anjiyogenezi inhibe edenler Anjiyogenezi uyaranlar
Trombospondin
Anjiyostatin (plasminojen kısmı) Endostatin (kollajen XVIII kısmı) AaAt (antithrombin III kısmı) Vazostatin Prolaktin Troponin 1 Anjiyopoietin-2 Alfa interferon Gamma interferon İnterlökin 12 Fibronektin Metalloproteinaz doku inhibitörleri
Plazminojen aktivatör inhibitör 1 Platelet faktör 4 (PF 4)
Pigment epitelial hücre faktörü Retinoik asid
Vasküler endotelial büyüme faktörü Ana Fibroblast büyüme faktörü Asit Fibroblast büyüme faktörü Platelet kaynaklı büyüme faktörü Hepatosit büyüme faktörü
Epidermal büyüme faktörü Insulin-benzeri büyüme faktörü Dönüşen büyüme faktörü a Dönüşen büyüme faktör b Tümör nekrosis faktör a Plasental büyüme faktörü Anjiyopoietin-1
Anjiyogenin Pleotrofin Interlökin 8
Granulosit-koloni uyarıcı faktör Proliferin
varsayılır. Bununla birlikte lenfanjiyoblastların veya prekürsörlerin varlığı da kanıtlanmıştır (15).
ŞEKİL 2.1. Anjiyogenezin başlangıç evreleri. VEGF; Vasküler endoteliyal büyüme
faktörü, ESM; Ekstraselüler matriks, MMP; Matriks metalloproteinaz, BM; Bazal membran (Expert Reviews in Molecular Medicine, Cambridge University Press, 2003).
2.1.2. Anjiyogenez ve Kardiyovasküler Sistem
Aterosklerotik kardiyovasküler hastalıkların etkin tedavisinde anjiyogenetik etkilere müdahale ederek prognozu yönlendirme çabaları yeni geliştirilen ilaçların bu alandaki etkinliklerinin araştırılmasını sağlamıştır. Miyokard perfüzyonunun sağlanması için vasküler devamlılık önemlidir. Kan akımının emboli, tromboz ve ateroskleroz gibi durumlarda kesintiye uğraması durumunda kollateral dolaşım doku perfüzyonu için hayati önem taşır (Şekil 2.2 ).
Terapotik Anjiyogenez; Dokuların perfüzyonu için gerekli olan vasküler
devamlılığın sağlanması için anjiyogenetik etki elde edilmesi yada en azından verilecek tedavilerin antianjiyogenetik etkilerinin minimalize edilmesi amaçlanmıştır. Bununla birlikte ateroskleroz gibi damar lümenini daraltan olaylarda fibromüsküler dokunun gelişiminini geriletmek veya vasküler stent gibi açıklığın sağlanmasına destek cihazların tıkanmasını
önlemek için antianjiyogenetik etkiler sağlanmaya çalışılmıştır (3). Yetersiz anjiyogeneze bağlı, yetersiz kan akımından kaynaklanan kalp ve diğer dokulardaki hipoksi birçok kardiyovasküler hastalıkların seyrini belirler. Koroner arter hastalığı, periferik arter hastalığı, diyabetin vasküler komplikasyonları ve inme gibi hastalıklar bu tip anjiyogenez bağımlı hastalık gruplarındandır. Normal şartlar altında, anjiyogenez stimülasyonu için büyüme faktörleri, proteinler, inflamatuvar ve immün etkilerin uyardığı bir dizi kimyasal sinyalin aktive olması gerekmektedir. Bu doğal sürece yara iyileşmesi iyi bir örnektir. Kardiyovasküler doku rejenerasyonu, anyiyogenezin uyarılması ile direkt ilişkilidir. Koroner tıkanıklıklarda, hipoksik miyokardın beslenmesi için kollateraller gelişmeye başlar. Bu etki kronik olaylarda akut hasarın önlenebilmesi için mutlaka gereklidir. Koroner anjiyogenezisin sağlanmasında VEGF dışında, FGF, PIGF, PDGF, anjiyoproteinler gibi daha birçok anjiyogenetik faktörler, neovaskülarizasyona katkıda bulunur. Tedavi amaçlı anjiyogenez, kardiyovasküler hastlalıklar, DM ve kalp-damar sistemini etkileyen diğer kronik problemlerin komplikasyonlarının tedavisi için büyük umutlar vaat edilmektedir (16-23).
Başlangıçta yapılan çalışmalar kardiyovasküler hastalıklarda tedavi amaçlı anjiyogenezin faydalarına değinse de, güncel çalışmaların bir kısmı da artmış anjiyogenezin kardiyovasküler mortaliteyi artırabileceğine değinmiştir. Özellikle endotelial öncül hücrelerin artış göstermesi stent restenozları, vasküler darlığın artışı gibi durumlardan sorumlu tutulmuştur. Bazı çalışmalar ise primer aterosklerotik lezyonu etkilemediğini iddia edilmiştir. Kısacası bozulmuş dinamik dengenin her iki tarafa çekilmesinin de pozitif ve negatif etkileri olabileceği bildirilmiştir (24,25).
Neovaskülarizasyon hakkında biçok mekanizma tanımlanmıştır. Bunlardan biri var olan kan damarlarından endotelial hücrelerin önce proliferasyonu sonra migrasyonunu takiben tübüler vasküler yapılara organize olmalarını içeren tomurcuklanma anjiyogenezidir. Bir diğeri ise var olan kan damarlarının lümeni içerisinde transvasküler doku perdesinin oluşumu ve takiben kan damarının bu perde ile ayrılarak iki yeni damar oluşturmasını ifade eden intussusseptif anjiyogenezdir (26). Yeni damarlar, dolaşan endotelial progenitör hücreleri kullanarak da gelişebilirler. Şimdi artık kapsamlı veriler bu hücrelerin varlığını ve yeni damar oluşumuna olan katkılarını desteklemektedir (27,28).
Nitrik oksidin de bu mekanizmadaki rolü sıkça tartışılmıştır. Bazal vasküler tonusun önemli bir belirleyicisi olan nitrik oksit trombosit aktivasyonunu önler, endotele lökosit adezyonunu sınırlar ve miyokardiyal kontraktiliteyi düzenler (29-31). Kardiyovasküler sistemde modülatör görevi üstlendiği belirtilen nitrik oksidin neovaskülarizasyon üzerine etkileri tartışılmaya başlanmıştır. Doku iskemisinde antioksidan mekanizmalarla birlite,
endotel hücrelerinden nitrik oksit salınımının arttığı gösterilmiştir (32). Nitrik oksit salınımının VEGF üzerinden anjiyogenez oluşumuna katkıda bulunduğu bildirilmiştir. Hatta tedavi amaçlı anjiyogenezin araştırıldığı bazı çalışmalar, nitrik oksit üzerinden yürütülmüştür (33,34). Bu çalışmaların sonucunda nitrik oksidin de anjiyogenezi ve vasküler permeabiliteyi arttıdığı gösterilmiştir (32- 35).
ŞEKİL 2.2. Vasküler devamlılığın kollateral dolaşımla sağlanması (LifeART Colection
Images Copyright © 1989-2001 by Lippincott Williams & Wilkins, Baltimore, MD)
2.1.3. Fizyolojik ve Patolojik Süreçlerde Anjiyogenez
Anjiyogenez yara işileşmesi ve epitelizasyon için çok önemli bir basamaktır. Yaralanan dokunun iyi beslenmesi ve yeterli kan akımının sağlanması iyileşmeyi etkileyen önemli bir parametredir. Anjiyogenez olmazsa oksijen ve besin desteği olmayacaktır, dolayısıyla yara yerine makrofaj ve fibroblastların invazyonu da gerçekleşmeyecektir. Anjiyogenez, hipoksi, büyüme faktörleri, matriks komponentleri ve metabolik durum gibi birçok faktörden etkilenebilmektedir (36). Yara yerinde oksijen basıncının düşük olması, laktik asit birikimi, trombosit ve makrofajların transforme edici büyüme faktörü alfa (TGF -α), transforme edici büyüme faktörü beta (TGF - β) , TNF – α gibi anjiyogenik faktörleri salgılamalarını stimüle eder (37). Anjiyogenez için endotel hücre göçü ve kemotaktik
faktörler büyük öneme sahiptirler. Bu faktörler trombosit kökenli maddeler, heparin ve fibronektik olup, endotel hücrelerinin hareketini arttırırlar. Endotel hücreleri tarafından üretilen fibronektin ve kollajen gibi maddeler de bu hücre hareketine yardımcı olurlar. Platelet kökenli büyüme faktörü (PDGF) damar düz kası gelişimini uyarır. Kollajen sentez ve yıkımı da vasküler bazal membran oluşumunu düzenler (38). Yara iyileşmesinde inflamatuvar hücre infiltrasyonu, proliferasyonu ve matriks oluşumu sonrası skar dokusu gelişir.
Anjiyogenez regülasyonunun bozulması, diyabetes mellitustaki biçok patolojinin nedenidir (28,39). Diyabetes mellituslu hastalarda; retina ve böbrek vaskülopatisi yara iyileşmesinde yetersizlik, transplante edilen organın rejeksiyon riskinin artması ve koroner kollateral oluşumunda yetersizlik gibi durumlar gözlenir. Diyabetes mellitusta gelişen anjiyogenez regülasyonunun bozulmasını açıklamak için birçok mekanizma öne sürülmüştür: Birincisi, endotelyal ve vasküler düz kas bozuklukları ile karakterize vasküler disfonksiyonun varlığıdır. İkincisi, proteinlerin non enzimatik glikolizasyonuna ve yeni kan damarlarının bozulmuş yapılanmasına neden olan kronik hiperglisemidir. Üçüncüsü ise diyabetin büyüme faktörü sinyali (39,40) ve /veya ekspresyonunu (41) etkileyerek vasküler büyüme faktörlerinin lokal dengesini bozmasıdır. Diyabetik retinopatide esas rolü VEGF oynar ve salınımı bFGF, plasenta büyüme faktörü 1 (PIGF-1), TNF , TGF- β , interlökin -1 (IL -1) gibi birçok faktör tarafından artırılır. Anormal anjiyogenezin eşlik ettiği diyabetik nefropatide VEGF lokal düzeyinin çok yükseldiği ve anjiyotensin II salınımının artmış olduğu tespit edilmiştir (23). Diyabetik ayak ülserleri, bası yaraları gibi kronik yaraların bulunduğu durumlarda kan akımındaki bozulma yara iyileşmesinde gecikmeye neden olabilir (36,42). Son dönemde yeni kan damarı oluşumunu indüklemek ve lokal iskeminin dokularda neden olduğu olumsuz etkilerden kaçınmak amacıyla anjiyogenez ile ilgili birçok çalışma yapılmıştır (36,43).
2.2. Anti –Anjiyogenik Yaklaşımlar
Tümör gelişiminin anjiyogeneze bağımlı olduğu hipotezinin ortaya konmasının ardından ilk olarak 1971 yılında J. Folkman (44,45) tarafından anjiyogenez inhibisyonunun tedavi avantajı sağlayabileceği düşüncesi geliştirilmiştir.
Dört aşamalı olarak tariflenen anjiyogenez mekanizmasının (I-Bazal membranın proteolitik enzimler tarafından yıkılması, II-Endotel hücre proliferasyonu ve göçü, III-Tubul oluşumu ve olgunlaşma, IV-Ekstraselüler matriksin yeniden şekillenmesi.) her bir basamağı ayrı ayrı antianjiyogenik yaklaşımı içinde barındırır. Antianjiyogenik tedavinin optimizasyonu için spesifik seçenekler sunar. (Tablo 2.2).
Tablo 2.2. Anti anjiyogenik yaklaşımların ana hedefleri
Büyüme faktörlerinin antogonistleri
Anjiyogenik faktör üretiminin durdurulması
Büyüme faktörlerinin monoklonal antikorları Çözünür büyüme faktörü reseptörleri Tirozin kinaz reseptörlerinin inhibisyonu Protein kinaz C inhibisyonu
Endotelyal proliferasyonun durdurulması
Hücre siklusu inhibitörleri Vasküler hedefli ajanlar
Endotel progenitör hücrelerin baskılanması
Matriks degradasyonunun durdurulması
Seçici veya seçici olmayan MMP inhibitörleri
Plazminojen aktivatörünün inhibisyonu
Endotel hücre yüzey markerlarının hedeflenmesi Anti-integrin antikorları
Siklik peptidler
2.3. Koriyoallantoyik Membran Modeli
Anjiyogenezde bulunan başlıca in vivo modeller tavuk embriyosu KAM modeli, tavşan kornea modeli (‘micropocket’), rodent mezenter emboli, sünger (‘sponge’) implant modeli, matrijel ve klasik tümör modeli ve zebrafish modelidir. Uygulaması en kolay, basit, tekrarlanabilir ve anjiyogenetik yanıtın kantitatif ölçümüne imkan veren çalışma modellerinin tavuk embriyosu KAM modeli ve tavşan modeli olduğu kabul edilmektedir (46,47).
KAM modeli, ilk olarak 1956 yılında Folkman (48) tarafından anjiyogenez çalışmalarında kullanılmaya başlanmıştır. Tavuk embriyosu modeli , tümör gelişimi, anjiyogenez ve tümör hücresi yayılımı üzerine , in vivo çalışmalarda değerli bir yöntemdir. Doku kompozisyonu ve KAM’ın deneysel müdahaleler için kolay ulaşılabilir olması , tavuk embriyosu KAM modelini tümör hücrelerinin davranışını mikroskobik olarak izlemek için uygun bir yöntem haline getirmektedir (Tablo 2.1.). Tavuk embriyosu model sistemi , spontan metastaz modelinde tümör hücre intravazasyonu, deneysel metastaz modelinde tümörce uyarılmış anjiyogenez gibi kanser hücresi yayılımının spesifik evre ve yönlerinin ayrıntılı
analizine imkan tanır. Ekstraembriyonik bir membran olan KAM, üzerindeki vasküler yapının kolaylıkla makroskobik olarak izlenebilmesi sayesinde, antianjiyogenez çalışmalarında yaygın olarak kullanılmaktadır (Şekil 2.3). KAM, tavuk embriyosu fizyolojisinde gaz alış – verişini sağlayan solunum organı ve atık ürünler için mesane işlevleri yürütmektedir (49).
Şekil 2.3. Tavuk embriyosu ve KAM’ın stereoskopik mikroskop altındaki görünümü.
Bu model sistemlerinin özü, primer tümör ve anjiyogenez için eşsiz bir ortam sağlayan özel bir dokunun, KAM’ın kullanılmasıdır. Tavuk embriyosu inkübasyonu sırasında, 5.-6. Günlerde KAM, koriyon ve allantoisin birleşimi ile oluşur (49,50). Embriyonun akciğer işlevini gören KAM hızla gelişir ve inkübasyonun 12. gününde tüm embriyoyu çevreler. KAM oldukça ince bir yapıdır, nadiren üç tabakanın toplam kalınlığı 100 µm’u geçer. Parafin kesitlerinin hematoksilen – eozin ile boyanması, bir veya iki katlı epitelyal tabaka ve sıklıkla eritrositlerce doldurulmuş olan ince sirküler açıklıklar olarak görünen kapiller pleksustan oluşan ektoderm, stromal hücreler, kollajen lifleri ve ektodermin hemen altında yerleşik bulunan terminal kapillerler de dahil farklı çaplarda kan damarlarından oluşan mezoderm ve
tek hücre tabakalı düz endodermi ortaya koyar. Ektoderm kapiller pleksus, tavuk embriyo metastazı ve anjiyogenez modelleri için KAM’ın en önemli histolojik özelliklerinden biridir.
KAM’da anjiyogenez, gelişimsel olarak 3 safhadan oluşur: 1. Erken faz (5.günden 7.güne kadar)
2. Ara faz (8.günden 12.güne kadar) 3. Geç faz (12.veya 13.günden itibaren)
Kapiller ağın filizlenmeye başladığı dönem erken faza denk gelir. Ara fazda filizlenme sona erer ve mikrovasküler ağ gelişimi başlar. Geç fazda ise koriyoallantoyik öğeler genişlemesini tamamlar ve koruyucu bir membrana dönüşür. KAM modelinde uygulamalar 5. günden itibaren yapılabilir (51). Diğer bir görüş ise damarlanmanın olgunlaştığı 12.günden sonraki dönemin anjiyogenez çalışmaları için daha uygun olduğu savunur (52).
Tablo 2.1. KAM modeliyle çalışmanın avantaj ve dezavantajı (53)*.
Avantajlar Dezavantajlar
Teknik olarak basittir Oksijen değişikliklerine hassastır
Ucuzdur Yeni damar oluşumunun ayırt edilmesi güçtür
Temini kolaydır Memeli olmayan bir modeldir
Geniş taramalar için uygundur Embriyoniktir
Noninvaziv gözleme uygundur Non-spesifik inflamatuvar reaksiyonlar yaygındır Sonuçları kolay ve çabuk
değerlendirilebilir
Metabolik aktivasyona ihtiyaç duyan ilaç çalışmaları için uygun değildir
Memeli ksenograflarla uyumludur Etik kurul onayı gerektirmez
Cerrahi girişimler için oldukça uygundur
*(Özgürtaş T. Anjiyogenezde bir in-vivo model: Civciv koriyoallantoyik membran. Gülhane
Tıp Dergisi 2009;51:67-69)
2.4. Pentoksifilin
idrarla atılır. Biyoyararlanımı oldukça yüksektir. Plazma proteinlerine çok düşük oranda bağlandığı bildirilmiştir. Pentoksifilin oral ve parenteral yoldan uygulanabilir. 1V. enjeksiyonların yatar pozisyonda yapılması önerilmektedir. Non spesifik bir fosfodiesteraz inhibitörü olan pentoksifilin periferik arter hastalığında FDA tarafından onaylanmış bir ilaçtır (54).
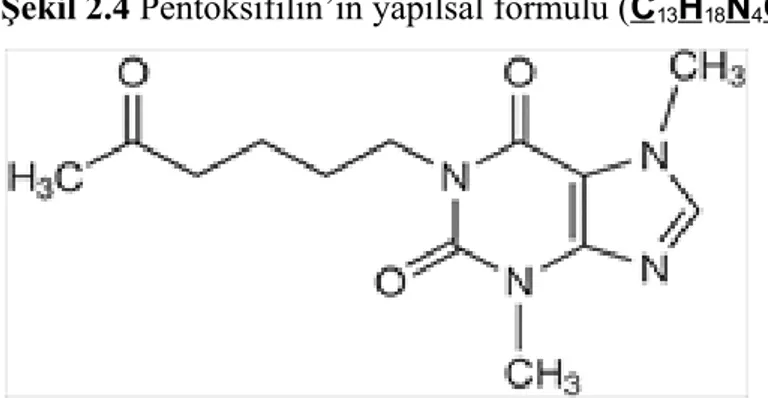
Şekil 2.4 Pentoksifilin’in yapılsal formülü (C13H18N4O3)
Bimetilksantin türevi olan pentoksifilin'in farmakolojik özellikleri kafein ve teofilin'den farklıdır. Alyuvarların deformabilitesini (parçalanabilirliğini) arttırarak, çok küçük çaplı kılcal damarlardan geçişlerini kolaylaştırır ve bu şekilde iskemik dokularda kan akımım artınr. Kan
fibrinojeninin konsantrasyonunu düşürür. Pentoksifilin düşük dozlarda alyuvarların agregasyonunu
önlemektedir. Son yıllarda prostasiklin (PGI2) sentez ve salınımını artırdığı gösterilmiştir. Bu etkisiyle
trombosit adenilat siklazını aktive edip trombosit sAMP düzeyini artırmaktadır. Pentoksifilin
yüksek dozlarda trombosit membranında sAMP fosfodiesteraz ilişikisini de inhibe etmektedir. Bu etkide intraselüler sAMP'yi daha çok artırır. sAMP düzeyindeki artış, siklooksijenazı inhibe ederek platelet agregasyonunu uyaran tromboksan sentezini azaltmaktadır. Değişik araştırmalar periferik damar bozukluğu olanlarda pentoksifilinin trombositler üzerine pozitif etkisi olduğunu ortaya koymuştur. 3 mg/kg pentoksifilin i.v. infüze edildiğinde kan viskozitesinde ve trombosit
agregasyonunda azalma olduğu saptanmştır. Pentoksifilin ayrıca interlökin-1 ve tümör nekrozis
faktörün (TNF) polinükleer nötrofiller üzerindeki etkilerini ve oluşumlarını azaltır. Sitokinlerin neden
olduğu adezivite artışı ve süperoksid, hidrojen peroksid iyonlarının aşırı serbestlenmesini önler. Pentoksifilin damar düz kas lifleri üzerinde gevşetici bir etkiye sahip olduğundan periferik vasküler hastalıklarda mikrosirkulatuvar bozukluğu düzeltebilmektedir. Aynca antitrombotik özelliği ile de damar cerrahilerini izleyen reoklüzyonlan önleyebilmektedir.
Pentoksifilin, arteriyosklerotik, diyabetik ve iltihab orijinli periferik arteriyel ve arteriyovenöz bo-zukluklarda, anjiyonöropatilerde, gözün dolaşım bozukluklarında ve serebral dolaşım bozukluklarında endikasyonu vardır.
Dolaşan kanser hücreleri kapiller ve venüllerin damar endoteline yapışma eğilimi gösterirler. Bunun sonucu da trombosit agregasyonu ve koagülasyon sistemi aktive olur. Trombositler yapışkanlığı
artmış olan tümör hücreleri üzerinde toplanır, multihücre kompleksleri şeklinde mikrovasküler bölgelerde akım zorlaşır, bu da trombüs formasyonunu ve metastazların gelişimini kolaylaştırır. Tromboembolik komplikasyonlar ve dissemine intravasküler koagülasyon kanser hastalannda önemli komplikasyonlardır. Pentoksifilin gibi fosfodiesteraz inhibitörleri trombosit agregasyonunu inhibe ederek kanser hücrelerinin lokalize olup metastaz yapmalarını önleyebilirler. Ayaklarda obliteran kronik arteriopatileri intermitent tedavisinde ve TNF'ün aşırı salgılanmasının görüldüğü bazı septik şoklarda kullanılmaktadır (55).
Preklinik hayvan çalışmalarında pentoksifilin, iyi tolere edilen , toksik olmayan bir ilaçtır. Malign melanoma karşı in vivo ve in vitro çalışmalarda antianjiyogenik ve antimetastatik aktiviteye sahip olduğu gösterilmiştir (56).
Pentoksifilin , yüksek düzeyde metastatik meme kanseri hücrelerine karşı antimetastatik olduğu gösterilmiştir (57). Subtoksik dozlarda pentoksifilin , normal hücreler için herhangi bir toksisite olmadan in vitro ve in vivo olarak tümör büyümesinde, insan melanom hücrelerinin metastazını inhibe ettiği gösterilmiştir (58).
2.5. Bevasizumab
Solid tümörlerin varlığını sürdürebilmesi, büyümesi, invazyon ve metastaz yapmasındaki öneminden dolayı, anjiyogenezin inhibe edilmesine yönelik tedaviler, tümör tedavisinde gittikçe artan bir biçimde yer almaktadır. Bu amaçla kulanılan ilaçlar içerisinde en çok tercih edilenleri VEGF ve VEGF reseptörleri inhibitörleridir, bunlar VEGF’ye ve VEGF reseptörlerine bağlanan monoklonal antikorlardır. Bevasizumab rekombinant humanize edilmiş monoklonal bir IgG1 antikorudur ve VEGF’nin nonspesifik bir inhibitörüdür.
Anjiyogenetik faktörler arasında endoteliyal hücre mitojenlerinin en potent ve spesifik olanı VEGF’dir (59,60). VEGF, greft edilmiş ve doğal olarak oluşmuş tümörlerce en çok üretilen , damar endotel hücrelerine özgü , homodimerik glikoprotein yapısında, 45 kiloDalton (kDa) büyüklüğünde heparin bağlayıcı bir büyüme faktörüdür (61). VEGF, anjiyogenez ve lenfanjiyogenejzi stümüle eder ve vasküler permeabiliteyi artırır (62). Ayrıca, endotel hücrelerinin migrasyonunu stimüle eder. MMP’lar ile uPA ve tPA salınımını uyararak hücre dışı matriks yıkımına yol açar. Bu durum tümör invazyon ve metastazına neden olur (63). VEGF reseptörlerinin aktivasyonu hücre içi sinyal iletim proteinlerini fosforile ederek endotel hücrelerinin proliferasyonunu, migrasyonunu ve farklılaşmasını sağlar (64). VEGF ile uyarım sonucu oluşan NO, endotel hücre migrasyonunda rol alır (65,66).
VEGF, yedi üyeden oluşan bir büyüme faktörü ailesini temsil eder: VEGF-A, VEGF-B, VEGF –C, VEGF-D, VEGF-E, VEGF-F, PIGF-1, PIGF-2 (8,67). Bu faktörlerin VEGF reseptörlerine bağlanma özellikleri farklıdır.
-VEGF-A; Genellikle yalnızca VEGF olarak ifade edilir. VEGF-A, 43-46 kDa ağırlığında homodimerik bir glikoproteindir (68,69). Anjiogenezle en güçlü ilişkisi olan ve üzerinde en çok çalışma yapılan faktördür, patolojik anjiyogenzde de rol oynar. Ayrıca hipoksi ile aktive olduğu gösterilmiş tek VEGF üyesidir. Bu nedenle anti-VEGF tedavilerin çoğu bu faktör üzerine yoğunlaşmaktadır (70). VEGF-A ‘nın içerdikleri aminoasit sayısına göre adlandırılan üç ana izoformu mevcuttur. Bunlardan VEGF121 ve VEGF165 dolaşımda bulunan asıl formlardır. Üçüncüsü ise VEGF145 formudur (71-73).
-VEGF-B; Endotel hücre fonksiyonunu düzenler. Hücre dışı matriks yıkımı, hücre adezyonu ve göçünde rol oynar. Kalp, iskelet kası ve pankreasta fazla miktarda bulunur (74).
-VEGF-C ve VEGF-D; Lenfanjiyogenezi düzenler(90). VEGF-C aynı zamanda yara iyileşmesi üzerine etki eder (75).
-VEGF-E ve VEGF-F; VEGF-A’nın insan dışı canlılardaki homologlarıdırlar (76).
-PIGF-1 ve 2; Hematopoetik kök hücre toplanması için gereklidir (77). Endotel hücrelerinde en çok bulunan VEGF üyesi olan PIGF, VEGF-A’ya bağlı endotel hücre çoğalmasını uyarır (70,78).
VEGF ailesi üyeleri VEGF reseptörlerine bağlanarak etki ederler. Bu reseptörler ilk kez endotel hücreleri üzerinde saptanmışlardır (74). Endotel hücrelerinde transmembran proteini olarak bulunan bu reseptörlerin VEGF eksprese eden hücrelerle yakın komşuluk içerisinde olmaları, VEGF’nin jukstakrin/parakrin sinyal yolağıyla fonksiyon gösterdiğine işaret etmektedir (3). VEGF reseptörleri ; VEGF reseptör 1, VEGF reseptör 2, VEGF reseptör 3 , nörofilin -1 ve nörofilin -2 reseptörleridir (75,79-81).
VEGFR-1’in pozitif ve negatif anjiyogenik etkisi vardır (82). Endotel hücreleri , makrofajlar, monositler, hematopoetik kök hücreleri, damar düz kas hücreleri, perisitler, osteoblastlar ve kolorektal tümör hücrelerinde bulunur (74). VEGFR-2 , VEGF-A’nın anjiyogenik, mitojenik ve vasküler permeabilite artışı etkilerinden sorumludur. VEGFR-2, endotel hücrelerinde, megakaryositlerde, hematopoetik kök hücrelerde, damar düz kas hücrelerinde, retina öncesi hücrelerde ve bazı tümör hücrelerinde (küçük hücreli olmayan akciğer tümörleri, nöroblastom, meme ve mide kanserlerinde) bulunur (74). VEGFR-3, primer olarak lenfatik damarlardaki anjiyogenik etki ile ilişkilidir (78,82-84). Nörofilin -1 , VEGF165’ in VEGFR-2’ye ilgisini artırma işlevinde bulunur (76). VEGFR-3, endotel hücrelerinde , nöronlarda ve aynı zamanda tümör hücrelerinde bulunur (74,86). Nörofilin -2, VEGF165, VEGF145 ve
PIGF’yi bağlar (71). A , VEGFR-1 ve VEGFR-2’ye , B, VEGFR-1’e , VEGF-C ve VEGF-D, VEGFR-1 ve VEGFR-2’ye, PIGF ise VEGFR-1’e bağlanır.
VEGF düzeyi, insan epidermal büyüme faktörü reseptörü 2 (HER-2) , RAS, SRC onkogenleri, p53 gen mutasyonu, PDGF, TGF-β , insülin benzeri büyüme faktörü-1 (IGF-1), TNF-α, interlökin -1β 1β), interlökin – 6 6) , interlölin-10 10), interlökin-13 (IL-13), hipofiz hormonları ve nitrik oksit (NO) gibi birçok endojen ajan ile düzenlenmektedir (56,71,81). Salınım oksidatif stres ile artan hipoksiyle uyarılabilir transkripsiyon faktörü-1 (HIF-1) de VEGF salınımına yol açar (59,60,86,87).
Bevasizumab insan IgG1 iskeleti (%93) ve fare VEGF-bağlayan tamamlayıcı –belirleyici bölgeler içerir (%7). Bu bölgeler VEGF-A izoformlarının endotel hücre yüzeyinde yer alan reseptörlere (VEFR-1) bağlanmasını engelleyerek VEGF’nin biyolojik aktivitelerini inhibe eder. Kanser tedavisinde kullanılmak üzere onay almış ilk antianjiogenik ajan olan Bevasizumab’ın, faz I çalışmalarında kemoterapi ile birlikte kullanıldığında serum VEGF seviyelerini ölçülemeyecek seviyelere kadar düşürdüğü ve farklı tümörlerde büyümeyi inhibe ettiği saptanmıştır(88). Faz III randomize çalışmalarda Bevasizumab’ın ilerlemiş kolorektal kanserler, meme kanserleri ve küçük hücreli olmayan akciğer kanserlerinde kemoterapi ile kombine edildiğinde, yalnızca kemoterapiyle karşılaştırıldığında terapötik yarar sağladığı gösterilmiştir(88-92). Kolorektal kanserli hastalarda 5-florourasil, lökoverin ve oksaliplatin tedavisine eklendiğinde sağ kalımı artırdığının gösterilmiş olmasından sonra, 2006 yılında Bevasizumab’ın metastatik kolon ve rektum kanseri tedavisinde kullanımı onaylanmıştır. İleri evre metastatik meme kanserinin tedavisinde de kemoterapiye ek olarak kullanılmaya başlanan ilacın renal hücreli karsinom, pankreas kanseri, over kanseri ve hormona yanıt vermeyen prostat kanserinde klinik etkinliğine dair çalışmalar devam etmektedir (92). Bevasizumab, genel olarak güvenli kabul edilen bir ilaç olup, kombine edildiği kemoterapötik ilaçların yan etkilerinde ciddi bir artışa neden olmaz. Bevasizumab’ın en sık bilinen yan etkileri proteinüri, hipertansiyon, tromboz, kanama eğilimi ve yara iyileşmesinde gecikmedir.
3.1.Pelletlerin Hazırlanması
Anjiyogenez üzerindeki etkilerini değerlendirmek üzere çalışmamızda pentoksifilin ve bir VEGF monoklonal antikoru olan Bevasizumab kullanıldı. Pentoksifilin ve Bevasizumab’ın kendi sunum formu çözünmüş infüzyon solüsyonu şeklindeydi. İlaçların uygulamasında dört değişik konsantrasyon (10-2 M, 10-3 M , 10-4 M ve 10-5 M) kullanıldı.
İlaçların önce 10-2 M konsantrasyonları hazırlandı. Daha dilüe konsantrasyonlar 10-2 M’lık
stok solüsyonun seyreltilmesi ile elde edildi. Diskin 10 µL’lik final hacminde 10-4 M ‘lık ilaç
konsantrasyonunu sağlayacak ilaç miktarını bulabilmek için klasik molarite formülü kullanıldı. (M=m/V). Her çalışma setinde kayıplar da göz önüne alınarak yaklaşık 90 disk hazırlanarak uygulandı. Bu nedenle , her ilaç için yaklaşık 1 mL’lik agar ve ilaç karışımı hazırlandı. (10µLx100 =1mL)
Kolay uygulama için, solüsyonların pelletleri 5 mm çaplı sirküler paslanmaz çelik yüzeyde 10 µl’lik damlalar şeklinde hazırlanmış ve hızla oda ısısına bırakılarak katılaştırıldı.
3.2.KAM Deneyi
Ross 308 cinsi döllenmiş tavuk yumurtaları temin edildi. Çalışmamız için Dicle Üniversitesi Tıp Fakültesi Hayvan Etik Kurulu’ndan 07.06.2013 tarihli ve 2013/14 sayılı etik kurul onayı alındı.
Döllenmiş tavuk yumurtaları 37.5 0C ‘ de %80 rölatif nemli ortamda horizontal
pozisyonda kuluçkaya yerleştirildi (Şekil 3.1 ve 3.2). Kuluçkanın beşinci gününde yumurtanın künt tarafından enjektör yardımıyla 5-10 ml albumin alındı ve yumurtanın diğer ucundan 2-3 cm çapında kabuk kesilerek çıkarıldı. Kabuktaki bu açıklık laboratuar filmi ile kapatılarak 72 saat daha inkübe edildi (Şekil 3.3). KAM yaklaşık 2 cm çapa ulaştığında her bir yumurtaya bir pellet olacak şekilde koriyoallantoyik membran üzerine etken madde içeren pelletler yerleştirildi (Şekil 3-4). İlaç uygulamasından sonra 24 saatlik ek inkübasyon süresi tanındı. Stereoskopik mikroskop altında Bürgermeister ve ark.nın (93) skorlama sistemi (Tablo 3.1) kullanılarak pellet uygulama bölgesindeki damar yapısı değerlendirildi (Şekil 3.5).
Şekil 3.1. Döllenmiş tavuk yumurtasının şematik gösterimi
Şekil 3.3 Kuluçkanın 5. gününde yumurtaların açılması.
Şekil 3.4. KAM modelinde Pentoksifilin çalışılması aşamaları
A. Albüminin enjektör ile çekilmesi. B. Yumurtada açılan bir pencere ile koriyoallantoyik membrandaki (KAM) anjiyogenezin değerlendirilmesi (x8). D. İlaçla KAM’daki anjiyogenezin inhibisyonu (skor):0.5 (x8)
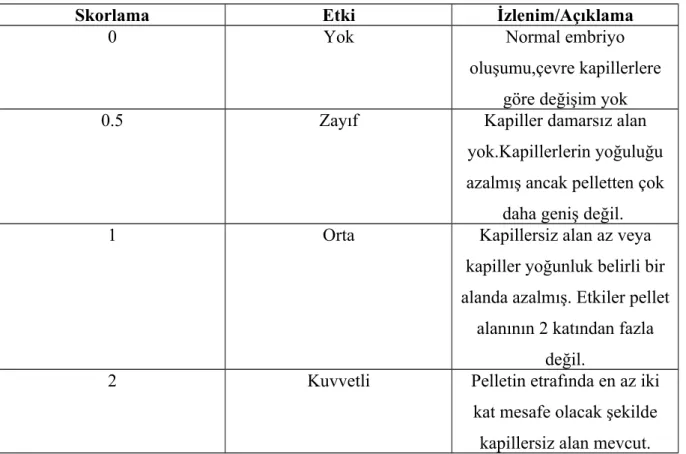
Tablo 3.1. Koriyoallantoyik membran üzerinde anjiyogenik etkinin değerlendirilmesi için
kullanılan skor değerleri.
Skorlama Etki İzlenim/Açıklama
0 Yok Normal embriyo
oluşumu,çevre kapillerlere göre değişim yok
0.5 Zayıf Kapiller damarsız alan
yok.Kapillerlerin yoğuluğu azalmış ancak pelletten çok
daha geniş değil.
1 Orta Kapillersiz alan az veya
kapiller yoğunluk belirli bir alanda azalmış. Etkiler pellet
alanının 2 katından fazla değil.
2 Kuvvetli Pelletin etrafında en az iki
kat mesafe olacak şekilde kapillersiz alan mevcut. Her bir test bileşiği için en az 20 yumurtaya uygulama yapılmıştır. Her deney grubu için sadece agar içeren pelletlerin uygulandığı kontrol yumurtaları da değerlendirilmeye alındı. Tüm testlerin sonuçları iki kez değerlendirildi. Sonuç olarak toplam 142 Uygulama değerlendirilmeye alındı. İlaç gruplarına göre yapılan uygulama sayısı Tablo 3.2’de gösterildi.
10-2 M 10-3 M 10-4 M 10-5 M
Pentoksifilin 17 14 20 17
Bevasizumab 16 19 19 20
Toplam 142
Uygulama sonrası koriyoallantoyik membran (KAM) dışına çıkan ve irritasyon gözlenen yumurtalar değerlendirme dışı bırakılmıştır.
KAM üzerinde kullanılan etken maddelerin değerlendirilmesi için Bürgermeister ve ark. tarafından geliştirilen ortalama skorlama sistemi kullanıldı (88). Ortalama skorun belirlenmesi için kullanılan denklem şudur:
Ortalama skor =[Yumurta sayısı(Skor 2) x 2 + Yumurta sayısı (Skor 1) x ] / [Toplam Yumurta Sayısı(Skor 0,1,2)
Bu ortalama skor sistemine göre ; Skor<0,5 : antianjiyogenetik etki yok,
Skor 0,5-1 : zayıf düzeyde antianjiyogenik etki,
Skor > 1: güçlü antianjiyogenik etki olarak değerlendirilmektedir.
3.3. İstatistiksel Değerlendirme
Veriler n (%) ve ortanca %25-75 interkuartil aralık olarak ifade edildi. Kolmogorov-Smirnov testi ile normal dağılıma uymayan verilerin analizi için Kruskal –Wallis ve Mann-Whitney U testleri kullanıldı. Yanılma düzeyi 0,05 olarak alındı. Çalışmanın sonuçlarına göre power analiz yapıldı.
Pentoksifilin ve kontrol grubu olan bevasizumabın 4 ayrı konsatrasyonunu her biri için 20 ayrı tavuk embriyosu üzerinde uygulandı. (Tablo 4.1).
Bulgularımız , kullandığımız araştırma modelinde Pentoksifilin’in yüksek konsantrasyonlarda (10-2 M, 10-3 M) zayıf antianjiyogenik etkiye sahip olduğunu gösterdi. Düşük dozlarda (10-4
M, 10-5 M) ise 0,5 > olarak izlenerek antianjiyogenik etki görülmedi.
Tablo 4. 1. Pentoksifilinin ve kontrol grubu olan bevasizumabın farklı konsatrasyonlardaki
skorları. Her bir konsantrasyon için 20 adet denek kullanıldı.
Skor 0:Etkisiz, Skor 1: Orta etkili, Skor 2: Etkili, Skor 3: Değerlendirme dışı
Pentoksifilinin 10-2 M, 10-3 M, 10-4 M, 10-5 M konsatrasyonlarda antianjiyogenik ekti
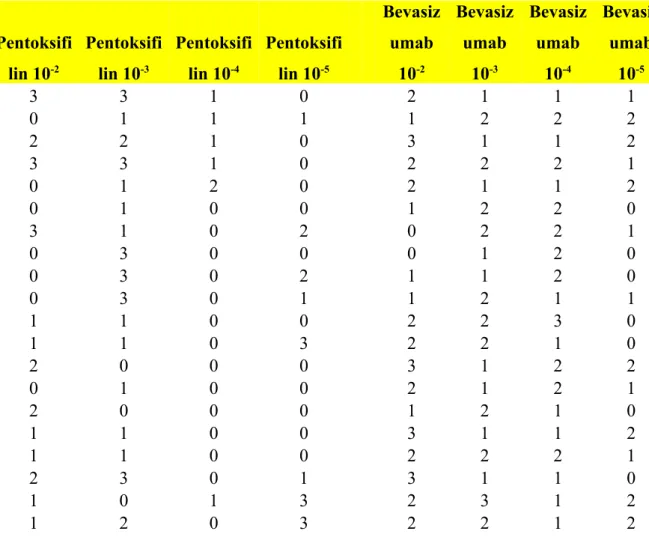
puanları sırasıyla 0.82, 0.92, 0.35,0.41 olarak hesaplandı. Pentoksifilinin birbirleri ile yapılan grup ortalamalarında istatistiksel olarak anlamlı fark vardır (Tablo 4.2.). 10-2 ve 10-3
gruplarında zayıf antianjiyogenik etkinlik saptanmıştır.
Pentoksifi lin 10-2 Pentoksifi lin 10-3 Pentoksifi lin 10-4 Pentoksifi lin 10-5 Bevasiz umab 10-2 Bevasiz umab 10-3 Bevasiz umab 10-4 Bevasiz umab 10-5 3 3 1 0 2 1 1 1 0 1 1 1 1 2 2 2 2 2 1 0 3 1 1 2 3 3 1 0 2 2 2 1 0 1 2 0 2 1 1 2 0 1 0 0 1 2 2 0 3 1 0 2 0 2 2 1 0 3 0 0 0 1 2 0 0 3 0 2 1 1 2 0 0 3 0 1 1 2 1 1 1 1 0 0 2 2 3 0 1 1 0 3 2 2 1 0 2 0 0 0 3 1 2 2 0 1 0 0 2 1 2 1 2 0 0 0 1 2 1 0 1 1 0 0 3 1 1 2 1 1 0 0 2 2 2 1 2 3 0 1 3 1 1 0 1 0 1 3 2 3 1 2 1 2 0 3 2 2 1 2
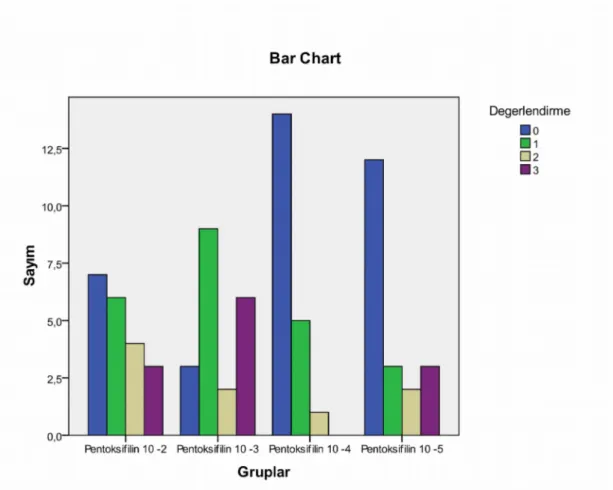
Şekil 4.1. Pentoksifilinin farklı dozlardaki skor-sayım grafiği. (Skor 0:Etkisiz, Skor 1: Orta etkili, Skor 2: Etkili, Skor 3: Değerlendirme dışı)
N Mean Std. Deviation Std. Error 95% Confidence Interval for Mean
Minimum Maximum Gruplar Lower Bound Upper Bound Ölçüm Pentoksifilin 10-2 20 1,15 1,089 ,244 ,64 1,66 0 3 Pentoksifilin 10- 3 20 1,55 1,099 ,246 1,04 2,06 0 3 Pentoksifilin 10 -4 20 ,35 ,587 ,131 ,08 ,62 0 2 Pentoksifilin 10 -5 20 ,80 1,152 ,258 ,26 1,34 0 3 Total 80 ,96 1,084 ,121 ,72 1,20 0 3 K-Ölçüm Pentoksifilin 10 -2 20 1,75 ,910 ,204 1,32 2,18 0 3 Pentoksifilin 10 -3 20 1,60 ,598 ,134 1,32 1,88 1 3 Pentoksifilin 10 -4 20 1,55 ,605 ,135 1,27 1,83 1 3 Pentoksifilin 10 -5 20 1,00 ,858 ,192 ,60 1,40 0 2 Total 80 1,48 ,795 ,089 1,30 1,65 0 3
Ölçüm grupları için sonuç F=5,128 P=0.003 Grup ortalamaları farklıdır. K- Ölçüm için sonuç : F=3,758 0.01 Grup ortalamaları farklıdır
Bulgularımız, kullandığımız araştırma modelinde bevasizumabın yüksek
konsatrasyonlarda belirgin olmak üzere antianjiyogenik etkiye sahip olduğunu gösterdi. Bevasizumabın 10-2 M, 10-3 M, 10-4 M, 10-5 M konsatrasyonlarda antianjiyogenik ekti puanları
sırasıyla 1.68, 1.58, 1.55 ve 1.15 olarak bulundu.
5.TARTIŞMA
Anjiyogenez embriyonal gelişme, menstrüel siklus, yara iyileşmesi gibi birçok fizyolojik olayda rol alan ve proanjiyogenik ve antianjiyogenik faktörlerle sıkı bir biçimde kontrol edilen bir süreçtir (94-96). Erişkin insanlardaki vasküler endoteliyal hücreler tipik olarak düşük yarılanma ömrü hızında olmalarına rağmen, yaşamları boyunca yeni kan damarları oluşturacak çoğalma kapasitesine sahiptirler.
Bu süreç, embriyonik gelişim, normal doku büyümesi, yara iyileşmesi, miyokardiyal iskemi, gözdeki neovasküler hastalıklar, Von-Hippel-Lindau Hastalığı (retinal veya SSS hemanjioblastomuna dair aile hikayesi varlığı ile birlikte renal tümörler, pankreatik kist veya tümörler, feokromasitoma, epididimin papiller kistadenomu varlığı), Herediter Hemorajik Telenjektazi gibi genetik hastalıklar, romatoid artrit gibi kronik inflamatuvar hastalıklar ve kadınlarda üreme döngüsü (ovülasyon, menstrüasyon ve plasenta gelişimi) içinde olduğu gibi malign tümörlerin büyüme ve metastatik yayılımlarında da yer almaktadır (95-98).
Kardiyovasküler hastalıklarda tedavi amaçlı anjiyogenezin faydaları olsa da , güncel çalışmaların bir kısmı da artmış anjiyogenezin kardiyovasküler mortaliteyi artırabileceğine değinmiştir. Özellikle endotelial öncül hücrelerin artış göstermesi stent restenozları , vasküler darlığın artışı gibi durumlardan sorumlu tutulmuştur. Kısacası bozulmuş dinamik dengenin her iki tarafa çekilmesinin de pozitif ve negatif etkileri olabileceği bildirilmiştir.
Pentoksifilin, iyi tolere edilen , toksik olmayan bir ilaçtır. Malign melanoma karşı in vivo ve in vitro yapılan çalışmalarda antianjiyogenik ve antimetastatik aktiviteye sahip olduğu gösterilmiştir.
Bu açıdan çalışmamızda antianjiyogenez özelliği net olarak ortaya konmuş pozitif grup (bevasizumab) oluşturularak periferik arter hastalığında kullanılan non selektif fosfodisesteraz inhibitörü olan pentoksifilinin anjiyogenez inhibisyonu üzerine etkileri karşılaştırıldı.
Bevasizumab, VEGF'nin monoklonal antikorudur ve bazı kanser türlerinin tedavisinde kemoterapiyle kombine olarak uygulanması gittikçe artan bir biçimde kabul görmektedir. Lokal rekürren veya metastatik meme kanseri, skuamöz olmayan küçük hücreli dışı akciğer kanseri, metastatik kolorektal kanser ve metastatik renal hücreli kanser tedavisinde kemoterapi ile birlikte uygulandığında sağ kalımı ve ilk tercih tedaviye yanıt oranını artırdığı saptanmıştır (99,100). VEGF ayrıca diyabetik retinopati ve yaşla ilişkili maküler dejenerasyona ikincil gelişen intraoküler neovaskülarizasyonda da rol oynamaktadır. Neovasküler yaşla ilişkili maküler dejenerasyon ve proliferatif diyabetik retinopatinin tedavisinde intravitreal Bevasizumab uygulamasının yararlı olduğu belirlenmiştir (99,100). Bu bulgular, Bevasizumab'ın in vivo potent antianjiyogenik etkisi ile ilişkilendirilmektedir. Bu nedenle çalışmamızda pozitif kontrol grubunda Bevasizumab kullanılmıştır.
Çalışmamızda, Bevasizumab'ın ortalama antianjiyogenik skorunun l'in üzerinde olduğu, yani güçlü antianjiyogenik etki gösterdiği belirlenmiştir. Pentoksifilinin ise; yüksek molar konsantrasyonlarda zayıf antianjiyogenik ( 10-2 M, 10-3 M, 10-4 M, 10-5 M
konsatrasyonlarda antianjiyogenik ekti puanları sırasıyla 0.82, 0.92, 0.35,0.41 olarak hesaplandı) olduğu gösterilmiştir.
Alyuvarların deformabilitesini (parçalanabilirliğini) arttırarak, çok küçük çaplı kılcal damarlardan geçişlerini kolaylaştıran ve bu şekilde iskemik dokularda kan akımını artıran pentoksifilin; kan fibrinojeninin konsantrasyonunu düşürür. Pentoksifilin düşük dozlarda alyuvarların agregasyonunu önlemektedir. Son yıllarda prostasiklin (PGI2) sentez ve salınımını artırdığı gösterilmiştir. Bu etkisiyle trombosit adenilat siklazını aktive edip trombosit sAMP düzeyini artırmaktadır. Pentoksifilin yüksek dozlarda trombosit membranında sAMP fosfodiesteraz ilişikisini de inhibe etmektedir. Bu etkide intraselüler sAMP'yi daha çok artırır. sAMP düzeyindeki artış, siklooksijenazı inhibe ederek platelet agregasyonunu uyaran tromboksan sentezini azaltmaktadır. Değişik araştırmalar periferik damar bozukluğu olanlarda pentoksifilinin trombositler üzerine pozitif etkisi olduğunu ortaya koymuştur. Pentoksifilin ayrıca interlökin-1 ve tümör nekrozis faktörün (TNF) polinükleer nötrofiller üzerindeki etkilerini ve oluşumlarını azaltır. Sitokinlerin neden olduğu adezivite artışı ve süperoksid, hidrojen peroksid iyonlarının aşırı serbestlenmesini önler. Pentoksifilin damar düz kas lifleri üzerinde gevşetici bir etkiye sahip olduğundan periferik vasküler hastalıklar da mikrosirkulatuvar bozukluğu düzeltebilmektedir. Pentoksifilin , yüksek düzeyde metastatik meme kanseri hücrelerine karşı antimetastatik olduğu gösterilmiştir. Subtoksik dozlarda pentoksifilin , normal hücreler için herhangi bir toksisite olmadan in vitro ve in vivo olarak tümör büyümesinde, insan melanom hücrelerinin metastazını inhibe ettiği gösterilmiştir. Aynca antitrombotik özelliği ile de damar cerrahilerini izleyen reoklüzyonlan önleyebilmektedir.
6.SONUÇ ve ÖNERİLER
Doku perfüzyonunun devamı, hücresel canlılığın ve işlevselliğin korunması için anjlyogenez büyük önem kazanmaktadır, özellikle iskemiye duyarlı miyokard gibi dokularda bu durum daha ön plana çıkmaktadır. Ancak kardiyovasküler hastalıklarda tedavi amaçlı
anjiyogenezin faydaları olsa da , güncel çalışmaların bir kısmı da artmış anjiyogenezin kardiyovasküler mortaliteyi artırabileceğine değinmiştir. Özellikle endotelial öncül hücrelerin artış göstermesi stent restenozları , vasküler darlığın artışı gibi durumlardan sorumlu tutulmuştur. Kısacası bozulmuş dinamik dengenin her iki tarafa çekilmesinin de pozitif ve negatif etkileri olabileceği bildirilmiştir.
Tavuk embriyosu KAM modeli düşük maliyetli, kolay uygulanabilir ve hızlı sonuç veren bir yöntem olması nedeniyle ilaçların antianjiyogenik etkilerinin araştırılmasında gittikçe artan bir biçimde tercih edilmektedir.
Çalışmamızda;
1. Antianjiyogenik etkileri incelenen pentoksifilin’in, bu yöntemle
antianjiyogenik etkinliği net olarak ortaya konmuş bevasizumab ile karşılaştırılmasında net bir antianjiyogenik etki oluşturmadığı, ancak yüksek dozlarda bu etkinin zayıf olabileceği belirlendi.
2. Pentoksifilin’in 10 -2 M ve 10 -3 M konsantrasyonda antianjiyogenik etki puanının, 10 -4 M ve 10 -5 M konsantrasyonlardan yüksek olduğu bulundu.
3. Artmış anjiyogenezin (proanjiyogenik-antianjiyogenik dengenin bozulması) kardiyovasküler mortaliteyi artırabileceği özellikle endotelial öncül hücrelerin artış göstermesi nedeniyle stent restenozları, vasküler darlığın artışı gibi durumlarda; yüksek dozlarda sağladığı zayıf antianjiyogenik etkinlik ve antitrombotik özelliği ile de damar cerrahilerini izleyen reoklüzyonları önleyebilmesi nedeniyle pentoksifilin , periferik arter hastalıkarında tedavi protokollerinde yer alabilir.
4. Bizim çalışmamızın aksine pentoksifilinin proanjiyogenik etkilerinin de ortaya konulması için anjiyogenez aktivasyonunu araştıran çalışmalar klinisyenlere yol gösterici olabilir.
Çalışmamızın sonuçları, periferik arter hastalığı vv e kronik iskemik kalp hastalığında doku kanlanmasının artırılması hedeflendiğine göre, pentoksifilinin antitrombotik özelliği ve antianjiyogenetik olması nedeniyle mevcut aterom plaklarının stabilizasyonunda, stent ve greft restenozunun önlenmesinde mevcut antikoagülan, antitrombotik tedaviye destek amaçlı kullanılabilir.
7.KAYNAKLAR
1. Carmeliet P. Angiogenesis in health and disease. Nat Med. 2003;9(6):653-660. 2. Folkman J ve Klagsbrun M. Angiogenic factors. Science 1987;235(4787):442-447. 3. Zimmerman MA, Selzman CH, Raeburn CD, Calkins CM, Barsness K, Harken AH. Clinical applications of cardiovascular angiogenesis. J Curd Surg. 2001 Nov-Dec; 16(6):490-4. Ribatti D, Vacca, Presta M. The discovery of angiogenic factors: a historical review. Gen Pharmacol. 2000; 35(5):227-231
5. Risau W.Mechanisns of angiogenesis. Nature 1997; 386(6626):671-674
6. Konukoğlu D ve Turhan MS. Anjiyogenezin temel moleküler mekanizmaları ve tümör anjiyogenezi. Cerrahpaşa Tıp Dergisi 2005; 36(l):42-48.
7. Varner JA. The role of vascular cell integrins alpha v beta 3 and alpha v beta 5 in angiogenesis. EXS. 1997; 79:361-390.
8. Ferrara N, Gerber HP, LeCouter J. The biology of VEGF and its receptors. Nat Med. 2003; 9(6):669-676.
9. Asano Y, Ihn H, Yamane K, Kubo M, Tamaki K. Increased expression levels of integrin alphavbeta5 on scleroderma fibroblasts. Am J Pathol. 2004; 164(4):1275-1292.
10.Haubner R. Alphavbeta3-integrin imaging: a new approach to characterise angiogenesis? Eur J Nucl Med Mol Imaging 2006; 33(l):54-63.
11. Greenberg DA ve Jin K. From íinglogenesls to neuropathology. Nature 2005; 438(7070):954~959.
12. Haroon ZA, Peters KG, Greenberg CS, Dewhirst MW. Angiogenesis and Oxygen Transport in Solid Tumors. In: Totowa, New Jersey, Tehicher BA (eds). Antiangiogenic Agents in Cancer Therapy. 3-21 Humana Press, 1999.
13. Al-Rawl MA, Mansel RE, Jiang WG. Molecular and cellular mechanisms of lymphanglogenesls. Eur J Surg Oncol. 2005; 31(2):117-121,
14. Alltalo K ve Carmellet P. Molecular mechanisms of lymphanglogenesls In health and disease. Cancer Cell. 2002; l(3):219-227.
15.Schneider M, Othman-Hassan K, Christ B, Wilting J. Lymphangioblasts in the avian wing bud. Dev Dyn. 1999 ;216(4-5):311-319.
16. Zachary I ve Morgan RD. Therapeutic angiogenesis for cardiovascular disease: biological context, challenges, prospects. Heart. 2011; 97(3):181-9.
17. Buysschaert I, Carmellet P, Dewerchin M. Clinical and fundamental aspects of angiogenesis and anti-angiogenesis. Acta Clin Belg. 2007; 62(3):162-9.
18.Grote K, Salguero G, Ballmaier M, Dangers M, Drexler H, Schieffer B. The angiogenic factor CCN1 promotes adhesion and migration ofcirculating CD34+ progenitor cells: potential role in angiogenesis and endothelial regeneration. Blood. 2007; 110(3):877-85. 19. Patan S. Vasculogenesis and angiogenesis. Cancer Treat Res. 2004; 117:3-32.
20. Patan S. Vasculogenesis and angiogenesis as mechanisms of vascular network formation, growth and remodeling. J Neurooncol. 2000; 50(1-2):1- 15.
21. Schachtner SK, Wang Y, Scott Baldwin H. Qualitative and quantitative analysis of embryonic pulmonary vessel formation. Am J Respir Cell Mol Biol. 2000; 22(2):157-65.
22. Atkins GB, Jain MK, Hamik A. Endothelial differentiation: molecular mechanisms of specification and heterogeneity. Arterioscler Thromb Vase Biol. 2011; 31(7):1476-84. 23. Robbins RM ve Beitel GJ. Vascular lumen formation: negativity will tear us apart. Curr Biol. 2010; 20(22):973-5.
24. Hill JM, Zalos G, Halcox JP, Schenke WH, Waclawiw MA, Quyyumi AA. ve ark. Circulating endothelial progenitor cells, vascular function, and cardiovascular risk. N Engl J Med 2003; 348: 593-600.
25. Hibbert B, Chen YX, O'Brien ER. c-kit-immunopositive vascular progenitor cells populate human coronary in-stent restenosis but not primary atherosclerotic lesions. Am J Physiol Heart Circ Physiol. 2004; 287(2):H518-24.
26. Burri PH, Hlushchuk R, Djonov V. intussusceptive angiogenesis: its emergence, its characteristics, and its significance. Dev Dyn. 2004; 231(3):474-488.
27. Ribatti D. The involvement of endothelial progenitor cells in tumour angiogenesis. J Cell Mol Med. 2004; 8(3):294-300.
28. Hristov M ve Weber C. Endothelial progenitor cells: characterization, pathophysiology, and possible clinical relevance. J Cell Mol Med. 2004; 8(4):498-508.
29. Loscalzo J ve Welch G. Nitric oxide and its role in the cardiovascular system. Prog Cardiovasc Dis. 1995;3 8(2):87-104.
30. Miranda KM, Paolocci N, Katori T, Thomas DD, Ford E, Bartberger MD. ve ark. A biochemical rationale for the discrete behavior of nitroxyl and nitric oxide in the
cardiovascular system. Proc Natl Acad Sei U S A . 2003; 100(16):9196-201.
31. Moncada S ve Higgs EA. The discovery of nitric oxide and its role In vascular biology. Br J Pharmacol. 2006; 147(1):193-201.
32. Murohara T, Asahara T, Silver M, Bauters C, Masuda H, Kalka C. ve ark. Nitric oxide synthase modulates angiogenesis in response to tissue ischemia. J Clin Invest. 1998; 101(ll):2567-78.
33.Fukumura D, Gohongi T, Kadambi A, Izumi Y, Ang J, Yun CO. ve ark. Predominant role of endothelial nitric oxide synthase in vascular endothelial growth factor-induced angiogenesis and vascular permeability. Proc Natl Acad Sci U S A . 2001; 98(5):2604-9
34.Hiasa K, Ishibashi M, Ohtani K, Inoue S, Zhao Q, Kitamoto S, Sata M. ve ark. Gene transfer of stromal cell-derived factor-lalpha enhances ischemic vasculogenesis and angiogenesis via vascular endothelial growth factor/endothelial nitric oxide synthase-related pathway: next-generation chemokine therapy for therapeutic neovascularization. Circulation. 2004; 109(20):2454-61.
(176 Pt l):213-54.
36.Buemi M, Galeano M, Sturiale A, lentile R, Crisafulli C, Parisi A. ve ark. Recombinant human erythropoietin stimulates angiogenesis and healing of ischemic skin wounds. Shock 2004; 22(2):169-173.
37.Townsend CM, Beauchamp DR, Evers MB, Mattox KL (Eds). Sabiston textbook of surgery: the biological basis of modern surgical practice. 17th ed. Philadelphia, Elsevier Saunders; 2004.
38. Hunt TK. Wound Healing. In: Doherty GM (Eds). Current Surgical Diagnosis and Treatment, 12th ed. United States of America, McGraw Hill; 2006:75-88.
39.Waltenberger J. Impaired collateral vessel development in diabetes: potential cellular mechanisms and therapeutic implications. Cardiovasc Res. 2001; 49(3):554-560.
40. Boodhwani M, Sodha NR, Mieno S, Xu SH, Feng J, Ramlawi B. ve ark. Functional, cellular, and molecular characterization of the angiogenic response to chronic myocardial ischemia in diabetes. Circulation 2007; 116(11):I31-I37.
41. Brownlee M. The pathobiology of diabetic complications: a unifying mechanism. Diabetes 2005; 54(6):1615-1625.
42.Buemi M, Vaccaro M, Sturiale A, Galeano MR, Sansotta C, Cavallari V. ve ark. Recombinant human erythropoietin influences revascularization and healing in a rat model of random ischaemic flaps. Acta Derm Venereol. 2002; 82(6):411-417.
43. Altavilla D, Saitta A, Cucinotta D, Galeano M, Deodato B, Colonna M. ve ark. Inhibition of lipid peroxidation restores impaired vascular endothelial growth factor expression and stimulates wound healing and angiogenesis in the genetically diabetic mouse. Diabetes 2001; 50(3):667- 674. 44.Folkman J: Tumor angiogenesis: Therapeutic implications. N Eng1 Med 285:1182-1186, 1971 45. Folkman J: Tumor angiogenesis: A possible control point in tumor growth. Ann Intern Med 82:96-100, 1975
46. Vallee BL, Riordan JF, Lobb RR, Higachi N, Fett JW, Crossley G. ve ark. Tumor-derived angiogenesis factors from rat Walker 256 carcinoma: an experimental investigation and review. Experientia 1985;41(1):1-15.
47. Auerbach R, Auerbach W, Polakowski I. Assays for angiogenesis: a review. Pharmacol Ther. 1991; 51(1):1-11.
48.Ribatti D, Nico B, Vacca A, Roncali L, Burri PH, Djonov V. Chorioallantoic membrane capillary bed: a useful target for studying angiogenesis and anti-angiogenesis in vivo. Anat Rec. 2001; 264(4):317- 324.
49. Melkonian G, Munoz N, Chung J, Tong C, Marr R, Talbot P. Capillary plexus development in the day five to day six chick chorioallantoic membrane is inhibited by cytochalasin D and suramin. J