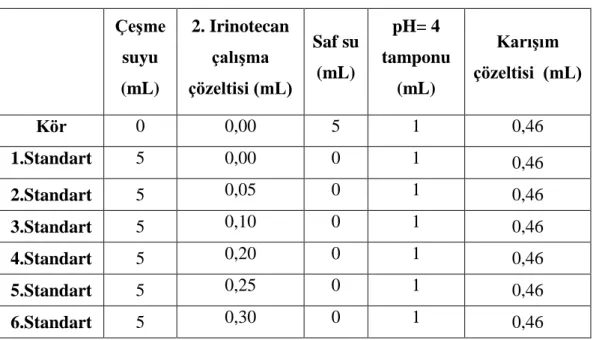
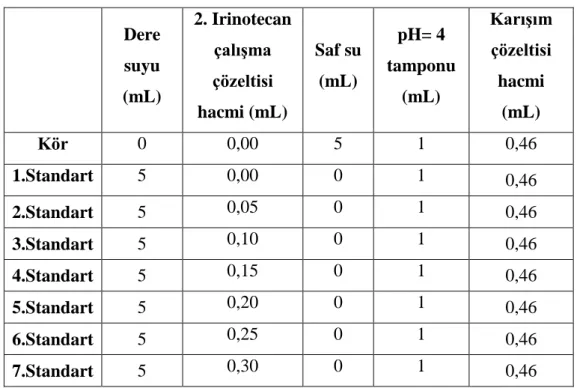
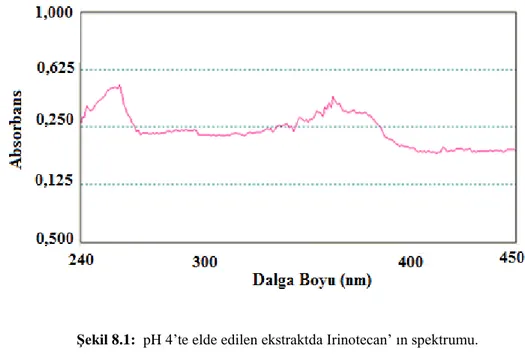
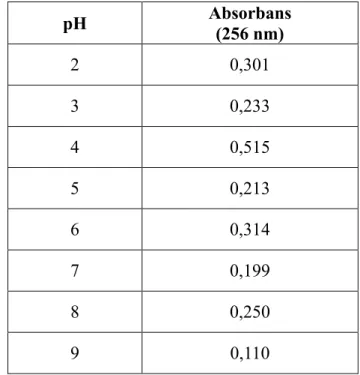
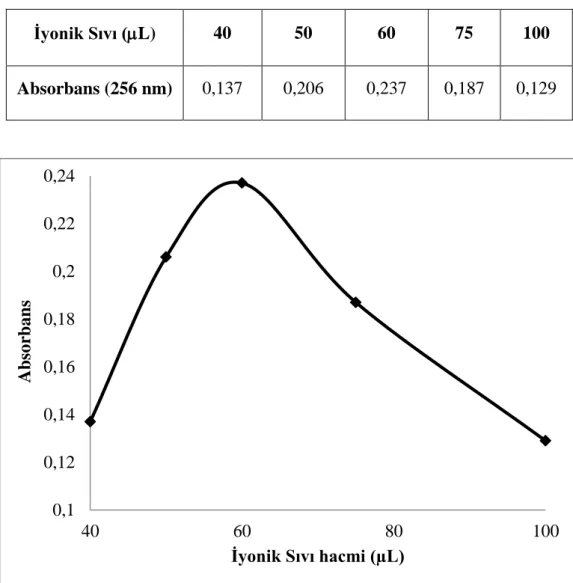
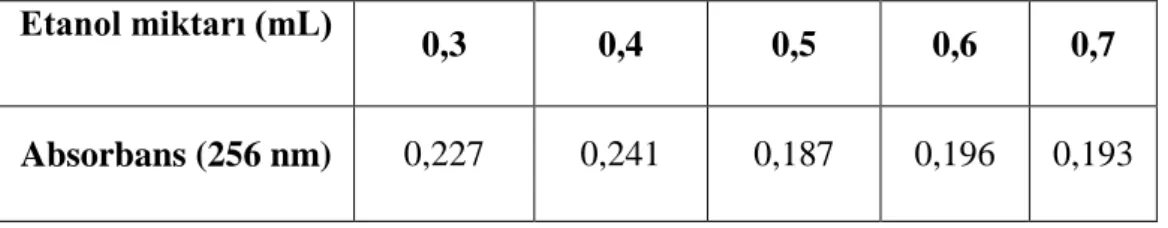
Dispersif sıvı-sıvı mikroekstraksiyonu yöntemi ile irinotecan'ın önderiştirilmesi ve UV-görünür bölge spektrofotometresi ile tayini
Tam metin
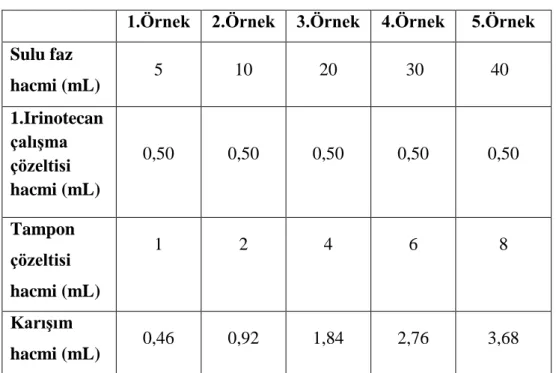
Şekil

Benzer Belgeler
Yoğun işleriniz arasında toplantılara katılmanızı rica edemiyeceğimizi biliyoruz; fakat, Tarih Araştırma Komitesi'nin danışma kuruluna zâtıâlinizi dahil
臺北醫學大學今日北醫: 生命轉角 遇到愛 北醫附設醫院安寧緩和病房啟用典禮 生命轉角 遇到愛
• Eğitim Sen kadınların sorunlarına kulaklarını tıkamayan, genel olarak tüm üniversite emekçilerinin, özel olarak kadınların sorunlarını en iyi bilen ve
Benzer flekilde 2003 y›l›nda medikal onkoloji ünitesinde yatarak tedavi gören kanser hastalar›n›n de¤erlendirildi¤i bir çal›flmada da hastalar›n taburculukta %84
occurring during firing, new crystalline phases are formed, due to which the materials under study acquire the necessary physical and technical properties. By
İkinci olarak, rotorun değişken hızla dönmesi halinde, bir serbestlik dereceli model üzerinden sayısal çözüm aracılığıyla, sistemin bazı parametre bileşimlerinde kaotik
Malzeme toplama sistemi için geliştirilen heterojen filolu rota oluşturma algoritması, ayrık dağıtımı gözeten rota iyileştirme algoritması ve araç atama ve rota çizelgeleme
Deney grubunun yapılan eğitimin meme kanseri ve KKMM inançlarına etkisinin değerlendirmesinde; bu çalışmada girişim öncesi deney ve kontrol grubunun KKMM’ ye