T.C.
SELÇUK ÜNĐVERSĐTESĐ FEN BĐLĐMLERĐ ENSTĐTÜSÜ
ORTAÖĞRETĐM FEN VE MATEMATĐK ALANLAR KĐMYA EĞĐTĐMĐ ANABĐLĐM DALI
BAZĐK AZOT ATOMU TAŞIYAN BAZI KALĐKS[4]AREN TÜREVLERĐNĐN
SENTEZĐ VE ÖZELLĐKLERĐNĐN ĐNCELENMESĐ
HĐLAL ÖZEN KOCABAŞ YÜKSEK LĐSANS TEZĐ
KĐMYA EĞĐTĐMĐ ANABĐLĐM DALI KONYA 2008
ÖZET
YÜKSEK LĐSANS TEZĐ
BAZĐK AZOT ATOMU TAŞIYAN BAZI KALĐKS[4]AREN TÜREVLERĐNĐN SENTEZĐ VE ÖZELLĐKLERĐNĐN ĐNCELENMESĐ
Hilal ÖZEN KOCABAŞ
Selçuk Üniversitesi
Fen Bilimleri Enstitüsü Kimya Anabilim Dalı (Kimya Öğretmenliği Programı)
Danışman: Prof. Dr. Abdulkadir SIRIT 2008, Sayfa: 97
Bu çalışmada p-t-bütilkaliks[4]aren kiral altı yeni amin ve imid türevi (4, 5, 6, 7, 8, 16); 25, 27-Bis(3-bromopropoksi)- 26,28-dihidroksi-5,11,17,23- tetra-t-butil kaliks[4]aren (2), 25,27 Bis (4bromobutoksi) 26,28 dihidroksi 5,11,17,23tetra
-t-butil kaliks[4]aren (3), 5,11,17,23-tetra-t-bütil-25,27 dietoksikarbonilmetoksi-26,28-dihidroksi kaliks[4] aren (14) ile R-(-)- siklohekzil etilamin, S-(+)- siklohekzil etilamin, tartarik asit, (3S,4S)-1-N-benzil-3,4-dihidroksipirolidin-2,6-dion ve L-pirolin metilesteri ile tepkimeye sokularak elde edilmiştir.
Gerçekleştirilen tüm reaksiyonlar ĐTK ile izlenmiş ve elde edilen ürünler kolon kromatografisi ile saflaştırılarak yapıları IR ve 1H NMR, 13C NMR ve FAB MS teknikleriyle aydınlatılmıştır.
.
ABSTRACT
M.Sc. Thesis
THE SYNTHESIS OF SOME CALIX[4]ARENES DERIVATIVES BEARING BASIC NITROGEN ATOM AND EXAMINING OF PROPERTIES
Hilal ÖZEN KOCABAŞ
Selcuk University
Graduate School of Natural and Applied Science Department of Chemistry Education
Supervisor : Prof. Dr. Abdulkadir SIRIT 2008, Page: 97
In this study, six novel chiral imide and amine derivatives of p-t-butylcalix[4]arene (4, 5, 6, 7, 8, 16) have been synthesized from the reaction of 25, 27-Bis(3-bromopropoxy)- 26,28-dihydroxy-5,11,17,23- tetra-t-butyl calix[4]arene (2), 25,27- Bis (4-bromobutoxy)- 26,28- dihydroxy- 5,11,17,23-tetra -t-butyl calix[4]arene (3), 5,11,17,23-tetra-t-butyl-25,27 diethoxycarbonylmethoxy-26,28-dihydroxy calix[4] arene (14) with R-(-)- cyclohexylethylamine, S-(+)- cyclohexyl ethylamine, tartaric acide, (3S,4S)-1-N-benzyl-3,4-dihydroxypyrrolidine-2,6-dion and L-pyroline methylester.
The reactions were monitored by TLC and pure compounds were obtained after crystallysation, column chromatography or both. The structures of synthesized compounds were identified by IR, 1H NMR 13C NMR and FAB MS measurements were also included.
ÖNSÖZ
Bu çalışma, Selçuk Üniversitesi Eğitim Fakültesi Kimya Eğitimi Anabilim Dalı öğretim üyelerinden Prof. Dr. Abdulkadir SIRIT danışmanlığında hazırlanarak, Selçuk Üniversitesi Fen Bilimleri Enstitüsü’ ne Yüksek Lisans Tezi olarak sunulmuştur. Bu çalışma aynı zamanda S. Ü. Bilimsel Bilimsel Araştırma Projeleri Koordinatörlüğü tarafından 07201025 no lu proje ile desteklenmiştir.
Yüksek lisans tez konusunun seçiminde, hazırlanmasında ve çalışmamın her safhasında yardımlarını esirgemeyen, beni bilgi ve tecrübeleriyle yönlendiren değerli danışman hocam Sayın Prof. Dr. Abdulkadir SIRIT’ a saygı ve şükranlarımı sunarım.
Tezimin her aşamasında yardım ve desteklerini gördüğüm çalışma arkadaşım Yüksek Lisans öğrencisi Fatma ATEŞ’ e, Arş. Gör. Mustafa DURMAZ’ a, Doktora Öğrencisi Selahattin BOZKURT’ a, diğer yüksek lisans öğrencileri Burcu KENDĐ ve Havvanur DEMĐRTAŞ’ a ve Gaziantep Üniversitesi Fen- Edebiyat Fak. Kimya Bölümü Öğretim üyelerinden sevgili dostum Yrd. Doç. Dr. Ayşegül KARAKÜÇÜK ĐYĐDOĞAN’ a teşekkür ederim.
Çalışmalarım boyunca devamlı yardım ve desteklerini gördüğüm Fen Edebiyat Fakültesi Kimya Bölümü Öğretim Üyelerinden Sayın Prof. Dr. Mustafa YILMAZ’ a, Selçuk Üniversitesi Eğitim Fakültesi Kimya Eğitimi Anabilim Dalı’ndaki ve Fen-Edebiyat Fakültesi Kimya Bölümü’ndeki diğer hocalarıma, IR spektrumlarımı almamda yardımını hiç esirgemeyen Arş. Gör. Elif YILMAZ ÖZMEN’e teşekkür ederim.
Eşim ve çalışma arkadaşım Erdal’ a bana gösterdiği sonsuz sevgi, destek ve sabır için teşekkür ediyorum. Ayrıca öğrenim hayatım boyunca benden destek ve sevgilerini hiçbir zaman esirgemeyen, her zaman yanımda olmalarından güç aldığım değerli aileme sevgi ve şükranlarımı sunarım.
En önemlisi en güzel anlarında yanında olamadığım, dünyadaki en değerli varlığım; oğlum Emir’ ime, 3 yıl boyunca gösterdiği sabır için sonsuz teşekkürler.
Hilal ÖZEN KOCABAŞ
ĐÇĐNDEKĐLER
ÖZET ... i
ABSTRACT... ii
ÖNSÖZ...iii
ĐÇĐNDEKĐLER ... iv
ŞEKĐLLER LĐSTESĐ ... vii
ÇĐZELGELER LĐSTESĐ ... xi
1. GENEL BĐLGĐLER... 1
1.1. Kaliksarenler ... 2
1.2. Kaliksarenlerin Adlandırılması ... 2
1.3. Kaliksarenlerin Yapısı ve Sentezi... 4
1.3.1. Tek Basamaklı Sentez ( Bazik Ortamda Sentez ) ... 4
1.3.2. Bazik Ortamda Kaliksarenlerin Sentez Mekanizması ... 6
1.3.3. Çok Basamaklı Sentez ... 8
1.3.4. Asit Katalizli Kaliksaren Sentezi ... 9
1.4. Kaliksarenlerin Konformasyonları ... 9
1.5. Fonksiyonlandırılmış Kaliksarenlerin Sentezi ... 12
1.5.1. Fenolik –OH’lar (Lower Rim) Üzerinden Fonksiyonlandırma ... 13
1.5.2. para-Pozisyonları (Upper Rim) Üzerinden Fonksiyonlandırma ... 14
1.6. Kaliksarenlerin Fiziksel Özellikleri... 16
1.7. Kaliksarenlerin Kullanım Alanları ... 17
1.7.1. Kaliksarenlerin Molekül veya Đyon Taşıyıcı Olarak Kullanılması ... 17
1.7.2. Kaliksarenlerin Enzim Mimik Olarak Kullanılması ... 24
1.7.3. Enantiyomerlerin Tanınmasında Kaliksarenlerin Kullanılması ... 25
1.7.4. Kaliksarenlerin Kromatografide Kullanılması... 33
1.7.5. Kaliksarenlerin Katalizör Olarak Kullanılması ... 35
2. KAYNAK ARAŞTIRMASI ... 40
4. DENEYSEL BÖLÜM... 54
4.1. Çalışmanın Amacı ... 54
4.2. Kiral Kaliks[4]aren Türevlerinin Sentezi ... 57
4.2.1. 5,11,17,23-Tetra-t-bütil-25,26,27,28-tetrahidroksikaliks[4]aren (1) ... 57
4.2.2. 25, 27-Bis(3-bromopropoksi)- 26,28-dihidroksi- 5,11,17,23- tetra (ter-butil) kaliks[4]aren (2) ... 58
4.2.3. 25,27- Bis (4-bromobutoksi) - 26,28- dihidroksi- 5,11,17,23-tetra (ter-butil) kaliks[4]aren (3) ... 58 4.2.4. Bileşik 4 ... 59 4.2.5. Bileşik 5 ... 60 4.2.6. Bileşik 6 ... 60 4.2.7. Bileşik 7 ... 61 4.2.8. Bileşik 8 ... 61
4.2.9. 25,27- Dimetoksi - 26,28- dihidroksi- 5,11,17,23 - tetra (ter-butil) kaliks[4]aren (9)... 62
4.2.10. 25,27- Dimetoksi- 26,28- di-(karbometoksimetoksi)- 5,11,17,23-tetra (ter-butil) kaliks[4]aren (10) ... 62
4.2.11. 25,27- Dimetoksi- 26,28- di-(2-hidroksietoksi)- 5,11,17,23-tetra (ter-butil) kaliks[4]aren (11) ... 63
4.2.12. 25-27- Dimetoksi- 28,28- di (etansülfoniloksietoksi)- 5,11,17,23-tetra (ter-butil) kaliks[4]aren (12) ... 64
4.2.13. Bileşik 13 ... 64
4.2.14. 5,11,17,23-tetra-ter-bütil-25,27 dietoksikarbonilmetoksi-26,28-dihidroksi kaliks[4] aren (14) ... 65
4.2.15. Bileşik 15 ... 65
4.2.16. Bileşik 16 ... 66
4.2.17. (3R,4R)-1-N-Benzil-3,4-dihidroksipirolidin-2,6-dion (17) ... 66
4.2.18. (3R,4R)-1-N-Benzil-3,4-dihidroksipirolidin (18)... 67
5. ARAŞTIRMA SONUÇLARI VE TARTIŞMA... 68
5.1. Çalışmanın Amacı ... 68
6. SONUÇ VE ÖNERĐLER... 77
8. EKLER... 87 ÖZGEÇMĐŞ... 97
ŞEKĐLLER LĐSTESĐ
Şekil 1.1. Supramoleküllerin yapısı (Siklodekstrinler, crown eterler, kaliksarenler .. 1
Şekil 1.2. Kaliks[4]arenin adlandırılması için numaralandırma sistemi... 3
Şekil 1.3. Siklik tetramerlerin sentezi... 4
Şekil 1.4. Kaliksarenlerin tek basamaklı sentezi ... 5
Şekil 1.5. Formaldehit ve p-substitüe fenolün baz katalizli reaksiyon sonucunda hidroksimetil fenolü oluşturması ve ardından diarilmetil bileşiklerinin oluşumu ... 6
Şekil 1.6. Lineer tetramer ... 7
Şekil 1.7. Birbiriyle yaklaşık olmayan çok basamaklı sentez ... 8
Şekil 1.8. p-t-Bütilkaliks[4]arenin ve sübstitüe kaliks[4]arenlerin konformasyonları ... 10
Şekil 1.9. Farklı konformasyonlardaki kaliks[4]arenlere ait metilen köprülerinin 1H NMR ve 13C NMR sinyalleri ... 11
Şekil 1.10. Kaliks[4]arenin p-konumunun ve fenolik OH’larının şematik gösterimi ... 12
Şekil 1.11. p-t-Bütilkaliks[4]aren’in para- pozisyonu ve fenolik -OH üzerinden fonksiyonlandırılması ... 15
Şekil 1.12. p-Alkilkaliks[4]aren’ in kompleks oluşturma mekanizması ... 17
Şekil 1.13. Çalışmada sentezlenen kaliks[4]aren diamid türevleri... 19
Şekil 1.14. Kiral kaliks[4](azoksa)crown-7 bileşiğinin sentezi... 20
Şekil 1.15. Kiral kaliks[4](azoksa)crown-7 türevinin Li+ ve geçiş metali katyonlarıyla yaptığı kompleksleşmenin mekanizması ... 21
Şekil 1.16. para-Pozisyonuna üre bağlı kaliks[4]aren türevlerinin uygun guestler varlığında dimerik kapsül oluşturması... 21
Şekil 1.17. Dimerler tarafından enkapsüle edilen guest moleküller ... 22
Şekil 1.18. Kaliks[4]aren diamit türevlerinin kromat anyonuyla farklı pH’ larda yaptığı etkileşme grafiği. ... 23
Şekil 1.19. Kaliks[4]aren diamit türevlerinin kromat anyonuyla yaptığı muhtemel etkileşme. ... 23
Şekil 1.21. 12-17 bileşiklerinin kataliz ettiği p-nitrofenil benzoat (PNB) ve asetat
(PNA)... 24
Şekil.1.22. Metalloenzimler için etkili kaliks[6]aren yapısı... 25
Şekil 1.23. p-Allilkaliks[4]arenin propranolol amit türevi (6) ve (S)-2-dinaftilprolinol kaliks[4]aren türevi (7) (kiral merkezler yıldızla gösterilmiştir) ... 26
Şekil 1.24. Fenilalaninol ve fenilglisinolün enantiyomerleri... 26
Şekil 1.25. Çalışmanın genel sentez şeması. ... 27
Şekil 1.26. Ekstraksiyon çalışmasında kullanılan aminler. ... 28
Şekil 1.27. Optikçe aktif α, β-amino alkol grupları taşıyan kiral kaliksarenler... 29
Şekil 1.28. NMR spektrumları (a) 9a (5mM); (b) 9a (5mM) ve 10a (20mM) kompleksi; (c) 9a (5mM) ve 10a (92mM) kompleksi; (d) 9b (5mM); (e) 10b (5mM); (f) 9b (5mM) ve 10b (5mM) kompleksi... 30
Şekil 1.29. Çalışmanın genel sentez şeması. ... 31
Şekil 1.30. Ekstraksiyon çalışmasında kullanılan seçilmiş amino asit metil esterleri. ... 31
Şekil 1.31. Çalışmada kullanılan kaliksaren ve resorsinaren durgun fazları. ... 33
Şekil 1.32. Đncelenen analitlerin yapıları. ... 33
Şekil 1.33. p-t-Butil kaliks[6]-1,4-benzocrown-4 bağlı durgun fazın sentez şeması. ... 34
Şekil 1.34. Çalışmada faz transfer katalizörü olarak kullanılan kiral kaliksaren türevleri. ... 35
Şekil 1.35. Benzofenon glisin imin esterinin katalitik alkilasyonu ile α-alkil α-amino asit esterlerinin sentezi... 36
Şekil 1.36. Çalışmada gerçekleştirilen aldol reaksiyonu ve katalizör olarak kullanılan kaliksaren türevleri... 37
Şekil 1.37. Pendant grupları içeren kiral kalik[4]aren türevleri ... 38
Şekil 1.38. Ti(IV)/kaliksaren kompleksinin katalizör olarak kullanıldığı asimetrik aldol kondenzasyonu... 39
Şekil 2.1. Dikromat anyonlarının ekstraksiyonu için kullanılan kaliks[4]aren diamit türevleri ... 40
Şekil 2.2. 5 – 10 reseptörlerinin dikromat ekstraksiyon yüzdeleri ... 41
Şekil 2.3. Kaliks[6]arenin kiral türevleri ... 41
Şekil 2.5. Çalışmada kullanılan amino sülfonamit bileşiğinin sentez şeması. ... 43
Şekil 2.6. Çalışmada kullanılan kiral sülfonamit bileşiğinin sentez şeması. ... 45
Şekil 2.7. Kiral katalizör varlığında gerçekleştirilen reaksiyon ve reaksiyona ilişkin sonuçlar. ... 45
Şekil 2.8. Farklı aldehitler kullanarak kiral katalizör ve Et2Zn varlığında gerçekleştirilen reaksiyonlar ve bunların sonuçlarına ilişkin veriler. ... 46
Şekil 2.9. Çalışmada kullanılan kiral Kaliks[4]crown bileşiğinin sentez şeması. .... 48
Şekil 2.10. (a) 2 no.lu bileşiğin; (b) Rasemik mandelik asidin ve (c) 5mM 2. bileşik ve 5 mM rasemik mandelik asit karışımının CDCl3 içindeki 1H NMR spektrumu... 48
Şekil 2.11. Çalışmada kullanılan kaliks[4]aren bileşiğinin sentez şeması. ... 49
Şekil 2.12. Duble kaliks[4]aren bileşiğinin sentez şeması. ... 50
Şekil 2.14. Kaliks[4]arenin 8-hidroksikinolin türevinin sentez şeması... 51
Şekil 2.15. Kaliks[4]arenin 8-hidroksikinolin türevinin aromatik bölge 1H-1H COSY NMR spektrumu... 52
Şekil 4.1. Kaliks[4]arenin kiral amin ve imid türevinin sentez şeması ... 54
Şekil 4.2. Kaliks[4]arenin kiral amin ve imid türevinin sentez şeması ... 55
Şekil 4.3. Tartarik asitten çıkarak imid ve pirolidin sentez şeması ... 56
Şekil 5.1. p-t-Bütilkaliks[4]arenin sentezi ... 68
Şekil 5.2. p-t-Bütilkaliks[4]arenin dibrom türevlerinin sentezi ... 68
Şekil 5.3. Bileşik 4... 69
Şekil 5.4. Bileşik 5... 69
Şekil 5.5. Bileşik 17 nin sentezi... 70
Şekil 5.6. Bileşik 6’nın sentezi ... 70
Şekil 5.7. Bileşik 7 nin sentezi... 71
Şekil 5.8. Bileşik 8’ in sentezi ... 71
Şekil 5.9. 9 numaralı bileşiğin sentezi ... 72
Şekil 5.10. 25,27- dimetoksi- 26,28- di-(karbometoksimetoksi)- 5,11,17,23-tetra (ter-butil) kaliks[4]arenin sentezi ... 72
Şekil 5.11. 25,27- dimetoksi- 26,28- di-(2-hidroksietoksi)- 5,11,17,23-tetra (ter-butil) kaliks[4]arenin sentezi... 73
Şekil 5.12. 25-27 Dimetoksi- 28,28- di (etansülfoniloksietoksi)- 5,11,17,23-tetra (ter-butil) kaliks[4]arenin sentezi ... 73
Şekil 5.14. p-t-Bütilkaliks[4]arenin diester türevinin sentezi... 74
Şekil 5.15. 15 nolu bileşiğin sentezi ... 75
Şekil 5.16. Bileşik 16 nın sentezi... 75
ÇĐZELGELER LĐSTESĐ
Çizelge 1.1. Ligandlarla metal pikratlarının sıvı –sıvı ekstraksiyon yüzdeleri ... 20 Çizelge 1.2. Kiral guest bileşiklerinin kloroform içerisinde 25 ˚C’de yaptığı kompleksleşmeler için bağlanma sabitleri (K), enantiyoseçicilikler (KR/KS) ve
termodinamik parametreler... 28 Çizelge 1.3. Seçilmiş amino asit metil esterleri ile 1,2,3 ve 4a ‘ün ekstraksiyon yüzdeleri... 32 Çizelge 1.4. Katalitik enantiyoselektif faz transfer benzilasyonu için kullanılan FTK.’den elde edilen sonuçlar. ... 36 Çizelge 1.5. 1 ile 2a’ nın 3a ürününü vermek üzere gerçekleşen aldol reaksiyonu . 38 Çizelge 2.1. Amino asit metilesterlerinin 16 ve 17 ligandlarıyla ekstraksiyon yüzdeleria... 42 Çizelge 2.2. Çalışmada (R,R)-2 kodlu bileşiğin varlığında gerçekleştirilen Mannich reaksiyonu ve elde edilen sonuçlar. ... 44 Çizelge 2.3. Farklı ketonlar ve Et2Zn varlığında kiral katalizör kullanılarak
1. GENEL BĐLGĐLER
Supramoleküler Kimyada birinci ve ikinci kuşak olarak anılan crown eterler ve siklodekstrinlerden sonra üçüncü kuşak olarak tanımlanan kaliksarenler, glukoz birimlerinden oluşan siklodekstrinler ve etilen birimlerinden oluşan crown eterlere benzer olarak fenol ve metilen birimlerinden oluşan metasiklofan sınıfına ait bileşiklerdir (Şekil 1.1). (Gutsche 1989). Bu bileşiklerin sahip olduğu özelliklerin yanında artı özelliklere de sahip olan kaliksarenler büyük miktarlarda sentezlenebilir ve çok kolay fonksiyonlandırılabilirler. Sabit halka yapıları nedeniyle de metal iyonlarını ve nötral molekülleri seçici olarak tutma özeliğine sahiptirler. Bu yüzden sentez ve uygulama alanları büyük önem kazanmaktadır. (Karaküçük 2006)
O OH O H OH O O OH O H O OH O O OH OH O O H O OH OH O O H O OH O H O H O O OH O H OH n O O O O O O OH HO OH OH R R R R n n
Şekil 1.1. Supramoleküllerin yapısı (Siklodekstrinler, crown eterler, kaliksarenler
1.1. Kaliksarenler
Kaliksarenler, bilerek veya bilmeyerek 1870’ li yıllardan beri sentezlenmektedir. Tekararlanabilir sentezi ve kesin yapısının tayini ise ancak 1980’ li yıllarda gerçekleştirilebilmiştir. Supramoleküler ve biomimetik davranışa sahip olan makrosikliklerin bu sınıfı oldukça uzun bir geçmişe sahiptir. Đlk sentezi 1872 yılında Alman organik kimyacı Adolph Von Baeyer tarafından gerçekleştirilmiştir (Thurman 1982). Daha sonraları Baekeland 20. yüzyılın başlarında yine fenol türevi olarak katı ve esnek bir reçine elde etmiş ve bu reçineye bakalit adını vermiştir (Baekeland). 1941 yılında Zinke ve ark. p-t-butilfenol ve formaldehiti NaOH varlığında etkileştirmiş ve sonunda 340 derece erime noktasına sahip, yüksek molekül ağırlıklı ve çözünürlüğü az olan bir ürün elde etmişlerdir(Zinke 1944). 1955 yılında Cornforth tarafından kaliksarenin alkil eterlerinin antituberkular etkileri ile ilgili bir çalışma yayınlanmıştır ama kaliksarenlerin özellikle de kaliks[4]arenlerin sentezi için gerekli optimum şartlar ve yapı tayini Gutsche tarafından belirlenmiştir. Günümüze kadar kaliksarenlerin sentezi ve uygulama alanları ile ilgili yüzlerce yayın ve kitap yazılmıştır. Özetle tanımlamak gerekirse; kaliksarenler, fenolik boşluğa sahip metilen köprüleri birbirine bağlı fenol halkalarından oluşan 2,6 metasiklofanlardır.
1.2. Kaliksarenlerin Adlandırılması
Kaliksarenleri ilk sentezleyen Zinke ve Ark. onları (1952) “Cyclischen Mehrkernmethylenephenol verbindungen” şeklinde adlandırmışlardır. Conforth ve ark. (1955) kaliksarenleri “tetrahydroxycyclotetra-m-benzylenes” şeklinde, Hayes ve Hunter (1958) ise “Cyclicetetranuclear novolaks” şeklinde adlandırmışlardır. Kaliksarenler metasiklofan sınıfına ait bileşikler olması sebebiyle de Patrick ve
Egan (1977) tarafından siklofan bileşiklerine benzerliklerinden dolayı “Metacyclophane olarak adlandırılmışlardır.
Kaliksarenlerin, IUPAC tarafından da kabul edilen pratik ve kısa adlandırılması ise bu bileşiklerin yapısı tam olarak aydınlatılmış ilk sentezini gerçekleştiren Gutsche (1978) tarafından yapılmıştır. Gutsche bu makrosiklik bileşikleri “Calix Creater” olarak bilinen yunan vazosuna benzettiği için “Calix[n]arenes” olarak adlandırmıştır. Burada “Calix” kelimesi yunancada vazo anlamında olan “chalice” kelimesinden gelmektedir. “Arene ise aromatik halkayı ifade etmektedir. “n” harfi ise yapıdaki aromatik halka sayısını ifade etmektedir. IUPAC’ a göre kaliksarenlerin sistematik adlandırılması için numaralandırma sistemi kullanılmıştır. Şekil. 1.2. de görülen, kısa ve pratik adı p-t- butil-kaliks[4]aren olan bileşik “5,11,17,23-tetraalkil-25,26,27,28-tetrahidroksi kaliks[4]aren olarak adlandırılır.
OH OH R R HO OH R R 1 2 3 4 5 6 7 8 11 17 23 25 26 27 28 9 10 12 13 14 15 16 18 19 20 21 22 24
1.3. Kaliksarenlerin Yapısı ve Sentezi
Makrosiklik kaliksarenler p-substitue fenoller ve formaldehitin aşağıda belirtilen prosedürlerden biri ile p-substitue fenoller ve formaldehitin kondensasyonundan elde edilebilmektedir.
1.3.1. Tek Basamaklı Sentez ( Bazik Ortamda Sentez )
Makrosiklik kaliksarenlerin yapısı ilk defa 1941 yılında Zinke ve Ziegler tarafından açıklanmıştı. Onlar p-substitue fenoller ve formaldehiti bir baz varlığında ve yüksek sıcaklıkta muamele etmişler ve sonuçta Şekil 1.3’ de gösterildiği gibi yüksek erime noktasına sahip siklik tetramerik yapılar elde etmişlerdir.
OH R CH2O OH CH2 OH R 4 + + H2O
R=metil, siklohekzil, t-butil, fenil, izobutil....vb.
-Şekil 1.3. Siklik tetramerlerin sentezi
Bununla birlikte elde edilen ürünler karışıktı ve tekrarlanabilir verimler elde edilememişti. Hatta Zinke ve Ziegler, oluşan bu ürünlerin konformasyonel
özelliklerini ve enzim mimik özellik gösterebilecek moleküler uygun madde olma potansiyellerini değerlendirememişlerdir.
1970’li yılların başında, Gutsche enzim mimikler için potansiyel adaylar olan Zinke’nin siklik tetramerleriyle ilgilenmiş ve onlar için kullanışlı ve kolay bir sentez metodu önermiştir.
p-tert-butil fenolden yola çıkılarak; çözücüler, bazlar, reaktanların oranları ve diğer şartlar değiştirilerek siklik tetramer, hekzamer ve oktamer yapıları yüksek bir verimle Şekil.1.4’ de gösterildiği gibi elde edilmiştir.
OH CH2O CH2 OH 4 OH CH2O CH2 OH 6 OH CH2O CH2 OH 8 + + H2O 4 4 0,045 eq NaOH
difenil eter , refluks 4
+ + H2O 6 6 0,34 eq KOH ksilen , refluks 6 %50 %85 + + H2O 8 8 0,03 eq NaOH ksilen , refluks 8 %65
1.3.2. Bazik Ortamda Kaliksarenlerin Sentez Mekanizması
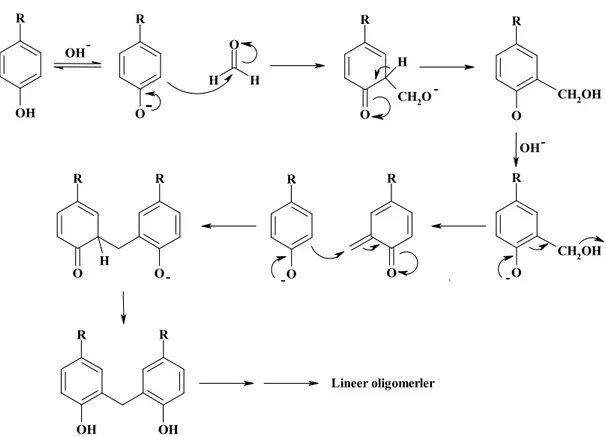
Kaliksarenlerin bazik ortamdaki sentezlerinin ilk basamağı Şekil 1.5’de görüldüğü gibi fenolat anyonunun, hidroksimetilfenol oluşturmak üzere formaldehitle kondenzasyonunu içerir.
Bu tip bileşikler; uzun yıllar önce sulu formaldehitin fenolle bazik bir çözelti içerisinde, oda şartlarındaki reaksiyonu sonucunda hazırlanmıştır (Wegler, 1963). Hidroksimetilfenolün başlangıç fenolü ile müteakip kondenzasyonu sonucunda lineer dimerler, trimerler, tetramerler vd. oluşur ve bu prosesler nispeten ılıman şartlar altında gerçekleşir. Lineer dimer, trimer ve tetramerlerin oluşumu hidroksimetilfenollerin su kaybetmesiyle oluşan o-kinonmetit ve fenolat anyonları ara ürünleri arasındaki Michael katılması tipi reaksiyonu sonucu gerçekleşir.
R OH R O O H H R O H CH2O R O CH2OH OH OH R O CH2OH R O R O R O R O H R OH R OH -Lineer oligomerler
Şekil 1.5. Formaldehit ve p-substitüe fenolün baz katalizli reaksiyon sonucunda hidroksimetil fenolü oluşturması ve ardından diarilmetil bileşiklerinin oluşumu
Oluşan dimerik yapı, reaksiyonun devam etmesi sonucunda önce trimerik ardından da tetramerik yapıya dönüşür (Şekil 1.6.).
OH R OH R OH R OH R OH
Şekil 1.6. Lineer tetramer
Elde edilen karışımın HPLC analizi sonucunca 36 dan fazla siklik olmayan bileşenin varlığı belirlenmiştir ancak hiç siklik bileşen tespit edilememiştir (Gutsche 1989). Bu karışımdan siklik oligomerlerin nasıl oluştuğu ise hala belirsizliğini korumaktadır; fakat hidrojen bağının bu proseste önemli bir rol oynadığı yönünde kanıtlar bulunmaktadır. Kaliksarenlerin çok güçlü molekül içi hidrojen bağlarına sahip olduğu infrared spektrumlarında yaklaşık 3200 cm-1 de görülen OH gerilme bantları ile belirlenmiştir. p-tert-bütilkaliks[4]aren’in X-ray kristalografyası katı halde koni konformasyonunda bulunduğunu göstermektedir ki bu durumda dört tane OH grubu birbirine çok yakın konumda bulunmaktadır.
1.3.3. Çok Basamaklı Sentez
Kaliksarenler para pozisyonlarının hepsinde aynı substituentlerin kullanılmasıyla tek basamaklı olarak sentezlendiği gibi farklı substituentler kullanılarak da çok basamaklı olarak sentezlenebilmektedir. Birbiriyle yaklaşık olmayan sentez tipinde başlangıç maddesi olarak o-bromo-p-alkil fenol kullanılarak gerçekleştirilen kondensasyon basamakları sonucunda hidroksi metil grupları bağlı lineer oligomer yapılar elde edilir. Bu lineer yapıdaki ürünün dehalojenasyonundan seyreltik şartlar altında halkalaşma gerçekleşir (Şekil.1.7.).
OH R 1 Br2 OH R 1 Br CH2O OH R 1 Br OH OH R 2 OH R 1 Br OH R 2 OH OH R 1 Br OH R 2_3 OH OH R 4 CH2 OH R 1_4 4 OH
1.3.4. Asit Katalizli Kaliksaren Sentezi
Her ne kadar p-alkilfenoller formaldehit ile oldukça kolay biçimde asit katalizli kondenzasyona uğrasa da bu reaksiyon sonucunda kaliksarenlerin oluştuğuna dair herhangi bir kanıt yoktur. Kaliksarenler yerine oluşan ürünler önemli ölçüde zincir uzunluğuna sahip lineer oligomerlerdir (Burke 1956). Bununla beraber p-t-bütilfenol ile s-trioxane, kloroform içerisinde p-toluen sülfonik asit varlığında oldukça yüksek verimli kaliksarenler sentezlenebilmektedir (Gutsche 1990).
1.4. Kaliksarenlerin Konformasyonları
Serbest fenolik hidroksil grupları içeren kaliksarenlerin hepsi oda sıcaklığında çözelti içersinde konformasyonel olarak hareketlidir. Đlk defa Cornforth ve ark. (1955) kaliksarenlerin konformasyonel izomeriye sahip olduğunu fark etmişlerdir. Gutsche bu izomerleri, koni, kısmi koni, 1,2 karşılıklı ve 1,3 karşılıklı olarak tasnif etmiştir.
OH O H OH OH OH OH OH OH OH OH OH OH OH HO OH OH R R R R R R R R R R R R R R R R Koni Kısmi koni 1,3-karşılıklı 1,2-karşılıklı koni kısmi koni 1,3-karşılıklı 1,2-karşılıklı
Şekil 1.8. p-t-Bütilkaliks[4]arenin ve sübstitüe kaliks[4]arenlerin konformasyonları
Birbirlerine en uygun uzaklıkta bulunan serbest hidroksil gruplarına sahip kaliksarenlerin kristal yapılarının hepsi katı durumdayken koni konformasyonuna sahiptir. Burada hidroksil grupları arasındaki molekül içi hidrojen bağlarından dolayı yapı bu konformasyonda kararlı haldedir.
Kaliksarenler 1H-NMR spektroskopisinden çok rahat görüleceği üzere çözelti içerisinde koni konformasyonu dışında da bulunabilir. p-tert-butil kaliks[4]arenler koni konformasyonu için 1H-NMR spektroskopisinde Ar-H, -OH ve C(CH3)3 protonları singlet verirken köprüdeki metilen gruplarının her bir hidrojeni
için ise bir çift dublet verir. Zaten kaliksaren konformasyonlarının yapıları da özellikle bu metilen köprülerindeki sinyallere bakılarak tespit edilir.
Şekil 1.9. Farklı konformasyonlardaki kaliks[4]arenlere ait metilen köprülerinin 1H NMR ve 13C NMR sinyalleri
Konformasyonlar; sentezde kullanılan çözücü, bazdaki metalin atom çapı ve reaksiyon sıcaklığına bağlı olarak farklılıklar gösterebilir. Eğer sentezde çözücü olarak kaliksaren türevleri ile kompleks oluşturan aprotik çözücüler (toluen, brombenzen, karbontetra klorür….vs.) kullanılırsa konformasyon dönüşüm hızının azaldığı görülmüştür. Aprotik çözücülerin tersine aseton, asetonitril, piridin gibi protik çözücüler kullanıldığında ise bu tip çözücülerin molekül içi hidrojen bağını zayıflatmalarından dolayı konformasyon dönüşüm hızı artar. Kaliksarenlerin sentezinde kullanılan bazın metalinin atom çapıda konformasyonda etkilidir. Eğer sentezde atom çapı küçük (NaH, Na2CO3,….vs.) bir metale sahip baz kullanılırsa
karşılıklı konformasyonun da kaliksarenler elde edildiği görülmüştür (Iwamoto 1990). Kaliksarenlerin konformasyonlarının sıcaklığa bağlı olarak değiştiği 1H NMR spektrumu incelenirse açıkça görülür. Düşük sıcaklıklarda metilen köprülerine ait protonlar bir çift dublet verirken yüksek sıcaklıklarda keskin bir singlet verir (Gutsche 1985). Kaliksarenler fonksiyonlandırılırken yapıya bağlanan moleküllerde konformasyonu etkiler. Eğer yapıya upper rim veya lower rim kısmından hacimli gruplar bağlanırsa konformasyon dönüşüm hızı en aza indirilmiş olur (Arnaud-Neu,1992). Yine yapının her bir aril halkasına molekül içi köprüler kurulmasını sağlayacak crown eter grupları bağlayarak konformasyon dönüşüm hızı en aza indirilebilir (Takeshita 1995).
1.5. Fonksiyonlandırılmış Kaliksarenlerin Sentezi
Kaliksarenler fenol hidroksi gruplarının bulunduğu fenolik -OH veya diğer adıyla dar (narrow) rim kısmından ve aril halkasına göre para pozisyonundaki t-butil gruplarının bulunduğu p-pozisyonu veya diğer adıyla geniş (wide) rim kısmından fonksiyonlandırılabilirler. R 1 O H R 3 O H R 2 R 4 OH O H O H O H O H O H para po zisyonu fenolik -O H kısm ı
1.5.1. Fenolik –OH’lar (Lower Rim) Üzerinden Fonksiyonlandırma
Kaliksarenlerin lower rim üzerinden fonksiyonlandırılmaları; alkil, karbonat, asetat, ester, amit, keton, amin, imin, oksim ve kiral alkil gruplar gibi birimlerin bağlanmasıyla gerçekleştirilir (Bott 1986, Arduini 1984, McKervey 1985, Ungaro 1984, Sırıt, 2005, Yılmaz 2005, Durmaz 2006). Eter türevleri Williamson eter
sentezi’ne göre alkil halojenürlerle reaksiyon sonucu elde edilir. α-halokarbonil bileşikleri ile olan reaksiyonlar da özel bir öneme sahiptir; çünkü esterler, asitler, amit ve keton türevleri iyonofor olarak kullanılabilecek özelliktedir.
Tüm OH grupları üzerinden fonksiyonlardırma yaygındır, fakat seçimli modifikasyon da mümkündür (Yoshimura 1996). p-tert-bütilkaliks[4]aren’in tetraalkil eterleri ve esterleri oluşturmak üzere tamamen alkillenmesi ya da açillenmesi farklı reaksiyon şartları altında gerçekleştirilebilir ve eğer hacimli gruplar lower rime bağlanırsa olası tüm konformasyonların karışımı oluşur (Groenen 1991). Stereokimyanın kontrolü uygun baz ve çözücünün seçimi ile sağlanabilir. Bu sayede kaliks[4]arenin 1,2-di, 1,3-di, tri ya da tetra eter ya da ester türevleri kolaylıkla hazırlanabilir. Örneğin; p-tert-bütilkaliks[4]aren’in alkilasyonu baz olarak NaH ve çözücü olarak ise DMF ve THF kullanılarak gerçekleştirilirse sadece koni konformasyonu oluşur. Bu reaksiyonda mono, di ya da tri alkillenmiş ürünler gözlenmemiştir (Shinkai 1993). Asetonitril içerisinde sezyum karbonatın kullanılması ile 1,3 karşılıklı konformasyon elde edilirken, benzen içerisinde potasyum tert-bütoksitin kullanılması ile kısmi koni konformasyonlu ürünler elde edilir. 1,2 karşılıklı konformasyon ise dört basamakta gerçekleştirilir.
Farklı reaksiyon şartları altında bu konformasyonların seçici oluşumlarına ilişkin mekanizmalar henüz belirlenmemiştir. Kaliksarenlerin lower rimden seçici fonksiyonlandırılmasına ilişkin birkaç metot geliştirilmiştir. Kemo-seçici fonksiyonel grup bağlanmasının ardındaki dayanak noktası kaliks[4]arendeki fenolik hidroksil gruplarının asitlik farklılığına dayanır. Genellikle, sezyum florür gibi zayıf bir bazın aşırısı çözücü olarak DMF içerisinde alkilleme reaktifinin aşırısı ile etkileştirilirse monoalkoksi kaliks[4]aren elde edilir. 1,3-dialkoksi kaliksarenler, kemoseçici olarak aseton ya da asetonitril içerisinde potasyum karbonat; 1,2-dialkoksi kaliksarenler ise çözücü olarak DMF, baz olaraksa sodyum hidrür ve 2.2
ekivalan alkilleme reaktifi kullanılarak elde edilir. DMF içerisinde baryum hidroksit/baryum oksit kullanılmasıyla trialkoksi kaliksarenler elde edilir.
1.5.2. para-Pozisyonları (Upper Rim) Üzerinden Fonksiyonlandırma
Kaliksarenlerin sentezinde başlangıç maddesi olarak p-t-bütilfenolün kullanılmasının en önemli avantajları verimin yüksek olması, tek bir ürün oluşması ve tersiyer bütil gruplarının kolaylıkla giderilebilmesidir. Fenolik halkanın para pozisyonuna da birçok fonksiyonel grup bağlanarak kaliksaren türevleri elde edilebilir (Gutsche 1985, 1986, 1988, Shinkai, 1986, Memon 2001, Sırıt 2004, Karaküçük 2005).
Tersiyer bütil gruplarının dealkilasyonu kaliksaren kimyasında anahtar bir reaksiyondur. Çünkü bu reaksiyonla kaliksarenlerin para pozisyonu boşaltılmış olur. Çözücü olarak toluenin kullanıldığı bir ortamda AlCl3 ve fenol varlığında
dealkilasyon reaksiyonu gerçekleştirilebilir. Böylece doğrudan elektrofilik sübstitüsyon reaksiyonu ile para pozisyonuna açil, alkil, sülfo ve nitro gibi farklı sübstituentler bağlanabilir.
Kaliksarenlerin upper rim üzerinden fonksiyonlandırılması için halojenasyon (Gutsche 1985, Hamada 1990, Arduini 1990, Timmerman 1994), sülfolama (Gutsche 1985, Shinkai 1986), nitrolama (Loon 1992, Verboom 1992), açilleme (Gutsche 1986), klorsülfolama (Morzherin 1993), diazonyum tuzları bağlama (Deligöz 2002, Shinkai 1989), klormetilasyon (Almi 1989, Nagasaki 1993), formilasyon (Arduini 1991, Van Loon 1992), aminometilasyon (Gutsche, Nam 1988, Alam 1994) gibi elektrofilik “kinon metit” tipi sübstitüsyon reaksiyonları kullanılmaktadır.
Fenolik halkanın para pozisyonundan fonksiyonlandırma için kullanılan metotlardan p-Claisen çevrilmesi metodunda ise, fenolik oksijene bağlanmış olan alil eter gruplarının p-pozisyonuna transferi gerçekleştirilir (Gutsche 1985). Elde
edilen çift bağa katılmalar sonucu farklı fonksiyonel gruplara dönüşüm sağlanabilmektedir.
Hem fenolik OH hem de fenolik halkanın para pozisyonu üzerinden fonksiyonlandırma ile kaliksarenlerin pek çok farklı türevi elde edilmiştir. Bu metotlar gelecekteki çalışmalara da ışık tutacaktır. Fonksiyonlandırma metotları şematik olarak Şekil.1.11 de gösterilmiştir.
Şekil 1.11. p-t-Bütilkaliks[4]aren’in para- pozisyonu ve fenolik -OH üzerinden fonksiyonlandırılması OH Bu 4 4 OH H 4 OH R 4 OH R 4 OH R 4 OH R Bu 4 OR Bu 4 OR R=SO3H R=NO2 R=Br R=CH2CH2NH2 R=CHO R=CH2CH2CN R=CH=NOH R=CH2CH2OH R=CH2CH2N3 R=CH2COH R=CH2CN R=CH2OCH3 R=CH3 R=CH2N3 R=CH3 R=CH2CH3 R=C6H5 R=CH3 R=CH2COR R=CH2COONH2 R=CH2COOR R=CH2C6H5 R=COCH3 R=COC6H5 p-Kinonmetit metodu t t t fenolik OH p-pozisyonu Elektrofilik Substitusyon p-Claisen Çevrilmesi p-Klormetilasyon Metodu Dealkilasyon
1.6. Kaliksarenlerin Fiziksel Özellikleri
Kaliksarenler, oda sıcaklığında kristal yapıda ve katı halde bulunan bileşiklerdir. Fiziksel özellikleri fenolik -OH grupları arasındaki intramoleküler hidrojen bağlarıyla belirlenir. Erime noktaları 300°C’ nin üzerindedir. Örneğin p-t-bütilkaliks[4]arenin erime noktası 342-344 ˚C iken; p-t-bütilkaliks[6]aren için 380-381 ˚C ve p-t-bütilkaliks[8]aren için 411-412 ˚C dir. Ancak türevleri daha yüksek veya düşük sıcaklıklara sahiptir. Örneğin eter ve ester türevlerinin erime noktaları 200°C civarındadır (Gutsche, 1991). Organik çözücülerde çözünürlükleri az olduğu için ayrılmaları, saflaştırılmaları ve yapılarının belirlenmesi zordur. Ancak kloroform, piridin, karbon disülfür, dimetil formamit ve dimetil sülfoksit gibi organik çözücülerde yeterli miktarda çözünürler. Kaliksarenlerin fonksiyonlandırılmasıyla, hem organik çözücüler içerisindeki hem de sudaki çözünürlükleri değişebilmektedir Örneğin ester, sülfonat ve amino gibi fonksiyonel bir grup bulunduran kaliksarenlerin sudaki çözünürlüğü artmıştır (Arduini 1984). Bununla beraber çözünürlüğe etkisi olan bir diğer durum ise, kaliksarenlerin para pozisyonunda bulunan grupların farklılığıdır. Öyle ki para pozisyonunda oktil gibi uzun zincirli alkil gruplarının bulunması çözünürlüğü önemli şekilde artırmıştır.
Spektroskopik özelliklerine bakıldığında 280 nm civarında absorbansı olduğu görülür. Kaliksarenlerin IR spektrumlarında ise parmak izi bölgeleri (900-1500 cm-1) aynıdır. Ayrıca fenolik -OH gruplarına ait titreşim pikleri 3150-3300 cm-1 de görülür. Bu spektrumlar molekül içi hidrojen bağlarından dolayı yayvandır. Kaliksarenlerin yapı tayininde ve konformasyonlarının tespitinde en çok 1H NMR spektrumları kullanılır. Fenolik -OH gruplarına ait hidrojenlerin piki 10 ppm civarında olması gerekirken molekül içi hidrojen bağlarının perdeleme etkisinden dolayı yukarı alana kaymıştır ve bir singlet verir. Para pozisyonundaki tersiyer bütil gruplarına ait hidrojenler yüksek sıcaklıkta singlet verirken düşük sıcaklıklarda bir çift dublet verir. Aril halkaları arasındaki metilen köprüsü hidrojenlerinin pikleri ise konformasyona göre değişir ve 3.0-4.5 ppm arasındadır.
1
H NMR ile çözelti içerisindeki kaliksarenlerin konformasyonları tespit edilebilirken katı fazdaki kaliksarenlerin konformasyonları X-ray kristalografisinden yararlanılarak bulunabilir. Kaliksarenlerin yapılarının belirlenmesinde kütle
spektrofotometresinden de yararlanılır. FAB MS tekniği ile kaliksaren türevlerinin kütlesi belirlenebilir.
1.7. Kaliksarenlerin Kullanım Alanları
1.7.1. Kaliksarenlerin Molekül veya Đyon Taşıyıcı Olarak Kullanılması
Kaliksarenler farklı konformasyonları ve yapılarında bulunan halka boşluğu sayesinde iyonları ve küçük nötral molekülleri tersinir olarak tutabilirler. (Şekil.1.12.) Bu kompleksler endo- ve ekzo- kompleksler şeklindedir.
R R R
R
OH
OH OH
HO
Nötral Guest (Konuk)
Đyonik Guest (Konuk)
veya
Endo- Kompleks
Ekzo- Kompleks Host (Ev sahibi)
+
R R R R OH OH HO OH R R R R OH OH HO OHŞekil 1.12. p-Alkilkaliks[4]aren’ in kompleks oluşturma mekanizması
Bu komplekslere p-t-butilkaliks[4]arenin benzen, ksilen, toluen ve anisol gibi çözücülerle verdiği tersinir moleküler kompleksler örnek verilebilir. Kaliksarenlerin
organik moleküllerle verdiği komplekslerin 250°C’ nin üzerinde bile uzaklaştırılamaması çok sağlam kompleksler verdiğini göstermektedir. Kaliksarenler fenolik -OH gruplarındaki hidrojenlerin güçlü bazların etkisiyle iyonlaşabilmesi zayıf asidik karakterde olduğunu gösterir. Bundan dolayı aminlere proton vererek kompleks yapabilirler (Gutsche, 1987).
Kaliksarenler hem polar hem de apolar bölgeler içerirler. Kaliksarenlerin polar bölgesi alkoller, esterler, eterler ve amid gruplarının oksijenleri arasına metal iyonlarını bağlayabilen bir boşluktan oluşur. Metal iyonlarıyla kaliksarenlerin kompleksleşmesiyle ilgili ilk çalışma Izatt ve ark. (1983) tarafından gerçekleştirilen alkali metal iyonlarının özellikle de Cs+ iyonunun kaliksarenleri kullanarak sulu fazdan organik faza taşınmasını inceledikleri çalışmadır.
Yılmaz ve ark. 2008 yılında yaptıkları bir çalışmada polimere bağlı kaliks[aza]crown türevlerini sentezlemişler ve bu yapıların metal ekstraksiyon özelliklerini incelemişlerdir. (Şekil 1.13.)
Şekil 1.13. Çalışmada sentezlenen kaliks[4]aren diamid türevleri
Sırıt ve ark (2005), koni konformasyonunda yeni bir kiral kaliks[4](azoksa)crown-7 türevini sentezlemişler ve alkali, toprak alkali ve geçiş metallerinin sıvı-sıvı ekstraksiyonu çalışmalarında kullanmışlardır (Şekil 1.14.)
OH OH O O O O OMe OMe OH OH O O O O N N O O O Ph Ph H H 5 6
Şekil 1.14. Kiral kaliks[4](azoksa)crown-7 bileşiğinin sentezi
Ekstraksiyon sonuçlarına bakıldığında diğer alkali metaller arasından Li+ metal katyonunun sulu fazdan organik faza çok yüksek miktarda taşındığı ve geçiş metalleri için bu kaliksaren türevinin iyi ekstraksiyon yeteneğine sahip olduğu tespit edilmiştir (Çizelge 1.1.).
Çizelge 1.1. Ligandlarla metal pikratlarının sıvı –sıvı ekstraksiyon yüzdeleri
Ekstrakte edilen metal pikrat yüzdesi (%)
Ligand Li+ Na+ K+ Cs+ Co2+ Cu2+ Cd2+ Ni2+ Pb2+ Hg2+ 5 <1.0 <1.0 <1.0 <1.0 <1.0 <1.0 <1.0 3.7 22.3 29.2 6 22.9 1.0 8.7 <1.0 42.2 61.5 47.3 26.3 82.3 83.3
H H O OH OH O O O O N N O O Ph Ph M nPic n+ OH OH O O O O N N O O O Ph Ph H H Li Pic +
Şekil 1.15. Kiral kaliks[4](azoksa)crown-7 türevinin Li+ ve geçiş metali katyonlarıyla yaptığı kompleksleşmenin mekanizması
6 nolu bileşiğin Li+ katyonunu büyük oranda sulu fazdan organik faza taşımasının nedenini muhtemelen kaliksaren boşluğunun bu katyonun geometrik yapısına uygun olması şeklinde açıklamışlardır. Kaliksarene bağlı bulunan crown yapısındaki üç tane oksijen atomunun elektrostatik olarak Li+ katyonuyla etkileşmesi sonucu küçük iyon çapına sahip olan katyon bu boşluğa girerek yapının sabit kalmasını sağlar. Daha büyük atom çapına sahip geçiş metallerinde ise etkileşim yapıda bulunan beş oksijen ve iki azot atomuyla olmaktadır (Şekil 1.15.). Rebek (2000) yaptığı bir çalışmada Ken tarafından sentezlenen üre birimleri bağlı kaliks[4]aren türevlerini ve uygun guestler varlığında yaptığı kompleksleri modellemiştir (Şekil 1.16. ve Şekil 1.17.).
Şekil 1.16. para-Pozisyonuna üre bağlı kaliks[4]aren türevlerinin uygun guestler varlığında dimerik kapsül oluşturması
Şekil 1.17. Dimerler tarafından enkapsüle edilen guest moleküller
Kaliksarenlerin anyonlarla yapılan kompleksleşme çalışmaları katyonlarla yapılan kompleksleşme çalışmalarına göre daha azdır. Anyonlarla yapılan çalışmalarda genellikle reseptör olarak kaliksarenlerin amit türevleri kullanılmıştır (Beer, 1995). Kaliksarenlerin kompleks yapma gücünü anyonun büyüklüğü ve hidrojen bağları etkiler. Ayrıca kullanılan anyonların lewis bazları olması da kaliksarenlerin kompleks yapmasını kolaylaştırır.
Sırıt ve ark. (2005) yaptıkları bir çalışmada kaliks[4]arenin diamit türevlerini sentezlemişler ve bu bileşiklerin dikromat anyonu ile farklı pH değerlerinde ekstraksiyonlar yapmışlardır. Düşük pH’ larda bileşiklerin dikromat anyonunu ekstrakte ederken yüksek pH’ larda bu etkinin azaldığı görülmüştür.
Şekil 1.18. Kaliks[4]aren diamit türevlerinin kromat anyonuyla farklı pH’ larda yaptığı etkileşme grafiği.
Şekil 1.19. Kaliks[4]aren diamit türevlerinin kromat anyonuyla yaptığı muhtemel etkileşme.
1.7.2. Kaliksarenlerin Enzim Mimik Olarak Kullanılması
Kaliksarenler enzim mimik özellik gösterebilecek şekilde uygun gruplarla fonksiyonlandırılırsa enzimin aktif bölgesini oluşturarak substratların katalitik olarak ürünlere dönüşmesini sağlayabilir.
Dospil ve ark. (2001), kaliks[4]arenin upper rimi üzerine farkı pozisyonlarda imidazol grupları bağlamışlar ve tampon çözeltisi içersinde p-nitrofenil ester bileşiğinden p-nitrofenolü elde etmek için açil transferaz enzimine benzer şekilde katalizör olarak kullanmışlardır.
N N OR OR O H OR N N N N OR OR O H OH N N N N OR OR O H OR 12 (R = H; 70%) 13 (R = Bz; 72%) 14 (R = H; 90%) 15 (R = Bz; 85%) 16 (R = H; 70%) 17 (R = Bz; 81%)
Şekil 1.20. Açiltransferaz aktivite gösteren kaliks[4]aren türevleri.
O O2N R O OH O2N MeOH/H2O yada MeOH/MeCN Katalizör R = Ph, PNB R = Me, PNA
Şekil 1.21. 12-17 bileşiklerinin kataliz ettiği p-nitrofenil benzoat (PNB) ve asetat (PNA)
Reinaud ve ark. (2002), kaliks[6]aren türevlerini sentezlemişler ve bunların bakır komplekslerini oluşturmuşlardır. Oluşturdukları bu yapı metalloenzimlerde aktif merkeze substrat kanal girişi için güzel bir model örneğidir. (Şekil.1.22.)
Şekil.1.22. Metalloenzimler için etkili kaliks[6]aren yapısı.
1.7.3. Enantiyomerlerin Tanınmasında Kaliksarenlerin Kullanılması
Kiral tanınma biyolojik sistemlerde önemli bir rol oynar. Örneğin, sadece L-amino asitler proteinlerin yapıtaşlarıdır. Amino asitlerin hidrojen bağı protein içerisinde onun üç boyutlu yapısına ve buna bağlı işlevselliğine katkıda bulunur. Amino asitler ve peptitleri taşıyan makrosiklik platformlar biyolojik sistemlerdeki organizasyonel ve moleküler tanınma proseslerinde kullanılmak üzere tasarlanmıştır (Bügler 1998, Schneider 2000). Her ne kadar basit kaliksarenler moleküler tanınma için uygun bir boşluğa sahip olsalar da onların çok büyük olan simetrik yapıları bunları akiral kılar. Bu nedenle, biyolojik aktiviteye sahip kaliksarenlerin mutlaka kiral olması gerekir.
N O 4 O O H O N O 4 O O H 6 7 * *
Şekil 1.23. p-Allilkaliks[4]arenin propranolol amit türevi (6) ve (S)-2-dinaftilprolinol kaliks[4]aren türevi (7) (kiral merkezler yıldızla gösterilmiştir)
Kiral kaliksarenlerle ilgili özellikle kiral seçicilik ve enantiyomerik tanınma üzerine çok sayıda çalışma yapılmıştır. Örneğin, Diamond ve ark. (2002) kaliks[4]arenin floresans özellik gösteren kiral türevlerini (Şekil 1.23.) sentezleyerek fenilalaninol ve fenilglisinolün enantiyomerleri arasındaki seçicilikleri kaliksarenin floresansının söndürülmesinden yararlanarak incelemişlerdir.
OH H NH2 * OH NH2 H * (R ve S) fenilalaninol OH H N H2 * OH N H2 H * (R ve S) fenilglisinol
Sırıt ve ark. 2008 yılında yaptıkları bir çalışmada kaliks[4]arenin kiral mono ve diamit türevlerini sentezlemişler bu maddelerin R ve S aminlerle olan etkileşimini incelemişlerdir.
CH3 H N H2 CH3 H N H2 CH3 H N H2 CH3 H N H2 (S)-(-)-1-feniletilamin (R)-(-)-1-feniletilamin (S)-(-)-1-siklohekziletilamin (R)-(-)-1-siklohekziletilamin
Şekil 1.26. Ekstraksiyon çalışmasında kullanılan aminler.
Çizelge 1.2. Kiral guest bileşiklerinin kloroform içerisinde 25 ˚C’de yaptığı kompleksleşmeler için bağlanma sabitleri (K), enantiyoseçicilikler (KR/KS) ve
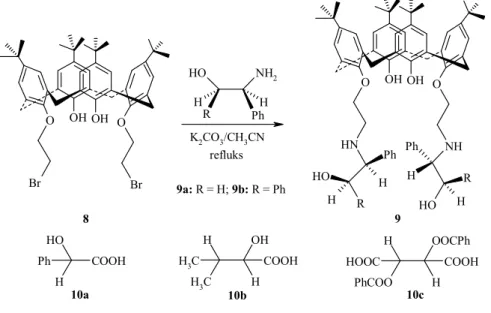
Zheng ve ark. (2004) lower riminde optikçe aktif α, β-amino alkol grupları taşıyan kaliksaren türevleri sentezlemişler ve 1H NMR spektroskopisini kullanarak bu molekülleri rasemik mandelik asit, 2,3-dibenzoiltartarik asit ve 2-hidroksi-3-metilbütirik asitin kiral tanınmasında kullanmışlardır (Şekil 1.27. ve Şekil 1.28).
8 O Br Br O OH OH NH2 O H R H H Ph K2CO3/CH3CN refluks O N H NH O OH OH R HO O H H R H H H Ph Ph 9 9a: R = H; 9b: R = Ph O H H Ph COOH H3C H C H3 OH H COOH H PhCOO OOCPh H COOH HOOC 10a 10b 10c
Şekil 1.28. NMR spektrumları (a) 9a (5mM); (b) 9a (5mM) ve 10a (20mM) kompleksi; (c) 9a (5mM) ve 10a (92mM) kompleksi; (d) 9b (5mM); (e) 10b (5mM); (f) 9b (5mM) ve 10b (5mM) kompleksi
Yılmaz ve ark. 2006 yılında yaptıkları bir çalışmada yeni kiral kaliks[4]aren triamid türevlerini sentezlemişler ve bu türevlerin sıvı-sıvı ekstraksiyon metoduyla seçilmiş amino asit metil esterlerine karşı ekstraksiyon özelliklerini incelemişlerdir.
Şekil 1.29. Çalışmanın genel sentez şeması.
Çizelge 1.3. Seçilmiş amino asit metil esterleri ile 1,2,3 ve 4a ‘ün ekstraksiyon yüzdeleri. Ligand D-AlaOMe L-AlaOMe D-PheOMe L-PheOMe D-TrpOMe L-TrpOMe 1b <0.1 <0.1 <0.1 <0.1 <0.1 <0.1 2 <0.1 <0.1 <0.1 <0.1 <0.1 <0.1 3 54.1 56.5 71.3 68.5 68.4 69.7 4 59.5 57.4 65.8 67.5 62.6 68.3
a Sulu faz, {amonyum pikrat] = 2 X 10-5 M; organik faz, diklormetan, [ligand]= 1 X 10-3 M; 25 °C; 1 saat. b Organik faz olarak kloroform kullanıldı.
Yapılan çalışmada 1 ve 2 nolu reseptörlerin seçilen aminoasit metil esterleri için iyi bir ekstraktant özelliği göstermediği görülmüştür. Fakat 3 ve 4 nolu reseptörlerin iyi seçicilik özelliği göstermesede iyi bir ekstraktant olduğu gözlenmiştir.
1.7.4. Kaliksarenlerin Kromatografide Kullanılması
Jira ve ark. 2002 yılında durgun faza bağlı kaliksaren ve resorsinaren türevlerini HPLC’ de kolon dolgu maddesi olarak kullanmışlar ve thioxanthene, dibenz[b,e]oxepin’ in cis ve trans izomerlerini ayırma çalışmalarını gerçekleştirmişlerdir.
Şekil 1.31. Çalışmada kullanılan kaliksaren ve resorsinaren durgun fazları.
N N S OH CF3 N N S OH Cl N S CF3 O N
flupentiksol klopentiksol kloropprotiksen doksepin
Şekil 1.32. Đncelenen analitlerin yapıları.
Liu ve ark. 2004 yılında yaptıkları çalışmada p-tert-butil kaliks[6]-1,4-benzocrown-4 bağlı durgun fazının sentezi ve karakterizasyonunu gerçekleştirmişler
ve bu polimer yapıyı sıvı kromatografide aromatik bileşiklerin ayrılması için kullanmışlardır. OH OH ClCH2CH2OH NaOH OCH2CH2OH OCH2CH2OH SO2Cl C H3 OCH2CH2OTs OCH2CH2OTs 6 K2CO3, Toluene O O O O 6 O Si OH O C H2 O (CH2)3 Si OMe OMe
OMe toluen, trietilamin refluks, N2 O Si O Si (CH2)3 O CH2 O toluen, NaH katalizör, refluks O Si O Si (CH2)3 O CH2 CH OH CH2 O 6 O O 1 (OH)6 1 (OH)4 2 + + 2 (OH)3
p-tert-butil-kaliks[6]-1,4-benzocrown-4-bağlı silikajel durgun fazı 3-glisidoksipropil bağlı faz
Şekil 1.33. p-t-Butil kaliks[6]-1,4-benzocrown-4 bağlı durgun fazın sentez şeması.
Zuo ve ark. (2004), aminosilanla türevlendirilmiş p-tert-butil kaliks[4]aren türevini hazırlayıp aktive edilmiş silika jelle etkileştirilerek p-tert-butil kaliks[4]aren türevinin durgun fazını ede etmişlerdir. Sıvı kromatografide bu durgun faz polar ve
apolar ve aromatik bileşikler, temel aromatik bileşikler ve bazı izomerlerin ayrılması için kullanılmıştır. Özellikle alkil benzenlerin ayrılmasında Kromasil-C18-SiO2
kolon dolgu maddesine göre daha iyi sonuçlar verdiğini gözlemişlerdir.
1.7.5. Kaliksarenlerin Katalizör Olarak Kullanılması
Sırıt ve ark. 2008 yılında yaptıkları bir çalışmada α-amino asitlerin enantioselektif sentezi için cinchona alkaloid türevli kaliksaren bazlı kiral faz-transfer katalizörlerini sentezlemişlerdir.
OH OH O O Br Br n n OH OH OH HO Cinchonidine kuru CH3CN Br Br Br Br n OH OH O O N+ N+ N OH N O H n n K2CO3 Toluen 21 n : 1 22 n : 2 23 n : 3 24 n : 1 25 n : 2 26 n : 3
Şekil 1.34. Çalışmada faz transfer katalizörü olarak kullanılan kiral kaliksaren türevleri.
N O O Ph Ph BnBr , PTC N O O Ph Ph O O NH3 H+ Cl (5 mol %) %50 baz, çözücü * + *
Şekil 1.35. Benzofenon glisin imin esterinin katalitik alkilasyonu ile α-alkil α-amino asit esterlerinin sentezi.
Çizelge 1.4. Katalitik enantiyoselektif faz transfer benzilasyonu için kullanılan FTK.’den elde edilen sonuçlar.
PTC Çözücü T (°C) Baz Verima(%) %ee
b konfig 1 3a Toluen/CHCl3 7:3 -20 KOH 87 25 (S) 2 3a Toluen/CHCl3 7:3 -20 NaOH 89 46 (S) 3 3a Toluen/CHCl3 7:3 0 NaOH 95 57 (S) 4 3b Toluen/CHCl3 7:3 rt NaOH 92 52 (S) 5 3b Toluen/CHCl3 7:3 rt KOH 92 15 (S) 6 3c Toluen/CHCl3 7:3 -20 KOH 90 10 (S) 7 3c Toluen/CHCl3 7:3 -20 KOH 91 12 (S) 8 3c Toluen/CHCl3 7:3 -20 NaOH 95 17 (S) 9 3c Toluen/CHCl3 7:3 0 NaOH 96 28 (S) 10 3c Toluen/CHCl3 7:3 0 KOH 97 22 (S) 11 3c Toluen/CHCl3 7:3 rt KOH 98 18 (S) 12 3c Toluen/CHCl3 7:3 rt NaOH 97 24 (S) 13 3c CH2Cl2 -20 KOH 89 9 (S) 14 3c CH2Cl2 0 KOH 93 15 (S) 15 3c CH2Cl2 rt KOH 93 12 (S) 16 3c CH2Cl2 -20 NaOH 85 7 (S) 17 3c CH2Cl2 0 NaOH 88 14 (S) 18 3c CH2Cl2 rt NaOH 91 13 (S) a Đzolasyon verimi b
Enantiomeric excess kiral kolon (DIACEL Chiralcel OD-H) ve hekzan/izopropanol çözücü karışımı kullanılarak HPLC ile belirlenmiştir.
c
Mutlak konfigürasyon literatürde ürün 6 için verilen spesifik çevirme açısı değerlerinin karşılaştırılmasıyla belirlenmiştir.
Neri ve ark. 2003 yılında yaptıkları çalışmada benzaldehitle Chan’in dieninin aldol kondensasyonu reaksiyonu sadece %8 mol kaliks[n]aren/Ti(O-i-Pr)4
içeren kompleksleri ile katalizlendi. Çalışmalar kaliksaren molekülünün çapı ve hidroksil gruplarının sayısına bağlı olarak reaksiyon veriminin etkilendiğini göstermiştir.
Şekil 1.36. Çalışmada gerçekleştirilen aldol reaksiyonu ve katalizör olarak kullanılan kaliksaren türevleri.
OH OH O H O OH O OH OH O H O OR O N O OMe H OBut OBu O OBu O N H t t NH NH OMe O O NH OMe O L-Aminoasit veya Mirtenol DCC, DMAP, CH2Cl2 R :
Çizelge 1.5. 1 ile 2a’ nın 3a ürününü vermek üzere gerçekleşen aldol reaksiyonu
Kaliks[n]aren Verim (%)a 6 77 7 96 8 56 Ti(O-i-Pr)4 4 6a 95 6b 10 6c 17 6d - 6e 69 8a 44 8b 58b
a Verimler 1H NMR analizinden elde edildi. b Çözücü olarak toluen kullanıldı.
Gaeta ve ark. (2005) kiral pendant grupları içeren kaliks[4]aren türevlerini sentezlemişler kaliks[4]arenin lower rimi üzerine amino asit (L-tirosin, L-aspartik asit, L-valin ve L-triptofan), pinene benzeyen gruplar (mirtenil ve homomirtenil) ve binaftil amin birimlerini bağlamışlardır (Şekil 1.37.).
OSiMe3 OMe Me3SiO O2N H O O2N OH O O OMe Ti(IV)/Kaliksaren THF +
Elde ettikleri bu bileşiklerin Ti(IV) komplekslerini oluşturarak Chan’s siloksidienin p-nitrobenzaldehitle asimetrik aldol reaksiyonlarında enantiyoseçimli kataliz için ligand olarak kullanmışlardır (Şekil 1.2.34.). Oluşan ürünlerin e.e. sini (%) HPLC’ de kiral kolon olarak Chiralpak AD kullanarak belirlemişlerdir. Fakat sınırlı ölçüde enantiyoseçicilik gözlemişlerdir.
Şekil 1.38. Ti(IV)/kaliksaren kompleksinin katalizör olarak kullanıldığı asimetrik aldol kondenzasyonu
2. KAYNAK ARAŞTIRMASI
Sırıt ve ark. (2007) yaptıkları bir çalışmada kaliks[4]aren diesterlerinin aminolizi ile yeni p-t-bütilkaliks[4]aren ve kaliks[4]aren diamit türevlerini sentezlemişler ve bu bileşiklerin Cr2O72-/HCr2O7- anyonlarıyla kompleksleşme
özelliklerini araştırmışlardır (Şekil 2.1).
OH OH O O R R R R O O OEt OEt OH OH O O R R R R O O NH NH R' R' 3 - 4 5 - 10 3: R = But 4: R = H 5: R = But, 6: R = H, 7: R = But, 8: R = H, 9: R = H, 10: R = H, R' = a R' = a R' = b R' = b R' = c R' = d N R': a b c d O N N
Şekil 2.1. Dikromat anyonlarının ekstraksiyonu için kullanılan kaliks[4]aren diamit türevleri
1,5 2,5 3,5 4,5 5 6 7 8 9 10 0 20 40 60 80 100 pH % E
Şekil 2.2. 5 – 10 reseptörlerinin dikromat ekstraksiyon yüzdeleri
Yılmaz ve grubu (2006) tarafından yapılan başka bir çalışmada ise, 5,11,17,23,29,35-tert-butil-37,38-dimetoksi-39,40,41,42-(p-tosiletoksi)kaliks[6]aren 15 D-/L- fenilalaninol ile kuru THF içerisinde etkileştirerek p-tert-butilkaliks[6]arenin kiral türevleri (16 ve 17) sentezlenmiş (Şekil 2.3.) ve bunların bazı amino asit metilesterleri ve amino alkollere karşı ekstraksiyon özellikleri sıvı – sıvı ekstraksiyon tekniği ile araştırılmıştır (Çizelge 2.1. ve Çizelge 2.2.).
2 OR 4 OMe R = CH2CH2OTs THF D-fenilalaninol THF L-fenilalaninol 2 O 4 OMe N H O H H N H O H H O 2 4 OMe 15 16 17
Çizelge 2.1. Amino asit metilesterlerinin 16 ve 17 ligandlarıyla ekstraksiyon yüzdeleria
Ligand L-AlaOMeb
D-AlaOMe L-PheOMe D-PheOMe D-TrpOMe L-TrpOMe
16 91.4 89.1 90.3 90.7 87.5 93.2
17 84.3 89.6 87.2 82.5 85.4 89.8
a
Sulu faz, [amonyum pikrat] = 2.0 × 10-5 M; organik faz, diklormetan, [ligand] = 1.0 × 10-3 M; 25°Cde, 1 saat.
b Amino asit metilesterleri HCl tuzları olarak kullanılmıştır.
Amino alkol grupları taşıyan kiral p-tert-bütilkaliks[6]aren türevleri bazı aminoasit metil esterleri ve amino alkollere karşı ekstraksiyon ve kiral tanıma özelliklerini araştırmak amacıyla sentezlenmiştir. Kiral kaliks[6]aren türevleri 16 ve 17 her ne kadar kullanılan tüm amino asit ve amino alkoller için mükemmel ekstraktantlar olsa da herhangi bir kiral seçicilik gözlenmemiştir.
Maruoka ve grubu (2006) L- tartarik asitten çıkarak pyrrolidin temelli amino sülfonamid bileşikleri sentezlemişler ve bunları Mannich reaksiyonlarında kiral katalizör olarak kullanmışlardır (Şekil.2.4).
O H OH CO2H HO2C N OH O H O O N OMs MsO O O N N3 N3 N NH2 N H2 N NHTf TfHN N NHTf TfHN H L-tartarik asit a b, c d e f g
(a)benzilamin, o-ksilen, refluks, %99(b) NaBH4, BF3-OEt2, THF, refluks(c) McCl, Et3N, CH2Cl2, rt,
%61(d) NaN3, DMF, 100 °C, %52 (e) H2, Pd/C, EtOH, rt, %99 (f) Tf2O, Pr2NEt, CH2Cl2, -78 °C,
%76 (g) H2, Pd/C, AcOH, rt, %93
Çizelge 2.2. Çalışmada (R,R)-2 kodlu bileşiğin varlığında gerçekleştirilen Mannich reaksiyonu ve elde edilen sonuçlar.
R R' O H N CO2Et PMP R O R' N H CO2Et PMP H O H O H O O O 10 mol % kat. THF + 1 2 3 4 5 6 7 c f b d
Substrat Reaksiyon Koşulları(0C, saat) % Verim
ee % -20, 2 -20, 1 -20, 24 rt, 1 rt, 4 rt, 35 rt, 70 82 93 88 99 95 98 56 94 95 90 95 95 93 92
a3 eq karbonil bileşiği ve α-imino ester 3 ün katalizör varlığında THF deki reaksiyonu bĐzolasyon verimi
c H NMR ile belirlenmiş d HPLC ile belirlenen ee değerleri e (R-R)-2 %2 mol oranında kullanılmıştır f (R-R)-2 %0,5 mol oranında kullanılmıştır
Wang ve ark. (2006) tartarik asitten kiral sülfonamid türevli katalizörler sentezlemiş ve bunları dietilzink ortamında enantiyoselektif addition reaksiyonlarında kullanmışlardır. Çalışmada çeşitli aldehit ve ketonlarda kiral katalizör varlığında kiral merkez oluşturulmuş ve oluşan ürünün hangi enantiyomerce zengin olduğu kiral HPLC ile belirlenmiştir.
Şekil 2.6. Çalışmada kullanılan kiral sülfonamit bileşiğinin sentez şeması.
Ligand mol% Çözücü T°C Zaman (saat) Verim% eea %
1 4 5 Toluen 20 1 85 20 2 5 5 Toluen 20 1 95 70 3 5 5 Hekzan 20 2 93 64 4 5 5 THF 20 5 95 62 5 5 5 CH2Cl2 20 10 - - 6 5 10 Toluen 20 4 70 43 7 5 15 Toluen 20 1 96 58 8 5 3 Toluen 20 3 90 63 9 5 5 Toluen 20 18 82 64 10 5 5 Toluen 0 4 90 58 11 5 5 Toluen -20 18 84 41 12 5 5 Toluen -35 24 75 13 13 5 5 Toluen 40 1 95 60 14 5 5 Toluen 60 1 95 60
a ee kiral HPLC ile belirlenmiştir.
Şekil 2.7. Kiral katalizör varlığında gerçekleştirilen reaksiyon ve reaksiyona ilişkin sonuçlar.
R H O Et2Zn Ti(OPr)4 R OH + + 5 (5 mol %) Toluen/ rt R Verima Zaman eeb % (saat) % 1 C6H5 90 2 65 2 4- FC6H4 93 1 75 3 4- ClC6H4 95 1 70 4 4- MeC6H4 81 12 60 5 4- MeO C6H4 83 12 58 6c 4- MeO C6H4 97 2 63 7 2- Cl C6H4 92 3 38 8 2- Me C6H4 96 2 81 9 2- MeO C6H4 90 3 54 10c 2- MeO C6H4 95 2 63 11 1- Naftil 85 3 83 12 Sinnamil 95 3 31 a Đzolasyon veimi
b Kiral HPLC ile elde edilmiş ee değerleri c 3 eq Et
2Zn
Şekil 2.8. Farklı aldehitler kullanarak kiral katalizör ve Et2Zn varlığında
Çizelge 2.3. Farklı ketonlar ve Et2Zn varlığında kiral katalizör kullanılarak
gerçekleştirilen reaksiyonlar ve bunların sonuçlarına ilişkin veriler.
R mol% L* Çözücü T°C Zaman (saat) Verima % eeb % 1. 4- ClC6H4 5 Toluen 20 48 60 58 2. 4- ClC6H4 5 Hekzan 20 50 72 76 3. 4- ClC6H4 10 Hekzan 20 50 72 80 4. 4- ClC6H4 10 Tol/Hekc 20 50 72 81 5. 4- ClC6H4 15 Tol/Hek 20 50 75 81 6. 4- ClC6H4 7 Tol/Hek 20 50 73 81 7. 4- ClC6H4 7 Tol/Hek 0 50 62 80 8. 4- ClC6H4 7 Tol/Hek 40 36 65 79 9. 4- FC6H4 7 Tol/Hek 20 40 78 83 10. 4- BrC6H4 7 Tol/Hek 20 40 78 80 11. C6H5 7 Tol/Hek 20 50 70 99(S) 12. 4- MeOC6H4 7 Tol/Hek 20 56 68 35 13. 4- MeC6H4 7 Tol/Hek 20 48 70 70 14. 4- PhC6H4 7 Tol/Hek 20 40 80 78 15. d 2- Furan 7 Tol/Hek 20 36 88 10 16. d 2-Tiyofen 7 Tol/Hek 20 40 75 18 17. 2- Naftil 7 Tol/Hek 20 48 80 82 a Đzolasyon veimi
b Kiral HPLC ile elde edilmiş ee değerleri ( Kolon OD-H ve OJ-H ) c Reaksiyonda kullanılan çözücü karışımı oranı 1:6 dır.
d 3 eq Et 2Zn
Zheng ve grubu (2006) yaptıkları bir çalışmada mandelik asidin kiral tanınması için kaliks[4]arenin azot içeren kiral türelerini sentezlemişlerdir. Rasemik mandelik asidin etkileşimini 1H NMR ile izlemişlerdir.
O Br Br O OH OH NH2 O H H H Ph Ph K2CO3/CH3CN O OH OH O O NH Ph Ph H H 1 refluks 2 9a: R = H; 9b: R = Ph
Şekil 2.9. Çalışmada kullanılan kiral Kaliks[4]crown bileşiğinin sentez şeması.
Şekil 2.10. (a) 2 no.lu bileşiğin; (b) Rasemik mandelik asidin ve (c) 5mM 2. bileşik ve 5 mM rasemik mandelik asit karışımının CDCl3 içindeki 1H NMR spektrumu.
Çalışmada 2 numaralı bileşikle etkileşen rasemik mandelik asidin yarılma ve kayma sonucu enantiyomerlerine ayrılması NMR spektrumu ile açıklanmışlardır.
Roundhill ve ark. (2000) yaptıkları bir çalışmada 2-merkaptaetoksi türevli kaliksarenler sentezlemişler ve bu maddelerin Hg+2 iyonu ile kompleksleşmelerini incelemişlerdir. OH 4 BrCH2CO2Et K2CO3 4 O O OEt LiAlH4 4 O OH 4 O OTs TsCl piridin CH3COSK 4 O S CH3 O 4 O SH HCl 1 2 3 4 5 6
Tuntulani ve çalışma ekibi (2005) duble kaliks[4]aren ve kaliks[4]quinon bileşiklerini sentezleyerek bunların alkali metal katyonlarıyla kompleksleşmelerini ve elektrokimyasal özelliklerini incelemişlerdir.
R1: H, CH3 Br OR2 O OR1O O R1O OR2 OR2 O O LiAlH4 THF OR1O O R1O OH OH R1:H R2:Et R1: CH3 R2:Me R1: H, CH3 MsCl Et3N DMAP CH2Cl2 OR1O O R1O OMs OMs K2CO3/CH3CN R1: H, CH3 OR1 O O R1O OR1O O R1O OR1OH OHR1O baz 8 ;9 10, 11, 12,13 8 veya 9 14,15 6
OR1 R1O O O O O OR1 R1O O O n O O O O O O n O O O O Tl(CF3CO2)3 CF3CO2H X X O O O O MeO 4, n=0, R=H 5, n=1, R=H 6, n=0, R=Me 1, n=0, X= 2, n=1, X= 3, n=0, X=
Şekil 2.13. Kaliks[4]quinon bileşiklerinin sentez şeması.
Toma ve ark. (2000) yaptıkları bir çalışmada kaliks[4]areni 8-hidroksiquinolin ile modifiye etmişler ve oluşan molekülün Eu+3 ve Tb+3 iyonları ile lüminesans ve enerji transfer özelliklerini incelemişlerdir.
Şekil 2.15. Kaliks[4]arenin 8-hidroksikinolin türevinin aromatik bölge 1H-1H COSY NMR spektrumu
Çalışmada oksiquinolin türevli kaliks[4]arenin Eu+3 ve Tb+3 iyonları ile etkileşimi sırasındaki π→ π* geçişleri incelenmiştir.
![Şekil 1.9. Farklı konformasyonlardaki kaliks[4]arenlere ait metilen köprülerinin 1 H NMR ve 13 C NMR sinyalleri](https://thumb-eu.123doks.com/thumbv2/9libnet/4694612.88297/24.892.181.799.334.672/şekil-farklı-konformasyonlardaki-kaliks-arenlere-metilen-köprülerinin-sinyalleri.webp)
![Şekil 1.10. Kaliks[4]arenin p-konumunun ve fenolik OH’larının şematik gösterimi](https://thumb-eu.123doks.com/thumbv2/9libnet/4694612.88297/25.892.187.735.757.1003/şekil-kaliks-arenin-konumunun-fenolik-larının-şematik-gösterimi.webp)
![Şekil 1.12. p-Alkilkaliks[4]aren’ in kompleks oluşturma mekanizması](https://thumb-eu.123doks.com/thumbv2/9libnet/4694612.88297/30.892.215.696.562.948/şekil-p-alkilkaliks-aren-in-kompleks-oluşturma-mekanizması.webp)
![Şekil 1.13. Çalışmada sentezlenen kaliks[4]aren diamid türevleri](https://thumb-eu.123doks.com/thumbv2/9libnet/4694612.88297/32.892.236.776.105.756/şekil-çalışmada-sentezlenen-kaliks-aren-diamid-türevleri.webp)
![Şekil 1.16. para-Pozisyonuna üre bağlı kaliks[4]aren türevlerinin uygun guestler varlığında dimerik kapsül oluşturması](https://thumb-eu.123doks.com/thumbv2/9libnet/4694612.88297/34.892.221.755.846.1051/şekil-pozisyonuna-bağlı-türevlerinin-guestler-varlığında-dimerik-oluşturması.webp)
![Şekil 1.18. Kaliks[4]aren diamit türevlerinin kromat anyonuyla farklı pH’ larda yaptığı etkileşme grafiği](https://thumb-eu.123doks.com/thumbv2/9libnet/4694612.88297/36.892.316.644.102.390/şekil-kaliks-türevlerinin-anyonuyla-farklı-yaptığı-etkileşme-grafiği.webp)
![Şekil 1.20. Açiltransferaz aktivite gösteren kaliks[4]aren türevleri.](https://thumb-eu.123doks.com/thumbv2/9libnet/4694612.88297/37.892.194.770.444.648/şekil-açiltransferaz-aktivite-gösteren-kaliks-aren-türevleri.webp)