T.C.
EGE ÜNİVERSİTESİ TIP FAKÜLTESİ
İÇ HASTALIKLARI ANABİLiM DALI
ÜST GASTROİNTESTİNAL SİSTEM YAKINMALARI
OLAN HASTALARDA PARAZİT SIKLIĞI
Dr. Elvina ALMURADOVA
TEZ DANIŞMANI
Doç. Dr. Rukiye VARDAR
UZMANLIK TEZİ
2017
II ÖNSÖZ
Asistanlık dönemimde birçok değerli bilgiler öğrendiğim, tecrübe ve yaklaşımından meslek hayatım boyunca yararlanacağım, eğitimimde büyük emeği geçen başta Prof.Dr.Fehmi AKÇİÇEK ve Doç.Dr.Rukiye VARDAR olmak üzere tüm hocalarıma,
Tezimim yapılması aşamasında emeği geçen Doç.Dr. Şebnem ÖKTEM ÜSTÜN’e
Çok büyük sevgi ve saygı duyduğum uzman abi ve ablalarıma,
İkinci ailem İç Hastalıkları Anabilim Dalının tüm değerli çalışanlarına,
Başta Afag AHMADOVA olmak üzere Terane NAĞIYEVA, Feyza TAN, Gülay ALP, Cansu MUTLU ve tüm asistan arkadaşlarıma,
Hayatım boyunca desteklerini esirgemeyen her zaman, her yerde yanımda ve arkamda olan sevgili annem Gülhar, babam Ağamoğlan, kardeşim Emil’e,
Asistanlığım süresince, tez hazırlama ve bitirme dönemimde sabır ve desteğini esirgemeyen, sevgili eşim Farid ALMURADOV’a,
En çok sevip, en az zaman ayırdığım küçücük yavrularım Yusuf ve Yunus’a Çok Teşekkür ederim!
Elvina ALMURADOVA İzmir, 2017
III
İÇİNDEKİLER
Tablolar Listesi ... VI Şekiller Listesi ... VI Grafikler Listesi ... VII Kısaltmalar Dizini ... VIII Özet ... IX Abstract ... XI
1. Giriş-Amaç ... 1
2. Genel Bilgiler ... 4
2.1. Üst Gastrointestinal Sistem Yakınmaları ... 4
2.2. Dispepsi ... 4
2.2.1. Etyoloji ... 6
2.2.2. Organik Nedenlere Bağlı Olarak Gelişen Dispepsi ... 6
2.2.3. Helicobakter Pylori ... 7
2.2.4 Fanksiyonel Dispepsi ... 10
2.3. Barsak Parazitozu ... 13
2.3.1. Giardia İntestinalis (Lambl, 1859) Alexieff, 1914 Ve Parazitliği ... 13
2.3.1.1. Parazitlik Ve Epidemiyoloji ... 14
2.3.1.2. İmmunoloji ... 14
2.3.1.3. Patojenite Ve Klinik Belirtiler ... 15
2.3.1.4. Tanı ... 16
2.3.2. Entamoeba Histolytica Schaudinn, 1903 Ve Parazitliği ... 17
2.3.2.1. Morfoloji Ve Evrim ... 17
2.3.2.2. İmmunoloji ... 18
2.3.2.3. Patojenite Ve Klinik Belirtiler ... 19
2.3.2.4. Tanı ... 20 2.3.3. Cryptosporidium Spp. (Clarke, 1895) ... 21 2.3.3.1. Morfoloji Ve Evrim ... 21 2.3.3.2. Epidemiyoloji ... 22 2.3.3.3. Klinik Ve Patogenez ... 22 2.3.3.4. Tanı ... 23
IV
2.3.4.1. Morfoloji Ve Evrim ... 23
2.3.4.2. Epidemiyoloji ... 25
2.3.4.3. İmmunoloji ... 25
2.3.4.4. Patojenite Ve Klinik Belirtiler ... 26
2.3.4.5. Tanı ... 27
2.3.5. Enterobius Vermicularis (Linnaeus, 1758) Leach, 1853 Ve Parazitliği ... 28
2.3.5.1. Morfoloji Ve Evrim ... 28
2.3.5.2. Epidemiyoloji ... 28
2.3.5.3. İmmunoloji ... 29
2.3.5.4. Patojenite Ve Klinik Belirtiler ... 29
2.3.5.5. Tanı ... 30
2.4. Asit Sekresyon Fizyolojisi ... 31
2.4.1. Hcl Asit Sekresyonu... 31
2.5. Proton Pompa İnhibitörleri Etki Mekanizmaları ... 33
2.6. Ppi Kullanımı Ve Gastrointestinal Enfeksiyon Riskinde Artış ... 34
2.7. H.Pylori Ve Ppi Kullanımının Gastrointestinal Mukozaya Etkisi ... 35
3. Materyal Ve Metod ... 38
3.1. Hasta Seçimi... 38
3.1.1. Çalışmaya Alınma Kriterleri ... 38
3.1.2. Çalışmaya Alınmama Kriterleri ... 38
3.1.3. Çalışmadan Çıkarılma Kriterleri ... 38
3.2. Olgu Rapor Formu ... 39
3.3. Üst Gis Endoskopisi ... 39 3.3.1. Patolojik İnceleme... 40 3.3.2. Parazitolojik İnceleme... 41 3.4. İstatiskitsel Analiz ... 41 4. Bulgular ... 42 4.1 Cinsiyet Dağılımı ... 42 4.2. Yaş Dağılımı ... 43 4.3 Parazit Sıklığı ... 43 4.4. Sigara/Alkol ... 44 4.5 Histopatolojik Bulgular ... 45 4.5.1. Antrum ... 45
V
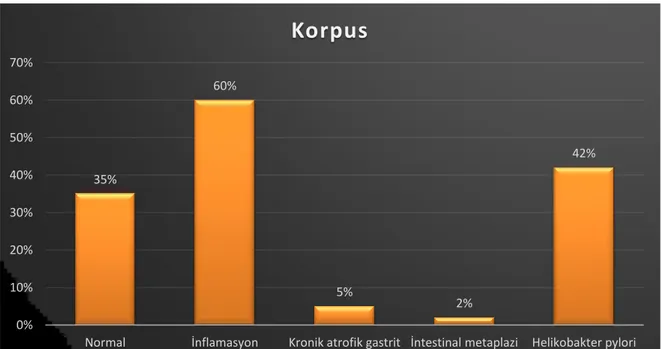
4.5.2. Korpus ... 46
4.5.3. Genel Olarak Mide Mukozası ... 47
4.6. PPİ Kullanımı ... 48
4.7. PPI Kullanımının Histopatolojik Bulgular Üzerine Etkisi ... 48
4.8. PPİ Kullanımıyla Parazit Saptanma Sıklığı Arasında İlişki ... 50
4.9. H. Pylori Pozitif Ve Negatif Olan Hastalarda Sydney Bulgularında Farklılık ... 50
5. Tartışma ... 53
VI
TABLOLAR LİSTESİ
Tablo 1 Dispepsi Tanımlamaları ... 5
Tablo 2 Dispepsi Nedenleri ... 9
Tablo 3 ROME IV Kriterleri ... 11
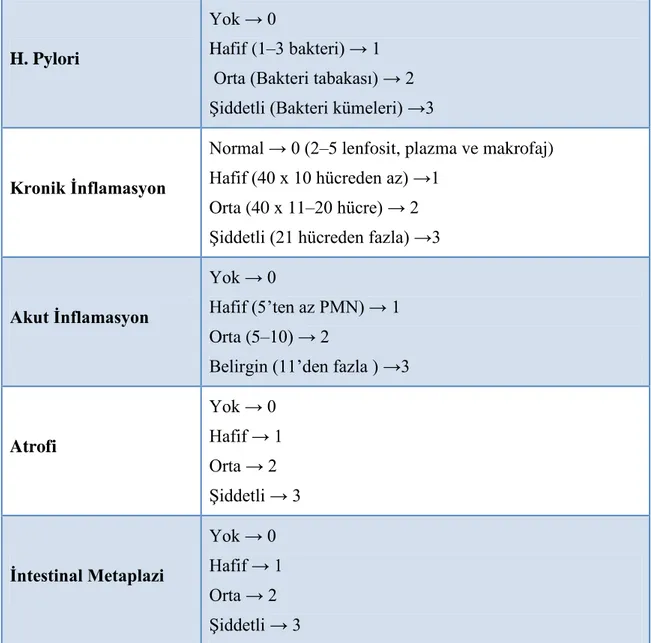
Tablo 4 Sydney-Houston Sınıflaması ... 40
Tablo 5 Antrum Histopatolojik Bulgular ... 45
Tablo 6 Korpus Histopatolojik Bulgular ... 46
Tablo 7 Mide Mukozası Histopatolojik Bulgular ... 47
Tablo 8 PPİ kullanımı ve Histopatolojik Bulgular ... 49
Tablo 9 H.Pylori ve Histopatolojik Bulgular ... 51
ŞEKİLLER LİSTESİ Şekil 1 FD ... 12
Şekil 2 Gastrik Asit ... 32
VII
GRAFİKLER LİSTESİ
Grafik 1 Cins Dağılımı ... 42
Grafik 2 Yaş Ortalaması ... 43
Grafik 3 Parazit Sıklığı ... 44
Grafik 4 Sigara/Alkol ... 44
Grafik 5 Antrum Histopatolojik Bulgular ... 45
Grafik 6 Korpus Histopatolojik Bulgular ... 46
Grafik 7 Mide Mukozası Histopatolojik Bulgular ... 47
Grafik 8 PPİ kullanımı ... 48
Grafik 9 PPİ kullanımı ve Histopatolojik Bulgular ... 49
Grafik 10 PPİ kullanımı ve Parazit sıklığı ... 50
Grafik 11 H.Pylori ve İntestinal Metaplazi ... 51
VIII KISALTMALAR LİSTESİ
Fonksiyonel Dispepsi : FD
PPİ : Proton Pompa İnhibitoleri
HCL : Hidroklorik Asit
Hp : Helikobakter Pylori
NÜD : Non Ülser Dispepsi
GÖRH : Gastro Özofageyal Reflü Hastalığı SSGİ :Serotonin Gerialım İnhibitorleri
PZR : Polimeraz Zincir Reaksiyonu
NSAİ : Non Steroid Antiinflamatuar İlaçlar G.intestinalis : Giardia İntestinalis
E.histolytica : Entamoeba Histolytica A.lumbricoides : Ascaris Lumbricoides E.vermicularis : Enterobius Vermicularis
H2RA : Histamin Reseptör Antagonistleri ECL : Enterokrommafin hücreler
IX ÖZET
Amaç: Bu çalışmada üst gastrointestinal sistem yakınmaları olan olgularda gastrointestinal parazit sıklığını araştırmak amaçlanmıştır. Çalışmanın ikincil amacı PPİ kullanımının gastrointestinal sistemde parazit sıklığına ve histopatolojik bulgulara etkisini araştırmaktır.
Materyal ve metod: Üst GİS yakınmaları nedeniyle üst GİS endoskopi tetkiki endikasyonu konularak Ege Üniversitesi Tıp Fakültesi Gastroenteroloji Kliniği Endoskopi laboratuarına sevk edilen 18 yaş üzeri 40 hasta çalışmaya alındı. Üst GİS endoskopik inceleme yapılarak, histolojik değerlendirme için antrum ve korpusdan biyopsi örnekleri, parazitolojik değerlendirme için mide ve duodenumdan aspirat sıvısı alındı. Ayrıca hastalardan parazitolojik açıdan değerlendirmek üzere gayta örneği de istendi. Biyopsi preparatları Ege Üniversitesi Patoloji laboratuarında, diğer örneklerler Gastroenteroloji Kliniğinin Parazitoloji laboratuvarında incelendi.
Bulgular: Toplam 40 hastanın 29’u (%72,5) kadın, 11’i (%27,5) erkekdi. Kadınların yaşı ortalama 54± 4,6,erkeklerin 38.4± 18.7 idi. Hastaların 10’u (%25) 65 yaş üstü ve 30’u (%75) 65 yaş altındaydı. Hastaların 7’si (% 17,5) sigara, 4’ü (%10) alkol tüketiyordu. Hastalanın %35’i (14/40) PPİ kullanmıyor ve %65’i (26/40) PPİ kullanan kullanmaktaydı. Hastaların sadece 3’ünde (%7,5) parazit tespit edildi. PPİ kullanan hastaların %7,7(2/26) ve kullanmayan hastaların %7,1’inde (1/14) parazit saptandı. PPİ kullanmakla parazit sıklığı arasında anlamlı fark saptanmadı. Olguların %50’sinde (20/40) Hp pozitif olarak saptandı. İnflamasyon H.pylori negatif olan hastaların %60’da (12/20), pozitif olanların %100‘de (20/20) görüldü (p=0.002). Hp pozitif olguların %100’ünde (20/20) Hp negatİf olguların %10’unda (2/20) intestinal metaplazi pozitifliği saptandı. Hp pozitif olgularda Hp negatif olgular ile karşılaştırıldığında intestinal metaplazi görülme sıklığı istatiksel olarak anlamlı yüksekti (p=0.00001). PPİ kullanımının histopatolojik bulgulara etkisinin istatistiksel anlamlı olmadığı görüldü.
X Sonuç: Çalışmamızda;
-Dispeptik yakınması olan hastalarda parazit sıklığı %7.5
-PPİ kullanımının parazit sıklığı ve histopatolojik bulgular üzerine etkisinin istatiksel olarak anlamlı olmadığı
-Üst GİS yakınması olan hastaların %50’sinde H.pylori (+) liği
- Hp pozitif olgularda inflamasyon ve intestinal metaplazinin Hp negatif olgular ile karşılaştırıldığında istatistiksel olarak anlamlı sık olduğu saptandı.
-
XI ABSTRACT
Objective: The goal of this research is determination of gastrointestinal parasits as the reason of upper gastrointestinal symptoms. Our seconder purpose was to determine effect of PPİ’s on gastrointestinal parasits and hystopatologycal findings.
Material and Metod: Forty patients >18 age who haved upper gastrointestinal symptoms were involved in the study. Patients underwent upper gastrointestinal endoscopy during which we took biyopies from gastric mucosa and aspiration from gastric and duodenal fluids. Patients also gave fecal samples for parasitolojic examination. Biopsy spesimens were evaluated by pathologist . Gastroduodenal aspirates and fecal samples were evaluated by parasitologist.
Findings: From forty patients 29 (%72,5) were women and , 11(%27,5) were men. Mean age was 54± 14,6 in women, and 38.4± 18.7 in men . 10 patients (%25) were >65 and 30 (%75) of them were <65 age. 7 (% 17,5) of them were smokers ve 4 (%10) of them were alcohol user. %35 (14) of patients were using PPİ.
We obtained parasites only in three (%7,5) patients. %7,7(2/26) of them were PPİ user and %7,1(1/14) didn’t use PPİ. %50 of patients were (20/40) Hp (+) .İnflamation in H.pylori (-) grup was %60’da (12/20), where in (+) was %100 (20/20) (p=0.002). İntestinal metaplasia in Hp (+) patients was %100’ünde (20/20) but in Hp (-)group %10(2/20) .There was statistically significant value in metaplasia of Hp(+)patients when compared Hp (-)patients(p=0.00001).
Results: İn our research we obtained:
- Parasites were obtained in 7.5% of the patients with upper gastrointestinal semptoms -There were not relation between PPİ use and hystopatological fındings or in parasit rates
- Metaplasia and inflamatiıon on gastric muvcosa was statistically significant when compared between Hp- and Hp+ group.
1
1 GİRİŞ-AMAÇ
Üst gastrointestinal sistem semptomları, dispeptik yakınmalar, epigastrik ağrı, pirozis, regürjitasyon ve bulantı-kusmadır. Dispeptik yakınmalara gastrit, gastrik ve duodenal ülser, gastroözofageal reflü hastalığı, malign hastalıklar, motilite bozuklukları, safra kesesi ve pankreas hastalıkları neden olabilir. Her yıl dünya populasyonunun %25’nin dispeptik şikayetleri olduğu bildirilmektedir. Dispepsi tarifleyen hastaların %25’inde organik neden bulunduğu halde %75 hastada altda yatan hastalık veya organik bir neden bulunamaz. Bu grup hastalara fonksiyonel dispepsi (FD) tanısı konur (1-4).
Roma IV kriterlerine göre FD aşağıdaki subgruplara ayrılır: Postprandial dolgunluk hissi
Erken doyma hissi Epigastrik ağrı Epigastrik yanma
Organik nedenler: Peptik ülser hastalığı, gastroözofageal reflü hastalığı, gastrik malignansi, biliyer ve nonsteroid ilaç ile ilşkili dispepsi, çölyak hastalığı, kronik pankreatit, eozinofilik gastrit, Crohn hastalığı, metabolik hastalıklar, intestinal damarsal hastalıklar ve barsak parazitozudur (5). Barsak parazitozları diyare, konstipasyon, iştahsızlık, steatore, malabsorbiyon, abdominal ağrı, epigastrik yanma, şişkinlik gibi çok çeşitli klinikle karşımıza çıkabilir. Parazitozun saptanması için duodenal sıvı ve gayta örneklerinin incelenmesi gerekir (6).
Proton pompası inhibitörleri (PPİ) mide pariyetal hücrelerde yer alan HCL asit sekresyonunun son basamağında görevli hidrojen/potasyum ATPaz enzim sistemini geri dönüşümsüz olarak bloke ederek etki gösterirler. Böylece midedeki Hidroklorik Asit (HCL) sekresyonunu inhibe ederek mide pH’nın yükselmesine neden olurlar (7).
Normal şartlarda mide lümeninde varolan pH 1-1.5 düzeyi sayesinde ağız yolu ile alınan bakteriler mide ve ince barsakta kolonize olamaz. Mide asit bariyeri, gastrik atrofi varlığında ve PPİ tedavisi sırasında bozulur. Böylece midede bakteriler kolonize
2
olabilir ve enterik enfeksiyon gelişimi kolaylaşabilir. PPİ kullanılması ile pH’nın 4’ün üstüne yükselmesi mide asidinin koruyuculuğunu engelleyerek Clostridium Difficile ile ilişkili diyare ve enterik enfeksiyonların oluşmasına neden olabilir. Aklorhidri Vibrio Kolera, Shigella, Campylobacter, Listeria ve Salmonella gibi enfeksiyonlara karşı risk oluşturabilir (8,9). Mide asidi mikroorganizmaların sporlarını öldüremese de vejetatif formunu öldürür, böylece enfeksiyon yapma şanslarını azaltır. pH 4’ün üzerine çıktığında ise bakterilerin vejetatif formları öldürülemez. Son zamanlarda, giderek artan oranda omeprazol, esomeprazol ve lansoprazol gibi PPİ kullananlarda kollajenöz kolit ve lenfositik kolit olguları bildirilmektedir( 10,11).
Giardia intestinalis insanın ince barsağında, genellikle duodenumunda, jejunumun üst kısmında, seyrek olarak da safra yollarında ve safra kesesinde yerleşerek sindirim sisteminde semptom ve bulgulara yol açabilen kamçılı bir protozoondur. Giardiazis ile ilişkili yapısal ve fonksiyonel anormallikler sıklıkla ince barsakta görülür. İnsanlardaki enfestasyonda barsaklarda ışık mikroskobu ile hiç anormallik görülmeyebileceği gibi hafif villöz atrofiden subtotal villöz atrofiye uzanan değişiklikler saptanabilir. Artmış derinlikte kriptler de görülebilir. Bu mikroskopik değişikliklere ek olarak, epitelyal fırçamsı kenar enzimlerde (örneğin laktaz enzimi) de eksiklik gelişebilir. Epitel hücreleri üzerine yapışan parazit, emilimi engeller. Yağ emilimi bozulduğundan dışkı yağlıdır (steatore). Ayrıca yağda eriyen A vitamininin emilimi bozulur. Kanda bu vitaminin düzeyi düşer ve avitaminöz belirir. Yine parazit, glikoz, ksiloz, laktoz ve B12 vitamininin emilimini de etkilemektedir. Enfestasyon asemptomatik olsa bile karbonhidrat, vitamin ve yağların malabsorbsiyonu gelişebilir. Bu da vitamin A, B12 eksikliğine, folat eksikliğine, hipoalbuminemiye ve laktaz eksikliğine yol açar. Tanı için duodenal aspirat ve biopsi alınması gerekebilir. Bu testler genelde diğer non invaziv testlerden sonuç alınmadığında ya da ince barsak yapısının incelenmesi gereken durumlarda yapılır. PPİ kullanan hastalarda hem gastroenterit tablosu hem de B12 vit eksikliği görüldüğü için bunun giardiyazisle ilişkili olabileceği öne sürülmektedir. PPİ kullanımının gastrointestinal traktda parazit varlığı üzerine etkisini araştıran çalışmalar çok kısıtlıdır (8,9). PPİ’ların B12 vitamin eksikliği başta olmak üzere vitamin ve mineral malabsorbsiyonu yaptığı ise kanıtlanmıştır. PPİ kullanımının paraziter enfestasyonlar üzerindeki etkisinin araştırılması ve özellikle giardiazis sıklığının saptanması uzun sureli PPİ kullanan olgulardaki emilim sorunlarının kaynağını anlamamızı sağlayabilir.
3 Bu çalışmada;
1. Üst gastrointestinal sistem yakınmasıyla başvuran hastalarda parazite rastlanma sıklığını saptamak amaçlanmıştır.
Çalışmanın sekonder amacı;
2. PPİ kullanan hastalar arasında parazite rastlanma sıklığı
3. PPİ kullanan ve kullanmayan hastaların endoskopik biyopsilerinin histopatolojik bulguları arasındaki farkın değerlendirilmesidir.
4
2 GENEL BİLGİLER 2.1 Üst Gastrointestinal Sistem Yakınmaları
Üst gastrointestinal sistem yakınmaları dispeptik yakınmalar, pirozis, bulantı kusma ve regurgitasyondur.
2.2 Dispepsi
Üst batında ve / veya epigastriumda hissedilen, tekrarlayıcı veya devamlı karakterde ağrı veya rahatsızlık hissi şeklinde tanımlanabilir. Dispepsi tek bir semptom değil, bir semptomlar topluluğudur.Rome IV kriterlerine göre semptomların en az 3 aydan beri bulunması ve tanıdan 6 ay önce başlamış olması gerekir (4).
Dispepsi yakınması ile başvuran olgularda öncelikle üst gastrointestinal sisteme ait bir rahatsızlık olduğu düşünülmeli ve organik sebepler uygun araştırma ile ekarte edilmelidir (12). Dispepsi terim olarak Yunanca; dys: kötü, peptein: pişirme veya sindirim anlamı taşır. Bu köklere göre dispepsinin en uygun çevirisi ‘kötü sindirim’dir. Dispepsi için şimdiye kadar yirmiden fazla tanımlama önerilmiştir, fakat bunların çoğu biribirine zıttır ve bazıları hiç kabul görmemiştir (13). Dispepsi için değişik zamanlarda yapılan değişik tanımlar Tablo 1’de gösterilmiştir.
5 Tablo 1 Dispepsi Tanımlamaları
Rhind 1968
Yemekten sonra ortaya çıkan epigastrik rahatsızlık; sıkı giysilerin gevşetilmesi ihtiyacı doğuran şişkinlik hissi, geçici bir rahatlamayla birlikte geğirme, ağza ekşi sıvı gelmesi ve pirozis (flutan dispepsi)
Crean 1982
Sarılık ve gastrointestinal kanama dışında, her türlü epizodik ya da persistan abdominal rahatsızlık hissi ya da sindirim sistemi ile ilişkili diğer semptomlar
Thompson 1984 Kronik, yineleyici, sıklıkla öğünlerle ilişkili epigastrik rahatsızlık
Lagarde 1984 Aralıklarla ortaya çıkan üst abdominal ağrı ya da rahatsızlık
Talley 1985
Üst gastrointestinal sistemle ilişkili aralıklı ya da sürekli ağrı, rahatsızlık ya da bulantı; en az 1 ay veya daha uzun sürelidir; egzersize bağlı değildir. İstirahatle geçer. Sarılık, kanama ya da disfaji ile ilişkili değildir.
Nyren 1987
Başlıca semptomlar epigastrik ağrı ya da rahatsızlık, irritabl barsak semptomlarının ve organik hastalığın yokluğu (epigastrik distres sendromu)
Talley 1988 Yiyeceklerle ilişkili olan ya da olmayan, kronik ya da
yineleyici üst abdominal ağrı ya da bulantı; en az 3 ay sürelidir
Colin-Jones 1988
Sindirim sisteminin proksimal bölgesiyle ilişkili olduğu düşünülen üst abdominal yada retrosternal ağrı, rahatsızlık, pirozis, bulantı, kusma veya diğer semptomlar
Barbara 1989
Genellikle öğünlerle ilişkili biçimde ortaya çıkan ve hastaların ya da hekimlerin gastrointestinal sistemin proksimal
bölgesindeki bozukluklara bağlı olduklarını düşündükleri epizodik ya da persistan abdominal semptomlar
Heading 1991
Ağrı ya da rahatsızlık dahil olmak üzere epizodik ya da
persistan abdominal semptomlar; dispepsi terimi, semptomların gastrointestinal sistemin proksimal kısmı dışındaki
bölgelerinden kaynaklandığı düşünülen hastalara uygulanmaz Talley 1999 Abdomenin üst bölümünde odaklanan ağrı ya da semptomlar
6 2.2.1. Etyoloji:
Dispepsinin etiyolojisinde gastrit, mide-duodenum ülseri, eroziv duodenit, özofajit, ilaç ve gıda intoleransı, gastrointestinal trakt disfonksiyonu, Helikobakter pylori(HP) enfeksiyonu, pankreatik hastalıklar, neoplazik hastalıklar, nonülser dispepsi (NÜD) ve diğer organik nedenler yer alır. Organik nedenlerden en yaygın peptik ülser hastalığı, gastrit ve gastroözofageyal reflü hastalığı (GÖRH) dır.
Populasyonun %25 nin etkilendiği dispepsi kendi içinde %25 organık nedenlere bağlı olarak gelişse de %75’i “nonülser dispepsi” veya en sık kullanılan terim “FD” olarak tanımlanır (5,13).
2.2.2. Organik Nedenlere Bağlı Olarak Gelişen Dispepsi
Mide ve duodenum hastalıkları: peptik ülser, GÖRH, gastroparezi, mide ve özofagus malign tümörleri, midenin infiltratif hastalıkları (amiloidoz vb.), malabsorbsiyon sendromları, kronik intestinal iskemi vb. nedenler dispepsiye yol açabilir.
Gıda ve ilaç intoleransı: Ani gelişen hazımsızlık durumu, aşırı ve hızlı yemek yeme, yüksek yağ içerikli yiyecekler tüketme, stres altında yemek yeme, çok fazla alkol veya kahve tüketme dispeptik yakınmalara neden olabilir. Aspirin, nonsteroidal anti-inflamatuar ilaçlar, antibiyotikler (metronidazol ve makrolidler), antidiyabetik ilaçlar (metformin, akarboz, amilin analogları, GLP-1 reseptör antagonistleri), antihipertansifler (anjiyotensin dönüştürücü enzim inhibitörleri, anjiyotensin reseptör antagonistleri), kolesterol düşürücü ajanlar (niasin, fibrat), nöropsikiyatrik ilaçlar (kolinesteraz inhibitörleri, donepezil, rivastigmin), selektif serotonin gerialım inhibitörleri (SSGI), kortikosteroidler, östrojenler, demir içeren ilaçlar ve opioidler dispepsiye neden olabilir.
Pankreatik hastalıklar: Pankreas kanserleri ve kronik pankreatit dispepsiyle ortaya çıkabilir.
Safra yolları hastalıkları :Epigastrik ve sağ üst kadranda başlayan ağrılar (kolelitiazis ve koledokolitiazis) dispeptik yakınmalarla kendini belli edebilir
7
Diğer nedenler: Diabetes mellitus, tiroid hastalıkları, kronik böbrek hastalıkları, miyokardial iskemi, intraabdominal maligniteler, hiatal herni, gebelik gibi durumlarda dispeptik şikayetler olabilir. (5)
2.2.3.Helicobakter Pylori
Özellikle vurgulanması gereken bir konu olan H.Pylori enfeksiyonu ülser, gastrit, dispepsi ve hatta kanser etyolojisinde çok büyük öneme sahipdir. Hp ile ilgili araştırmaların dönüm noktası 1983 yılında R. Warren ve B. Marshall adlı araştırmacıların kronik aktif gastritte spiral yapılı bakterilerin rol oynadığını ve peptik ülser etiyopatogenezinde de önemli olabileceğini bildirmeleri olmuştur . Morfolojik ve fizyolojik özellikleri Campylobacteriler’e benzerlikleri ve ilk izolasyon yeri dikkate alınarak önceleri Campylobacter pyloridis olarak tanımlanmıştır. Daha sonra bu organizma üzerinde yoğun araştırmalar yapılmış ve genetik özellikleri dikkate alınarak 1989’da Hp şeklinde yeniden isimlendirilmiştir (14).
Hp; küçük (0,5–3 μm), spiral, kıvrımlı, 4–6 adet flagellası olan hareketli, mikroaerofilik, gram (-) bir bakteridir .
Epidemiyoloji : Tüm dünyada en sık görülen enfeksiyonlardan biridir ve dünya
nüfusunun yaklaşık yarısı bu mikroorganizmayı taşımaktadır (15). Türkiyede enfeksiyon sıklığı bölgelere göre değişmekle birlikte %60–85 arası oranlar bildirilmiştir (16). Hp genellikle çocukluk çağında alınır ve uzun yıllar boyunca asemptomatik seyreder.
Hp için insan midesi bilinen en önemli rezervuardır. Esas bulaş yolu fekal-oral ve oral-oral yoldur (17).
Patogenez
Mide mukozası bakteriyel enfeksiyonlara karşı iyi korunmuştur. Mide asidi birçok enterik mikroorganizmayı etkisiz hale getirmekle birlikte Hp’nin mideye yerleşmesini engelleyemez. Spiral yapısı ve flagellaları ile sağladığı hareketler sayesinde Hp, gastrik mukozanın mukus tabakasının altındaki epitel hücrelerine penetre olur ve mukus tabakası içinde yüzer. Mukus tabakası da bakteriyi asid etkisinden korur (15). Üreaz enzimi üreyi parçalayarak amonyak ve karbondioksite dönüştürür.
8
Amonyak da asit ortamda amonyuma dönüşür. Oluşan bu amonyum mukus tabakası içinde bakterinin canlılığını sürdürmesinde önemli rol oynar. Esas yerleşim yeri midedir. Fakat ektopik gastrik mukoza, metaplazik gastrik epitelin bulunabildiği duodenum, özofagus gibi gastrointestinal sistemin herhangi bir bölgesine de yerleşebilir (18). Hp’nin invaziv bir bakteri olmaması, mukus tabakası içinde barınması, mide bezlerinin lümeni içine saklanabilmesi, konakçının savunma sisteminden kendini korumasına olanak sağlamaktadır (15).
Virulans Faktörleri
Hp virülans faktörlerinden oldukça zengin bir bakteridir. Konakta oluşan yanıt çoğu kez konağa minimal zarar verirken bazı olgularda çeşitli mide hastalıkları ortaya çıkmaktadır . Birçok Hp suşu, 29 gen içeren 37 kb’lık bir genom parçacığı olan cag patojenite adacığına (cag PAI ) sahiptir (19).
Cag A; cag PAI’nın bir parçası olan cag A geni tarafından kodlanan, aşırı antijenik bir proteindir (17). Cag A geni taşıyan Hp suşları, çok daha güçlü interlökin (IL)-8 yanıtı oluşturur ve cagA pozitif suşların varlığında gastrik mukoza inflamasyonu daha şiddetli olmaktadır (19). Bu geni taşıyan Hp suşları, bu geni taşımayanlara kıyasla peptik ülser ve mide karsinomu olgularıyla daha sık ilişkili bulunmuştur (20).
Bütün Hp suşlarında bulunan vac A geni sitoplazma içi vakuollerin oluşumu ve epitel hücrelerinin apopitozunu doğrudan uyaran bir ekzotoksin olan vac A proteinini şifreler . Tüm Hp suşları vac A genine sahipse de, bunların sadece yarısı aktif sitotoksin salgılar . Cag A ve vac A proteinlerinin varlığı ve yokluğuna göre Hp iki tipe ayrılmaktadır. Tip I suşlar, cag A ve vac A proteinlerinin üretimini kodlayan cag A ve vac A genlerinin her ikisine de sahipken, tip II suşlar bu proteinleri üretmemektedir. Tip I’in, duodenum ülseri ve aşırı inflamasyonla birlikteliğinin sık olduğu gösterilmiştir (21).
Hp’nin katalaz ve süperoksit dismutaz enzimleri, polimorfonükleer lökositlerce öldürülmeye karşı dayanıklılıkta etkendir . Gram (-) bakterilerin en önemli virülans faktörü, lipopolisakkarit yapısındaki endotoksinidir. Hp’nin lipopolisakkaritinin biyolojik aktivitesi düşük olduğundan bu özellik bakteriye uzun yaşam şansı tanıdığı gibi, neden olduğu enfeksiyonun da onlarca yıl sürüp gitmesine yol açmaktadır (22).
9
Tanı
Hp tanısında kullanılan yöntemler endoskopi gerektirip gerektirmediklerine göre invaziv ve non-invaziv testler olmak üzere 2’ye ayrılır (23).
İnvaziv testler Non-invaziv testler Üreaz testi Üre-nefes testi
Histopatoloji Seroloji Kültür Gaita antijen testi
PZR(Polimeraz Zincir Reaksiyonu)
Tablo 2’de dispepsiye neden olan esas patolojiler sıralanmıştır.
Tablo 2 Dispepsi Nedenleri FD (%60 ‘ dan fazlası)
Yapısal yada biyokimyasal hastalıklara bağlı dispepsi Peptik ülser
Gastroözofagial reflu hastalığı Bilier kolik
Kronik karın duvarı ağrısı Gastrik yada özofagial kanser Gastroparezi
Pankreatit
Karbonhidrat malabsorbsiyonu
İlaçlar (potasyum ilaveli ilaçlar, dijitaller, demir, teofilin, oral antibiotikler (ampisilin, eritromisin gibi), NSAI (Non Steroid Antiinflamatuar İlaçlar), kortikosteroidler, niasin, gemfibrozil, narkotikler, kolşisin, quinidin, östrojenler, levodopa)
Midenin infiltratif hastalıkları (örneğin; crohn hastalığı, sarkoidoz) Metabolik bozukluklar (hiperkalemi, hiperkalsemi)
Hepatoma
İskemik barsak hastalığı
Sistemik hastalıklar (diabetes mellitus, tiroid ve paratiroid hastalıkları, bağ dokusu hastalıkları)
Barsak parazitleri (Giardia, Strongyloides) Abdominal kanserler, özellikle pankreatik kanser
10 2.2.4. Fonksiyonel Dispepsi
Çok sayıda klinik araştırmacılardan oluşan uluslararası bir komite literatür taraması sonucu; yılda yaklaşık % 25 oranında populasyonu etkileyen, oldukça büyük iş gücü kaybı ve sağlık harcamalarına sebep olan dispepsinin tanımını; Roma kriterleri adı altında onaylamıştır (4).
2016 senesinde yayınlanan Roma 4 kriterleri olarak onaylanan bu kriterlerler aşağıdaki tabloda verilmiştir (Tablo3).
11 Tablo 3 Rome IV Kriterleri
B1: FD
Diyagnostik kriterler:
1.Bunlardan biri veya daha fazlası a.Posprandiyal dolgunluk
b.Erken doyma c.Epigastrik ağrı d.Epigastrik yanma ve:
2.Semptomlara neden olabilicek strüktür bozukluğunun olmaması(üst gis endoskopi dahil)
B1a.
Posprandiyal distress sendrom
Diyagnostik kriterler:
Bu semptomların birinin ve ya her ikisinin en az haftada 3 gün olması
1.Postprandiyal dolgunluk (günlük aktiviteleri engelleyecek düzeyde) 2.Erken doyma (her zamanki yemek porsiyonunu bitiremeyecek düzeyde)
Bu semptomları açıklayacak organik, sistemik, metabolik hastalığın olmaması (üst endoskopik incelenme dahil)
Destekleyici semptomlar
1.Posprandiyal epigastrik ağrı ve yanma, kusma, şişkinlik 2. Kusma başka hastalığın olmasına işaret edebilir
3.Yanma dispeptik semptom değil ama genelde eşlik eder
4.Gaz ve gayta çıkışıyla rahatlayan semptomlar dispepsi olarak kabul edilmez.
Dispeptik semptomlara gastroözofageyal reflü ve iritabl barsak sendromu semptomları eşlik edebilir
B1b.
Epigastrik ağrı sendromu
Diyagnostik kriterler:
Aşağıdakı semptomlardan en az birinin haftada en az 1 kere olması 1.Epigastrik ağrı (günlük aktiviteyi kısıtlamaya yetecek kadar) ve/veya
2.Epigastrik yanma (günlük aktiviteyi kısıtlamaya yetecek kadar) Bu semptomları açıklayacak organik, sistemik, metabolik hastalığın olmaması(üst endoskopik incelenme dahil)
Destekleyici semptomlar
1. Ağrı yemeyi yerken başlayıp veya geçebilir veya açken olabilir 2.Postprandiyal bulantı şişkinlik kusma eşlik edebilir
3.Persistan kusma farklı patolojinin olduğunu gösterir 4.Yanma dispeptik semptom değil ama eşlik edebilir 5.Ağrı biliyer ağrı kriterlerine uymaz
6. Gaz ve gayta çıkışıyla rahatlayan semptomlar dispepsi olarak kabul edilmez.
12
Dispeptik şikayetlerle başvuran hastaların üçte ikisinde organik bir nedene dair kanıt bulunamadığından ve önemli bir kısmında şikayetleri açıklayacak bir bulgu saptanmamış olduğundan, bu grup hastalara FD tanısı konulur. FD’si olan hastalardaki semptomlar artmış visseral sensitivite, gastrik boşalma zamanında gecikme, bozulmuş gastrik akomodasyon ve psikososyal stresler gibi nedenler ile ortaya çıkabilir (24,25).
Şekil 1 FD
FD tedavisi güç ve hastanın hayat kalitesini etkileyen kronik bir hastalıktır.
Fonksiyonel Dispepsi Bozulmuş Bağırsak-İmmunite İlişkisi Psiko-sosyal Faktörler Viseral hassasiyet Anormal Üst Gİ Motor ve Refleks Fonksyonları Genetik Faktörler? Bozulmuş Beyin-Bağırsak İlişkisi
13 2.3 Barsak Parazitozu
Dispepsi nedenleri arasında özel yeri olmasına rağmen barsak parazitozu en sık gözden kaçabilen nedendir. Bizim çalışmamızın esas amacı üst gastrointestinal sistem yakınmaları olan hastalarda parazite raslanma sıklığının saptanmasıdır. Bağırsak parazitozları, geri kalmış, gelişmekte olan ve hatta yüksek sağlık standartlarına sahip ülkelerde bile önemli bir sağlık sorunu olarak güncelliğini korumaktadır.
Türkiye; coğrafi konumu, iklim şartları, kötü hijyenik durum, diğer sosyo-ekonomik ve kültürel şartlar nedeniyle bağırsak parazitlerinin sık görüldüğü bir ülkedir. Son 20 yılda yapılmış çalışmalara bakıldığında bağırsak parazitlerinin, toplumumuzun her yaş ve grubunda ve tüm yörelerinde yaygın olarak bulunduğu anlaşılmaktadır (26).
Parazitozların tanısı etken parazitin kendisi veya evrim şekilleri bulunarak veya gelişen özgül immün cevap reaksiyonları incelenerek konmaktadır. Parazitozlu kişilerin kan ve dokularında eozinofil sayısının ve kan serumunda IgE düzeylerinin arttığı bildirilmiştir . Bağırsak paraziti olan kişilerde genel olarak bulantı, karın ağrısı, kusma, ishal, kabızlık, iştah artması ve iştahsızlık gibi çeşitli gastrointestinal sistem belirtileri görülmektedir. Parazitlerin toksi-alerjik etkileri ile ürtiker benzeri döküntülerden, angio-nörotik ödeme kadar giden tablolar bildirilmiştir. Bunlar arasında en sık görülen ise dispeptik yakınmalar ve defekasyon alışkanlığı bozukluğudur.
Hem direkt, hem de diğer hastalıklara zemin hazırlayarak uzun sürede dolaylı ölümlere yol açabilmesi ve ekonomik iş gücü kaybı yaratması nedeniyle bu enfestasyonların tanısının konulması önemli sağlık sorunudur. En sık hastalık yapan parazitlerden aşağıda bahsedilmiştir.
2.3.1 Giardia intestinalis (Lambl, 1859) Alexieff, 1914 ve parazitliği Morfoloji ve Evrim:
G. intestinalis ince bağırsakta özellikle duodenumda yaşayan kamçılı bir protozoondur. Bu parazitin evriminde trofozoit ve kist olmak üzere iki morfolojik şekil bulunur. Trofozoitleri 9-21 µm boyunda, 5-10 µm enindedir. Vücudun ön kısmına yakın iki büyük çekirdek vardır. Arkaya doğru daralma gösteren protozoonun dorsali dışbükeydir. Ventralde vücudun 3/4’ünü kaplayan emici bir disk mevcuttur. Simetrik yerleşmiş iki çekirdek, iki aksostil, dört çift blepharoplast ve dört çift kamçı vardır.
14
Kistleri 9-18X6-9 μm boyutlarında, eliptik veya söbemsi bir yapıdadır. Sayısı iki veya dört olan çekirdekler kistin bir yarısında toplanmıştır. Kist formları gelişimine ince bağırsakta başlayıp, kolonun üst kısmında tamamlar (27).
G. intestinalis için doğal konak insandır. Ancak değişik omurgalı hayvanlarda da morfolojik olarak benzer türler gözlenmiştir. G. intestinalis trofozoit döneminde ikiye bölünerek eşeysiz çoğalır. Trofozoitler kist olacağı zaman aksonemleri ve kamçılarını çeker, sitoplazmaları yoğunlaşır ve kist duvarı yaparlar. Yeni kistlenen parazitlerin çekirdekleri iki adet olup, bunlar daha sonra ikiye bölünür ve dört adet olurlar. Dört çekirdekli bu kistler oral yolla alınınca, sindirim sisteminde enzimlerinin etkisiyle kist duvarı açılır ve iki trofozoit oluşur (27).
2.3.1.1 Parazitlik ve Epidemiyoloji:
Keme, fare, tavşan, kunduz, kedi, köpek gibi hayvanlarda bulunan Giardia’ların insanda parazitlik yapan türle aynı olmadığı görüşü yaygındır. İnsan ve köpek, ayrıca kunduz ve köpek arasında karşılıklı bulaşmalar olabilir.
Giardia enfestasyonuna, yavrularda daha yüksek oranda olmak üzere, koyun ve sığırlarda da rastlanmaktadır. Yapılan araştırmalarda koyun ve insan Giardia’larının morfolojik ve antijenik yapılarının birbirine benzerlik gösterdiği ortaya konulmuştur. Bu bulgulara dayanarak giyardiyazın zoonoz ve hatta zooantropoz olduğu ileri sürülmektedir (28).
Giardiasis, bütün dünyada yaygın olan bir enfestasyondur. Enfeksiyon kaynağı dışkıları ile etrafa kist bulaştıran insanlardır. Bulaşma kirli eller, besin ya da sularla etkenlerin sindirim sistemine oral yolla alınması sonucu olur. Dünya Sağlık Örgütünün 1975-1981 yılları arasında yaptığı çalışmalarda dünyada 200 milyonun üstünde giyardiyozlu insanın olduğu bildirilmiştir. Ülkemizde yapılan araştırmalarda prevalansın %4-25 arasında değiştiği saptanmıştır (29).
2.3.1.2 İmmunoloji
G. intestinalis’e karşı dirençte kişilere göre farklılıklar görülür. Bağışıklık sistemini baskılayıcı ilaçlar ve midede HCl yokluğu giyardiyozun yerleşmesini kolaylaştırır (29). Giyardiyozlu kişilerde bağırsakta IgA, IgG ve IgM seviyesinin
15
yükseldiği bildirilmiştir. Enfeksiyonun vücuttan temizlenebilmesi, bu antikorlara bağlanmaktadır. Bu nedenle B hücrelerinin bağışıklık için önemli olduğu birçok araştırmacı tarafından kabul edilmektedir. Giardia trofozoitlerinin IgA tarafından sarılarak etkisizleştirilmesi ve bağırsak mukusu ile vücuttan atılması mümkündür (27).
2.3.1.3 Patojenite ve Klinik Belirtiler
Giardia trofozoitleri, başta duedonum olmak üzere ince bağırsağın üst kısımlarına yerleşerek bağırsak villuslarında atrofi ve tahribata bağlı olarak sindirim sistemi bozukluğuna neden olur. Emici diskleri ile mukozaya yapışan parazitler, hem yapıştıkları bölgedeki yüzeyi tahrip eder, hem de o bölgedeki besin emilimini olumsuz yönde etkilerler (30). Bu parazitin ishali tetikleyebilecek herhangi bir enterotoksini tespit edilmemiştir. Ancak klinik olarak hastalarda bazen kanlı da olabilen ishal görülür ve sindirim bozukluğuna bağlı olarak ortaya çıkan yağlı dışkı karakteristik belirti olarak kabul edilir (27). Bazı vakaların jejunum biyopsilerinde, villusların kısalıp küntleştiği, mukoza epitel hücrelerin boyunun kısaldığı ve lamina propria’da hücre sayısının arttığı görülmüştür. Ayrıca parazitin B12 vitamininin absorbsiyonunu da engellediği bildirilmiştir (31).
Akut Giardiazis: Giardia ile enfekte hastaların yarısından azında görülür. Aşağıdaki semptomları içerir:
• Diare (ani, sulu)(% 90) • Huzursuzluk hissi (% 85) • Kötü kokulu yağlı dışkı (%70) • Geğirmek (% 75) • Bulantı (% 70) • Kilo kaybı (% 65) • Kusma (%30) • Ateş(% 10-15 )
16
Kronik Giardiazis: Akut fazı takip edebilir veya önceki hastalıktan bağımsız olarak gelişebilir.
•Yumuşak kıvamlı dışkılama •Yağlı dışkılama
•Kilo kaybı •Malabsorbsiyon •Huzursuzluk hissi •Yorgunluk
•Depresyon semptomlarını içeren hastaların % 30-50’ sinde kronik giardiazis gelişebilir. Kronik giardiazisin diğer semptomları arasında; abdominal kramplar, gurultu, geğirme, şişkinlik yer alır. Bu semptomlar aylarca sürebilir. Malabsorbsiyon giardiazisde ciddi kilo kayıplarının sebebidir. Emilim bozukluğuna bağlı olarak B12 ve demir eksikliği ve buna bağlı olarak anemi kliniği gelişmesi de literatürde bildirilmiştir (31).
2.3.1.4 Tanı
G. intestinalis’in teşhisi parazitin dışkıda kist ya da trofozoit formunun görülmesi ile yapılır. Ayrıca duedonum aspirasyon sıvısı ve duedonum biyopsi materyali incelendiğinde de parazitin trofozoit formları görülebilir (32).
Tanıda direkt yöntemlerin dışında indirekt yöntemler de kullanılmaktadır. Bunlar hastanın kanında Giardia’ya karşı oluşmuş antikorların belirlenmesi şeklinde olabileceği gibi dışkı örneğinde immunolojik yöntemlerle Giardia antijeninin belirlenmesi ile de olabilmektedir. Giardiasisin tanısına IFA, ELISA, Western Blot gibi serolojik ve immunolojik yöntemlerle yaklaşım gittikçe gelişmektedir. Giardia için spesifik DNA problarının geliştirilmesinden sonra DNA bazlı moleküler tanı yöntemleriyle dışkı tetkiklerinin yapılması da mümkün olmaktadır (27).
17
2.3.2 Entamoeba histolytica Schaudinn, 1903 ve parazitliği 2.3.2.1 Morfoloji Ve Evrim:
E. histolytica’nın evriminde trofozoit, prekist, kist, metakist ve metakistik trofozoit olmak üzere beş morfolojik şekil bulunur (30).
Trofozoit: Bağırsak boşluğunda bulunan trofozoitler 12-20 µm çapındadır. Dokuda
bulunanlar ise 20-40 µm, bazen 50-60 µm çapında olabilmektedir. E. histolytica’nın dokuda kist şekli yoktur. Trofozoit formu aktif olarak hareket eden, beslenen, büyüyen ve çoğalan şekildir. Sabit şekli yoktur, yalancı ayakların oluşması sonucu sürekli şekil değiştirir. Yalancı ayakların çıktığı bölgelerde ektoplazma ve endoplazma kolay ayırt edilir. Boyanmış trofozoitin çekirdeği tipik bir görünüme sahiptir. Çekirdek zarının iç yüzünde hepsi aynı büyüklükte olan kromatin tanecikleri bulunur ve karyozom tam merkezdedir (30).
Prekist: Trofozoitin kist dönemine geçişinin ilk basamağıdır. Trofozoit formunun
çoğalmasını sürdürebilme koşullarının güçleştiği, hastalık belirtilerinin azaldığı durumlarda meydana gelen formdur. Bu formun beslenme ve hareketi durmuş, şekil olarak yuvarlaklaşmıştır. Endoplazma ve ektoplazma ayrımı yapılamaz. Çekirdek, trofozoit formundakine göre daha da küçülmüştür ve endoplazmada uçları küt çomakçıklar şeklinde kromatoid cisimcikler görülür (31).
Kist: Çapı 11-12 µm kadar olup, genellikle 15 µm’den küçüktür. Prekist’ten meydana
gelir ve genellikle yuvarlak bir şekildedir. Bazen söbe ya da hafif simetrisiz olabilir. Boyanmamış preparatlarda çekirdek ve glikojen vakuolü fark edilmez ancak; kromatoid cisimcikler görülebilir. Boyanmış preparatlarda çekirdek yapısının trofozoitlerinin çekirdek yapısından farksız olduğu görülür. Enfeksiyonun bulaşması bakımından önemli olan şekil dört çekirdekli olgun kistlerdir (30,31).
Metakist ve metakistik trofozoit: Oral yolla alınan dört çekirdekli kistin kist duvarı ince
bağırsağın son kısmına gelince kaybolur, ortaya dört çekirdekli bir trofozoit çıkar ki, buna metakist denir. Daha sonra metakistin sitoplazması çekirdek sayısı kadar bölünür ve bir kistten dört trofozoit oluşur; bunlara ise metakistik trofozoit denir (29).
18 2.3.2.2 İmmunoloji
Hücresel immün savunma mekanizmalarının, invaziv hastalığın sınırlanmasında ve tedaviden sonra bir nüks oluşmasında etkili olabildiği bildirilmiştir. Hücresel yanıt, E. histolytica trofozoitlerini öldürmek için makrofajları aktive etme yeteneği olan lenfokinlerin (interferon-γ) oluşumu ile antijene spesifik lenfositlerden oluşur. Ayrıca beş gün boyunca E. histolytica antijeni ile uyarılmış immün T hücrelerinin in-vitro inkübasyonu, E. histolytica trofozoitlerine karşı sitotoksik T lenfosit aktivitesini sağlar. AIDS’li hastalarda şiddetli invaziv amoebiosis insidansının yüksek olması, bu hastalarda konak direncinin hücre aracılığı ile olan mekanizmaları içermediğinden kaynaklandığı tahmin edilir. Bu hastalığa karşı etkili ve emniyetli aşı geliştirme çalışmaları devam etmektedir (27).
E. histolytica enfeksiyonu sırasında geçici immünosupresyon oluşur. T lenfositlerin fonksiyonları, makrofajlara bağlıdır ve ameobiosisli hastalarda makrofaj fonksiyon bozuklukları, T lenfositleri tetikler. E. histolytica’dan salınan sekresyon ve atılım ürünleriyle, eriyik proteinlerin makrofajlardaki araşidonik asit metabolizmasını stimüle ederek prostoglandin E2 ve lökotrien C4 salınımının artması immün yanıtın zayıflamasıyla ilişkili görülür. E. histolytica’nın enfeksiyon oluşturması, hastalığın akut fazı esnasında vücut immun yanıtının zayıflamasıyla ilişkili görülür (27,33).
E. histolytica, kalın bağırsaklarda mukus salgılanmasına neden olur. İn-vitro çalışmalarda kalın bağırsak mukus salgılarının, amebik tutunmayı ve kolon epitel hücre lizisini engellediği gösterilmiştir. Amiplerin bağırsak mukozasına yapışmasına karşı IgA cevabının oluşması, parazitin kolon hücrelerinin salgıladığı sadece kolonik mukuslara yapışmasını sağladığı ve dolayısıyla amiplerin bağırsak dokusuna yapışmasının önlenebildiği ve invaziv bir hastalığın oluşmadığı bildirilmiştir. E. histolytica trofozoitlerinin, hücre dışı matriks proteinlerini ve hücre membranlarını bozabilen sayısız proteolitik enzim salgıladığı bilinir. Bu salgıların esas itibariyle cystein katalitik mekanizmalarla harekete geçtikleri bilinmekte olup, sekiz farklı cystein proteaz patojenik salgısının E. histolytica'da bulunduğu gösterilmiştir. Bu proteaz salgıları optimal olarak pH: 7.0-8.0’de çalışmakta olup kültürde üreyen trofozoitlerle salgılanabildikleri ve cystein proteaz inhibitörleri tarafından salgılanmasının önlenebildiği gösterilmiştir. Son zamanlarda bu proteinazın salgılanmasını sağlayan bir gen saptanmıştır. Ayrıca invaziv amibiyazlı hastaların bu proteaza karşı antikor geliştirdikleri belirlenmiştir (33).
19 2.3.2.3 Patojenite ve klinik belirtiler
E. histolytica’nın en belirgin özelliği bağırsak duvarına yerleşebilmesidir. Bağırsak epiteline yapışan amipler burada salgıladıkları hücre eriten enzimlerle dokuyu eritir, daha derinlere girer ve submukozaya geçer (24). Bu protozoonun kökenleri arasında virulens bakımından farklılıklar vardır. Parazitin hastalık yapmasında, trofozoitlerden salınan enzimlerin, enterotoksin veya sitotoksinlerin ve ayrıca amibin, dokuya temasıyla hücre erimesinin rolü olduğu bildirilmiştir (30,31).
Patojen şekle geçen E. histolytica trofozoitleri dokularda ödem, fibrinleşme, nekroz ve erimeye neden olur. Bağırsak epiteline yapışan amipler, saldıkları kollegenaz ve major nötral proteinaz gibi birçok proteolitik enzimle dokuları eritir ve kandaki eritrositleri fagosite ederek beslenir. Submukozaya geçip yanlara doğru yayılarak ağzı dar bir şişe tarzında amip ülserleri meydana getirirler. Amipler bağırsak çeperinde oluşan ülserlerin genellikle kenarlarında ve dibinde bulunur ve erimiş epitel hücreleri ve eritrositlerle beslenir. Ülserlere en çok çekum, rektum ve sigmoid kolonda, ağır vakalarda kalın bağırsağın her tarafında rastlandığı gibi ince bağırsak ve appendiksde de görülebilir (27).
Amipli dizanterinin komplikasyonları arasında amoeboma, peritonit, amipli appendisit, bağırsak invaginasyonu, mesane-sigmoid fistülü, bağırsakta daralma, amipli anüs granülomu ve vajinaya yayılma sayılabilir. E. histolytica’dan kaynaklanan amibik karaciğer apsesinde basit hepatit, amip hepatiti ve amip apsesi görülür. Karaciğer apsesi plevra, akciğer, deri, bağırsak, perikard, periton, safra yolları ve damarlara açılabilir (27).
E. histolytica akut dizanteriye neden olabilir. Akut amipli dizanteride mukuslu ve kanlı dışkı karakteristiktir. Sonraki aşamalarda ateş, baş ağrısı ve soğuk algınlığı belirtileri görülebilir. Kronik vakalarda irritan bir bağırsak sendromu ve bazen de spesifik olmayan semptomlar vardır. Bağırsak amibiyazında semptomlar çok belirgin olabildiği gibi bazen hiçbir belirti de vermeyebilir. Karın ağrısı, ishal, iştahsızlık, kilo kaybı, kronik halsizlik gibi belirtiler olabilir. Bu protozoon karaciğer, akciğer, deri, dalak, perikard, beyin, üreme organı ve idrar yollarına yerleşebilir (30).
Bağırsak amibiyazının neden olduğu bir komplikasyon da karaciğer amibiyazıdır. Genellikle kolonda yerleşmiş etkenin, vena porta yolu ile karaciğere taşınması ile gerçekleşir ve lenf yolu ile geçişin nadir olduğu bilinir. Karaciğere ulaşan
20
amip kolonilerinin ve nekrotik hücrelerin artması ile lökosit infiltrasyonu başlar. Karaciğer apselerinin %85’i sağ lopta, %15’i sol lopta, %15-25’i ise her iki lopta görülür. Akut karaciğer amibiyazında ağrı, ateş ve hepatosplenomegali önemli klinik bulgulardır. Karaciğerde sağ üst kadranda ağrı, intermittant tipte bir ateş, safralı kusma, bulanık görme belirtiler arasında yer alır. Hepatik apseler deriye de taşınabilir (30).
Karaciğer amip apsesinin diyafram yoluyla akciğere doğru açılmasıyla veya kan yolu ile E. histolytica trofozoitlerinin bağırsaktan doğrudan akciğere taşınmasıyla akciğer amibiyazı oluşur. Öksürükle çıkan balgamda karaciğer hücreleri de görülebilir. Apse bronşlara açılmışsa çikolata renkli balgam görülür. Hafif dispne, yüksek ateş, toraksın yarısını kaplayan ağrı, yorgunluk ve ara sıra görülen öksürük belirtiler arasında yer alır. Beyin, plevra, perikard, dalak, safra kesesi, deri, idrar ve üreme organlarında E. histolytica trofozoitleriyle gelişmiş apseler veya ülserler görülebilir ve bunlar bağırsak dışı odaklı amibiyaz olarak değerlendirilir. Tutulan organa göre değişen ağrı, ateş yükselmesi ve lökositoz görülür (27). E. histolytica’ya karşı insanlar oldukça dirençlidir. Bir kökenle insanlara bulaştırma deneyleri sonucunda bazı kişilerde hastalığın şekillendiği, bir kısmında ise enfeksiyonun meydana gelmediği bildirilmiştir. Amibiyazda konakta hem hücresel hem de humoral bağışıklığın geliştiği bildirilmiştir. Bu tip bağışıklığın gelişebilmesi için E. histolytica trofozoitlerinin dokuda yerleşmesi gerekmektedir. Bazı araştırmacılar, insanların amiplere karşı hücresel bağışıklık ile korunduğunu göstermiştir. Steroidler, ışınlama ya da antimakrofaj serumla, bağışıklığın bastırılması ile hayvanlarda hastalığın ağırlaştığı bildirilmiştir (34).
2.3.2.4 Tanı
E. histolytica’nın kesin teşhisi laboratuar incelemesine dayanır. İncelenecek örnekler, dışkı, rektum kazıntı materyali, apse materyali, biyopsi ve otopsi materyali olabilir (26). Bir hastada mikroskobik olarak amip bulunmadığını bildirmek için en az altı gün üst üste alınan dışkı örneklerinin incelenmesi gerekir. Dışkıların bu şekilde incelenmesi ile amibiyaz olgularının %90’ından fazlasının saptanabileceği bildirilmiştir (34).
Amebiyazın tanısında günümüzde mikroskopi, kültür yöntemleri, izoenzim analizi, antijen saptama yöntemleri ve PCR gibi moleküler yöntemler kullanılmaktadır.
21
Özellikle bağırsak dışı amibiyazın tanısında IHA, komplement birleşmesi, IFA ve ELISA gibi serolojik yöntemler önem taşır (30).
Bağırsak amibiyazı, özellikle basilli ve Balantidium coli’ye bağlı dizanteri, schistosomiasis, ülserli kolit, kalın bağırsak kanseri olmak üzere, bütün kalın bağırsak hastalıklarını taklit eder. Bu nedenle kesin tanım, dışkı veya kalın bağırsaktan sigmoidoskopi ve rektoskopi yardımı ile elde edilen kazıntıda E. histolytica’nın ortaya konulması ile yapılır. Tomografi, ultrasonografi ve radyoizotoplarla yapılan incelemeler de tanımda yardımcı olur. Radyolojik incelemeler ile darlıklar ve amoebomalar saptanabilir. Karaciğerin amipli apsesinde diyafram hareketi azalır, plevrada sıvı, akciğer alanında kollaps ve akciğer apsesi saptanır. Antibiyotikler, antiasitler, bağırsak yıkamaları, radyolojik inceleme amacı ile içilen maddeler trofozoitlerin bulunmasını zorlaştırır (34).
Trofozoitlere genellikle sulu, kistlere ise şekilli dışkılarda rastlanır. Dışkının bazı kısımlarında çok miktarda parazit bulunduğu halde, bazı kısımlarında hiç bulunmayabilir. Katı dışkıların sümüklü-kanlı olan kısımlarından preparasyon yapılır. Çok kanlı ve tedavi gören şahıslara ait dışkı örneklerinde trofozoitlerin bulunması zordur. Trofozoitleri tipik olarak ve canlı halde görebilmek için dışkının soğumamış olması gerekir (27,29).
2.3.3 Cryptosporidium spp. (Clarke, 1895)
Önceden bilinen koksidian parazitlerin aksine ookistlerin içindeki sporozoitleri çevreleyen sporokistlerin olmaması nedeni ile cryptosporidium (gizli sporokistler) olarak isimlendirilmitir (35). Bu cinse ait farklı hayvanlarda parazitlenen 20 ayrı tür tespit edilmiştir.
2.3.3.1 Morfoloji Ve Evrim
Cryptosporidium' lar özellikle baırsak mikrovilluslarında hücre içine yerleşerek burada izogonik, gametogonik döllenme ekilleri olutururlar. Besinlerle sporlu ookistlerin alınmasından birkaç gün sonra merozoit içeren izontlarla izogoni ortaya çıkar. Tip 1 merontlarmda 6-8 merozoit oluur. Bunlar hücreleri parçalayıp serbest kaldıktan , sonra dier hücreleri enfekte ederler. Bir kısmı Tip 2 merontlarını olutururlar,
22
bu merontlar izogoni oluşturmazlar. Bunlardan oluşan merozoitler mikrogamotosite, sonra mikrogamete, bazı merozoitler ise makrogamotosite sonra makrogamete dönüşürler. Mikrogametin makrogameti döllemesi ile zigota, zigot ookiste dönüür. Ookistler dıkı ile veya solunum yollarında toplanmısa ekspektorasyonla dıarıya atılırlar. Ookistlerin % 80' i kaim, % 20'si ince çeperlidir (otoenfeksiyonda rol oynar). Ookistler, 4-5 m çapında, yuvarlaımsı, içinde 4 sporozoit bulunan yapılardır. Sindirim veya solunum yolundan alındıklarında açılırlar, serbest kalan sporozoitler, epitel hücrelerinin yüzeyinde yerleşip trofozoitlere dönüşürler (35) .
2.3.3.2 Epidemiyoloji
İnsana bulaşmada ev hayvanlarının özellikle buzağıların dışkısı rol oynar, fakat insandan insana da bulaş da olmaktadır. Sessiz infeksiyonlular ve hastalık bittikten sonra hala ookist saçanlar bulamada önemini korumaktadır. Aslında bir zoonoz olan bu protozoon insandan insana yakın temasla, bebek bezlerinin değitirilmesi sırasında da geçebilmektedir. Ookistlerle pistlenen sularla, çiğ sütlerle, özellikle sucuk, sosis ve sakatatla bulama olmakta, infeksiyon sıcak ve nemli mevsimlerde artmaktadır. Cryptosporidium için dışkı örneklerinde genelde %1.3 oranında rastlanabileceği kanısı yaygındır. C. parvum oldukça bulaşıcı olabilmesi nedeniyle aile içinde, toplu yaşanan yerlerde ve turistlerde diyare etkeni olarak kaşrılaşılmakta ve sudan kaynaklanan diyare salgıları ile ilişkili olduğu bildirilmektedir (36). Cryptosporodiosis, gelişmekte olan ülkelerde gelişmi ülkelere oranla daha fazla görülmektedir. İshalli olgularda yapılan epidemiyolojik çalımalarda % 1-5'lik bir prevalans saptanmıştır. Avrupa'da % l-2, Kuzey Amerika'da % 0.6-4.3, Asya, Avusturalya, Afrika, Orta ve Güney Amerika'da % 3-20 oranında Cryptosporidiosis'e rastlanılmakta olduu bildirilmektedir (35) Ülkemizin deiğişik bölgelerinde yapılan çalışmalarda oranın % 1-30 arasında değiştiği bildirilmektedir (36).
2.3.3.3 Klinik ve Patogenez
Sağlıklı kişilerde 1-2 haftada kendiliğinden iyileşen, diyarelere neden olan Cryptosporidium’ un, immünitesi düşük bireylerde en önemli klinik bulgusu diyaredir. Diyare karakteristik olarak bol ve su gibidir, mukus içerebilir ancak dışkıda kan ve lökosit nadiren bulunmakta, bu tabloya sıklıkla kilo kaybı da eşlik etmektedir.
23
Diyareden başka karın ağrısı, bulantı, kusma ve 39°C altında ateş görülmektedir. Nadiren halsizlik, başağrısı ve anoreksi gibi özgün olmayan belirtileri de gözlenebilmektedir. Bazı parazitler gibi konağın immün direncinin düşmesi ile daha sık ve ağır enfeksiyonlara yol açtığı bilinmektedir (37). Cryptosporidium sp. AIDS'li hastalarda en önemli fırsatçı patojenlerden biridir. Dünyadaki AIDS'li hastaların % 46' sında Cryptosporidium tanımlanmıştır. Gelişmekte olan ülkelerde Cryptosporidium, immun sistemi baskılanmış çocuklarda hem akut hem de sürekli diyareye neden olmakta ve zamanla ağırlaşarak ölüme yol açan en önemli unsur haline gelebilmektedir (35).
2.3.3.4 Tanı
Dışkı, balgam, safra örnekleri ve diğer vücut sıvılarında Cryptosporidium’ ların ookistlerinin görülmesiyle tanı konmaktadır. Bulaşdan 3 gün sonra dışkıda 4 sporozoitli ookistler görülmekle beraber Lugol ile esmer renge, ince yaymada Giemsa ile meneke rengine boyanmaktadır. Dışkı konsantrasyon yöntemleri Ritchie, santrifüj yöntemi, Kato yöntemi (Kato thick-smear yöntemi), eker flotasyon yöntemi ile Heidenheine'nin corbol fuschine boyası tanıda çok yararlı yöntemlerdir. Modifıye Ziehl-Nielsen ve Kinyoun Asid-Fast boyaları, insan ve hayvan dıkılarında Cryptosporidium’ların ookistleri ile mayalar arasındaki farkı ortaya koymaktadır. Auramine-Rhodamine boyama yönteminin en yüksek tanı değerine sahip, hızlı sonuç verebilen bir yöntem olduu ve ooksitlerin x250 büyütmede bile kolay ayırt edilebilmesi tanıda önemli olmaktadır (35). Son zamanlarda dışkıda ELISA aracılığı ile Cryptosporidium antijenlerini arayan yöntemler de geliştirilmiştir. İnsan ve hayvan Cryptosporidium antijenlerine karı hümoral cevaplar Western-Blot yöntemi ile kolayca saptanabilmektedir (35,37).
2.3.4 Ascaris Lumbricoides Ve Parazitliği Linnaeus, 1758 2.3.4.1 Morfoloji ve Evrim
İnsanlarda parazitlenen nematodların en büyüğü olan A. lumbricoides, silindirik bir yapıdadır ve iki uca doğru giderek incelenen vücudu kütikül tabakası ile örtülüdür. Kütikül üzerinde enine ince çizgiler bulunur. Ağızda biri dorsal ikisi ventral yüzeyde yer alan ve üzerinde ufak dişler taşıyan üç dudak bulunur. Üçgen şeklindeki
24
ağız bu üç dudağın ortasında yer alır. Erkeği 15-30 cm uzunluğunda, 3-5 mm çapındadır. Arka ucu, karın yüzüne doğru çengel şeklinde kıvrılmış olup, bu kıvrımın uç kısmında iki tane spikül bulunur. Dişisi 20-40 cm uzunluğunda, 5 mm çapındadır. Vulva, vücudun ön 1/3 kısmıyla, orta 1/3 kısmın birleştiği yerde, karın yüzüne açılan oval bir deliktir. Yumurtaları kahverengi, oval ve bazen yuvarlak olabilir. En dışta girintili çıkıntılı bir yapıda olan protein tabakası, ortada yumurtanın direncini sağlayan kalın, renksiz, saydam ve düz yapıda olan membrana lucida ve en içte embriyoyu saran askarosit zar olmak üzere üç tabakadan oluşur. Döllenmiş ve döllenmemiş olmak üzere iki tip yumurtaları vardır. Döllenmemiş yumurtalar 88-94 µm uzunluğunda ve 39-44 µm genişliğinde genellikle simetrisiz olup, bazen dikdörtgen, üçgen ya da yamuk gibi şekillerde de görülebilir. Bu durum, bağırsakta erkek nematodlar bulunmadığında, tüm dişiler döllenemediğinde ya da enfeksiyon kendiliğinden iyileşmeye başladığında görülür. Bu yumurtaların enfektif özelliği yoktur. Döllenmiş yumurtalar simetrili, söbemsi yapıda olup, yumurta hücresi ve kabuğu arasında boşluk vardır. Bu yumurtaların boyu 45-75 µm, eni 35-50 µm’dir (30).
A. lumbricoides’in erişkinleri, insanların ince bağırsaklarında yaşar. En fazla yerleştikleri organ jejunum olmakla beraber ileumun ortalarına kadar da yerleşim gösterebilirler. Bu parazitin dar kanallara girme eğilimi vardır ve bu suretle safra kanallarına girebilir ayrıca mide ve özefagusa da geçebilir. Beslenmeleri sindirilmeye hazır konak besinlerinin doğrudan bağırsak lümeninden alınmasıyla olur. Domuz askarisleriyle yapılan çalışmalarda, parazitlerin bağırsak lümeninde antiproteolitik enzim salgılayarak, pepsin ve tripsin gibi konak sindirim enzimlerinden korundukları gösterilmiştir (27).
Erişkin parazitler, insan bağırsağında bir yıl, nadiren 17 ay kadar canlı kalabilir. Bir dişi parazitin hayatı boyunca 25-27 milyon kadar yumurta yapabilecek kapasitede olduğu, erkek parazitle erken dönemde çiftleşme meydana geldiğinde dişilerin bir günde 200.000 kadar yumurta yapabileceği ve bu suretle dışkıda yumurta sayımı yapılarak insan ince bağırsağında bulunan parazit sayısı hakkında bilgi edinilebileceği bildirilmiştir (27).
Uygun şartlarda dişi tarafından yumurtlanan döllenmiş yumurta içerisinde tek bir embriyon hücresi (blastomer) bulunur. Dış ortamda yumurtaların içinde embriyon gelişebilmesi için en uygun sıcaklık 25 ºC olup, yumurtalar 21-30 ºC sıcaklıkta da gelişebilir. Düşük sıcaklık derecesinde embriyonun gelişmesi yavaşlar. Embriyonun
25
gelişmesi için ortamda nem ve oksijenin de bulunması gerekir. Kuru ve çok nemli ortamın da yumurta içerisinde embriyonun gelişmesini yavaşlattığı bildirilmiştir. Larva yumurta içinde S şeklinde kıvrılır ve yumurtadan dış ortamda çıkmaz. Dışkı ile dışarı atıldıktan sonra dış ortamda uygun sıcaklık, nem ve oksijenin varlığında, yumurta içerisinde 2-3 haftada ikinci dönem larva oluşur. Bu yumurtalar insan için enfektiftir. Enfektif yumurta yiyecek, içecek ve kirli ellerle ağız yoluyla alındığında, kalın kabuğuyla mide asidinden etkilenmeden duodenuma gelir. Burada sindirim enzimlerinin etkisiyle yumurta kabuğu incelip erir ve sonunda larva serbest kalır. Bu larva 200-300 µm uzunlukta olup ağız kapsülünden sonra gelen uzun silindirik özefagusunun sonunda ampul şeklinde şişkinlik bulunur ve bu nedenle larvaya rhabditiform larva adı verilir. Larva bağırsak çeperinden geçerek karaciğere gelir ve burada 3-4 gün kaldıktan sonra kan dolaşımı ile kalbe buradan da akciğere geçer. Akciğerde 5-10 gün içerisinde evrimini tamamlar ve trake, farinks, özefagus ve mideden geçip ince bağırsağa gelir ve burada yerleşir. Dişi parazit bulaşmadan 60-90 gün sonra yumurtlamaya başlar (30).
2.3.4.2 Epidemiyoloji
A. lumbricoides, ülkemizde yaygın olarak görülen bir parazittir. Dünyada yaklaşık 1.25 milyar kişinin bu parazit ile enfekte olduğu tahmin edilmektedir.
Askariyazda parazit kaynağı, bağırsağında erişkin dişilerin bulunduğu insanlardır. Bu dişilerin ömrü genellikle on aydan azdır. Enfeksiyon, içerisinde enfektif larva olan yumurtanın su, toprak ve besinlerle yutulması ile sindirim yolundan bulaşır. Yumurtalar dirençli oldukları için toprakta uygun şartlarda yıllarca enfektif olarak kalır. A. lumbricoides yumurtalarının gelişebilmesi için 15 oC’nin üstünde bir sıcaklık ve en az %50 nispi nem gereklidir. İnsan dışkısının gelişigüzel etrafa saçıldığı ya da gübre olarak kullanıldığı bölgelerde, açık lağım suları geçen yerleşim alanlarında bu enfeksiyona daha sık rastlanır (29).
2.3.4.3 İmmunoloji
Askariyazda larvalara karşı bir bağışıklık gelişirken, erişkinlere karşı gelişmez ya da çok düşük seviyede olur. Peritona ya da diğer organlara giden Ascaris larvalarının etrafında granülom oluşması hücresel bağışıklığa bağlanmıştır. Hayvanlar üzerinde özellikle Ascaris ile yapılan deneylerde az çok bir bağışıklığın geliştiği bildirilmektedir.
26
Ascaris ile enfekte insanlarda IgE, IgM, IgG ve IgD’nin düzeyinde artma olduğu bildirilmiştir (30,31).
İntestinal nematodların oluşturduğu enfeksiyonu takiben gelişen yardımcı T hücre yanıtları enfeksiyonun prognozu için önemlidir. İnsan askariyazında serum immunoglobulin seviyesindeki artışla birlikte polarize Th2-tip immun yanıtın görüldüğü bildirilmiştir. A. lumbricoides enfeksiyonunda oluşan sitokin yanıtını belirlemek için larva ve erişkin safhasındaki Ascaris antijenlerine karşı oluşan hücresel immun yanıt enfekte olmayan kontrol grubuyla karşılaştırılmış, enfekte olanlarda bu antijenlere karşı oluşan lenfoproliferatif yanıtın ve periferik kan mononükleer hücrelerinden IL-4 ve IL-5 salınımının belirgin oranda yüksek olduğu görülmüştür. IL-10 ve interferon gamma salınımında ise her iki grubun benzer olduğu görülmüştür (33).
2.3.4.4 Patojenite ve klinik belirtiler
A. lumbricoides’in yumurtadan çıkan larvaları bağırsak duvarından geçerken burada nokta halinde kanamalara ve küçük lezyonlara yol açarlar; aynı bozuklukları karaciğerde de yapabilirler. Akciğerdeki lezyonlar genellikle daha belirgindir. Larvalar kan damarlarını delerek solunum yollarına geçtiğinden kanamalar ve bazı reaksiyonlara neden olurlar (29). Akciğerlerde oluşan pnömoni tablosunda, kapiller damarların yırtılmasıyla yer yerkanamalar ve ayrıca alveol duvarlarında yangı ve hücre infiltrasyonu meydana gelir. Alveollerde biriken lökosit, makrofaj ve eozinofilden zengin kan hücreleri ile fibrin ve epitel hücreleri lobuler pnömoniye yol açar (27).
İnce bağırsaklarda fazla sayıda parazit olmadığı takdirde klinik belirti ortaya çıkmaz. Parazitlerin fazla sayıda olmaları ya da konağın çok duyarlı olması durumunda erişkin parazitler mekanik, toksik ve alerjik etki oluşturur. Bu parazitler bağırsak mukozasına kuvvetli dudaklarıyla tutunur ve mukozada yer yer yaralar, kanama odakları ve yangı oluşturabilir. Gerek çiftleşme için gerekse birbirlerine sarılma özelliklerinden dolayı bağırsak lümeninde yumak oluşturup bağırsak tıkanmalarına, bağırsak invaginasyonuna, dar kanallara girme özelliklerinden dolayı safra kanalları ve pankreas kanalında tıkanmalara, mukozaya kuvvetle tutunmaları esnasında bağırsak delinmelerine ve peritonite yol açarlar. Bağırsak mukozasında yaralanmalarla yerel ve zamanla genel bağırsak enfeksiyonlarına, metabolizma artıkları ve çıkartılarıyla toksik ve alerjik reaksiyonlara, meydana getirdikleri sindirim bozuklukları ile malnutrisyona
27
neden olurlar. İnce bağırsaklarda fazla sayıda bulunduklarında genellikle ileo-çekal geçiş bölgesinde tıkanmalara neden oldukları ayrıca, appendisit ve enterokolit olgularında da rollerinin olduğu bildirilmiştir (27).
Askariyazda belirtiler larval dönemlerin ve erişkin şekillerin meydana getirdiği belirtiler olarak iki bölümde incelenebilir. Larvalar karaciğer ve akciğerden geçerken hiçbir belirti vermeyebilir. Fakat bir defada fazla sayıda yumurta alındığında, çok sayıda larva aynı zamanda akciğerden geçeceği için özel bir tip olan Löffler pnömonisi görülebilir (34). Klinik belirtilerin şiddeti bağırsaktaki parazit sayısı ile doğru orantılıdır. Askariyazda özellikle göbek etrafında yoğunlaşan karın ağrısı, mide bölgesinde ağırlık, iştahsızlık, iştah sapması, hava yutma, geğirme, diyare, bulantı, kusma, gece ağızdan salya akması, burun kaşıntısı ve ürtiker benzeri döküntüler görülebilir. Parazit fazla sayıda olduğunda bağırsak tıkanabilir ve kusma gibi belirtiler de görülebilir. Dişi parazitlerin dar kanallara girmeye meyli vardır. Ayrıca, bağırsak koşullarındaki değişikliklerden etkilenip mideden geçerek yemek borusu yoluyla ağız, burun, dış kulak gibi açıklıklardan çıkabilir, bu göç esnasında solunum yollarına girerek ölüme bile neden olabilirler. Safra kanalından geçerek safra kesesine girebilir ve safra kanallarını tıkayabilir, vater ampullasından geçerek pankreasa girebilirler. Appendix’e girip apandisite yol açabilir, tifo gibi hastalıklar nedeniyle incelmiş bağırsak çeperini delerek peritona geçebilirler. Ameliyat olmuş hastalarda ise dikiş yerlerinden çıkabilirler (31).
2.3.4.5 Tanı
A. lumbricoides’in teşhisi dışkıda yumurtalarının ya da erişkinlerinin görülmesi ile yapılır. Eğer bağırsakta yalnız erkek parazitler ya da olgunlaşmamış solucanlar varsa parazitin teşhisinde ultrasonografik yöntemlerden yararlanmak mümkündür. A. lumbricoides yumurtalarının alınmasından sonra, larvalar akciğer göçü döneminde solunum belirtilerine neden olur; bu dönemde balgamda parazitin kurtçuk şekli aranır (Unat ve ark., 1995; Saygı, 1998). Bağırsak askariyazı tanısında çöktürme yöntemlerinden modifiye Ritchie (formol-etil asetat çöktürme yöntemi) iyi sonuç verir ve hem döllenmiş hem de döllenmemiş yumurtaların kolaylıkla görülmesine olanak sağlar. Yüzdürme yöntemleri uygulandığında ağır olan döllenmemiş yumurtaların yüzdürülmesi mümkün olamadığından negatif sonuç alınabileceği unutulmamalıdır.