T.C.
EGE ÜNİVERSİTESİ TIP FAKÜLTESİ
GENEL CERRAHİ ANABİLİM DALI
SENTİNEL LENF NODU POZİTİF HASTALARDA
NONSENTİNEL LENF NODU POZİTİFLİĞİNE ETKİ
EDEN FAKTÖRLER
TIPTA UZMANLIK TEZİ
Dr. Samed CİN
Tez Danışmanı
Doç. Dr. Levent YENİAY
ÖNSÖZ
Hiç bitmeyecekmiş gibi başlayıp göz açıp kapayıncaya kadar geçen genel cerrahi eğitim sürecinde, herbirinin üzerimde ayrı ayrı emeği olan, bizlerin iyi hekim, iyi cerrah olarak yetişmesinde gerek bilgi, birikim ve deneyimleri gerekse rol model olarak bizlere örnek olan hocalarım, başta Anabilim Dalı Başkanımız Prof. Dr. Mustafa Yılmaz’a, saygıdeğer hocalarım Prof. Dr. Rasih Yılmaz, Prof. Dr. Adem Güler, Prof. Dr. Mahir Akyıldız, Prof. Dr. Mustafa Ali Korkut, Prof. Dr. Cüneyt Hoşcoşkun, Prof. Dr. Ahmet Çoker, Prof. Dr. Erhan Akgün, Prof. Dr. Sinan Ersin, Prof. Dr. Gökhan İçöz, Prof. Dr. Murat Sözbilen, Doç. Dr. İlhami Solak, Doç. Dr. Cemil Çalışkan, Doç. Dr. Özgür Fırat, Doç. Dr. Özer Makay, Doç. Dr. Taylan Özgür Sezer ve Doç. Dr. Ömer Vedat Ünalp’e sonsuz teşekkürlerimi sunarım.
Tez çalışmam süresince benden tecrübelerini, desteğini ve hoşgörüsünü esirgemeyen değerli tez danışman hocam Doç. Dr. Levent Yeniay’a ayrıca teşekkür ederim.
Yenilikçi yaklaşımları, cerrahi teorik ve pratik bilgileri ile eğitimimde yadsınamaz payı olan Op. Dr. Tayfun Yoldaş, Op. Dr. Alper Uğuz, Op. Dr. Murat Özdemir, Op. Dr. Osman Bozbıyık abilerime sonsuz teşekküer ederim.
Asistanlığım süresince birlikte çalıştığımız destek ve dostluklarını minnetle ve özlemle anacağım tüm asistan arkadaşlarıma, hemşirelere ve personellere çok teşekkür ederim.
Bugünlere gelmemde asla ve asla ödenemeyecek emekleri olan annem, babam ve abime, Bana her daim destek olan hayat arkadaşım Merve Cin’e sonsuz teşekkürü borç bilirim.
Ege Genel Cerrahi ailesinin bir üyesi olmak gerçekten sonsuza dek bir ayrıcalık ve gurur kaynağı, iyiki varsınız
SAYGILARIMLA DrSamed CİN
İÇİNDEKİLER
Sayfa ÖNSÖZ ... ii İÇİNDEKİLER ... iii ÖZET ... v ABSTRACT ... viKISALTMA VE SİMGELER ... vii
TABLOLAR LİSTESİ ... ix ŞEKİLLER LİSTESİ ... xi 1.GİRİŞ ... 1 2.GENEL BİLGİLER 2.1- Memenin Anatomisi ... 2 2.2- Memenin Kanlanması ... 2 2.2.1. Memenin Arterleri ... 2 2.2.2. Memenin Venleri ... 2 2.3-Memenin Sinirleri ... 2 2.4- Lenfatik Sistem ... 2
2.4.1. Memenin Lenfatik Sistemi ... 2
2.4.2.Aksiller Lenf Nodülleri ... 2
2.4.3.Mammaryaİnterna Lenf Yolu ... 2
2.4.4. Diğer Lenf Yolları ... 2
2.4.4.1.Supraklaviküler Lenf Nodüllerine Giden Lenf Yolu ... 2
2.4.4.2.RektusAbdominus Kası Yoluyla Memeden Karaciğere Giden Lenf Yolu ... 2
2.5-Aksilla ... 2 2.6- Meme Kanseri ... 2 2.6.1- Epidemiyoloji ... 2 2.6.2- Etyoloji ve Patogenez ... 2 2.6.3- Risk Faktörleri ... 2 2.6.4- Klinik Özellikler ... 2
2.6.5- Meme Kanserinde Tanı Yöntemleri ... 2
2.6.6.Meme Tümörlerinin Histopatolojik Sınıflaması ... 2
2.6.8- Meme Kanserinin Tedavisi ... 2
2.6.9- Meme Kanserinde Aksillanın Tedavisi ... 2
2.6.9.1- Meme Kanserinde Prognoz Tayininde ALND’nin Rolü ... 2
2.6.9.2- Aksiller Lenf Nodülü Disseksiyonunun Komplikasyonları ... 2
2.6.10- Sentinel Lenf Nodülü Biyopsisi (SLNB) ... 2
2.6.10.1- Sentinel lenf nodu tanımı ve tarihçesi ... 2
2.6.10.2.-Sentinel Lenf Nodülü Biyopsisinde Görüntüleme Yöntemleri ... 2
2.6.10.3- Sentinel Lenf Nodülü Biyopsisinde Hasta Seçimi ... 2
2.6.10.4- SLNB Endikasyonları ... 2
2.6.10.5- SLNB Mutlak ve Rölatif Kontrendikasyonları ... 2
2.6.10.6- SLNB Komplikasyonları ... 2
2.6.10.7- SLNB’de Öğrenme Eğrisi ... 2
2.6.10.8- SLN’nin Patolojik Değerlendirilmesi ... 2
2.7. Sentinel Dışı Lenf Nodu Metastaz Olasılığını Belirleyen Modeller ... 2
2.7.1. MemorialSloan-Kettering Kanser Merkezi (MSKCC) nomogramı ... 2
2.7.2. Tenonnomogramı ... 2
2.7.3. Stanford nomogramı ... 2
2.7.4. Meme Hastalıkları Dernekleri Federasyonu Nomogramı (MF08-01) ... 2
3. GEREÇ VE YÖNTEM ... 2
4. BULGULAR ... 2
5.TARTIŞMA ... 2
6.SONUÇ ... 2
SENTİNEL LENF NODU POZİTİF HASTALARDA NONSENTİNEL
LENF NODU POZİTİFLİĞİNE ETKİ EDEN FAKTÖRLER
ÖZET
Amaç:Meme kanserinin cerrahi tedavisinde sentinel lenf nodu biyopsisi (SLNB) prosedürü,
aksiller lenf nodudiseksiyonuna (ALND) alternatif olarak geliştirilmiş ve düşük morbidite ile güvenli bir evreleme yöntemidir.Bu çalışmada meme kanseri tanısı ile başvuran ve sentinel lenf nodu pozitif olan hastalarda nonsentinel lenf nodu pozitifliğine etki eden faktörlerin neler olduğu belirlenmesi amaçlanmıştır.
Yöntem: Bu çalışma Ege Üniversitesi Tıp Fakültesi Genel Cerrahi AnabilimDalı’nda Haziran
2003-Ocak 2016 yılları arasında erken evre aksalla negatif meme kanseri nedeniyle sentinel lenf nodu biyopsisi uygulanan 17-87 yaş aralığındaki 2060 hasta retrospektif olarak tarandı. 54 hastanın patoloji sonuçlarında eksik veriler bulunmasından dolayı çalışmaya toplam 2006 hasta dahil edildi.Çalışmada yeralan 2006 hastanın sentinel lenf nodu sonucu 1474’ü benign, submikrometastaz; 532’si mikrometastaz, makrometastaz olarak raporlandı. 403 hastaya aksillerdiseksiyon uygulandı.23 hastanın SLN sonucu yalancı negatif olması üzerine 380 hasta nonsentinel lenf nodu pozitifliği açısından değerlendirildi. 219 hastanın nonsentinel negatif, 161 hastanın nonsentinel pozitif olduğu görüldü. Hastalara çeşitli tümör bağımlı parametreler çalışıldı. Hasta yaşı, tümör boyutu, tümör bölgesi, histolojik tipi, luminal sınıflandırma, metastaz varlığı ve boyutu, östrojen-progesteron reseptör statüsü, P53, Ki-67, Cerb-2, nükleer derece, modifiyeBloom-Richardson Skor (MBRS), metastatik odak yarıçapı, AD sırasında disseke edilen lenf nodu sayısı bakıldı.Çalışmada toplanan verilerin analizi, istatistiksel yazılım paketi SPSS 23 (Statistical PackagefortheSocialSciences – IBM®) kullanılarak yapıldı. İstatistiksel anlamlılık düzeyini belirlemek için, %95 güven aralığında ve p<0,05 anlamlı kabul edildi.
Bulgular: Çalışma kriterlerine uyan 2006 meme kanseri hastası çalışmaya dahil edilmiştir.
Benign+Submikrometastaz olan hastaların %48,6’sı 50 yaş ve üzeri, %51,4’u 50 yaş altı hastalar olduğu saptanmıştır. Mikrometastaz+Makrometastaz olan hastaların %51,6’sı 50 yaş ve üzeri, %48,4’u 50 yaş altı hastalar olduğu tespit edilmiştir. En küçük yaş 17 olurken en büyük yaş 87 olarak bulunmuştur. Araştırmada yer alan hastaların yaş ortalaması 51,76’dır. Çalışmada non SLN noddurumu ile yaş, tümör çapı, tümör tipi, Öströjen Reseptörü, Progesteron Reseptörü, P53 Geni, Ki67 Reseptörü, MBRS Reseptörü veMultifokalite Durumu arasında istatistiksel olarak anlamlı bir ilişki saptanmamıştır ( p>0,05). Fakat non SLN nod durumu ileLenfovaskulerİnvazyon, ModifiyeBloom Richard Grupları,Cerb-2 reseptörü veLuminal Gruplarıarasında istatistiksel olarak anlamlı bir ilişki saptanmıştır (p<0,05).
Sonuç: Sonuç olarak; çalışmanın tamamlandığı ve nonsentinel lenf nodu pozitifliğini, tümör
çapının artışı, lenfovaskülerinvazyon olması, yüksek nükleer grade ve progesteron reseptör pozitifliği artırdığı sonucuna varılmıştır. Nonsentinel lenf nodu pozitif hastalar aksillerdiseksiyondanterapötik fayda görürken, nonsentinel lenf nodu negatif hastalar net bir fayda görememektedir.
FACTORS AFFECTING POSITIVE NONCENTANNEL LENGTH POSITIVITY IN SENTINEL LYMPH NODE POSITIVE HOSPITALS
ABSTRACT
Objective: Sentinellymphnodebiopsy (SLNB) procedure has beendeveloped as an
alternativetoaxillarylymphnodedissection (ALND) in thesurgicaltreatment of breastcancerand is a safemethod of stagingwithlowmorbidity. Inthisstudy, it wasaimedtodeterminethefactorsaffectingthepositivity of thenonsentinellymphnode in patientswithbreastcancerdiagnosisandsentinellymphnodepositive.
METHODS: Thisstudywasretrospectivelyperformed on 2060 patientsbetweentheages of
17-87 yearswhounderwentsentinellymphnodebiopsyduetoearlystageaxal-negativebreastcancerbetweenJune 2003 andJanuary 2016 in Ege UniversityMedicalFaculty General SurgeryDepartment. A total of 2006 patientswereenrolled in thestudybecause of themissingdata in thepathologyresults of 54 patients. Inthestudy, 2006 patientsentinellymphnoderesultant 1474 wasdiagnosed as benign, submicrometastasis; 532
werereported as micrometastases, macrometastases. 403
patientsweretreatedwithaxillarydissection. 38
patientswereassessedfornonsentinellymphnodepositivitywhenthe SLN resultwasfalsenegative in 23 patients. 219 patientswerenegativefornonsentineland 161 patientswerepositivefornonsentinel. Varioustumor-dependentparameterswerestudied in thedisease. P53, Ki-67, Cerb-2, nucleargrade, modifiedBloom-RichardsonScore (MBRS), metastaticfocus, tumor size, tumor size, histologictype, luminalclassification, metastasis presence and size, estrogen-progesteronereceptorstatusTheradius, andthenumber of nodesdissectedduring AD weremeasured. Analysis of thedatacollected in thestudywasmadeusingstatistical software package SPSS 23 (Statistical PackagefortheSocialSciences - IBM®). Todeterminethestatisticalsignificancelevel, 95% confidenceintervaland p <0.05 wereconsideredsignificant.
Results: 2006 breastcancerpatientsmeetingthestudycriteriawereincluded in thestudy. 48.6%
of thepatientswithbenign + submychrometastasiswerefoundto be over 50 yearsoldand51.4% wereunder 50 yearsold. 51.6% of patientswithmicrometastasis + macrometastasiswerefoundto be over 50 yearsoldand48.4% wereunder 50 yearsold. Theyoungestagewas 17 yearsandthelargestagewas 87 years. Theaverageage of thepatients in thestudy is 51.76. Therewasnostatisticallysignificantrelationshipbetweennon SLN nodestatusandage, tumordiameter, tumortype, estrogenreceptor, progesteronereceptor, p53 genotype, Ki67 receptor, MBRS receptorandmultifocalstatus in thestudy (p> 0,05). However, therewas a statisticallysignificantrelationshipbetweennon-SLN nodestatusandLymphovascularInvasion, ModifiedBloom Richard Group, Cerb-2 receptorandLuminalGroup (p <0.05).
Conclusion: As a result; Theresult of thestudywascompleteandresulted in a positivenonsentinellymphnode, increasedtumordiameter, lymphovascularinvasion, increasedhighnucleargradeandprogesteronereceptorpositivity.
Nonsentinellymphnodepositivepatientshavetherapeuticbenefitfromaxillarydissection, whereasnegativepatientswithnon-nonsentinellymphnodehavenoclearbenefit.
KISALTMA VE SİMGELER
SLN: Sentinel Lenf NodülüSLNB: Sentinel Lenf Nodülü Biyopsisi ALND: Aksiller Lenf Nodülü Disseksiyonu SBR: ScarfBloomRichardson
İİAB: İnce İğne Aspirasyon Biyopsisi
BIRADS:BreastİmagingReportingand Data System PCNA: Prolifere Edici Hücre Nükleer Antijeni HER-2: İnsan Epidermal Büyüme Faktörü DCIS: DuktalKarsinoma İn Situ
LCIS: LobulerKarsinoma İn Situ
AJCC : AmericanJointCommitee on Cancer
MRM: Modifiye Radikal Mastektomi
AJCC: AmericanJointCommittee on Cancer
SEER: SurveillanceEpidemiologyandEndResults İHK: İmmunohistokimyasal
MKC: Meme Koruyucu Cerrahi
RM: Radikal Mastektomi LVI: Lenfovaskülerinvazyon GF: Growth Faktör
ER: Östrojen Reseptörü PR: Progesteron Reseptörü RT: Radyoterapi KT: Kemoterapi HT: Hormonoterapi AT: AtaksiaTelenjiyektazi LKİS: LobülerKarsinoma İn Situ DKİS: DuktalKarsinoma İn Situ
UICC: Union International ContreCancer NCCN: NationalComprehensiveCancer Network ml: Mililitre ark.: Arkadaşları n.:Nervus ort.: Ortalama
TABLOLAR LİSTESİ
Tablo 2.1. Meme tümörlerinin histopatolojik sınıflandırması Tablo 4.1. Hastalara Ait Yaş Verileri
Tablo 4.2Tümör Lokalizasyonu
Tablo 4.3. SLN Hastalarda Tümör tipi, Tümör Çapı, Nüklear Grade ve LenfovaskülerİnvazyonunGruplara Göre Büyüklükleri
Tablo 4.4. SLN Hastalarda Estrogenreceptor, Progesteronereceptor, P 53 Durumu, Ki-67 Durumu, Cerb-2 Durumu ve MBRS Ait Veriler
Tablo 4.5. SLN Durumu, Luminal Tipi, Multifokalite Verileri
Tablo 4.6. Negatif Non-SLN ve Pozitif Non-SLN Olan Hastalarına Ait Veriler
Tablo 4.7. Negatif Non-SLN ve Pozitif Non-SLN Durumunda Yeralan SLN Sayıları, Luminal Tipi, Multifokalite Verileri
Tablo 4.8. Non SLN Nod Durumu İle Yaş Grupları Arasındaki İlişki Tablo 4.9. Non SLN Nod Durumu İle Tümor Çapı (Cm) Arasındaki İlişki Tablo 4.10. Non SLN Nod Durumu İle Tümor Çapı (Cm) Arasındaki İlişki Tablo 4.11. Non SLN Nod Durumu İle Tümor Tipi Arasındaki İlişki
Tablo 4.12 NonSentinalNod Durumu İle ModifiyeBloom Richard Grupları Arasındaki İlişki Tablo 4.13. NonSentinalNod Durumu İle Lenfovaskulerİnvazyon Grupları Arasındaki İlişki Tablo 4.14 NonSentinalNod Durumu İle Öströjen Reseptörü Grupları Arasındaki İlişki Tablo 4.15. NonSentinalNod Durumu İle Progesteron Reseptörü Durumu Arasındaki İlişki
Tablo 4.16 NonSentinalNod Durumu İle P53 Geni Durumu Arasındaki İlişki
Tablo 4.18. NonSentinalNod Durumu İle Cerb-2 Reseptörü Grupları Arasındaki İlişki Tablo 4.19. NonSentinalNod Durumu İle MBRS Reseptörü Grupları Arasındaki İlişki Tablo 4.20.Non SentinalNod Durumu İle Luminal Grupları Arasındaki İlişki
Tablo 4.21.Non SentinalNod Durumu İle Multifokalite Durumu Arasındaki İlişki
Tablo 4.22. Non SLN durumu
ŞEKİLLER LİSTESİ
Şekil 2.1. Memenin makroskopik anatomisi Şekil 2.2 Memenin Fasya ile İlişkileri Şekil .2.3. AksillerFasya
Şekil 2.4. Memenin Sinirleri
Şekil 2.5. Memenin Lenfatik Sistemi Şekil 2.6. Aksiller lenf nodülleri
Şekil 2.7.Lenf bezlerinin yerleşimi ve düzeyleri
Şekil 2.8. RektusAbdominus Kası Yoluyla Memeden Karaciğere Giden Lenf Yolu Şekil 9.Evre 1Ave 1B Meme Kanseri
Şekil 10. MD Anderson (2008) Neoadjuvant tedavi Şekil 11. Katz Model (2008)
1.GİRİŞ
Meme kanseri kadınlarda en sık görülen kanser türü olarak güncelliğini korumaya devam etmektedir. Özellikle kadınlarda, 20-59 yaş arası kadınlarda kansere bağlı ölümlerinde ana sebebidir. Günümüzde erken tanı alan kanser olgularının sayısının artmasıyla daha az girişimsel teknik kullanarak tedavi etme yönünde bir eğilim oluşmuştur (1). Meme, modifiye apokrin bir organ olmanın dışında, kanser cerrahisi sonrasında kadınlarda beden algısının ve benlik saygısının bozulmasına neden olabilen, sosyal hayatın devamlılığı için önem taşıyan bir organdır. Meme kanserinin tedavisi planlanırken hastaların psikososyal açıdan da zarar görmemeleri için özen gösterilmelidir. Bu nedenle hastalığın tanı ve tedavisinde daha az girişimsel yöntemlerin tanımlanması ihtiyacı doğmuştur. Zaman içinde “radikal mastektomi” ile başlayan süreç günümüzde “meme koruyucu cerrahi” uygulamalarla devam etmektedir. Bu süreç içinde “aksiller lenf nodu diseksiyonu” uygun vakalar için yerini “sentinel lenf nodu biyopsisi”ne bırakmıştır. Bu sürecin devamı olarak aksilladaki sentinel dışı lenf nodlarının metastaz riskini önceden belirleyebilmek, bilim insanlarının yeni hedefi olmuştur (1,2).
Sentinel lenf nodu biyopsisi (SLNB) erken evre meme kanserlerinin evrelemesi ve tedavisi amacıyla günlük uygulamada sıkça kullanılan bir yöntemdir. Ne var ki SLNB sonucunda metastaz saptanmış olan hastaların aksiller diseksiyon (AD) materyalleri incelendiğinde %40-70 kadarında ilave lenf nodu metastazı saptanmamaktadır. Bu durumdaki hastalar için yapılan aksiller diseksiyonun evrelemeye ve tedaviye katkısı olmayacağı düşünülmektedir. Aksiller diseksiyonun seroma, uyuşukluk ve hissizlik, omuz ve kol bölgesinde ağrı, kolda lenfödem, omuz ve kol hareketlerinde kısıtlılık, yara enfeksiyonu gibi komplikasyonları da göz önünde bulundurulduğunda; bu hasta grubunu önceden belirleyebilmek önem kazanmıştır (3).
Meme kanserinin biyolojisi ve tedavisi, yüzyılı aşan bir süredir farklı hipotezlerle açıklanmaya çalışılmıştır. Tıp tarihinde meme kanseriyle ilgili en eski yazıt M.Ö. 3000-2000 yılları arasında yazıldığı tahmin edilen Edwin Smith Papirüsüdür. Imnohep tarafından yazıldığı sanılan belgede meme kanseri ve ülserinden bahsedilmektedir. 1970’li yıllara kadar meme kanseri radikal yöntemlerle tedavi edilmiştir. William Steward Halsted, 1890’lı yıllarda radikal mastektomi (RM) ameliyatını ilk tanımlayan cerrahtır.(4,5,6)
Halsted’in Hipotezi’ne göre meme kanseri lokal-bölgesel bir hastalıktır. Memede başlayan kanser, önce bölgesel lenf düğümlerine gider, daha sonra sistemik yayılım yapar. RM ile meme kanserinde lokal nüks ve yaşam süresi açısından çok önemli gelişmeler sağlanmıştır. Ancak Halsted, aksillası negatif olan hastaların %23’ünün RM yapılmasına rağmen, hastalığın yayılımı sonucu öldüğünü gözlemlemiştir (5,6,7,8) Bu bulgu meme kanserinin lokal bir hastalık olduğu teorisi ile çelişmektedir. Bu hipotez, 1970’li yıllara kadar, yaklaşık 100 yıl geçerliliğini korumuştur. Bu ameliyatın, kadınlarda ciddi toraks ve omuz deformitesi yapması ve araştırma sonuçlarına göre meme kanserinin bölgesel yayılım yapmadan uzak metastaz yapabilmesi, Bernard Fisher tarafından 1970’li yıllardan sonra kabul edilen yeni bir hipotez geliştirilmesine neden olmuştur. Sistemik Hastalık veya Fisher Hipotezi de denen bu görüş, meme kanserinde sistemik tedavinin önemini ortaya çıkarmış ve kemoterapinin kullanımını yaygınlaştırmıştır (9,10,11). Ayrıca meme kanserinin tedavisinde uygun olgularda meme koruyucu cerrahinin yapılabileceği, radikal mastektomi ile karşılaştırılan randomize klinik çalışmalarla gösterilmiştir (12,13,14)
Meme kanseri olan hastalarda, tümörün çok büyük boyutlara ulaşması ve bölgesel yayılım yapmasına rağmen uzak metastaz yapmaması, aksine bazı çok küçük tümörlerin sistemik metastaz yapması, meme kanserinde tümörün biyolojik davranışının kişiden kişiye farklılık gösterdiğini ve her hastanın ayrı olarak değerlendirilmesi gerektiğini belirten “Spektrum Hipotezi’ni ortaya çıkarmıştır.(14,15). Günümüzde halen bu hipotez daha fazla kabul görmektedir (16).
Meme kanserinin cerrahi tedavisi için uygulanan radikal ameliyatlarla, memeyi koruyucu ameliyatları karşılaştıran modern randomize klinik çalışmaların uzun dönem sağkalım sonuçları, iki ameliyat arasında bir fark olmadığını göstermiştir.(13,17,18). Ancak, lokal nüks oranı MKC yapılan hastalarda anlamlı olarak daha yüksektir. Bu sonuçlar, Meme koruyucu cerrahi (MKC) için hastalarınçok iyi seçilmesini ve lokal tedavilerin (cerrahi+radyoterapi) başarılı bir şekilde uygulanmasını gerektirmektedir. Meme koruyucu cerrahi (MKC), kozmetik ve psikolojik açıdan hastaların yaşam kalitesini arttırmaktadır. 1875’te Richard Van Volkman, meme dokusundaki lenfatik damarların aksiller lenf nodülleri ile ilişkisini ortaya koymuştur. Bunu takip eden yıllarda, aksiller lenf nodülleri meme kanserinde en önemli prognostik ve prediktif faktörlerden biri olarak kabul edilmiş ve ALND meme kanserinin cerrahi tedavisinin (mastektomi veya MKC) vazgeçilmiş bir parçası olarak yüzyıla yakın bir süre uygulanmıştır. Son 20 yıl içerisinde geliştirilen sentinel lenf nodülü biyopsisi, klinik olarak aksillası negatif olan hastalarda uygulanmakta ve SLNB
sonucu negatif olanlarda ALND yapılmamaktadır. Ancak, SLNB sonucu pozitif olan hastalarda bugün de ALND uygulanmaktadır (16).
İnvaziv meme kanserli hastalarda en güçlü ve güvenilir prognostik faktörlerin başında, histolojik olarak aksillada tutulum gösteren lenf nodülü sayısı (pN) gelmektedir.17 Aksiller disseksiyon, meme kanserinin tedavisinde prognozu belirlemek ve evreleme amacıyla yapılmaktadır. Mamografinin tarama amacıyla kullanılmasıyla birlikte meme kanserinin daha erken evrede tanınması ve daha konservatif metodlarla tedavi edilmeye başlanmasıyla, ALND’nin amaçları ve tekniğin kapsamı yeniden gözden geçirilmeye başlanmıştır. Rutin ALND’nin yapılması daha az radikal cerrahi istenmesi açısından giderek artan oranda sorgulanmaktadır (19). Nitekim aksiller disseksiyon; kol ödemi, seroma toplanması, aksilladan geçen damar ve sinirlerin zedelenmesi, kol hareketlerinde kısıtlılık, ağrı ve uyuşukluk gibi bir takım istenmeyen sonuçları beraberinde getirebilmektedir.( 20). Minimal girişimsel ve tanısal yöntemler operasyon öncesi aksiller evrelendirmeyi sağlayacaksa, metastatik lenf nodülü bulunmayan hastalarda aksiller disseksiyon yapılmayabilir. Bu doğrultuda yapılan çalışmalar sonucunda sentinel lenf nodülü biyopsisi tekniği geliştirilmiştir. SLNB, etkili bir şekilde primer tümörün drene olduğu ve metastatik olabilen ilk bölgesel lenf nodülünü gösterebilmeyi hedeflemektedir. Bu lenf nodüllerinde metastaz saptanmayan olgularda aksiller yayılımın olmadığı ve morbiditeyi arttıran ALND’nin bu hastalarda gereksiz olduğu kabul edilmektedir (21,22,23)
ALND sonucu görülebilen komplikasyonları olabildiğince azaltmak ve aksillası patolojik olarak negatif olan hastalarda ALND’den kaçınmak için ‘sentinel lenf nodülü biyopsisi’ çalışmaları 1990’lı yılların başında başlamıştır. 1993’te Krag ve arkadaşları, radyokolloid madde kullanarak lenfosintigrafi ve gama prob yardımı ile sentinel lenf nodülü biyopsisini yapmışlardır (24,25). Mavi boya (busulphan blue) kullanılarak yapılan SLNB ile ilgili ilk çalışma, 1994 yılında Armando Giuliano ve arkadaşları tarafından yayımlanmıştır (Giuliano 1994). Bundan sonra yapılan birçok çalışmada SLNB’nin, klinik olarak aksillası negatif olan hastaların yaklaşık %60’ında ALND’nin gerekliliğini ortadan kaldırabileceği gösterilmiştir (26,27). SLN’nin belirlenmesinde iki yöntem mevcuttur; mavi boya ve radyokolloid madde. İki yöntem ayrı ayrı veya birlikte de kullanılabilir.
SLNB günümüzde çoğu merkezde başarı ile uygulanmakta ve bu konuda birçok çalışma yürütülmektedir. Yayımlanan ve uzun dönem sonuçlarını içerençalışmalar, artık SLNB’nin meme kanseri tedavisinde standart bir tedavi olduğunu göstermektedir (27)
Bu çalışmada meme kanseri tanısı ile başvuran ve sentinel lenf nodu pozitif olan hastalarda nonsentinel lenf nodu pozitifliğine etki eden faktörlerin neler olduğu belirlenmesi amaçlanmıştır.
2.GENEL BİLGİLER 2.1- Memenin Anatomisi
Erişkin bir kadında meme glandı, ön göğüs duvarının yüzeysel pektoral fasyasının yüzeysel ve derin tabakaları arasında bulunur (28). Memeler 2. ile 7.kaburgalar arasında yer alırlar. İçte sternumun kenarından dışta ön ve orta aksiller çizgiye kadar uzanırlar. İnsanlarda embriyonel hayatın 6. haftasında aksilladan inguinal bölgeye doğru bir çizgi şeklinde uzanan ektodermal bir kalınlaşma olur (28,29). Süt çizgisi olarak isimlendirilen bu oluşumun alt 2/3’ü atrofiye olarak kaybolurken üst 1/3’lik parçasının orta kısmı daha belirgin bir şekil alarak memenin ilk taslağını oluşturur. Bu oluşum bir taraftan gelişmesine devam ederken diğer taraftan epitelyal tomurcuklar gelişir. Gebeliğin son üç ayında plasentaya ait seks hormonları fetal dolaşıma girerek bu epitelyal dokuların kanalize olmasını sağlar. Parankimin farklılaşması gebeliğin 32. ile 40. haftasında lobüler ve alveoler yapıların gelişmesiyle oluşur. Meme glandı kitlesinde bir artış olurken, meme başı-areola kompleksi gelişir ve pigmente olur. Erken çocukluk döneminde uç veziküller tekrar kanalize olur, büyüme ve dallanmalar ile birlikte duktal yapılar gelişir. Bundan sonra puberteye kadar gelişim yönünden pek az değişiklik olur. Puberte ile birlikte meme bezlerine ait elemanların, bağ ve yağ doku oranının artmasıyla kadın memesi gelişmeye başlar. Memenin duktal sisteminin dallanmasında belirgin bir artış olurken, puberteye kadar belli belirsiz ayırd edilebilen meme ucu ve areolada daha da belirginleşir (30).
Doğumda erkek ve kızlarda memeler benzerdir; sadece majör kanalların varlığı gösterilebilir. Kızlarda pubertede over kaynaklı östrojen ve progesterona yanıt olarak epitelyal ve bağ doku proliferasyonu olur. Memenin gelişimini tamamlaması gebelik ile olur (31).
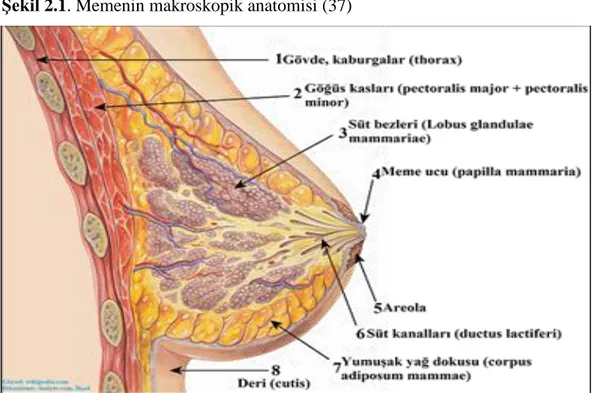
Meme, asini ve duktusları oluşturan epitelyal parankim ile onları destekleyen kas ve fasya elemanları, yağ, kan damarları, sinirler ve lenfatikleri içerir. Her biri ayrı bir salgı kanalı ile meme başına açılan 15-20 lob epitelyal parankimi oluşturur (32,33,34,35) Her lobda 20-40 lobül bulunur. Her bir lobülde, toplayıcı bir duktus çevresinde gruplaşmış, 10 ile 300 adet asini bulunur (36,37)
Meme başı ve areolanın epidermisi keratinize olmuş çok katlı yassı epitel ile örtülüdür. Puberte döneminde, meme başı ve areolanın pigmentasyonu artarak, meme başı
daha belirgin hale gelir. Bu artışın en fazla olduğu dönem gebeliktir. Areola ve meme başının derininde bulunan düz kas lifleri, dairesel ve ışınsal bir şekilde meme başına doğru uzanan laktifer duktuslar boyunca sıralanmışlardır (37). Bu düz kas lifleri, çeşitli uyarılara cevap olarak meme başının erekte olmasını sağlar. Areolada ter bezleri, sebase glandlar ve Montgomery glandları (Aksesuar areolar glandlar) bulunur. Meme başının uç kısmında fazla miktarda serbest duysal sinir ucu ve dermal papillada Meissner cisimcikleri mevcuttur (35,36).
Şekil 2.1. Memenin makroskopik anatomisi (37)
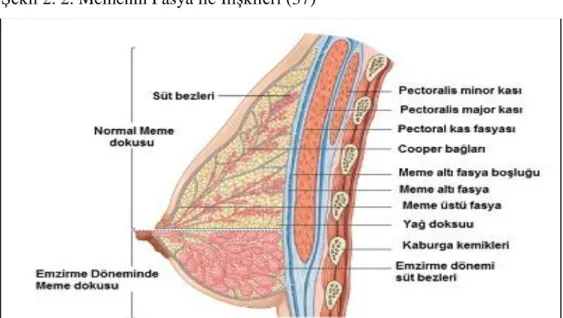
Meme glandı, aksillaya doğru uzanan bölümü hariç, yüzeyel fasyanın yüzeyel ve derin tabakaları arasında bulunur (bkz şekil 2.2). Mastektomi esnasında deri flepleri kaldırılırken, disseksiyonun yüzeyel fasyanın yüzeyel tabakasının hemen üzerinden yapılması uygun olur (36)
Meme dokusundan çevreye doğru uzanan fibröz çıkıntılara Cooper ligamanları denilmektedir. (38). Bu durum özellikle meme kanserinin önemli bulgularından biridir ve ‘meme cildi retraksiyonu’ olarak adlandırılır.
Memenin posteriyor yüzünde, yüzeyel fasyanın derin tabakası ile pektoralis majör kası ve göğüs duvarını örten derin fasya arasında, iyi sınırlı bir aralık bulunur (bkz şekil 2.2). Bu aralıkta bulunan gevşek gözeli doku, memenin göğüs duvarı üzerinde bir noktaya kadar hareketini sağlar. Yüzeyel fasyanın derin tabakasının uzantıları, memenin arkasındaki bu aralığı geçerek pektoral fasyayla birleşirler. Bunlar memenin arka asıcı bağlarını (suspensör ligamanlar) oluştururlar. (38).
Şekil 2. 2. Memenin Fasya ile İlişkileri (37)
Yüzeyel fasyanın derin tabakası, pektoral ve aksiller bölgede septumlar oluşturarak her iki pektoral kası sarar ve birbirinden ayırır. Aksiller boşluğu da bir köprü gibi katederek yukarıda deltoid kası ve klaviküladan, aşağıda göğüs duvarı kaslarına kadar uzanır. Aksiller fasyanın yüzeyel ve derin olmak üzere iki tabakası vardır (39). Yüzeyel olanı, pektoralis major kasını saran pektoral faysa, derin olanı da pektoralis minör kasını saran kostakorakoid fasya’dır (Şekil 2.3). Aksilladan geçen sinirleri, damarları ve lenfatikleri koruduğu gibi, aksillada bulunan yağ dokusu ile lenf nodüllerini bir arada tuttuğu için aksiller disseksiyon yapan cerrahlar için çok önemlidir(39).
Şekil 2.3. Aksiller Fasya
2.2- Memenin Kanlanması 2.2.1. Memenin Arterleri
1. İnternal mamarian arterin iki, üçve dördüncüanterior perforan dalları göğüs duvarını sternumun kenarından delerek memenin medialini ve orta kısımlarını besler. Bunlar memenin en büyük damarlarıdır. Laktasyon sırasında büyük oranda genişlerler.
2. Torasik aortadan çıkan iki, üç, dört ve beşinci posterior interkostal arterlerin perforan dalları göğüs kafesi yanında kasları deldikten sonra ikiye ayrılırlar. Ön dallar meme derisini ve parankiminin lateralini beslerken, arka dallar da kaslara gider.
3. Aksiller arterin dalları daha çok üst dış kadranı ve memenin kuyruğunu besler. Başlıca dört adet dal vardır. Lateral torasik arter, süperior torasik arter, torakoakromial arterin pektoral dalı, subskapular arter. (38)
Memenin yaklaşık %60’ını internal mamarian arterin perforan dalları, %30’unu da lateral torasik arter besler. Ancak tüm arterler arasında yaygın anastomozlar vardır. Latissimus dorsi kasının kanlanmasını sağlayan ve serratus magnus kasına birçok dal veren torakodorsal arter, lateral göğüs duvarından aşağıya doğru uzanım gösterir. Bu arteriyel dalların ve onlara eşlik eden venlerin önemi, radikal mastektomi sırasında olabilecek bir kanamanın kontrolünün zorluğudur. Bu zorluk nedeniyle bu alana ‘kanlı köşe’ adı verilmiştir. Torakodorsal arterinönemiyse, metastazların sık görüldüğü santral ve skapuler
lenf nodülleri grupları ile torakodorsal damarlar arasında çok yakın bir ilişki içerisinde olmasından dolayıdır. (30).
2.2.2. Memenin Venleri
Memenin venleri arterlerin dağılımına uymakta ve onlara eşlik etmektedir. Meme üzerindeki yüzeyel subkutanöz venler, süperfisyel fasyanın süperfisyel tabakasının hemen altındadır. Bunlar özellikle gebelik esnasında gözle görülebilecek şekilde genişlerler. Meme üzerindeki yüzeyel venler sıklıkla hastalık içeren bir meme sahasının üzerinde genişler ve belirgin hale gelirler.
Memenin ve göğüs duvarının kanını taşıyan üç derin ven grubu vardır:
1. İnternal meme veninin perforan dalları, memeden kan taşıyan en büyük venlerdir. İnternal meme venleri aynı taraftaki innominate venlere dökülürler.
2. Aksiller ven; göğüs duvarından, pektoral kaslardan ve memenin derin yüzeylerinden gelen birçok dalı alır. Bunlar genellikle aksiller arterin dallarına yandaşlık yaparlar. Bu venöz yol da akciğerlere karsinom embolilerinin ulaşması açısından önemlidir.
3. İnterkostal venler, memeden venöz drenajı sağlayan en önemli yollardan biridir. Bu venler ile vertebral venler ve döküldüğü azigos venler arasında ilişki vardır. Karsinom embolilerinin akciğere ulaşmasına neden olan üçüncü yolu oluşturur (39).
Bu venöz sistemde valv mevcut değildir ve içindeki basınç çok düşüktür. Retrograd kan akımı kolayca oluşur. Bu nedenle memeden gelen metastaz elemanları retrograd olarak doğrudan doğruya vertabralara geçebilir. (35)
2.3- Memenin Sinirleri
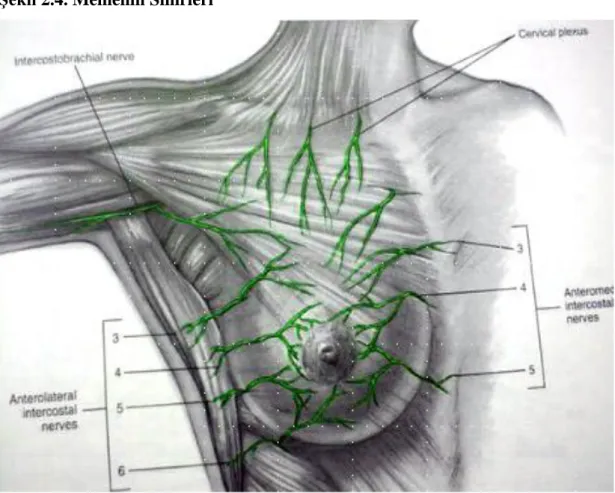
Memenin duysal innervasyonundan başlıca 2.-6. interkostal sinirlerin lateral ve anterior deri dalları sorumludur (36)
Memenin duysal inervasyonu başlıca 2.,3.,4.,5.ve 6. interkostal sinirler ile sağlanır (27). Aksiller diseksiyon sırasında, skapuler lenf nodlarından geçerek yol aldığı için korunması pek mümkün olmayan interkostobrakial sinirin (2. İnterkostal sinirin duysal dalı) kesilmesinin pek fazla sakıncası yoktur. Torakodorsal sinirin kesilmesi durumunda kolun adduksiyon ve iç rotasyonu yapılamaz. Özellikle dikkat edilecek sinir ise serratus anterior kasını inerve eden nervus torasikus longustur (Bell siniri). Aksiller disseksiyon esnasında bu sinir korunmalıdır. Kesilmesi serratus anteriorun felcine ve ‘skapula alata’ durumunun ortaya çıkmasına neden olur (27).
Şekil 2.4. Memenin Sinirleri
2.4- Lenfatik Sistem
2.4.1. Memenin Lenfatik Sistemi
Merkezi sinir sistemi, kıkırdak, timus, diş, tırnak, kıl, epidermis, plasenta, kemik ve kemik iliği dışında vücudun diğer doku ve organlarında bulunan lenfatik sistem, kan kapillerlerine paralel olarak görülen lenf kanalları ve lenf nodlarından oluşmaktadır. Lenfatik sistem venüller tarafından reabsorbe edilemeyen protein, eritrositler ve mikroorganizmaların dokulardan drenajı ile görevlidir. (40)
Genellikle kan kapillerlerine veya küçük venüllere yakın olarak yerleşen başlangıç lenfatiklerinin çapları, 10-50 µm arasında değişmektedir. İnterstisyel alanda kör uçlu lenfatikler halinde başlayan başlangıç lenfatikleri, dış duvarında bulunan flamentlerle doku aralığına bağlanarak, lümenin sürekli açık kalmasını sağlamaktadır. Bu flamentlerin kasılması sonucunda porlar açılmakta, doku aralığı sıvısı lümene geçmektedir. Bu lenfatiklerin iç duvarını, tek sıra, yassı endotel hücreler oluşturmaktadır. Dış katmanında ise devamlılığı olmayan bazal membran bulunmaktadır. Endotel hücrelerinin çapı, perinükleer alanda 2-4 µm, uçlarda ise 0,1 µm kadardır. Endotel hücreleri arasında bulunan 10-25 nm genişliğindeki porlar, doku aralığı sıvı basıncının artmasıyla açılarak, plazma proteinlerinin ve partiküllerin lümene geçmesine izin vermektedir. Endotel hücreleri oblik olarak üst üste gelerek bir kapak
görevi görmektedir. Bu kapaklar, lenf sıvısının lümene geçişine izin verirken, intraluminal basınç artışında kapanarak, lenf sıvısının lümen dışınaçıkmasını engellemektedir. Ayrıca endotel hücreleri, pinositoz yoluyla 30 nm den daha büyük partiküllerin, lümene geçmesinde rol oynamaktadır (41,42).
Lenfatik sistemde sıvı, ortalama 120 ml/saat hızında hareket eder. İnsan vücudunda 24 saatlik lenf akımı, 2-4 litre arasındadır. Akım hızı, iskelet kaslarının hareketlerine, inspirasyon sırasında oluşan negatif intratorasik basınca, lenfatik akımın sonlandığı venlerdeki akım hızına ve büyük lenfatiklerin duvar kasılmasına bağlıdır (39).
Bir tarafı hafif basık, küçük fasülye şeklindeki lenf nodları, lenfatik sistem boyunca belirli aralıklarla yerleşmiştir. Bu yerleşim alanları, ‘bölgese lenf nodu’ olarak adlandırılmaktadır. Bölgesel lenf gruplarındaki lenf nodları birbirleriyle bağlantılıdır. Vücutta ortalama 800 civarında bulunan lenf nodlarının boyutu, birkaç milimetreden 1 santimetreye kadar değişebilmektedir. Lenf nodunun dış kesimi korteks, iç kesimi ise medulla olarak adlandırılır. Korteks, hilusta izlenmemektedir. Lenf nodu, en dışta fibröz bir kapsül ile çevrilidir. Kapsülün hemen altında bulunan sinüsler, germinal merkezleri çevrelemektedir. Germinal merkezlerde çok sayıda fagositer hücre bulunmaktadır. Germinal merkezler “teknesyum 99m” ile işaretlenmiş sülfür kolloid gibi protein kolloidleri tutar, ancak vital boyalar burada tutulmazlar. (43,44)
Lenf sıvısı için bir filtre görevi gören lenf nodları, tümör hücreleri de dahil her türlü yabancı partikülü ve bakteriyi tutarak, immün sistemin önemli bir parçasını oluşturmaktadır. Ancak bazen lenf sıvısı, lenf nodu içinden veya üzerinden geçerek, doğrudan hilusa ulaşabilir. Bu durum, ilk lenf nodu yerine bir sonraki lenf nodunda konaklayabilen skip metastazı açıklayabilir.
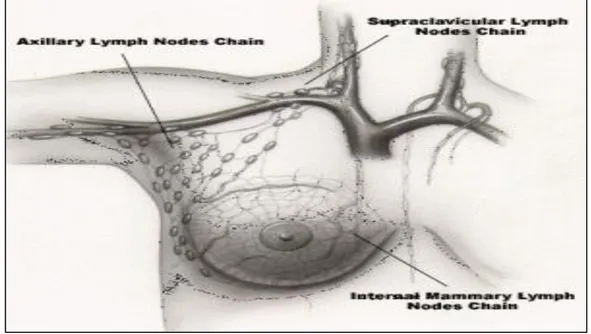
Şekil 2.5. . Memenin Lenfatik Sistemi
2.4.2. Aksiller Lenf Nodülleri
Aksiller lenf nodu sistemi, çoğu mikroskopik 30-50 adet lenf nodundan oluşmaktadır (45). Bu nodüller anatomik olarak beş alt grupta toplanmıştır:
1. Lateral (Brakial) Nod Grubu: Aksiller venin posteromedialinde bulunan bu grup, birkaç lenf nodundan oluşmaktadır. Üst ekstremiteden gelen lenf akımının, apikal lenf nodlarına dökülmesinde rol oynar.
2. Anterior (Pektoral) Nod Grubu: Pektoralis majör kasının inferior sınırında bulunan bu lenf grubu, memenin sentrilateral kısmının lenfini toplar.
3. Posterior (Subskapular) Nod Grubu: Aksillanın posterior duvarında bulunan bu grup, boynun inferoposterior bölgesinin lenfini toplar.
4. Santral Nod Grubu: Bu lenf grubu, aksiller yağ yatağında 3 ya da 4 adet büyük lenf nodu şeklinde bulunur. Bir önceki lenf gruplarından lenfi alarak, efferent lenfatikleri yoluyla apikal nodlara dökülür.Çok defa diğer gurupların lenfi santral nodüllere drene olduğu için metastazlar da en sık bu nodüllerde oluşur.
5. Apikal (Terminal) Nod Grubu:Aksillanın apeksinde bulunan bu lenf grubu, pektoralis majör kasının posterioru ve kısmen de kasın süperiorunda yerleşmiştir.
Şekil 2.6. Aksiller lenf nodülleri
Yukarıda bahsedilen lenf gruplarından gelen lenfatik akımı toplar.
Meme kanseri, aksiller lenf grupları arasında çoğunlukla belirli bir sıra takip etmektedir. Bu nedenle, aksiller lenf nodları, cerrahi uygulamalara kolaylık sağlamak amacıyla, pektoralis minör kasının neresinde bulunduğuna göre sınıflandırılmaktadır:
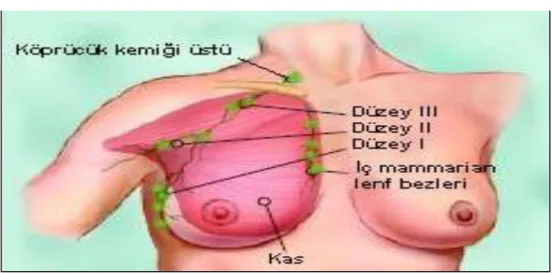
1. Düzey I lenf nodları: Pektoralis minör kasının lateral kenarında bulunan lenf nodları (brakiyal, pektoral, subskapular).
2. Düzey II lenf nodları: Pektoralis minör kasının arkasında bulunan lenf nodları (santral, apikal).
3. Düzey III lenf nodları:Pektoralis minör kasının medial kenarında bulunan lenf nodları (medialdeki apikal) (16).
Şekil 2.7.Lenf bezlerinin yerleşimi ve düzeyleri
2.4.3. Mammarya İnterna Lenf Yolu
Mammaria interna lenf yolu diyafragmanın üst yüzünün ön kısmında bulunan ön preperikardial lenf nodüllerinden kaynağını alır (30). Preperikardial lenf nodüllerine toplayıcı lenfatikler yoluyla aşağıdaki yerlerden lenf gelir: - Ligamentum falsiform yoluyla karaciğerin ön ve üst kısmından - Diyafragmanın ön kısmından - Rektus abdominus kasının üst kısmından - Rektus kılıfından - Meme glandının alt-iç kadranından Preperikardial lenf nodüllerinden çıkan mammaria interna lenfatik trunkusları sternumun her iki yanında mammaria interna damarlarının yakınında seyrederek yukarı doğru gider. İlk altı kıkırdak kaburganın arkasında bulunurlar. Mammaria interna lenfatik zinciri, göğüs duvarının bir parçasının, pariyetal plevranın ön kısmının, göğüs duvarının bu bölgesine rastlayan kasların ve üzerindeki meme dokusunun bir kısmının lenf drenajını sağlarlar. Mammaria interna lenfatik zinciri üzerindeki lenf nodülleri genellikle çok küçük olup nadiren 5-6 mm büyüklüğünde olabilirler (8).
2.4.4. Diğer Lenf Yolları
2.4.4.1. Supraklaviküler Lenf Nodüllerine Giden Lenf Yolu
Supraklaviküler lenf nodullerinde metastaz 3 şekilde ortaya çıkar: - Vena jugularis interna ile vena subklavianın birleşim yerinde, lenfatik sonlanma civarında bulunan sentinel nodüller karsinom ile tutulduğu ve lenfatik akım bu nodüller tarafından bir dereceye kadar bloke olduğu zaman, hastalık sentinel nodüllerle bağlantılı lenfatikler boyunca retrograd yönde supraklaviküler bölgedeki servikal grubun diğer lenf nodüllerine yayılır (9)
- Bazı olgularda aksiller nodüllerden doğrudan doğruya supraklaviküler nodüllere ulaşan direkt bir lenfatik yolun varlığı tespit edilmiştir. Barties ve Rouviere subklaviküler lenf nodüllerinden transvers servikal zincir nodüllerine giden efferent lenfatikler tespit etmişlerdir. (48,49). Bobbio ve arkadaşları yaptıkları lenfanjiografik tetkiklerde olgularının yarısında
kontrast maddenin aksiller ven nodüllerinden transvers servikal zincirin supraklaviküler nodüllerine ulaştığını göstermişlerdir.(46).
- Bazen de tümör hücrelerinin aksiller lenf nodülü filtresini atlayarak doğrudan doğruya supraklaviküler lenf nodüllerine gittiği bilinmektedir (47)
2.4.4.2. Rektus Abdominus Kası Yoluyla Memeden Karaciğere Giden Lenf Yolu
Mammaria interna lenf yolu falsiform ligamanın üzerinde, diyafragmanın üst yüzünde bulunan preperikardial lenf nodüllerinden başlar. Bu lenf nodüllerine memelerin alt iç kadranlarından, falsiform ligamandan, karaciğerin ön ve üst kısmından, diafragmanın ön kısmından, rektus abdominus kasının üst kısmından ve rektus kılıfından lenf gelir. Bu nodüllerden çıkan lenfatik trunkuslar yukarı doğru seyreder. Memelerin alt iç kadranlarından çıkan ve süperior epigastrik kan damarlarına eşlik eden lenfatikler rektus fasyasını delerek rektus abdominis kasına girerler ve daha sonra ön preperikardial lenf nodüllerine boşalırlar. Rektus abdominus kasının lenfatikleri, metastazların meme kanserinden karaciğere ulaşmasını sağlayan bir yol oluşturur. Mammaria interna lenf yolunda ilk üç interkostal aralık düzeyinde metastazlara bağlı bir blokaj oluştuğu zaman, lenfatik akımın yönü tersine çevrilebilir ve kanser embolisi rektus kasındaki lenfatik yolla memeden karaciğere ulaşabilir (50).
2.5- Aksilla
Aksillanın şekli, yüzleri birbirine eşit olmayan bir piramide benzer (36). Bu piramidin ön, arka ve iç olmak üzere üç yüzü ve aksillayı kapatan cildin oluşturduğu bir de tabanı vardır. Piramidin tepesi nokta şeklinde kapalı bir yer değildir. Burada serviko-aksiller kanal olarak isimlendirilen bir açıklık bulunur. Boyun bölgesinden gelerek kola giden damar ve sinirler bu kanaldan geçerler. Aksillanın ön duvarı cerrahi anatomi bakımından önemlidir. Pektoralis major ve minör kasları ve bunların fasyaları bu duvarı oluşturur. Pektoralis major kası sternumun ön yüzünden başlar. Bu kasın arkasında 18 pektoralis minör kası bulunur ve kostakorakoid fasya ile çevrelenmiştir. Aksillanın tam bir disseksiyonu için daima kesilmesi gerekir. Aksiller boşluğun iç duvarı; kostalar, interkostal kaslar ve serratus anterior kasının 4. ve 5. parçaları tarafından oluşturulur. Aksillanın arka duvarı esas olarak subskapuler ve latissimus dorsi kasları tarafından oluşturulur. Latissimus dorsi kası mastektomide aksiller disseksiyonun sınırını göstermesi bakımından da önemli bir yapıdır. Aksillada, aksiller damar-sinir demeti (aksiller arter ve ven, brakial pleksus) ve bunlardan ayrılan yan dallar, korakobrakial kas, biseps braki kasının birleşik tendonları, interkostal aralıktan gelen damar ve sinirler, meme dokusunun aksiller uzantısı (Spence kuyruğu), interkostal aralıklardan gelen damar ve sinirler, lenf nodülleri, bütün bu yapıları saran gevşek gözeli ve yağlı bir doku bulunur.(27). Brakial pleksusa ait elemanların, birkaç küçük yan dalın dışında, meme ile pek fazla ilişkisi yoktur. Buna karşılık aksiller ven ise, cerrahi bakımdan çok önemlidir. Zira aksiller disseksiyon esnasında aksiller veni çevreleyen fibröz kılıfın ve bu kılıf içinde bulunan lenf nodüllerinin birlikte çıkarılması gerekir. Aksillada brakial pleksustan iki önemli yan dal ayrılır. Bunlar; serratus anterior kasına giden uzun torasik sinir (n.torasikus longus, Bell siniri) ve latissimus dorsi kasına giden torakodorsal sinirdir. Bell siniri göğüs duvarında, serratus anterior kasının liflerine bitişik olarak aşağı doğru iner. Bu sinir aksiller diseksiyon esnasında dikkatli bir şekilde korunmalıdır. Sinirin kesilmesi serratus anterior kasının felcine ve “scapula alata” durumunun ortaya çıkmasına neden olur. Torakodorsal sinir ise brakial pleksustan ayrıldıktan sonra aşağıya ve dışa doğru ilerleyerek latissimus dorsi kasına ulaşır. Sinirin çevresindeki lenf nodüllerinde karsinom infiltrasyonu mevcutsa bu sinirin korunması olanak dışıdır. Kesilmesinin de bir sakıncası yoktur. İnterkostal aralıklardan memeye gelen sinir ve damarlar 1., 2., 3. ve 4. interkostal damar ve sinirlerin lateral perforan dallarıdır. Birinci interkostal sinirin lateral cilt dalı yoktur. İkinci interkostal sinirin lateral cilt dalı oldukça büyüktür ve aksillanın gevşek gözeli ve yağlı dokusu içinden geçtikten sonra
interkostobrakial sinir adını alır ve kolun iç tarafının cildini innerve eder. Bu sinir de mastektomi sırasında kesilmektedir. (50).
2.6- Meme Kanseri 2.6.1- Epidemiyoloji
Meme kanseri kadınlarda en sık görülen kanser türüdür ve 40-44 yaşarası kadınlarda kanser ölümlerinin başlıca nedenidir. Kadınlarda görülen kanserlerin %30’unu meme kanseri oluşturur ve kansere bağlı ölümlerin %19’undan sorumludur (9). Çok nadir olmakla beraber erkeklerde de görülebilir. Meme kanserinin erkek kadın görülme oranı1/100-125’dir (10).
Meme kanseri dünya çapında bir epidemiyolojik problemdir.Meme kanseri insidansı 1987-2001 tarihleri arasında yıllık 0.4 oranında ve 1975-1990 tarihleri arasındada yıllık 0.4 oranında artan bir seyirde gitmiştir. Mortalite oranları en fazla 27,7/100.000 ile İngiltere ve Galler’den verilmektedir. ABD’de 22,0/100.000 ve en düşük mortalite oranları 2,6/100.000 ile Güney Kore’den bildirilmektedir. Endüstriyel ülkelerde yaşayan kadınlarda gelişmemiş ülkelerde yaşayan kadınlara oranla meme kanseri daha fazla görülmektedir (3).
Epidemiyolojik bir problem haline gelen meme kanserinin mortalitesi, pekiyi bilinmeyen çeşitli nedenlerle sabit kalmıştır; mortalite 1971’den beri 50 yaşın altındakilerde %11 azalmış, 50 yaşın üzerindekilerde % 6 artmıştır (2, 32).
Sağlık Bakanlığı verilerine göre 1999 tarihinde Türkiye’de kadınlarda en çok görülen on kanser türü üzerindeki raporunda toplam 9.919 kanser hastasının insidansı yüzbinde 30.38 olarak bildirildi. Bunların da 2.390’ ı meme kanseri olup, tüm kanser türleri arasında %24,1’ini teşkil etmekte ve Türkiye’de meme kanseri kadınlarda en sık görülen kanser türü olarak bildirilmiştir. 1999 yılında meme kanseri gelişim insidansı yüzbinde 7.32 olarak tespit edilmiştir.Türkiye’de 1999 yılında 8.879 olan meme kanserli kadın sayısı, 2014 yılında 16.883’e yükselmiştir. Ayrıca ülkemizde tüm kanserlerin % 24,1’ini meme kanserlerinin oluşturduğu belirtilmektedir. Bu verilerden de anlaşıldığı gibi sağlık bilimlerindeki ilerlemelere erken tanı yöntemlerinin gelişmesine, toplumun bu konuda duyarlılığının artmasına karşın, meme kanseri yaşamı tehdit etmeye devam etmektedir. Bu tehditin azaltılmasında atılacak adımlardan birisinin de her toplumun kendi içinde meme kanseri risklerini ortaya koyması, risk gruplarını belirlemesi ve tarama programlarını yaygınlaştırmasıdır (9).
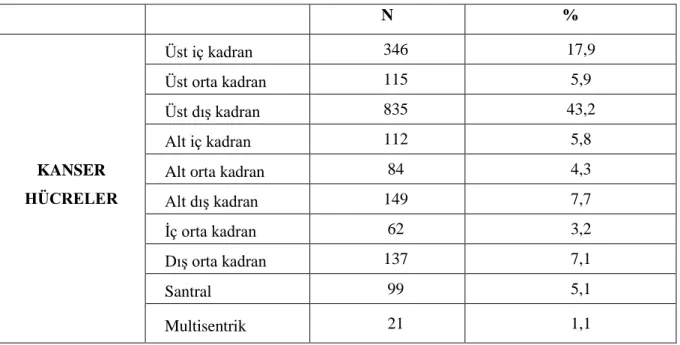
Kanserin meme dokusundaki yerleşimi kadranlara göre tanımlanmaktadır. 696 olguluk bir seride tümörlerin %48´inin üst dış kadranda , %15´inin üst iç kadranda, %11´inin alt dış
kadranda, %6´sının alt iç kadranda ve %17´sinin de santral bölgede ( areola ve çevresindeki 1 cm´lik alan ) yerleştiği bildirilmiştir. Tümörün sıklıkla üst dış kadranda bulunmasının nedeni bu kadrandaki meme dokusu hacminin büyüklüğüne bağlanmaktadır.
2.6.2- Etyoloji ve Patogenez
Meme kanseri biyolojik ve klinik açıdan heterojen özellikler göstermektedir. Meme kanserinde oluşan denetimsiz hücre çoğalması genellikle genomik instabilite belirtileri ve belirli epitelyal özelliklerin ortadan kalkması gibi değişiklikler göstermektedir. Bu nedenle kanser gelişimine sebep olan moleküler mekanizmaların ve her hastanın tümörünün özelliklerinin belirlenmesi ve buna en uygun tedavi rejiminin uygulanması çok önemlidir. Deney hayvanlarında ve in vitro meme tümörleri üzerinde yapılan çalışmalar, meme kanseri gelişiminde belli başlı üç etkinin önemli rol oynayabileceğini göstermiştir. Bunlar genetik değişiklikler, hormonal etkiler ve çevresel faktörlerdir.(51).
Genetik Etkenler: Asyalı kadınlarla batı ülkeleri kadınları arasında meme kanseri
görülme sıklığı ve mortalitesindeki belirgin farklar meme kanserli kişilerin ailelerinde iki üç kat artmış meme kanseri ortaya çıkışı, meme kanseri oluşumunda genetik etkilerin rol aldığını düşündürmektedir (52)
Meme kanserine ailesel yatkınlık, ilk olarak 1866’da Paul Broca tarafından kendi eşinin ailesinde dört nesil süresince 24 kadının 10’unda meme kanserinin ortaya çıkışı sonrası ileri sürülmüştür (53). Daha sonra Macklin, meme kanserli bir kişinin annesinde toplumdaki kadınlara göre meme kanseri gelişme olasılığının 2 kat fazla, kızkardeşinde ise 2.5 kat fazla olduğunu göstermiştir. (54). Anderson ve Badzioch yaptıkları araştırmalar sonunda meme kanserli bir kişinin annesinde meme kanserinin ortaya çıkması konusunda relatif risk 8.8 iken, kızkardeşinde 2,7, kızında ise 4,6 olarak bulunmuştur. (55). Menopoza girmiş meme kanserli bir kadının akrabalarında relatif risk artmazken, menopoz öncesi dönemde ortaya çıkmış ise 9 kat artmaktadır. Meme kanseri aile hikayesi olan kişilerde meme kanserinin ortaya çıkma yaşı daha erken olup, hastalık bilateral olmaya eğilimlidir ve hastalığın erken ortaya çıkışı özellikle annesinde meme kanseri olanlarda daha da belirgindir.
Genetik yatkınlığa sebep olduğu düşünülen genler BRCA1 (Breast 21 cancer susceptibility gene-meme kanserine yatkınlık geni) ve BRCA2’dir. Otozomal dominant bir gen olan BRCA1, 17. kromozomun uzun bacağı üzerinde yerleşmiş olup mutasyonların oluşması sonrası BRCA1 geninin ailevi meme kanseri ve over kanserinde etyolojik rol oynadığı kabul edilmektedir. (56). Meme kanserli olguların büyük bir kısmını oluşturan ve
herediter geçiş göstermeyen sporadik olgularda ise bu genin bir rolü yoktur.44 BRCA1 geninin mutasyona uğramış şeklini taşıyan bir kadında 70 yıllık yaşam süresi boyunca meme kanserine yakalanma riskinin % 85 olduğu hesaplanmıştır.( 57). BRCA2 ise 13. kromozom üzerinde bulunan ve ön değerlendirmelere göre ailevi olgularda hastalığın erken ortaya çıkışında ve bilateral hastalıkta rol oynayan bir gendir. (58) Bu geni taşıyan kadınlarda ise meme kanseri oluşma riski % 87 olarak hesaplanmıştır. BRCA2 geninin BRCA1’den farklı olarak artmış over kanseri sıklığı ile bir ilişkisi yoktur.
Endokrin Nedenler
1. Reprodüktik Etkenler: Erken menarşın meme kanseri gelişiminde bir risk faktörü
olduğu gösterilmiştir.(Pike 1981). Genel olarak menarşın her bir yıl gecikmesi ile meme kanseri riskinin % 20 azaldığı kabul edilmektedir. Meme kanseri riski yönünden mensturasyonun başlama yaşı yanında ilk düzenli menstruasyon yaşı da önemlidir.50 Menarşı takiben düzenli menstruasyonların bir yıl içinde başlaması, düzenli menstruasyonları 1 yıldan geç başlayanlara göre riski iki katına çıkarmaktadır. Menarşı erken (12 yaş veya öncesinde) başlayan ve kısa sürede düzenli menstrüel dönemlere geçen kişilerde kanser riskinin menarşı geç başlayan (13 yaş veya üzerinde) ve uzun süre düzensiz menstrüel dönemleri olan kişilere göre 4 kat fazla oldugu kabul edilmektedir. (59). Bu gözlemler düzenli ovulatuar dönemlerin kadınlarda meme kanseri riskini arttırdığını düşündürmektedir.
Meme kanseri riski ile menopoz yaşı arasında da bir ilişki mevcuttur. Menopoza 45 yaşından önce giren kadınlarda meme kanseri riski, 22 yaşından sonra menopoza giren kadınların yarısı kadardır. Yani aktif menstruasyon dönemi 40 yıl veya daha fazla süren kadınlarda risk aynı dönemi 30 yıl veya daha az olan kadınların iki katıdır.54 Bilateral ooferektomi veya pelvis bölgesi ışınlaması ile yapay menopoz oluşturulması da meme kanseri riskini azaltmaktadır.55 Fakat yapay menopozun 50 yaşından sonra oluşturulmasının meme kanseri oluşumunda risk azaltıcı etkileri olduğu gösterilememiştir. Mac Mahon ise hamileliğin ve ilk hamilelik yaşının meme kanseri riski ile ilişkili olduğuna dikkatleri çekmiş, evlenmemiş veya hiç doğum yapmamış kadınlarda kanser riskinin doğum yapmış kadınlara göre 1,4 kat daha fazla olduğunu belirtmiştir (60,61).
2. Hormonlar: Meme kanserinin overlerin aktivitesi ile yakından ilişkili olması
östrojenin hastalık patogenezinde önemli rolü olduğunu göstermektedir. Hayvanlardaki deneysel çalışmalarda dışarıdan verilen östrojenin ve özellikle östradiolün meme kanseri oluşumunu arttırdığı, overlerin çıkartılmasının veya dışarıdan antiöstrojenlerin verilmesinin ise kanser oluşumunu azalttığı bildirilmiştir. (62).Yapılan iki çalışmada, meme kanseri görülme sıklığının daha düşük olduğu Asyalı kadınlarda, sıklığın daha yüksek olduğu
Amerikalı kadınlara göre idrar östradiol ve plazma östradiol düzeylerinin daha düşük olduğu gösterilmiştir.
3. Çevresel Etkenler Beslenmenin ve özellikle yağdan zengin beslenmenin deney
hayvanlarında meme tümörleri oluşturduğu uzun zamandan beri bilinmekle birlikte insanlarda ilk defa Armstrong, ülkelerin yağdan zengin besin miktarları ile meme kanseri sıklığı ve mortalitesi arasındaki ilişkiyi göstermiştir. Doll ve Peto, ABD’deki meme kanserlerinin yaklaşık % 50’sinden yağdan zengin beslenmenin sorumlu olduğunu ileri sürmüşlerdir.. Bununla birlikte zeytinyağı alımının yüksek olması meme kanseri riskini düşürmektedir. Liften zengin gıdanın bilier sistemden barsağa dökülen östrojenlerin reabsorbsiyonunu inhibe ederek meme kanseri oluşumuna karşı koruyucu bir etkisinin olabileceği ileri sürülmüştür. Anti-oksidan özelliğe sahip olan A, E ve C vitamini üzerinde de çalışmalar yapılmıştır. Retinol’ün in vitro koşullarda insan meme kanserli hücrelerinin büyümesini önlediği gösterilmiş ve A vitamini ile meme kanseri riski ilişkisini araştıran olgu kontrol çalışmalarından ilkinde Graham, A vitamini alımının artması ile kanser riskinin azalacağını bildirmiştir. Daha sonra dokuz çalışmayı değerlendiren metaanalizde de A vitamininin meme kanseri oluşumu konusunda anlamlı bir koruyucu etkiye sahip olduğu gösterilmiştir. E vitamini ile yapılan prospektif çalışmalar da meme kanseri oluşumunda koruyucu bir etkiye sahip olduğu gösterilememiştir. C vitamini ile yapılan ilk olgu kontrol çalışmasında koruyucu bir etkinin ortaya konmamasına karşın aynı grup tarafından yapılan daha sonraki bir çalışmada C vitamininin meme kanseri oluşumuna karşı anlamlı bir koruyucu etkiye sahip olduğu gösterilmiştir.(63) C vitamininin koruyucu etkisi konusunda kesin konuşabilmek ancak yeni çalışmalar sonrası mümkün olacaktır. Meme kanseri riski ve beslenme faktörlerinin ilişkisi araştırıldığında en belirgin olarak ortaya konulmuş olan risk artırıcı faktör alkoldür. Oniki olgu-kontrol çalışmasının değerlendirildiği metaanalizde günde 12 gram alkol alan kadınlarda meme kanseri riski 1,4, günde 24 gr alkol alanlarda ise 1,7 olarak bulunmuştur. Kafeinin ise selim meme hastalıklarındaki etkisi göz önüne alınarak meme kanserinde bir risk faktörü olabileceği düşünülmüş ancak olgu kontrol çalışmalarında böyle bir etki gözlenmemiştir. Sigaranın östrojen metabolizmasını değiştirmesi ve menopoz yaşını erkene alması nedeniyle meme kanserine karşı koruyucu bir etkisi olabileceği düşünülmüş ancak yapılan geniş olgu-kontrol ve prospektif çalışmalar meme kanseri riski ile sigara içimi arasında hiçbir ilişki gösterilmemiştir. Fiziksel aktivitenin menarşı geciktireceği ve daha az süre östrojenin etkisine maruz kalacağı gözlenmiştir. Adolesan ve erişkin dönemde yapılan egzersizlerin meme kanseri riski üzerine etkisini araştıran yakın tarihli bir çalışmada egzersizin 40 yaşın altındaki kadınlarda meme kanseri riskini azalttığı ve haftada 4 saat veya
daha fazla egzersiz yapan kadınlarda kanser riskinin hiç egzersiz yapmayanlara göre % 60 daha az olduğu bildirilmiştir (63,64).
2.6.3- Risk Faktörleri 1-Aile Öyküsü
Ailede bir veya birden fazla birinci veya ikinci derece kan akrabalarında meme kanseri saptanmış olması ailevi meme kanseri serisi, kalıtsal meme/over kanseri sendromu olarak adlandırılmıştır. Ancak genel olarak bakıldığında, kız kadeş, anne veya kızında meme kanseri bulunan kadınların meme kanserine yakalanma riski 2,5–3 kat artmaktadır (8).
Son yıllarda, ailesel meme kanseri ile ilgili daha güvenilir genetik veriler oluşmaya başlamış ve konuyla ilişkili olduğu belirlenen bazı genler izole edilmiştir ilki BRCA1(Breast cancer susceptibility gene meme kanserine yatkınlık geni)’dir. 17. kromozomun uzun kolu (q) üzerine yerleşmiş olup, mutasyonların oluşması sonrası BRCA 1 geninin ailesel meme kanseri ve over kanserinde etyolojik rol oynadığı kabul edilmektedir. İkinci gen ise BRCA 2 genidir. Bu gen ise 13. kromozomun üzerinde bulunan ve ailesel olgularda hastalığın erken ortaya çıkışında ve her iki memede birden kanser gelişmesinde rol oynar. BRCA 1 ‘den farklı olarak artmış over kanseri sıklığı ile bir ilişkisi yoktur (65,66,67).
2-Kalıtsal Sendromlar
Herediter meme-over kanseri sendromu: Bu sendromlu tüm kişilerin mutant
BRCA1 genini taşıdığı kabul edilmiş ve 70 yıllık yaşam boyunca meme kanseri oluşma riski de %85 olarak hesaplanmıştır (66). Bölgeye spesifik herediter meme kanseri: BRCA2 geniyle yakın ilişkili olan bu sendromda hastalık premenopozal dönemde erken yaşta ortaya çıkmakta ve bilateral başlangıç göstermektedir. Bu kişilerde meme kanseri oluşma riski % 90 olarak hesaplanmıştır. (67).
Muir Sendromu: Multiple cilt tümörleri ve gastrointestinal sistemin multipl selim
ve habis tümörleri ile seyreden otozomal dominant geçişli nadir bir sendromdur. Bu sendromda kadınlarda özellikle menopoz sonrası dönemde olmak üzere meme kanseri oluşma riski oldukça yüksektir.
Heterezigot ataksi telenjektazi geni (ATM): Bu geni taşıyanlarda meme kanseri
riski beş kat artmıştır. 11q üzerindeki tek gen mutasyonun bu hastalığa sebep olduğu gösterilmiştir. (67).
Li-Fraumeni sendromu: sorumlu gen: P53 kromozamal lokalizasyon: 17p kanserle
ilişkisi: Premenopozal meme kanseri, çocukluk çağı sarkomu, beyin tümörleri, lösemi, adrenokortikal karsinoma
Cowdens sendromu: Sorumlu gen PTEN. kromozamal lokalizasyon; 10q 23
kanserle ilişkisi; meme kanseri, tiroid ve gastrointestinal maligniteler.
Peutz-Jeghers sendromu: sorumlu gen: STK11 kromozamal lokalizasyon; 19P
kanserle ilişkisi; meme, kolon, pankreas, mide, over maligniteleri.
3-Endokrin nedenler
MenarşYaşı: Menarş yaşının erken olması meme kanseri için bir risk faktörüdür
(65).
Menopoz Yaşı: 50 yaşından sonra menapoza girenlerde 2–4 kat artmış meme
kanseri riski gösterilmiştir (65).
İlk Hamilelik-İlk Doğum Yaşı: Hiç doğum yapmamış kadınlarda, kanser riskinin
doğum yapmış kadınlara göre 1,4 kat daha fazla olduğu gösterilmiştir. Artmış çocuk sayısıyla da riskin azalacağı gösterilmiştir (51).
Laktasyon: Postmenopozal kadınlardan, gebelik geçirmiş ve emzirmiş olanlarda
meme kanseri riski 4–7 kat azalmıştır.
Hormonlar:
Östrojenler: Östrojenler meme dokusundaki normal ve neoplastik hücrelerin
büyümesini uyarırlar. Ayrıca tümör hücreleri üzerine direkt etkileri ile mitojenik büyüme faktörlerinin salgılanmasına sebep olurlar.
Tamoksifen gibi antiöstrojenik ajanlar verildiğinde meme kanserinde erken etkili tedavi sağlaması, diğer memede meme kanseri insidansını azaltması ve primer meme kanseri oluşumunu azaltması östrojenin kanserojenik etkisini desteklemektedir (51).
Androjenler: Androjenlerin meme kanseri ile ilişkili bir risk olduğu gösterilmiştir.
Postmenopozal hastalarda androjen düzeyinin yüksek olması bu düşünceyi desteklemektedir.
OKS: Oral kontraseptifler (OKS) ve postmenopozal hormon replasman tedavisi gibi
ekzojen seks steroidlerinin meme kanseri riski ile ilişkisi olduğu çokça rapor edilmiştir. 10 yıl boyunca OKS kullanan genç bir kadında hiç OKS kullanmayan bir kadına göre meme kanseri oluşma riski %36 artmaktadır (21). OKS kullanan kadınlarda hiç OKS kullanmayanlara göre her OKS kullanım yılı için meme kanseri riski %3,8 artmaktadır. (68).
Hormon Replasman Tedavisi: Menapoz nedeni ile uzun süre östrojen tedavisi (10
yıldan fazla) gören kadınlarda, meme kanseri oranı artmaktadır. Fakat hormon tedavisi almayan kadınlarda da, kalp hastalıklarında ve osteoporoz gibi sorunlarda artış ortaya çıkmaktadır. Yapılan çalışmalarda beş yıl konjuge östrojen kullanımında meme kanseri rölatif riski 1,1 iken; 10 yıl kullanımda ise 1,4 olarak verilmiştir.
4-Çevresel Faktörler - Beslenme
Dünya üzerinde meme kanseri görülme sıklığının ülkeden ülkeye değişmesi ve göç eden insanlarda artan meme kanseri sıklığının sadece genetik nedenlerle açıklanamaması, dikkatlerin çevresel etkenler ve özellikle beslenme üzerine toplanmasına neden olmuştur (8).
- Vitaminler
A vitamininin içinde bulunduğu karotenoidler antioksidan özelliklere sahip olduklarında DNA hasarına yol açan reaktif oksijen radikallerine karşı hücresel savunmayı artırabilirler. (69,70).
- Alkol Alımı:
Çeşitli epidemiyolojik çalışmalarda alkol alımının kadınlarda meme kanseri gelişme riskini artırdığı bildirilmiştir. Bu risk artışı içilen alkollü içeceklerin türüne bağlı olmayıp, içilen miktara bağlıdır. Erken yaşta alkole başlamak önemli bir risk faktörü olabilir. Premenopozal kadınlarda alkol alımı total östrojen düzeylerinin ve östrojen biyoyararlanımının artışına yol açar. Son zamanlarda yapılan epidemiyolojik çalışmalar, alkol alımına bağlı meme kanseri gelişme riski artışının folat alımı ile azaltılabileceğini göstermiştir (71).
- Radyasyona Maruz Kalma
İyonize radyasyon maruziyeti meme kanseri için bilinen bir risk faktörüdür. Atom bombasına maruz kalanlarda ve doğum sonrası mastit, akne, hirsutizm gibi nedenlerle ışın tedavisi alanlarda düşük veya orta derece radyasyon dozlarından sonra meme kanseri gelişme riskinde artış gözlenmiştir (71).
- Fiziksel Etkenler
Yüksek düzeylerde fiziksel aktivitesi olan kadınlarda meme kanseri riskinin daha az olduğuna dair deliller mevcuttur. Adelosan ve erişkin dönemde yapılan egzersizlerin meme kanseri riski üzerine etkisi araştırılmış ve 40 yaşın altındaki kadınlarda meme kanseri riskini azalttığı gösterilmiştir (72,73 ).
2.6.4- Klinik Özellikler
Meme kanseri kadınlarda görülen kanserler arasında ilk sıraya otururken kanser sonucu ölümlerin de ikinci nedenidir. Meme kanseri genelde uzun ve sinsi bir seyire sahiptir. Meme kanserli kadınların % 70 kadarında ilk bulgu memede bir kitlenin varlığıdır. Kanser nedeni ile oluşan kitlelerin büyük çoğunluğu (% 45’i) üst-dış kadrandadır. Meme dokusunun koltuk altı uzantısında da (aksiller kuyruk) kansere rastlanır. Klinik ve laboratuar kontrollerde bu bölgede değerlendirilmelidir. Kitle, çoğu zaman ağrısızdır ve hasta tarafından rastlantı
sonucu bulunur. Kitle genelde serttir ve hareketsizdir. Ancak etrafındaki meme dokusu ile birlikte hareket eder. Bazen de tümör memede asimetri yaratabilir. Meme içerisinde büyüyen tümör, Cooper bağlarını infiltre ettiğinde retraksiyona yol açar. Meme asinüslerini saran lenf damarlarına giren tümör 27 hücreleri artarak lenf damarlarında daralmaya ve dolayısı ile lenfatik akımın yavaşlamasına yol açar. Deri kalınlaşır, kıl folikülleri içeri doğru çekilmiş gibi kalır ve bu durum deriye portakal kabuğu (peau d’orange) görünümü kazandırır. Peau d’orange ileri evre meme kanseri belirtisidir.
Memenin santral kadranında yer alan bir tümör meme başını içeri doğru çekerek meme başı retraksiyonuna yol açar. Bazı hanımlarda meme başı retraksiyonu yapısal olabilir. Çok az da olsa patolojik bir neden içermeyen tek taraflı meme başı retraksiyonu da vardır. Tek taraflı ve sonradan oluşan meme başı retraksiyonlarının ardında kanserle aynı sıklıkta kronik enfeksiyonlar veya enflamasyonlar bulunur ve bunların ayrımı için titiz araştırma gerekir. Meme kanserli kadınların ortalama % 10 kadarında ilk belirti meme başından olan akıntıdır (74). Kanserin neden olduğu meme başı akıntısı çoğunlukla tek taraflı ve kendiliğinden olan akıntıdır. Akıntının önemli bir özelliği de seröz, seröz-kanlı ya da kan oluşudur. Bu niteliği taşıyan akıntıların %8-10’unu kanserler, geriye kalanını da intra duktal papilloma ve duktal ektazi oluşturmaktadır. Hastaların % 2’sinde kanser kendini önce meme başı daha sonraları areolayı da içine alabilen ekzamatöz bir lezyon ve ileri dönemde ülserasyon ile ortaya koyar. Bu şekilde iyileşmeyen durumda Paget hastalığı düşünmeli ve biopsi yapılmalıdır. Hastaların % 2-4’ünde kanser enflamasyon bulguları ile ortaya çıkar. Meme derisi kızarır ve kalınlaşarak portakal kabuğu görünümü alır. Lokal ısı, hassasiyet ve ağrı vardır. Bu bulgular enflamatuar kanser tanısını düşündürmektedir. Kesin tanı biyopsi ile konulmaktadır.
2.6.5- Meme Kanserinde Tanı Yöntemleri
Kansere bağlı ölümler arasında en sık ikinci neden ve giderek artan sıklıkta meme kanserine yakalanma insidansı olması nedeniyle, memenin görüntülemesi her zaman radyolojinin en önemli dallarından biri olmuştur. Özellikle 1960 yılından bu yana mammografinin bir tarama yöntemi olarak kullanılmaya başlanması ve bunun tüm merkezler tarafından benimsenmiş olması bu önemi daha da arttırmıştır. Ultrasonografi teknolojisinde ise yüksek frekanslı yüzeysel doku transdüserlerinin geliştirilmesi, ultrasonografiyi mammografiye yardımcı önemli bir yöntem yapmıştır. Tarama mammografisi sayesinde nonpalpabl meme lezyonları ile daha çok karşılaşılmaya başlanmış ve bunun sonucu olarak gelişen girişimsel yöntemler meme görüntülemesine ayrı bir boyut kazandırmıştır. Son on yılda manyetik rezonans (MR), meme görüntülemesinde hızla gelişerek önemli bir yer
tutmaktadır. Artık MR’ın meme görüntülemesinde belirli endikasyonları olup rutin olarak kullanılmaktadır. Pozitron Emisyon Tomografisi meme kanserinin tanı, evreleme ve tedavi sonrası takibinde önemli rol oynayabilecek yeni yöntemlerden biridir. Meme kanserlerinde günümüzde kullanılan tanı yöntemleri ana başlıklar halinde şunlardır:
Non invaziv yöntemler:
1. Klinik muayene 2. Mammografi
3. Meme ultrasonografisi ve doppler ultrasonografi 4. Digital mammografi
5. Manyetik rezonans görüntüleme 6. Bilgisayarlı tomografi
7. Mamosintigrafi (Talyum–201, TC-99m tetrafosmin, Tc-99m sestamibi) 8. Pozitron emisyon tomografi
İnvaziv Yöntemler:
1. İnce iğne aspirasyon biyopsisi (FNAB) 2. Kesici iğne biyopsisi
3. İnsizyonel biyopsi 4. Eksizyonel biyopsi
5. Sterotaktik biyopsi (ultrasonografi veya mamografi eşliğinde)
2.6.6. Meme Tümörlerinin Histopatolojik Sınıflaması
Meme kanseri olgularında tümörün patolog tarafından değerlendirilen çeşitli özellikleri prognoz ve tedaviyi belirlemede büyük önem taşır. Tarama mammografileriyle ele gelmeyen meme karsinomu saptama sıklığındaki artışlar, koruyucu cerrahi yaklaşımlar, immünhistokimya ve moleküler tekniklerle ilgili prognostik faktörlerin ortaya çıkışı, patoloğa düşen görevi arttırmaktadır. Bu nedenle patoloji raporlarında tümörün patolojik özelliklerini yansıtan maksimum bilginin verilmesi meme kanserli hastalara yaklaşımdaki temel unsurlardan birisidir.(75) Prognoz ve tedaviyi belirlemede primer tümör ile ilgili en önemli verilerden biri tümörün histopatolojik türüdür. Bu amaçla yapılmış sınıflamalar içerisinde en yaygın kullanılanı Dünya Sağlık Örgütü Meme Tümörleri Sınıflaması’nın Azzopardi tarafından yeniden düzenlenen şekli olup Tablo 2.1’de görülmektedir.