15, 16 (1985) 15, 16 (1985)
E m m e T a b l e t l e r i Ü z e r i n d e F a r m a s ö t i k T e k n o l o j i k Ç a l ı ş m a l a r P h a r m a c e u t i c a l T e c h n o l o g i c a l Studies o n the T r o c h e s
A r a ş t ı r m a m ı z d a ü l k e m i z d e imalatı v e kullanımı gittikçe ö n e m k a z a n a n e m m e tabletlerinin u y g u n formülasyonlarının geliştirilmesi ve teknolojik olarak o p t i m a l imalatlarının ve ağızda u y g u n e r i m e özel-liklerinin sağlanması ü z e r i n d e çalışılmıştır. Bu a m a ç l a hazırlanan 18 a n a f o r m ü l ü n ö n c e granülleri ü z e r i n d e gerekli in-proses kontrolleri yapılmış ve u y g u n olanları belirlendikten sonra tabletlerin basımlarına geçilmiştir. Basımı takiben ve b a s ı m d a n 180 g ü n sonra yapılan k o n t -rollerde özellikle tabletlerin kırılmaya karşı d i r e n ç , d a ğ ı l m a süresi, a ğ ı z d a e r i m e süresi, a ğ ı z d a u y g u n e r i m e özelliği, görünüş ve tad du-rumlarına bakılarak en u y g u n özellikleri gösteren 7 f o r m ü l seçilmiştir. F o r m ü l l e r üzerinde etken m a d d e miktar tayinleri, d o z kesinliği ve ö n -stabilite d e n e m e l e r i d e yapılarak diğer m e k a n i k özellikler y a n ı n d a a ğ ı z d a u y g u n erime özelliği veren ve diğer o r g a n o l e p t i k m u a y e n e l e r d e en o l u m l u sonuçlar veren en iyi formüller belirlenmiştir.
T h i s study was m a d e o n the d e t e r m i n a t i o n o f o p t i m a l p r o d u c t i o n a n d dissolving properties o f drugs i n the f o r m o f troches, w h i c h are n o t well k n o w n arc n o t extensively used i n o u r country.
In the next step total eighteen different active materials a n d sub-sidiary materials w e r e investigated. T h e granulations were tested for
Redaksiyona verildiği tarih: 20.3.1985.
*Farmasötik Teknoloji Anabilim Dalı, Eczacılık Fakültesi, Ankara Üniversitesi
Kandemir CANEFE* Asuman ERCAN*
ÖZET
the necessary in-proses controls p r i o r to the tabletting, a n d the suitable granulations were c o m p r e s s e d in a single p u n c h tablet press. T h e fol-l o w i n g test were a p p fol-l i e d to the tabfol-lets b o t h just after p r o d u c t i o n a n d after 180 d a y s ; hardness, disintegration time, dissolving time, orga-noleptik tests. Seven formulations were c h o s e n a c c o r d i n g to the test results, a n d they were tested further for their active ingredient c o n -tent uniformity prestability properties. Finally best f o r m u l a t i o n g i v i n g the best dissolving p r o p e r t y a n d flavour, together with suitable disso-lution times a n d m e c h a n i c a l properties was d e t e r m i n e d .
A n a h t a r k e l i m e l e r :
E m m e tabletleri, Ö n - f o r m ü l a s y o n , F o r m ü l a s y o n , İn-proses kont-rolları, Ön-stabilite denemeleri, O r g a n o l e p t i k kontrollar.
E m m e tabletlerini kısaca, a ğ ı z d a ç i ğ n e n m e d e n v e u z u n sürede e m i l m e k sureti ile kullanılan, ağız ve b o ğ a z bölgesinde lokal etki gös-termesi beklenen, basık tablet b i ç i m i n d e , katı ilaç şekilleri olarak ta-n ı m l a m a k m ü m k ü ta-n d ü r ( 1 , 2 ) .
E m m e tabletlerinden b e k l e n e n v e b u a m a c a h i z m e t e d e n p r e p a ratlara ü l k e m i z d e genellikle "Pastil", diğer m e m l e k e t l e r d e ise ç o ğ u n -lukla " L o z e n g e s " v e y a " T r o c h e s " d e n i l m e k t e d i r ( 1 , 3 ) . Aslında e m m e tabletleri ile pastiller aynı a m a c a h i z m e t etmekle birlikte imalat y ö n t e m l e r i ve teknolojileri açısından farklılıklar göstermektedirler. Bu farklılıklar ö z e t o l a r a k ; E m m e tabletlerinin tablet m a k i n a l a r ı n d a basılarak i m a l edilebilmeleri, pastillerin ise plastik kıvamlı m a d d e l e r kullanılarak basınçla kalıplanmaları v e y a jelatin, gliserin v . b . sıvağ-l a r m eritisıvağ-lip, kasıvağ-lıpsıvağ-lara d ö k ü sıvağ-l ü p , soğutusıvağ-larak hazırsıvağ-lanmasıdır (4, 5, 6 ) .
O r a l tabletler g r u b u n a giren e m m e tabletleri yutularak kullanılan per-oral tabletlerden h e m etki h e m d e teknolojik y ö n d e n d a h a farklı y a p ı ve özellikler gösterirler.
Bu farklı y a p ı ve özellikler;
1 - H a z ı r l a n a n e m m e tabletlerinden ağız v e b o ğ a z bölgesinde lokal bir etki göstermesi b e k l e n d i ğ i n d e n , kullanılan etken m a d d e l e r i n z a m a n l a yavaş ve eşit bir şekilde ç ö z ü n e r e k mu-k o z a üzerinde u z u n süre mu-kalması, b ö y l e c e etmu-ken m a d d e n i n m u k o z a y ı t a m olarak etkilemesinin sağlanması istenir (7, 8, 9, 1 0 ) . Bu n e d e n l e etken m a d d e l e r y a r d ı m c ı m a d d e l e r ve f o r m ü l a s y o n şekilleri b e k l e n e n a m a c a u y g u n olarak seçilme-lidir ( 1 1 , 12, 13).
2- F o r m ü l a s y o n d a yer alan etken m a d d e l e r i n arzu edilen etki süresine bağlı olarak, e m m e tabletlerinin genellikle yüksek basınçla basılmış o l m a l a r ı ve f o r m ü l a s y o n l a r m d a dağıtıcı m a d d e i ç e r m e m e l e r i istenir. H a t t a hazırlanan granül tane-ciklerinin üst yüzeylerinin u y g u n bir eriticide ç ö z ü n m ü ş yağ, m u m ve katı parafin g i b i lipofil bir tabaka ile kaplanması, tabletlerin d a ğ ı l m a sürelerini geciktirdiğinden, beklenen a m a -ca u y g u n b u l u n m u ş t u r (8, 10, 14).
3 - E m m e tabletlerinin o l d u k ç a u z u n süre a ğ ı z d a tutulmaları v e sık sık a l ı n m a z o r u n l u ğ u n e d e n i y l e tad, koku ve g ö r ü n ü m ü n düzeltilmesi işlemleride ö n e m kazanmaktadır. B u n e d e n l e f o r m ü l hazırlanırken ortaya çıkabilen kötü tadları maskele-y e n u maskele-y g u n tad ve koku vericilerde f o r m ü l d e maskele-yer alabilir (9, 15). E m m e tabletlerinden beklenen b u a m a ç l a r ı n sağlanıp sağlanma-dığının incelenebilmesi i ç i n g e n e l d e yapılagelen tablet kalite kontrol-lerinin yanısıra, d a ğ ı l m a testlerinde tabletlerin 37 + 2 ° C deki su içe-risinde 2 0 - 6 0 dakika g i b i bir sürede dağılmaları, a ğ ı z d a y a p ı l a n eri-me d e n e y l e r i n d e ise şekillerini az ç o k k o r u y a r a k d a ğ ı l m a d a n erieri-meleri tad, koku, v.s. g i b i o r g a n o l e p t i k özelliklerinin u y g u n olması nitelik-leri ü z e r i n d e durulmuştur.
DENEL KISIM I . M a t e r y a l v e M e t o d
1.1. K u l l a n ı l a n M a l z e m e v e M a d d e l e r :
Ç a l ı ş m a m ı z d a e m m e tabletlerinden beklenen özelliklerin g ö z ö n ü n e alınmasıyla etken ve y a r d ı m c ı m a d d e l e r i n seçimi yapılmıştır. B u arada, y a r d ı m c ı m a d d e l e r d e n ü l k e m i z koşullarında k o l a y v e eko-n o m i k olarak t e m i eko-n edilebilecek olaeko-nlar tercih edilmişlerdir ( 1 6 ) .
B u a m a ç l a kullanılan etken v e y a r d ı m c ı m a d d e l e r :
B e n z o k a i n ( D o l d e r ) , Setilpiridinyum klorür ( S ı ğ m a ) , T o z edil-miş şeker1 ( T e k e l ) , M a n n i t o l ( M e r c k ) , Stearik asit1 ( M e r c k ) , K a t ı
parafin (Yerli ü r e t i m ) , L a k t o z ( M a m s a n ) , Polietilen glikol 6 0 0 02 1) T o z edilmiş şeker: Kristal şeker değirmenden geçirilerek 0.5 mm tanecik
büyük-lüğüne getirilerek kullanılmıştır.
2) PEG 6000, Stearik asit : Mikro değirmenden geçirildikten sonra 0.315 mm delik çap elekten geçenler kullanılmıştır.
( M e r c k ) , M a g n e z y u m stearat ( R i e d e l ) , K i t r e z a m k ı3 ( Y e r l i ü r e t i m ) ,
K a k a o (Nestle), Jelatin ( M e r c k ) , M e t i l sellüloz4 (Yerli ü r e t i m ) ,
Poli-vinil p i r o l i d o n (Basf), L i m o n ve çilek esansı ( N a a r d e n ) , Eter ( M e r c k ) . 1.2. K u l l a n ı l a n A r a ç v e G e r e ç l e r :
Elektrikli teraziler ( M e t t i e r : H 1 0 , P 2 0 3 , P 1 2 0 0 ) , Elektrikli de-ğirmenler (Fritsch: 4 . 7 0 2 ; M i k r o d e ğ i r m e n , J a n k e u n d K u n k e l , A 1 0 S ) , H a v a Cereyanlı Etüv ( E n d e r ) , N e m miktarı ö l ç m e aleti (Sa-uter, E n f r a m a t i c ) , Akış hızı tayin aleti (Erweka, D u r c h f l u B-Tester, T i p : G D T ) , M i k r o elek takımı (Erweka, D I N 4 1 8 8 ) , T a b l e t maki-nası (Eksantrik, K o r s c h , E K O ) , T a b l e t sertlik testi aleti (Strong-C o b b , D e L a m a r I n c . ) , T a b l e t d a ğ ı l m a testi aleti ( M a n e s t y , T D 9 2 T 175), Ufalanma-aşınma testi aleti ( R o c h e Friabilatörü, J. Engels m a n A G . ) , T a b l e t kalınlık ö l ç m e aleti ( M i k r o m e t r e , N S K ) , U V -Spektralfotometre ( P y e - U n i c a m , S P 8 - 1 0 0 ) , Çeşitli c a m m a l z e m e (Pyrex, Schott-Jena, T e k n i k - C a m ) , A n a l i z eleği ( A ğ genişliği: 0 . 8 0 m m ) .
I I . Y ö n t e m l e r v e D e n e y l e r
I I . 1 . F o r m ü l l e r v e İ m a l a t Y ö n t e m l e r i :
Ç a l ı ş m a m ı z d a m o d e l etken m a d d e olarak B e n z o k a i n v e Setilpiri-d i n y u m klorür seçilmişlerSetilpiri-dir. F a r m a k o l o j i k veriler g ö z ö n ü n e alınarak b e h e r tablette B e n z o k a i n ' i n 5 m g , Setilpiridinyum klorür'ün 2 mg d o z d a kullanılmasına karar verilmiştir (17, 18). A y r ı c a ağızda u z u n süre tutulması gereken bu tabletler i ç i n tad ve koku nitelikleri ö n e m k a z a n d ı ğ ı n d a n , formüllere K a k a o , L i m o n esansı ve Çilek esansının ilavesinin u y g u n o l a c a ğ ı b u d e n e m e l e r l e bulunmuştur. T o p l a m ola-rak 36 f o r m ü l d e n oluşan ön-formülasyon çalışmalarından yararlanılarak 18 ana f o r m ü l pilot imalatla hazırlanmış ve geliştirilmiştir. F o r -müller i ç i n gerekli miktardaki etken ve y a r d ı m c ı m a d d e l e r tartılarak ö n c e h o m o j e n karışım haline getirilmişler, d a h a sonra toz kültesi üzerine bağlayıcı m a d d e çözeltisinin azar azar ilavesi ile h a m u r k ı v a m ı n -daki kütleye ulaşılmıştır. E l d e edilen b u kütle 0 . 8 0 m m a ğ genişliğin-3) Kitre zamkı : Öğütülüp tanecik büyüklüğü yaklaşık 0.12 mm ye getirilerek kulla
nılmıştır.
4) Metil sellüloz: Mikro değirmende öğütülüp 0.315 mm delik çaplı elekten geçenler kullanılmıştır.
deki elekten geçirilen kuru sıcak h a v a d o l a b ı n d a 45 °C de kurutul-muş, kurutulan granulier tekrar aynı elekten geçirildikten sonra n e m miktarı k o n t r o l ü yapılmıştır.
G e n e l d e b u şekilde hazırlanan granüllerden " F K " k o d numarası verilenler başlıca; T o z edilmiş şeker, M a n n i t o l , K a t ı parafin, Stearik asit ve M a g n e z y u m stearat y a r d ı m c ı m a d d e l e r i n i içermektedirler. Yaş g r a n ü l a s y o n y ö n t e m i ile hazırlanan bu granüller draje k a z a n ı n d a K a t ı parafin ve Stearik asitin belli y ü z d e d e k i eter içerisindeki ç ö z e l -tileri ile kaplanmışlardır ( T a b l o 1 ) .
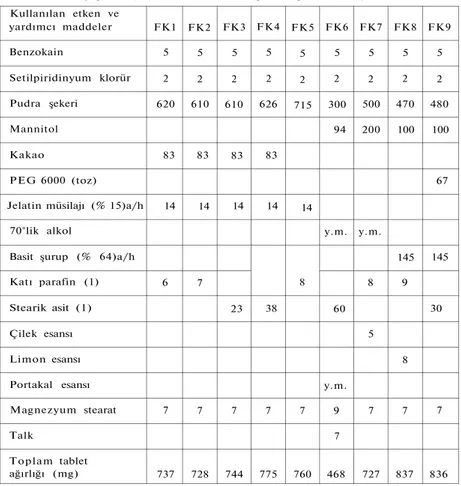
Tablo 1: Granüllerinde önceden kaplama yapılarak basılmış olan tabletlerin formülasyon yapıları (Miktarlar bir tablet için " m g " olaraktır).
Kullanılan etken ve yardımcı maddeler FK1 FK2 FK3 F K 4 FK5 FK6 FK7 FK8 FK9 Benzokain 5 5 5 5 5 5 5 5 5 Setilpiridinyum klorür 2 2 2 2 2 2 2 2 2 Pudra şekeri 620 610 610 626 715 300 500 470 480 Mannitol 94 200 100 100 Kakao 83 83 83 83 PEG 6000 (toz) 67
Jelatin müsilajı (% 15)a/h 14 14 14 14 14
70°lik alkol y.m. y.m.
Basit şurup (% 64)a/h 145 145
Katı parafin (1) 6 7 8 8 9
Stearik asit (1) 23 38 60 30
Çilek esansı 5
Limon esansı 8
Portakal esansı y.m.
Magnezyum stearat 7 7 7 7 7 9 7 7 7
Talk 7
Toplam tablet
" F " k o d numarası verilenler ise başlıca; T o z edilmiş şeker, M a n nitol, K i t r e zamkı, Polietilen glikol 6 0 0 0 ve M a g n e z y u m stearat y a r -d ı m c ı m a -d -d e l e r i n i içermekte-dirler ( T a b l o 2 ) .
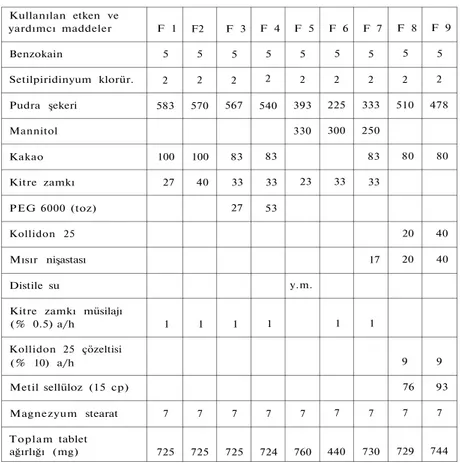
Tablo 2: Granüllerinde önceden kaplama yapılmadan basılmış olan tabletlerin formülasyon yapıları (Miktarlar bir tablet için " m g " olaraktır).
Kullanılan etken ve yardımcı maddeler F 1 F2 F 3 F 4 F 5 F 6 F 7 F 8 F 9 Benzokain 5 5 5 5 5 5 5 5 5 Setilpiridinyum klorür. 2 2 2 2 2 2 2 2 2 Pudra şekeri 583 570 567 540 393 225 333 510 478 Mannitol 330 300 250 Kakao 100 100 83 83 83 80 80 Kitre zamkı 27 40 33 33 23 33 33 PEG 6000 (toz) 27 53 Kollidon 25 20 40 Mısır nişastası 17 20 40 Distile su y.m.
Kitre zamkı müsilajı
(% 0.5) a/h 1 1 1 1 1 1 Kollidon 25 çözeltisi (% 10) a/h 9 9 Metil sellüloz (15 cp) 76 93 Magnezyum stearat 7 7 7 7 7 7 7 7 7 Toplam tablet ağırlığı (mg) 725 725 725 724 760 440 730 729 744
B ö y l e c e iki ayrı y ö n t e m l e hazırlanan granüller gerekli miktarda kaydırıcı ve kaypaklaştırıcı m a d d e ilavesi ile b a s ı m a hazır hale getiril-mişlerdir. Bu granüllerin basımı ise genellikle 12 m m ' l i k çentikli tab-let zımbası, ç o k az o l a r a k d a 10 m m ' l i k ikili draje zımbası kullanılarak yapılmıştır.
I I . 2 . K o n t r o l l e r :
H a z ı r l a n a n b u 1 8 ana f o r m ü l ü n granüllerinde " F K " k o d n u m a ralı o l a n l a r ı n d a k a p l a m a i ş l e m i n d e n ö n c e v e sonra, " F " k o d n u m a -ralı o l a n l a r ı n d a ise kaydırıcı-kaypaklaştırıcı m a d d e ilavesinden sonra o l m a k üzere şu kontroller yapılmıştır;
A) Y ı ğ ı n a ç ı s ı : H e r seferinde 40 g g r a n ü l kullanılarak 3 p a r a -lel d e n e y yapılmış, m e y d a n a gelen t o z yığınının " t a n 6" değeri hesap-lanarak ortalaması alınmıştır ( 1 9 ) .
B ) K ü m e d a n s i t e s i : 4 g g r a n ü l ü n u y g u n h a c i m d e k i ağzı k a -paklı m e z ü r d e h a c m i ö l ç ü l m ü ş , d e n e y 5 kez tekrarlanıp ortalaması alınmıştır ( 2 0 ) .
C ) A k ı ş h ı z ı : " E r w e k a " akış hızı tayin aletinin standart h u n i -sine k o n a n 40 g granül ile alet 4 titreşim h ı z ı n d a y k e n d e n e y 5 kez tekrarlanarak ortalaması hesaplanmıştır.
D ) N e m m i k t a r ı : K ı z ı l ötesi ışın ısıtmalı n e m miktarı tayin aleti kullanılarak lOg g r a n ü l d e % de n e m miktarı d o ğ r u d a n aletin skalasında o k u n m u ş t u r .
E ) T a n e c i k b ü y ü k l ü ğ ü d a ğ ı l ı m ı : " E r w e k a " firmasının D I N 4 1 8 8 n o l u standartına u y g u n hazırlanmış m i k r o elek takımı ile 10 g granül ç a l k a l a m a c i h a z ı n d a 4'er dakika süre ile 50 ve 80 k u v v e t i n d e elenmiş, eleklerin üzerinde kalan miktar % de olarak hesaplanmış-tır ( 1 7 ) .
Basılan tabletlerde b a s ı m d a n h e m e n sonra ve ayrıca basımı ta-kiben 180 g ü n sonraya kadar en u y g u n o l d u ğ u belirlenen 7 f o r m ü l ü z e r i n d e aşağıdaki tayin ve kontroller yapılmıştır.
A ) A ğ ı r l ı k s a p m a s ı : T ü r k Farmakopesi 1974'de y e r alan y ö n -t e m e g ö r e yapılmış-tır ( 2 1 ) .
B) Ç a p v e k a l ı n l ı k : B P 1980'de verilen y ö n t e m e g ö r e yapıl-mıştır.
C) U f a l a n m a - a ş ı n m a : R o c h e - F r i a b i l a t ö r ü kullanılarak % de ufalanma-aşınma miktarı saptanmıştır ( 2 2 ) .
D) Sertlik k o n t r o l ü : S t r o n g - C o b b sertlik testi c i h a z ı y a r d ı m ı ile imalatı takiben ve imalattan 180 g ü n sonra 10'ar tabletin sertlik-leri ölçülerek o r t a l a m a değerler hesaplanmıştır ( 2 3 ) .
E ) D a ğ ı l m a s ü r e s i k o n t r o l ü : M a n e s t y tablet d a ğ ı l m a testi cihazı y a r d ı m ı ile 3 7 ± 2 ° C deki su içerisinde disk k u l l a n ı l m a d a n her-b i r f o r m ü l i ç i n 10'ar taher-blet ile yapılmış, o r t a l a m a süre hesaplanmış-tır ( 2 1 , 24, 2 5 ) .
F ) A ğ ı z d a e r i m e s ü r e s i v e o r g a n o l e p t i k k o n t r o l l e r : H a -zırlanan 18 ana f o r m ü l ü n herbiri imalatı takiben ve imalattan 180 g ü n sonra ise en u y g u n özelliklerde o l d u ğ u anlaşılan 7 f o r m ü l , 10 ayrı kişiye verilmiş ve a ğ ı z d a ç i ğ n e n m e d e n e m i l m e k sureti ile tablet-lerin k a ç d a k i k a d a dağıldıkları saptanarak o r t a l a m a erime süreleri bulunmuştur. A y r ı c a kişilere ağızlarındaki tabletlerin yarattığı tad ve koku hisleri sorularak o r g a n o l e p t i k özelliklerde saptanmıştır ( 9 ) .
S O N U Ç ve T A R T I Ş M A 1 ) K ü m e D a n s i t e s i , Y ı ğ ı n A ç ı s ı , A k ı ş H ı z ı :
Ç a l ı ş m a m ı z d a k i 18 ana f o r m ü l ü n granüllerinin özelliklerinin saptanabilmesi a m a c ı ile y a p ı l a n k ü m e dansitesi, yığın açısı, akış hızı değerlerinin u y g u n s o n u ç verdiği, " F K " k o d numaralı granüller-d e y a p ı l a n k a p l a m a işleminin b u özellikleri genellikle granüller-d a h a granüller-d a o l u m l u y ö n d e artırdığı gözlenmiştir ( 1 6 ) . A y r ı c a , granüllerde y a p ı l a n kapla-ma işleminin basım sırasında tabletlerin kapla-matristen dışarı atılkapla-masını kolaylaştırdığı, d a h a parlak ve pürüzsüz yüzeyli tabletlerin elde edil-mesine y a r d ı m ettiği gözlenmiştir.
2 ) A ğ ı r l ı k S a p m a s ı , U f a l a n m a - A ş ı n m a :
i m a l a t ı takiben t ü m f o r m ü l l e r d e yapılan, imalattan 180 g ü n sonra ise en u y g u n tablet özelliklerinde o l d u ğ u g ö z l e n e r e k seçilen 7 f o r m ü l d e yapılan, ağırlık sapması kontrollarının T . F . 7 4 ' ü n sınırları içerisinde kaldığı, ufalanma-aşınma k o n t r o l ü n ü n ise t ü m tabletlerin genellikle teknolojik a ç ı d a n taşıma koşullarına dayanıklı o l d u ğ u n u gösterecek şekilde o l d u ğ u saptanmıştır ( 1 6 ) .
İ m a l a t t a n 180 g ü n sonra en iyi olarak belirlenen 7 f o r m ü l üze-r i n d e y a p ı l a n etken m a d d e miktaüze-r tayini sonuçlaüze-rının ise tabletleüze-rdeki etken m a d d e l e r i n herbir f o r m ü l ü n kendi içerisinde h o m o j e n olarak d a ğ ı l d ı ğ ı m gösterir şekilde o l d u ğ u görülmüştür.
H a z ı r l a d ı ğ ı m ı z e m m e tabletlerinde esas k o n t r o l kriteri olarak ö n e alınan değerlerin sonuçlarını ise şu şekilde sıralamak m ü m k ü n d ü r .
3 ) Sertlik K o n t r o l ü :
T ü m tabletlerde imalatı takiben y a p ı l a n sertlik k o n t r o l l e r i n d e ; " F K " k o d n u m a r a l ı tabletlerin sertlik değerlerinin 9 . 3 5 - 2 2 . 5 , " F " k o d n u m a r a l ı olanların ise 1 5 . 0 - 2 4 . 7 S t r o n g - C o b b ünitesi arasında yer aldığı g ö r ü l m e k t e d i r ( T a b l o 3 ) .
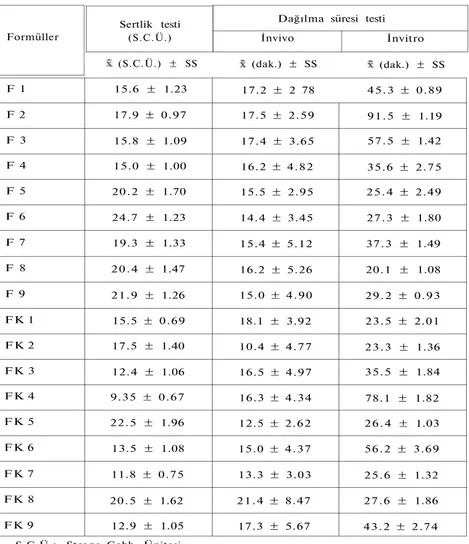
Tablo 3: " F " ve " F K " kod numaralı tablet formüllerinin basımı takiben yapılan sertlik, dağılma süresi ve ağızdaki erime süresi kontroluna ilişkin bulgular
F 1 15.6 ± 1.23 17.2 ± 2 78 45.3 ± 0.89 F 2 17.9 ± 0.97 17.5 ± 2.59 91.5 ± 1.19 F 3 15.8 ± 1.09 17.4 ± 3.65 57.5 ± 1.42 F 4 15.0 ± 1.00 16.2 ± 4.82 35.6 ± 2.75 F 5 20.2 ± 1.70 15.5 ± 2.95 2 5 . 4 ± 2.49 F 6 24.7 ± 1.23 14.4 ± 3.45 27.3 ± 1.80 F 7 19.3 ± 1.33 15.4 ± 5.12 37.3 ± 1.49 F 8 2 0 . 4 ± 1.47 16.2 ± 5.26 20.1 ± 1.08 F 9 21.9 ± 1.26 15.0 ± 4.90 29.2 ± 0.93 F K 1 15.5 ± 0.69 18.1 ± 3.92 23.5 ± 2.01 F K 2 17.5 ± 1.40 10.4 ± 4.77 23.3 ± 1.36 F K 3 12.4 ± 1.06 16.5 ± 4.97 35.5 ± 1.84 F K 4 9.35 ± 0.67 16.3 ± 4.34 78.1 ± 1.82 F K 5 22.5 ± 1.96 12.5 ± 2.62 2 6 . 4 ± 1.03 F K 6 13.5 ± 1.08 15.0 ± 4.37 56.2 ± 3.69 F K 7 11.8 ± 0.75 13.3 ± 3.03 25.6 ± 1.32 F K 8 20.5 ± 1.62 2 1 . 4 ± 8.47 27.6 ± 1.86 F K 9 12.9 ± 1.05 17.3 ± 5.67 43.2 ± 2.74 S.C.Ü.: Strong-Cobb Ünitesi SS: Standart Sapma Formüller Sertlik testi (S.C.Ü.)
Dağılma süresi testi
İnvivo İnvitro
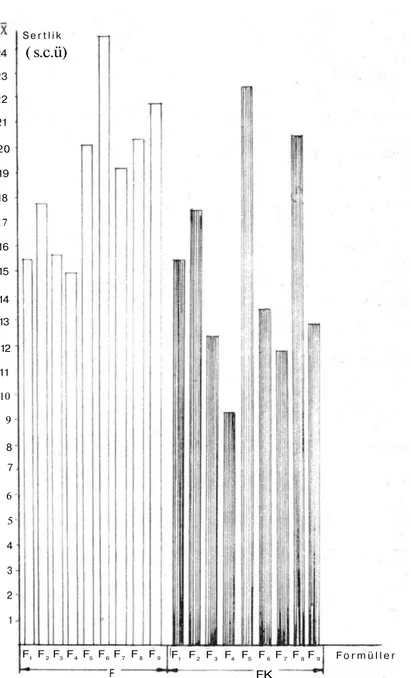
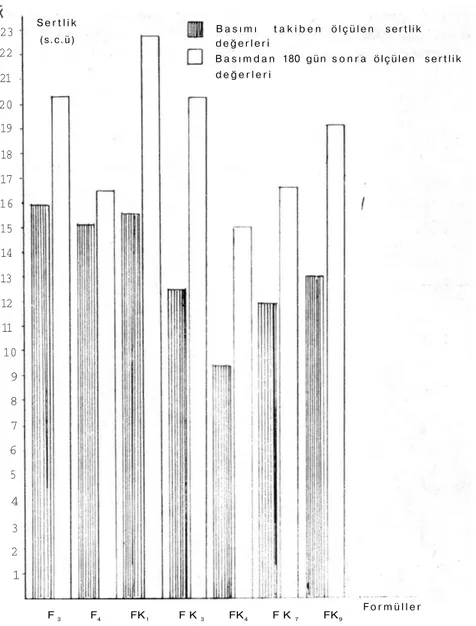
Şekil 1: Hazırlanan 18 tablet formülasyonundaki farklı formül yapıları ve imalat yöntem-lerinin, basımı takiben tabletlerde ölçülen ortalama sertlik değerlerine etkisini gösteren
grafikler. F1 F2 F3 F4 F5 F6 F7 F8 F9 F1 F2 F3 F4 F5 F6 F7 F8 F9 FK F F o r m ü l l e r S e r t l i k
( s.c.ü)
24 23 22 21 20 19 18 17 16 15 14 13 12 11 10 9 8 7 6 5 4 3 2 1Şekil l ' d e k o l a y c a izlenebildiği gibi, tablet makinasında m ü m -kün o l d u ğ u n c a aynı basınç uygulanarak basılmaya çalışılan bu for-m ü l l e r d e n " F K " k o d n u for-m a r a l ı olanların " F " k o d nufor-maralılardan d a h a düşük sertlik değeri vermesi formülasyonlarında yer alan K a t ı parafin ve Stearik asitin özelliklerine bağlanmıştır. A y r ı c a formüllere tad ve koku v e r m e k a m a c ı ile k o n u l a n K a k a o n u n d a içeriğindeki Ka-kao y a ğ ı n d a n d o l a y ı K a t ı parafin ve Stearik asitde g ö z l e n d i ğ i gibi tabletlerin sertlik değerini d ü ş ü r d ü ğ ü anlaşılmıştır.
i m a l a t t a n 180 g ü n sonra seçilen 7 f o r m ü l d e tekrar yapılan sertlik kontrollerinde tabletlerin basımı takiben gösterdikleri sertlik değer-lerine oranla artışlar o l d u ğ u saptanmıştır ( T a b l o 4., Şekil 2 ) . Ağızları kapaklı c a m k a v a n o z l a r d a ve n o r m a l saklama koşullarında bekletilen tabletlerde d o l g u m a d d e s i olarak kullanılan T o z edilmiş şekerin, or-tamdaki n e m i n d e etkisi ile, z a m a n l a bu artışa n e d e n o l d u ğ u düşünül-mektedir.
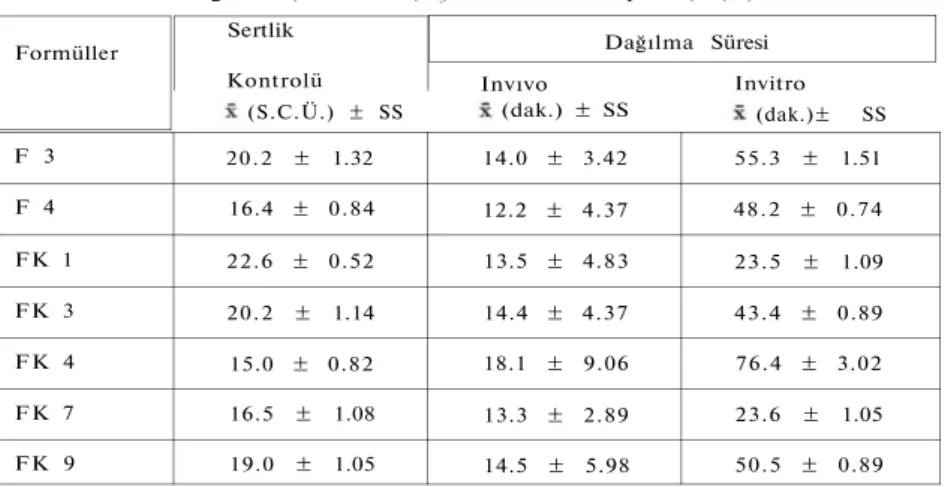
Tablo 4: Basımdan 180 gün sonra en uygun bulunan 7 formülün fiziksel kontrollerine ilişkin bulgular. (Ortalama ( ) ± Standart Sapma (SS) )
F 3 20.2 ± 1.32 14.0 ± 3.42 55.3 ± 1.51 F 4 16.4 ± 0.84 12.2 ± 4.37 48.2 ± 0.74 FK 1 22.6 ± 0.52 13.5 ± 4.83 23.5 ± 1.09 FK 3 20.2 ± 1.14 14.4 ± 4.37 43.4 ± 0.89 F K 4 15.0 ± 0.82 18.1 ± 9.06 76.4 ± 3.02 F K 7 16.5 ± 1.08 13.3 ± 2.89 23.6 ± 1.05 FK 9 19.0 ± 1.05 14.5 ± 5.98 50.5 ± 0.89 4 ) D a ğ ı l m a v e A ğ ı z d a E r i m e S ü r e s i K o n t r o l ü :
T ü m tabletlerde basımı takiben yapılan d a ğ ı l m a testi k o n t r o -l ü n d e ; 3 7 ± 2 ° C ' d e k i s u içerisinde " F K " k o d numara-lı formü-l-lerin
(S.C.Ü.) ± SS Invıvo (dak.) ± SS Invitro (dak.)± SS Formüller Sertlik Kontrolü Dağılma Süresi
23 22 21 20 19 18 17 16 15 14 13 12 11 10 9 8 7 6 5 4 3 2 1 F o r m ü l l e r
Şekil 2: Basımdan 180 gün sonra en uygun formüller olarak belirlenen 7 formülün ortalama sertlik değerlerinin, basımı takiben ölçülen ortalama sertlik değerleri ile karşılaştırmalı
grafikleri.
F3 F4 FK1 F K3 FK4 F K7 FK9
S e r t l i k
(s.c.ü) B a s ı m ı t a k i b e n ölçülen sertlik değerleri
B a s ı m d a n 180 gün s o n r a ölçülen sertlik d e ğ e r l e r i
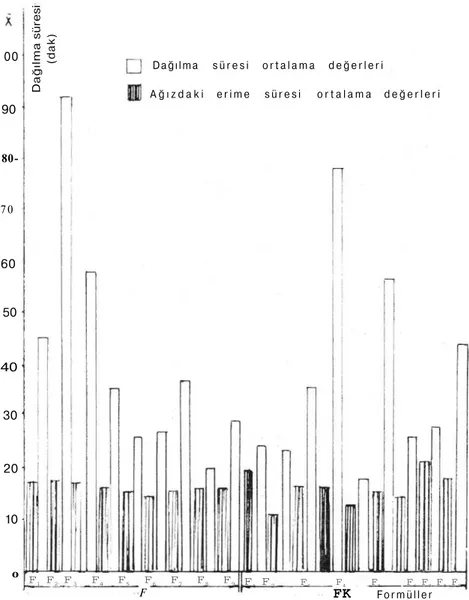
farklı f o r m ü l yapılarına g ö r e 2 3 7 8 dakika arasında, " F " k o d n u m a -ralı formüllerin ise 2 0 - 9 1 dakika arasında dağıldığı saptanmıştır. Bu sürelerin referans eserlerde e m m e tabletleri i ç i n belirtilen 2 0 - 6 0 da-kika sınırına genellikle u y d u ğ u belirlenmiştir (Şekil 3 ) .
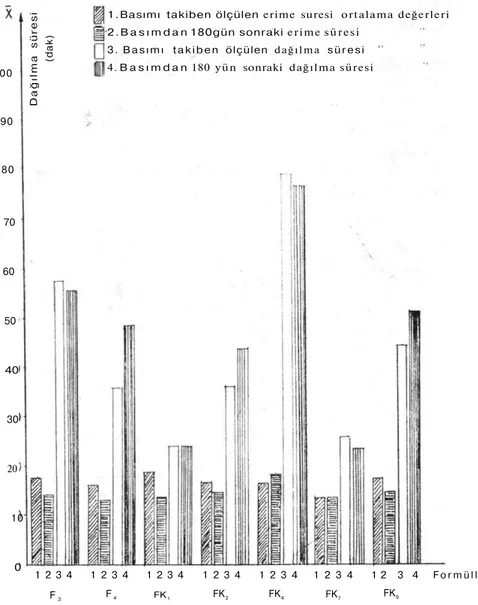
Şekil 3: Hazırlanan 18 tablet formülünde basımı takiben ölçülen dağılma ve ağızda erime sürelerinin ortalama değerlerinin, farklı formüller arasındaki dağılımını gösteren grafikler. 1 00 90 80-7 0 60 50 40 30 20 10 o F F1 F2 F3 F4 F5 F6 F7 F8 F9 F1 F2 F3 F4 F5 F6 F7 F8 F9 Formüller
FK
Dağılma süresi ortalama değerleri
A ğ ı z d a k i erime süresi o r t a l a m a d e ğ e r l e r i Dağılm a süres i (dak )
İ m a l a t t a n 180 g ü n sonra seçilen en u y g u n 7 f o r m ü l ü z e r i n d e tek-rar u y g u l a n a n d a ğ ı l m a testi s o n u ç l a r ı n ı n ise genellikle 2 3 - 7 6 d a k i k a arasında y e r aldığı b u s o n u ç l a r l a ilk d e ğ e r l e r k ı y a s l a n d ı ğ ı n d a b a z ı f o r m ü l l e r d e artış, b a z ı l a r ı n d a ise azalış o l d u ğ u belirlenmiştir ( T a b l o 4, Şekil 4 ) .
Y i n e t ü m f o r m ü l l e r d e b a s ı m ı t a k i b e n y a p ı l a n a ğ ı z d a e r i m e süresi s o n u ç l a r ı " F K " k o d n u m a r a l ı l a r d a 1021 dakika, " F " k o d n u m a r a
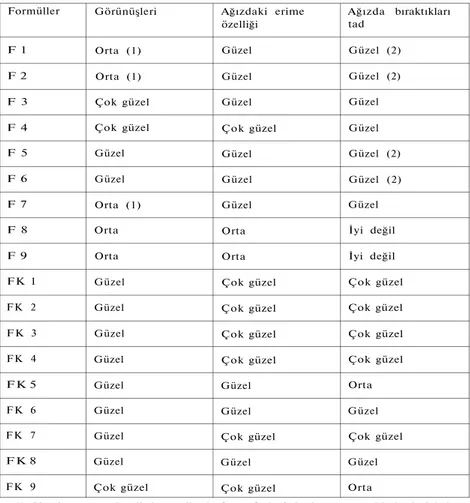
-Tablo 5: Emme tableti formüllerinin organoleptik kontrollerine ilişkin bulgular. Formüller Görünüşleri Ağızdaki erime
özelliği
Ağızda bıraktıkları tad
F 1 Orta (1) Güzel Güzel (2)
F 2 Orta (1) Güzel Güzel (2)
F 3 Çok güzel Güzel Güzel
F 4 Çok güzel Çok güzel Güzel
F 5 Güzel Güzel Güzel (2)
F 6 Güzel Güzel Güzel (2)
F 7 Orta (1) Güzel Güzel
F 8 Orta Orta İyi değil
F 9 Orta Orta İyi değil
FK 1 Güzel Çok güzel Çok güzel
FK 2 Güzel Çok güzel Çok güzel
F K 3 Güzel Çok güzel Çok güzel
FK 4 Güzel Çok güzel Çok güzel
F K 5 Güzel Güzel Orta
FK 6 Güzel Güzel Güzel
F K 7 Güzel Çok güzel Çok güzel
F K 8 Güzel Güzel Güzel
FK 9 Çok güzel Çok güzel Orta
1) Yapılan organoleptik kontrollerde 2. ve 3. haftalardan sonra tabletlerde lekelenme saptandı.
1 2 3 4 1 2 3 4 1 2 3 4 1 2 3 4 1 2 3 4 1 2 3 4 1 2 3 4 Formüller
FK1 FK3 FK4 FK7 FK9
Şekil 4: Basımdan 180 gün sonra seçilen en uygun 7 formülün dağılma ve ağızda erime süre-lerinin ortalama değersüre-lerinin, basımı takiben saptanan ağızdaki erime ve dağılma süresüre-lerinin
karşılaştırmalı grafikleri. F4 F3 100 90 80 70 60 50 40 30 20 10 0 Dağılm a süres i (dak )
1.Basımı takiben ölçülen erime suresi ortalama değerleri
2 . B a s ı m d a n 180gün sonraki erime s ü r e s i 3. B a s ı m ı t a k i b e n ölçülen d a ğ ı l m a s ü r e s i 4. B a s ı m d a n 180 y ü n sonraki dağılma süresi
lılarda ise 14-27 dakika arasında y e r almıştır. İ m a l a t t a n 180 g ü n sonra seçilen en u y g u n 7 f o r m ü l d e y a p ı l a n ağızdaki erime süresi so-nuçları ise 12-18 dakika arasında yer almış o l u p , imalatı takiben yapılan test sonuçları ile belirgin b i r farklılık göstermediği g ö r ü l m e k t e -dir (Şekil 4 ) . T a b l o 5'de g ö r ü l d ü ğ ü gibi, istatistiksel analizlerde ağız-daki e r i m e süresi sonuçlarının standart s a p m a değerlerinin yüksek çıkması, e m m e o l a y ı n ı n kişiden kişiye değiştiğini ve kesin sınırlarla standartlaştırılabilecek bir k o n t r o l y ö n t e m i o l m a d ı ğ ı n ı d a göstermek-tedir.
5 ) O r g a n o l e p t i k K o n t r o l l e r :
İ m a l edilen t ü m tabletlerde o r g a n o l e p t i k g ö z l e m l e r basımı taki-b e n taki-başlatılarak, taki-b a s ı m d a n 180 g ü n sonraya d e k sürdürülmüş ve elde edilen bulgular T a b l o 5'de özetlenmiştir.
B u g ö z l e m l e r s o n u c u , f o r m ü l y a p ı l a r ı n d a b a ğ l a y ı c ı a m a ç l a gerek kuru, gerekse müsilaj h a l i n d e K i t r e z a m k ı kullanılan f o r m ü l l e r d e basımı takip e d e n ikinci ve ü ç ü n c ü haftalardan sonra lekelenme g ö r ü l -m ü ş ( F 1 , F 2 , F 7 ) , f o r -m ü l y a p ı l a r ı n d a M e t i l sellüloz i ç e r e n ( F 8 , F 9 ) f o r m ü l l e r i n d e ise hoş o l m a y a n tad ve k o k u n u n K a k a o ile bile düzelti-l e m e d i ğ i ortaya çıkmıştır.
B u n a karşılık e m m e tabletlerinin imalatı i ç i n ü l k e m i z şartlarında genellikle k o l a y t e m i n edilebilecek d u r u m d a o l a n T o z edilmiş şeker, M a n n i t o l , Polietilen glikol 6000, Jelatin, K a t ı parafin v e K a k a o yar-d ı m c ı m a yar-d yar-d e l e r i n yar-d e n fayyar-dalanılmasının b e k l e n e n a m a c a u y g u n so-n u ç l a r verdiği saptaso-nmaktadır.
LİTERATÜR
1- British Pharmacopoeia (B. P. 1980), University Printing House, Cambridge (1980) 2- Ritschel, W.A., "Angewandte Biopharmazie", Wissenschaftliche-Verlagsgesellschaft,
M B H , Stuttgart (1973).
3- Trotter, G. F., Hawkins, D.K., Parrot, EX., Arn. Jour. Pharm., 128, 58 (1956) 4- Sprowls, J.B., Beal, H.M., "American Pharmacy", 6 th. edition, Philadelphia, J. P.
Lippincott Company (1970)
5- Izgü, E., "Genel-Endüstriyel Farmasötik Teknoloji II", Ankara Üniversitesi Basımevi, Ankara (1983)
6- Gonzales, M., Wolf, G., Am. J. Hosp. Pharm., 18, 396 (1961)
7- Gstirner, F., "Grundstoffe und Verfahren der Arzneibereitung", Ferdinand Enke-Verlag Stuttgart, (1966)
8- Ritschet, W. A., "Die Tablette", Editio Cantor, Aulendorf (1966)
9- Lieberman, H.A., Lachman, L., "Pharmaceutical Dosage Forms: Tablets", Lea-Febiger, Philadelphia (1980)
10- Münzel, K., Buchi, J.U., Schultz, O.E., "Galenisches Prakticum"', Stuttgart (1959) 11- Köhler, H., Deutsch. Apoth. Ztg; 102, 507 (1962)
12- Ostrup, P., Arch. Pharm. Og. Chem., 67, 105 (1960) 13- Ostrup, P., Arch. Pharm. Og. Chem., 68, 573 (1961)
14- British Pharmacopeia, (B. P. 1963), The Pharmaceutical Press, London (1963) 15- Specialty Sweeteners, "American Sugar Division", Amstar Corporation, 1251
Avanue of the Americas, Newyork (1981)
16- Ercan, A., "Emme Tabletlerinin Formülasyon Parametreleri ve İmalat Teknolojileri Üzerine Araştırmalar", Yüksek Lisans Tezi, A . Ü . Ecz. Fak., (1984)
17- Pharmaceutical Codex 11 th. Edition, The Pharmaceutical Press, London (1979) 18- The Extra Pharmacopoeia, 27 th. Edition, The Pharmaceutical Press, London (1979) 19- Chase, Gennaro, Gibson, Granberg, Harvey, King, Martin, Swiynard, Zink, "Remingtons Pharmaceutical Sciences", 16 th. Edition, Mack Publishing Company, Easton, Pennsylvania (1980)
20- Parrott, E.L., Saski, W., "Experimental Pharmaceutics", 4 th. Edition, Burgess Publishing Company, Minneapolis (1977)
21- Türk Farmakopesi 1974, Millî Eğitim Basımevi, Istanbul (1974)
22- Lachman, L., Lieberman, H.A., Kanig, J.L., " T h e Theory and Practice of Industrial Pharmacy", Lea and Febiger, Philadelphia, 2 th. Edition (1976)
23- Ercan, A., Canefe, K., "Katı İlaç Şekillerinin Sertlik ve Dayanıklılıklarının Saptan-masında Kullanılan Yöntemler", AEOB (Ek baskı), 5: 3 (1983)
24- T h e United States Pharmacopoeia ( U S P X X ) , 20 th. Rev. Mack Printing Co., Easton (1980)
25- Canefe, K., "Amoksilin trihidrat Tabletlerinin Formülasyon Parametreleri, Stabilite Kinetiği Ve Çözünme Hızı Kinetiği ile İlgili Çalışmalar", Doçentlik tezi, A . Ü . Ecz. Fak., (1980)