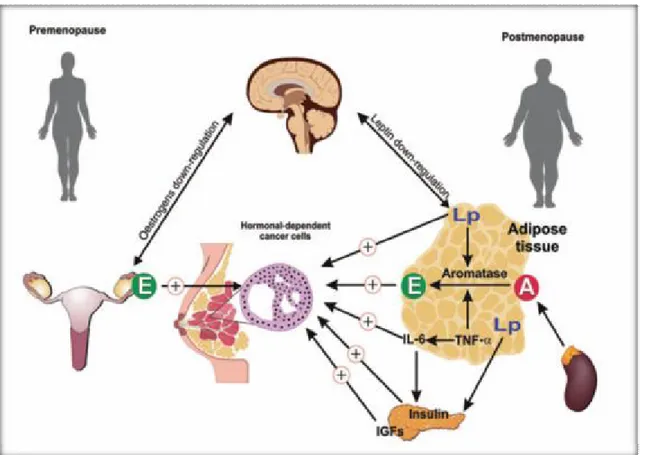
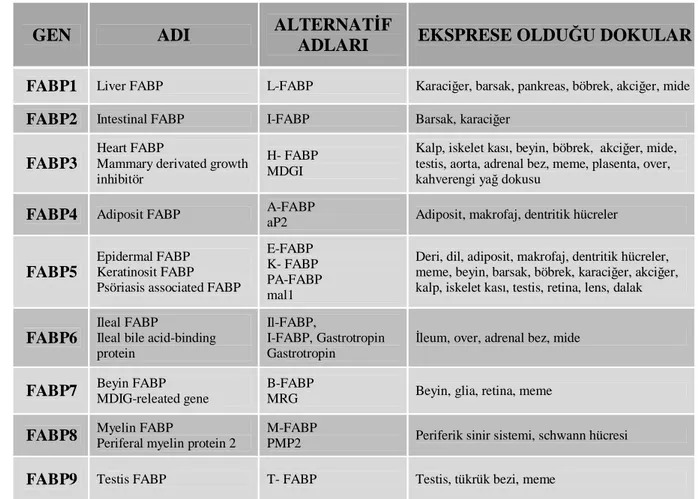
Meme kanseri olan hastalarda A-fabp ve Fasn'ın inflamasyon ve adipositokinlerle ilişkilerinin araştırılması
Tam metin
Şekil
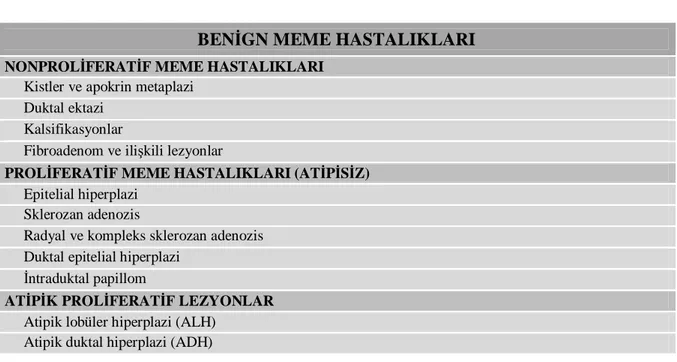


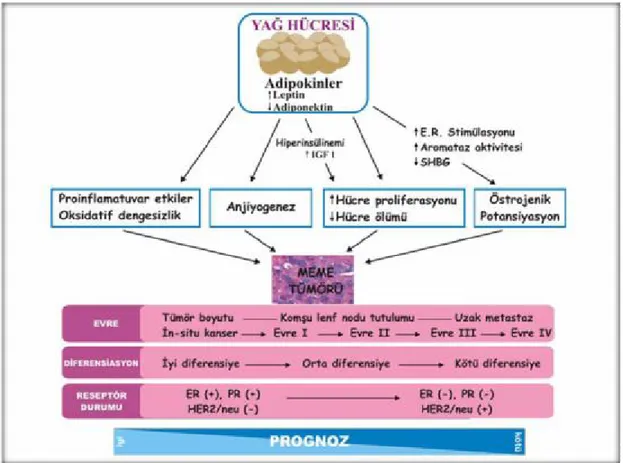
Benzer Belgeler
D) Lağım suları arıtılmaz ise balık ölümlerine neden olabilir. Kompost, organik maddelerin kontrollü koşullar altında biyolojik olarak ayrıştırılmasıdır. Organik
A)Vücudun dik durmasını sağlamak. B)Vücudu dış darbelere karşı korumak. C)Hızlı ve ritmik kasılır. 9)Resimdeki kasların altına türlerini yazınız.. 10)Güneş ve
4 1990 y›l›nda ‹stanbul’da yap›lan bir araflt›rmada hekime bafl- vurmadan reçetesiz ilaç alma oran› düflük sosyo-ekono- mik kültürel konumda olanlarda %56.7,
Hasat dönemlerine göre Iris rizomlarının uçucu yağ verimi, kuru rizom verimlerindeki artışa bağlı olarak artmış ve hasat sonrası rizomlarda 0,123-0,300 L/da
Çizelge 3.58 incelendiğinde, DASU-Tutum Ölçüm Modelinde ilgi gruplarının dikili ağaç satışı uygulamasını geliştirmeye yönelik tutumun ILT boyutu üzerinde
Bu çalışmada; Afyon Kocatepe Üniversitesi Tıp Fakültesi Hastanesi’nde çalışan hemşirelerin iş tatmin düzeylerini etkileyen faktörler, motive edici faktörler
In a recent study comparing GAS6 intron 8 c.834 + 7G4A polymorphism in subjects with type 2 diabetes, impaired glucose tolerance and controls, it was shown that AA genotype
The proposed scoring system based on cellular organi- zation, morphology and cohesiveness with an allocation of 3 points for high-grade features resulted in the highest