T.C.
DİCLE ÜNİVERSİTESİ
TIP FAKÜLTESİ ÜROLOJİ ANABİLİM DALI
UZMANLIK TEZİNİN ADI
RATLARDA OLUŞTURULAN PRİAPİZM VE İSKEMİ REPERFÜZYON
HASARI ÜZERİNE CURCUMİNİN KORUYUCU ROLÜ
DR. YAKUP YILMAZ TIPTA UZMANLIK TEZİ
DİYARBAKIR-2012
T.C.
DİCLE ÜNİVERSİTESİ
TIP FAKÜLTESİ ÜROLOJİ ANABİLİM DALI
UZMANLIK TEZİNİN ADI
RATLARDA OLUŞTURULAN PRİAPİZM VE İSKEMİ REPERFÜZYON
HASARI ÜZERİNE CURCUMİNİN KORUYUCU ROLÜ
Dr. YAKUP YILMAZ TIPTA UZMANLIK TEZİ
TEZ DANIŞMANI
YARD. DOÇ. Dr. MURAT ATAR
ÖNSÖZ
Eğitimim süresince bilgi ve tecrübelerini benden esirgemeyen, Dicle
Üniversitesi Üroloji Anabilim Dalı görev yapan değerli tüm hocalarıma,
İlgi, yardım ve sabırlarından ötürü; tez danışmanım Yard. Doç.Dr. Murat
ATAR’a, İstatistik analizlerde yardımlarından dolayı Yard. Doç. Dr.
Yaşar BOZKURT’A, histopatolojik incelemelerde yardımlarından dolayı
Yard. Doç. Dr. Uğur FIRAT’a, tez yazım aşamasında yardımlarını
esirgemeyen Yard. Doç. Dr. Haluk SÖYLEMEZ’e, Eğitimim süresince
bütün sıkıntılarıma ortak olan ve benden desteklerini esirgemeyen aileme
ÖZET
Amaç: Bu çalışma ratlarda iskemik priapizmin kavernozal dokularda oksidatif
etkilerini tanımlamak ve bir antioksidan olan curcuminin penil iskemi reperfüzyon modelinde biyokimyasal ve histopatolojik etkilerini değerlendirmek için yürütülmüştür.
Materyal ve Metod: Toplam 26 adet yetişkin erkek Sprague Dawley sıçan rastgele 3
gruba ayrıldı. I. Grup (Kontrol grubu, n=8): Sadece penektomi yapıldı ve VCI den 3 ml kan alındı. II. Grup (İskemi reperfüzyon grubu, I/R, n=8): Bir saat iskemik priapizm + 30 dakika reperfüzyon sonrası penektomi yapıldı ve çalışma için VCI’ dan 3ml. kan alındı. III. Grup (I/R+CURC grubu, n=10): İşlem öncesinde 7 gün boyunca 200 mg/kg/gün curcumin verildi. Ardından 1 saat iskemi ve sonrasında 30 dakika reperfüzyon sonrası penektomi yapıldı ve vena kava inferiordan 3ml. kan alındı. Deney işlemlerinden sonra plazma örneklerinde total oksidan seviye (TOS), total antioksidan seviye (TAS), paraoksonaz (PONX) seviyeleri ölçüldü ve histopatolojik olarak alınan dokular; kanama, ödem ve nekroz açısından incelenip skorlandı. İstatistiksel analizde Chi-kare testi, Kruskal-Wallis testi ve Mann-Whitney U testi uygulandı. P değeri 0.05’ten küçük sonuçlar anlamlı kabul edildi.
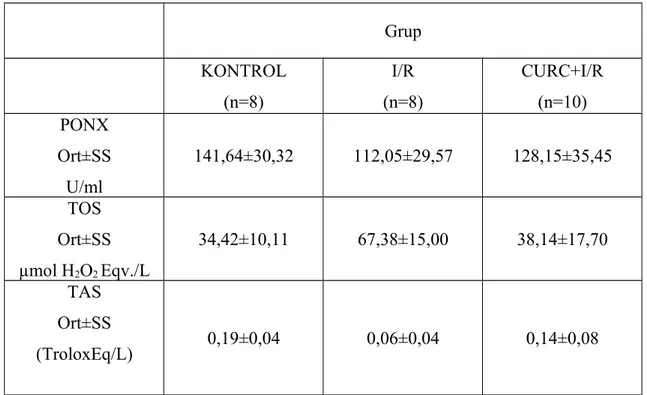
Bulgular: I/R grubunda kontrol grubuna göre TOS yüksek (p=0,002), TAS düşük
(p=0,001) bulundu. Curcumin verilen grupta I/R grubuna göre TAS’ın yükseldiği (p=0,003), TOS’un düştüğü (p=0,004) görüldü. Curcumin verilen grupta TAS ve TOS düzeylerinin kontrol grubuna yaklaştığı görüldü. PONX düzeyinin I/R ile arttığı (p=0,21) curcumin verilmesi ile azaldığı (p=0,53), ancak istatistiksel anlamlı fark oluşturmadığı tespit edildi. Histopatoljik incelemede kanama ödem ve nekroz açısından curcumin tedavisinde anlamlı fark görülmedi.
Sonuç: Bu çalışmada oluşturulan deneysel iskemik priapizm modelinde curcuminin,
iskemi reperfüzyon hasarına karşı oksidatif hasar parametrelerini düzelttiği ancak histopatolojik olarak kanama, ödem ve nekroz üzerinde olumlu etkileri olmasına rağmen anlamlı fark oluşturmadığı gözlendi.
Anahtar kelimeler: priapizm, total oksidan seviye, total antioksidan seviye,
SUMMARY
Objective: This study was carried out in rats to identify the oxidative stress effects
of the ischemic priapism on cavernosal tissues and to assess the biochemical and histopathological effects of curcumin as an antioxidant on this penile ischemia-reperfusion model.
Materials and Methods:
26 adult male Sprague Dawley rat were used in this study and were divided into three grups randomly. Group 1 (Control, n=8): Only penectomy were done and 3 ml blood sample obtained from vena cava inferior (VCI). Group 2 (ischemia-reperfusion group; I/R, n= 8): Penectomy after 1 hour ischemic priapism + 30 min reperfusion and 3 ml blood sample from VCI. Group III (I/R+CURC group, n=10): 200 mg/kg/day curcumin per orally before surgery for 7 days + Penectomy after 1 hour ischemic priapism + 30 min reperfusion and 3 ml blood sample from VCI. At the end of the experimental period, total oxidant status (TOS), total antioxidant status (TAS) and paraoxonase (PONX) levels were measured from serum samples. Tissue samples were investigated and scored histopathologically in terms of bleeding, edema and necrosis. Chi-square test, Kruskal-Wallis test and Mann-Whitney U test were used for statistical analysis and a value of p < 0.05 was used as a threshold for statistical significance.
Results:
TOS levels were higher (p=0,002), and TAS levels were lower (p=0,001) in I/R group than the control group. TAS levels were increased (p=0,003), and TOS levels were decreased (p=0,004) in I/R+CURC group than the I/R group as a result of curcumin treatment. In the treatment group (I/R+CURC) TAS and TOS levels were similar to levels in control group. PONX levels were increased with ischemia-reperfusion (p=0,21) and decreased with curcumin treatment (p=0,53), however this changes were not statistically siginificant. There was no significant difference between curcumin treated group and others according to histopatological findings in terms of bleeding, edema and necrosis.
This experimental iscemic priapism model study showed that curcumin treatment has preventive effects on oxidative stress parameters against ischemia-reperfusion injury. Also, histopathologically, it has preventive effects on bleeding, edema and necrosis without significance.
Key words: priapism, total oxidant status, total antioxidant status, paraoxonase,
İÇİNDEKİLER
Sayfalar
Önsöz ... i
Özet ... ii
İngilizce Özet (Abstract) ... iii
Simgeler ve Kısaltmalar Dizini ... vii
1. Giriş ve Amaç ...…. 1
2. Genel Bilgiler ... 3
2.1. Penis Anatomisi ve Histolojisi…... 3
2.1.1.Penis kanlanması……….………..…..……….……… 4
2.1.2.Penisin lenfatik drenajı………….……...………..……….….. 5
2.1.3.Penisin inervasyonu…………..………...……….…………..……….. 5
2.1.4.Penis histolojisi……….……….…....………...…... 6
2.2.EreksiyonFizyolojisi... 6
2.2.1.Ereksiyon evreleri ……... 7
2.2.2.Ereksiyonun moleküler fizyolojisi………..………...………... 8
2.2.3.Ereksiyonun santral kontrolü………...………...….. 9
2.2.4.Ereksiyonun periferal kontrolü………..…….…..….…. 10
2.3.Priapizm………...……….. 12 2.3.1.Tarihçe……….….…..…….... 12 2.3.2.Priapizm tanım………...……...…….. 13 2.3.3.Epidemiyoloji ve etiyoloji………..………....…..…….. 14 2.3.4.Priapizm Patofizyolojisi………..………...………. 15 2.3.5.Tanı………...………….……...….…. 18 2.3.6.Tedavi………...………..………...….. 19 2.4 İskemi ve Reperfüzyon………...………...………...….. 22 2.4.1 Mekanizmalar………...………...…..…………. 22 2.4.2. Serbest radikaller………..…...………….. 24
2.4.3. Antioksidan savunma sistemleri……….……... 28
2.5 Curcumin (TURMERIC)……….…………..……… 30
2.5.1 Metabolizması……….……… 30
2.5.2 Moleküler Özellikleri……….……. 31
2.5.3 Curcuminin Antioksidan Etkileri………...….….…...…… 31
2.5.4 Curcuminin Diğer Etkileri………...…...….. 32
3. GEREÇ ve YÖNTEM ... 33
3.1. Denekler……….…..…… 33
3.2 Anestezi ve Cerrahi İşlemler…………..……...……… 33
3.3. Biyokimyasal İnceleme Yöntemi………...……….……...……..…… 35
3.3.1 Total antioksidan seviye (TAS) ölçümü………..………..…………. 35
3.3.2 Total oksidan seviye (TOS)’nin ölçümü…..………..…………. 36
3.3.3 Paraoksonaz (PON1 (ölçümü)……….……….…….………… 36
3.4. Histopatolojik İnceleme Yöntemi…….………..…….………. 36
4.1 Biyokimyasal Analiz Sonuçları………….……….…..…….…… 40
4.1.1. Total antioksidan seviye (TAS) sonuçları ……….….….…. 40
4.1.2 Total oksidan seviye (TOS) sonuçları………..….…. 40
4.1.3 Paraoksonaz aktivitesi (PONX) sonuçları………...…..….……. 41
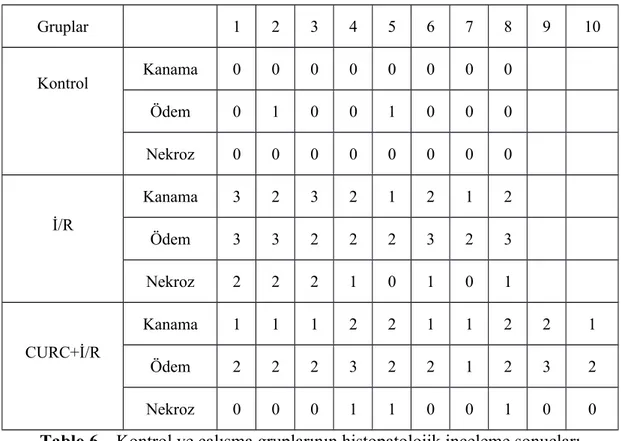
4.2 Histopatolojik İnceleme Sonuçlarının Karşılaştırılması……..….…… 41
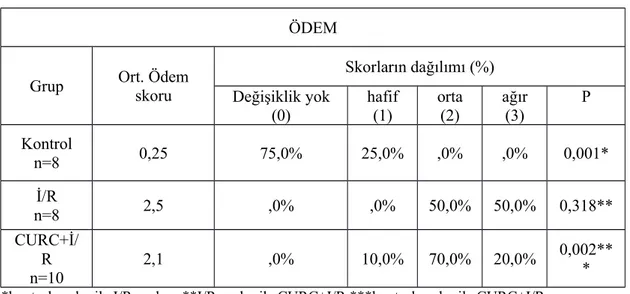
4.2.1. Kanama……….……… 42 4.2.2. Ödem……….……… 43 4.2.3 Nekroz……….……... 43 5. TARTIŞMA……….……... 44 6. SONUÇ……….…..… 50 7. KAYNAKLAR……….….…. 51
SİMGE VE KISALTMALAR CURC : Curcumin
DMSO : Dimetil sülfoksit DNA : Deoksiribonükleik asit ED: Erektil disfonksiyon GPx : Glutatayon peroksidaz H2O2 : Hidrojen peroksit HO• : Hidroksil radikali I/R : İskemi-reperfüzyon KAT : Katalaz KD : Ksantin dehidrogenaz KO : Ksantin oksidaz MDA : Malondialdehid NO : Nitrik oksit
NOS: Nitrik oksit sentaz O2. : Süperoksit radikali OHA: Orak hücreli anemi PONX: Paraoksonaz
RNS: Reaktif nitrojen türleri SOD : Süperoksid dismutaz SOR : Serbest oksijen radikalleri TAS: Total antioksidan seviye TOS: Total oksidan seviye VCI : Vena cava inferior
1. GİRİŞ ve AMAÇ
Priapizm Yunancadan Priapus sözcüğünden gelmiş ve cinsel istek, orgazm ve uyarıdan bağımsız, uzamış ereksiyon halidir (1). Priapizm yüksek akımlı, düşük akımlı ve tekrarlayan olarak ayrılabilir.
İskemik priapizm sık görülen ve düşük akımlı priapizm tipidir. Düşük akımlı (iskemik priapizm) %95 ile en sık görülen priapizm tipidir. Hızlı ve doğru yaklaşım gerektirir. Dört saatten fazla süren iskemik priapizm acil tıbbi müdahale gerektiren bir kompartman sendromudur. Venöz akımın obstrüksiyonu ve venöz staz, kalıcı belirgin erektil disfonksiyonla sonuçlanan hipoksi, asidoz ve fibrozise neden olmaktadır. Tedavi edilmezse veya tedavide geç kalınırsa (>24 saat) kavernozal düz kaslarda nekroz, irreversibl korporal fibrozis ve erektil disfonksiyon meydana gelmektedir(2).
Priapizmin erken evresinde, buz torbaları veya soğuk duş vazokonstriktif refleksi indükleyerek priapizmi hafifletebilir. Korporal aspirasyon ve intrakavernozal adrenerjik ajan enjeksiyonu ile priapizm süresi 12 saatten az olan olguların hepsinde, 12-24 saat arasında olanların %78’inde ve 24-36 saat arasında olanların %44’ünde erektil fonksiyonun spontan olarak ya da sildenafil ile korunabildiği bildirilmiştir (3). Priapizmde iskemik kalan erektil dokularda detümesans oluşması ile reperfüzyon sağlanır. Reperfüzyon, iskemik dokunun tamir mekanizmaları için gerekli olmasına rağmen, oksijenlenmiş kanın iskemik dokuya dönüşü dokuyu daha fazla zedeleyen bir reaksiyon sürecini başlatır. Reperfüzyon hasarı serbest oksijen radikalleri, endotelial faktörler ve nötrofillerin eşlik ettiği karmaşık bir mekanizmayla gerçekleşir. İskemik dokularda, serbest oksijen radikali üreten intraselüler mekanizmalar tam aktive edilmiş durumdadır. Ancak oksijen sağlanmasındaki eksiklikten dolayı fonksiyon görmezler. Kan akımı ve oksijen sağlanmasının restorasyonu ile büyük miktarlarda serbest oksijen radikali üretilerek reperfüzyon hasarı indüklenir. Organizmada serbest oksijen radikalleri ortaya çıktıktan sonra radikal reaksiyon dizileri başlar. Eğer bir serbest radikal, radikal olmayan bir molekülle reaksiyona girerse, binlerce reaksiyondan oluşan reaksiyon zincirlerini başlatır. Serbest oksijen radikalleri paylaşılmamış elektronlarından dolayı lipid, protein, karbonhidrat, nükleik asit gibi çeşitli makro moleküllerin oksidatif hasarına
neden olurlar (4,5). Oksidatif hasar artmış ROS ve serbest radikallerin doğal antioksidan mekanizmalarını aşması ile oluşur.
Değişik antioksidanlar değişik doku ve organ sistemlerinde I/R hasar üzerinde antioksidatif etkilerini göstermek üzere kullanılmıştır. İskemik piriapizm oluşması ve detümesansın sağlanması ile reperfüzyon sağlanması diğer organlardaki I/R hasarına benzemektedir.
Curcuminin antioksidan özellikleri ile böbrek, kalp, beyin dokusu ve karaciğerde İ/R hasarında oksidatif stresi ve doku hasarlanmasını azalttığı gösterilmiştir (6). CUR antioksidan etkinliğini ksantin dehidregenaz’ın ksantin oksidaz’a dönüşümünün önlenmesi, lipit peroksidasyonu oluşumunun engellenmesi ve iskemik ortamda bulunan serbest oksijen radikalerini (SOR) toplayarak gösterir (7). Ayrıca curcumin katalaz, süperoksid dismutaz ve glutatyon peroksidaz enzimlerinin aktivitelerini artırarak hücre zarında bulunan lipitlerin peroksidasyonunu da azaltır (8).
Bu deneysel çalışma ratlarda priapizmin kavernozal dokularda oksidatif etkisini tanımlamak ve curcuminin oksidatif hasarın biokimyasal parametrelere antioksidatif etkilerini ve histopatolojik değişikliklere etkilerini değerlendirmek için yapılmıştır. Bu çalışma, curcuminin deneysel rat priapizm modelindeki etkilerini araştıran literatürdeki ilk deneysel çalışmadır.
2. GENEL BİLGİLER
2.1. Penis Anatomisi ve Histolojisi
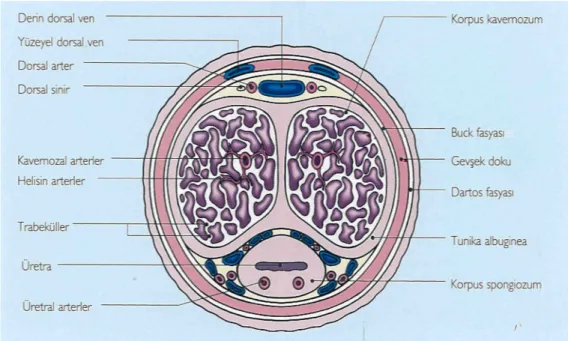
Penis radiks ve korpustan oluşan erektil bir organdır. Radiks ürogenital bölgede yerleşmiştir. İki krus ve bir bulbus olmak üzere üç erektil yapıya sahiptir. Her iki krus kendi etraflarındaki iskionun altına tutunur ve iskiokavernöz kas tarafından sarılırlar. Daha sonra her iki krus yan yana birlikte seyrederler. Bu noktadan itibaren kruslar “korpus kavernosum” olarak adlandırılırlar. Korpus kavernosum penis yapı olarak süngere benzer. Korpus kavernosumu dıştan saran ve “tunika albuginea korpus kavernosum” adı verilen zar sağlam bağ dokusundan oluşmuştur. Korpus kavernosumlar glans peniste sonlanırlar (9,10). Penis bulbusu yüzeyel perineal bölgede her iki krusun arasında yer alır. Bulbusun üst kısımları ürogenital diaframın alt kenarına tutunur ve bulbokavernöz kas ile örtülür. Başlangıçta bulbusu üstten penetre eden üretra daha sonra merkezde yer alarak bulbus içinde öne doğru ilerler. Bulbusun, korpus kavernosumların proksimal ucu ile komşu olan kısmından itibaren adı “korpus spongiosum” olur. Korpus spongiosum, korpus kavernosumlar arasındaki alt orta olukta yer alır (Şekil 2.1). Penisi uzunlamasına geçerken korpus spongiosum daralırsa da hemen sonra distal uçta genişleyerek glansı oluştururur. Korpus spongiosum penisin etrafını saran tunika albuginea ince ve gevşektir. Glans, penis korpusundan fiziksel olarak “sulcus coronarius” ile ayrılır. Glans penisin yapısı diğer erektil dokulardan farklıdır. Burada bulunan kavernalar geniş ve kıvrık damara benzer. Bu kavernalar arasında bağ dokusu çoktur. Bununla birlikte kas lifleri de çok az bulunur ve tunika albuginea yoktur. Glansın ucunda üretranın sonlandığı mea bulunur. Glans “prepusyum” adı verilen çift katlı penis cildi ile örtülüdür. Prepisyumun ön yüzünde bulunan “frenilum” cildin medial bir plisi olup meaya tutunur. Penisin derin ve yüzeyel olmak üzere iki fasyası vardır (9). Yüzeyel olan fasya “Colles fasyası” adını alır. Bu fasya skrotumun dartos fasyası ve süperfisiyal perineal fasya ile uzanır. “Buck fasyası” olarak adlandırılan penisin derin fasyası korpus kavernosumlar ve korpus spongiosumu saran kuvvetli bir fasyadır ve derin perineal fasyaya uzanır. Buck fasyası korpus kavernosumların distal ucunda son bulur ve glans penisi örtmez.
Şekil 2-1. Korpus kavernozum ve spongiozumun görünümü 2.1.1 Penis kanlanması
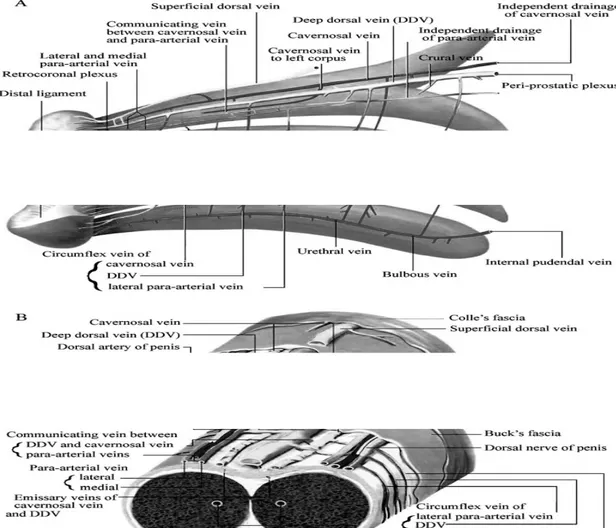
Penisin arteryel kanlanmasını başlıca a.dorsalis penis, a.profunda penis ve a.bulboüretralis gibi a.pudentalis internanın dalları sağlamaktadır (Şekil 2.2) (9). Ayrıca a.pudentalis externanın yüzeyel ve derin dalları a.pudentalis interna dalları ile anastomozlar oluşturan ve penil cildi besleyen birçok küçük dal vermektedir. Penisin venöz drenajı üç ayrı sistemden oluşur (9,11,12,13). İlk sistem, dartosun altındaki yüzeyel ven ağıdır, v.dorsalis penis superfisialis yolu ile v.saphena magna’ya drene olur. İkinci sistemi buck fasyası derininde bulunan ve v.dorsalis penis profunda’ya drene olan ven ağı oluşturur. Ayrıca korpus kavernosumlardan çıkan lateral, inferior ve superior emisser venler ile çok sayıda circumfleks penil ven drene olur. Üçüncü sistem ise korpus kavernosumları ve korpus spongiosumu drene eden bir grup derin venden oluşur. Korpus kavernosumu drene eden derin venler pudental pleksusa boşalır. Korpus spongiosum ise bulber ve üretral venlerden oluşan derin bir ven ağı aracılığı ile drene olur. Distal üretrayı ön ve arka üretral venler drene eder. Arka venler birleşerek pudental pleksusa veya bulber venlere boşalırlar. Üretral venlerin ön grubu sirkumfleks venöz sistemi oluşturmak üzere, sonradan posterior emisser venler ile birleşen birçok dala ayrılır (14).
Şekil 2-2. Penisin vasküler anatomisi 2.1.2 Penisin lenfatik drenajı
Penil cildin lenfatik drenajı superfisiyal inguinal lenf bezlerine, glans ve distal üretranın lenfatik drenajı ise derin inguinal ve eksternal iliak lenf bezlerine boşalmaktadır. Korpus kavernosum ve proksimal üretra ise internal iliak lenf bezlerine drene olmaktadır (9).
2.1.3 Penisin inervasyonu
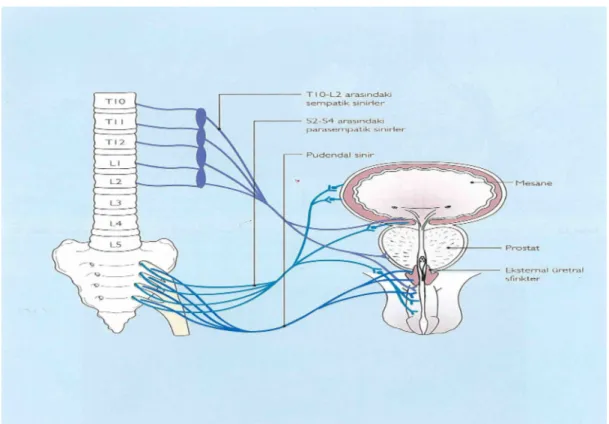
S2 – S4 spinal segmentten çıkan sinir lifleri ile sağlanmaktadır (Şekil 2.3). Sempatik innervasyon n. pudentalis’in terminal bir dalı olan n.dorsalis penis tarafından sağlanmaktadır. Cildin ve glans penisin innervasyonundan sorumludur. Penis kökünden. ilioinguinalis dalları innervasyona katkı sağlar. Kavernöz sistemin
parasempatik lifler erektil dokuları innerve etmektedir (9). Nörovasküler sinir demeti penis dorsumunda saat 11 ile 13 arasında yerleşmiştir, ayrıca nörovasküler demetten ayrılan küçük dallar korpus spongiusum içine girmektedir (15).
Şekil 2-3. Penisin nöral anatomisi 2.1.4 Penis histolojisi
Korpus kavernozumun tunike albugineası, kalın kollagen fibriller ve birkaç adet elastik liften oluşmuştur. Kollagen fibriller interstisyel kollagenlerden (Tip I – II – III) ve tropokollagenden meydana gelir. Tip I kollagen fonksiyonel olan birimdir. Elastik fibriller sıklıkla iki anatomik bölgede bulunur, bunlar proksimal krus ve distal tunikadır.
Penisin istirahati sırasında tunika çok gevşektir. Korpus spongiosum penis bol, düzensiz yapıda elastik fibriller içerir. Elastik ağ, glans penis yapısında da bulunur ve düzensiz dağılım gösterir (16). Korpus kavernozum bağ dokusu ve düz kasla birbirinden ayrılmış laküner aralıklar olarak tanımlanmıştır (17). Korpus kavernozumların fibröz iskeleti tunika albuginea ve sütunlarından oluşmaktadır.
Normal ereksiyon, sinir sistemiyle (santral, spinal, periferik) lokal faktörlerin ( sinüsoidal düz kaslar ve endotel) arasındaki etkileşimler ve bunları modüle eden birçok mediatörün katkısıyla gelişen hemodinamik bir olaydır. Normal ereksiyon iki fonksiyonun bütünleşmesine bağlıdır;
1. Kavernozal arterlerin genişlemesi ve trabeküler düz kasların tam gevşemesiyle sinüsoidal boşluklara kan girişinin artması,
2. Penise dolan kanın venöz dönüşünün engellenerek orgazma kadar geçen sürede ereksiyonun sürdürülmesi.
Venöz dönüşün engellenmesinde birçok mekanizma rol oynamaktadır;
1. Pasif venooklüzyon (flep valv mekanizma): Düz kas gevşemesiyle genişleyen ve dolan sinosoidal boşluklar tunika albuginea altındaki subtunikal venülleri, tunika albugineanın gerilerek içinden geçen emisser venleri, genişleyen kavernöz cisimlerin üzerindeki tunika albugineayla Buck fasyası arasında seyreden sirkumfleks ve derin dorsal venleri sıkıştırması pasif bir venooklüzyon oluşturur. 2. Aktif venöz kotraksiyon: Özellikle emisser venlerin yakınında yoğun olarak
bulunan nöropeptid-Y aktif ven kontraksiyonu oluşturmaktadır.
3. Trombosit tıkaçları: İlk kez 1952 de Conti, kadavra disseksiyonlarında, ince penil arter ve venlerde polster adını verdiği yastıkçıklar göstermiş ve bu yastıkçıkların eşgüdümlü kasılama ya da gevşemesiyle ereksiyon ve detümesans olaylarının geliştiğini göstermiştir. Son zamanlarda yapılan elektron mikroskobik çalışmalar, sinüsoiadal boşlukları, arter ve ven taraflarında polstere benzer kas yastıkçıklarının bulunduğunu göstermiştir. Ancak venöz tarafta bunların gevşemesi lümeni tümüyle kapatmamakta, daralan lümen trombositlerin birikimiyle tıkanarak venöz dönüş engellenmektedir.
4. Perineal çizgili kasların kontraksiyonu: Ereksiyonun rijiditesini arttırmada venöz dönüşü engelleyerek katkıda bulunurlar. Ancak vasküler sistemi normal olanlarda bu kasılmaların olmaması, koit için yeterli ereksiyon olmasını engellemez. Kavernöz venlerin krusları adelesiz bölgen terk etmesi, bu venookklüzyonun m. Bulbokavernosus ve m. İskiokavernosusun izole kasılmalarından çok tüm perine tabanının kasılmasına bağlı olduğunu düşündürmektedir.
2.2.1 Ereksiyon evreleri
Latent (Dolum) evresi Tümesans evresi Tam ereksiyon evresi Rijid ereksiyon evresi Detumesans evresi
2.2.2 Ereksiyonun moleküler fizyolojisi
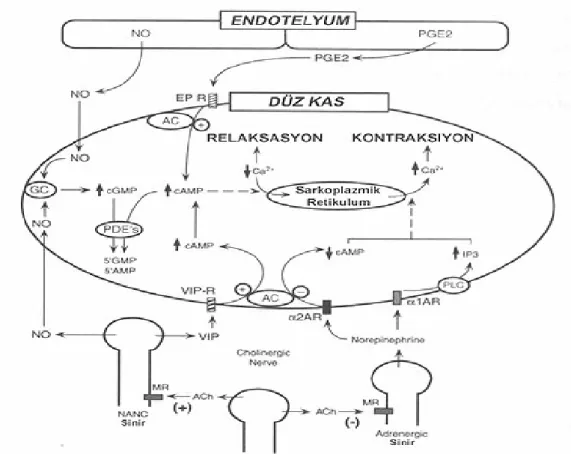
Aktin ve miyozinin (düz kasın kontraktil proteinleri) relaksasyonu ve kontraksiyonu intrakavernözal kan akımını belirler. Bu proteinlerin fonksiyonları intraseluler sitoplasmik serbest kalsiyum tarafından sıkı bir bicimde kontrol edilir (Şekil 2.4)
Nitrik oksit (NO)
Endotel hücrelerinde ve proerektil parasempatik sinir uçlarında, ortamda ko-substrat olarak moleküler oksijene ve kofaktor olarak indirgenmis NADPH, tetrahidrobiyopterin (BH4), flavin adenin dinukleotid (FAD ve flavin adenin mononukleotid (FMN)’e gereksinim duyularak NO sentaz (NOS) tarafından L-argininden sentezlenir. Fizyolojik şartlarda insanda sinir hücreleri kaynaklı (nNOS), endotel kaynaklı (eNOS), makrofaj kaynaklı (iNOS) olmak üzere 3 çeşit NOS tespit edilmiştir.
Voltaj bağımlı kalsiyum kanalları ile hücre dışından hücre içine kalsiyum girişi ve sarkoplazmik retikulumda depolanan kalsiyumun salınması ile hücre içi kalsiyum hemostazı sağlanır. Hücre içi kalsiyum yükseldiğinde, kalsiyum kalmoduline bağlanır ve bu değişiklik miyozin hafif zincir kinazı (MHZK) aktive eder. Myozinin adenozin trifosfat (ATP) ile fosforilasyonunu takiben, bu iki proteinin hafif zincirleri arasında bağlantılar (capraz kopruler) oluşmakta ve bu bağlantılar düz kasın kontraktil tonusunu sağlayacak mekanizmayı oluşturmaktadır. Siklik adenozin monofosfatın (cAMP) veya siklik guanozin monofosfatın (cGMP) akümülasyonu ya da hücre zarının hiperpolarizasyonuna yol açan potasyum kanallarının aktivasyonu ile hucre ici kalsiyum değeri dustuğunde kalmodulin kalsiyumdan ayrılır. Bu durum, miyosin hafif zincirde defosforilasyona neden olur ve aktin-miyozin ayrılması meydana gelir ve sonuç sinuzoidal düz kas hücresinin relaksasyonudur (18,19).
Şekil 2.4. Ereksiyonun moleküler fizyolojisi 2.2.3 Ereksiyonun santral kontrolü
Cinsel dürtü ile yönlendirilen seksüel aktivite döngüsü birçok santral ve periferal nöronların kontrolü altındadır. Eksitasyon, plato, orgazm, rezolüsyon olmak üzere dört fazda gerçekleşir. Santral supraspinal sistemler temel olarak limbik sistemde (olfaktor nukleus, medial preoptik alan, nukleus assumbens, amigdal nukleus, hipokampus), hipotalamus ve onun paraventrikuler ve ventromedial nukleuslarında lokalizedir (20). Hipokampus, hipotalamusun paraventrikuler nukleusu (PVN) ve medial preoptik alan (MPA) cinsel fonksiyon ve penil ereksiyon kontrolünde rol oynayan en önemli integrasyon merkezleridir (21). Sıçanlarda dorsal penil sinir uyarılarak beyindeki elektriksel aktivitenin % 80’inin MPA’da olduğu gösterilmiştir (22).
MPA’dan çıkan efferent yollar medial ön beyine ve oradan orta beyin tegmental bölgesine (substantia nigra yakınına) girer. Bu bölgelerdeki lezyonlara neden olan Parkinson hastalığı, multiple skleroz veya serebrovasküler olaylar bu iletinin bozulmasına ve bunun sonucunda erektil disfonksiyona neden olurlar (22).
Dopamin
Erektil yanıtı ortaya çıkarmakta önemli olduğu bilinen paraventrikuler nukleusta dopaminerjik yollar bulunmuştur (23). Dopamin agonisti olan Apomorfin’nin hipotalamusun paraventrikuler nukleusu ve medial preoptik alanda lokalize olan nöronları (D2>D1 nonselektif dopamin reseptor agonistleri) aktive ederek ereksiyonu uyardığı gösterilmiştir (24, 25, 26).
Serotonin
Beyin sapında medial rafe nukleusta, hipotalamus, limbik sistem, neokorteks ve medulla spinaliste yedi çeşit serotonin (5HT= 5 hidroksi triptamin) reseptörü bulunur. 5-HT-1A reseptör agonisti ereksiyonu inhibe ederken, ejekulasyonu arttırır. 2 agonistleri ereksiyonu engellerken emisyonu ve ejekulasyonu uyarır. 5-HT-2C reseptörünün stimulasyonu ise ereksiyonu uyarır (24, 27, 28).
Norepinefrin
Norepinefrin salgılayan hücreler, beynin lokus sereleus, pons ve medullasında bulunur. Bu hücrelerin, hipotalamusun paraventrikuler, supraoptik ve periventrikuler nukleuslar, talamus ve neokorteks ile aksonal bağlantıları vardır. Santral norepinefrin iletiminin cinsel fonksiyon üzerine etkisi olduğu düşünülmektedir (26).
Oksitosin
Erkek sıçanlarda hipotalamusun paraventrikuler nukleusundan ekstrahipotalamik beyin bölgesine ve spinal korda yönlenen oksitosinerjik nöronların oksitosinle uyarılması, NO sentaz aktivasyonu ile ereksiyon cevabı oluştuğu gösterilmiştir (29).
Prolaktin
Erektil disfonksiyon şikayeti olan hastalarda %1-5 oranında prolaktin yüksekliği görülür. Prolaktin seviyesinin yüksek olması LH salınımını azaltır ve sex hormon bağlayıcı globulin seviyesini düşürür. 5 α reduktaz enzimini inhibe eder. MPA’daki dopaminerjik aktiviteyi baskılar. Sonuç olarak serum testesteron seviyesini düşürür ve erektil disfonksiyona neden olur (30).
2.2.4 Ereksiyonun periferal kontrolü
Penisin nöral inervasyonu, parasempatik ve sempatik sinirler (kavernöz sinir içinde) ve somatik sinirler (pudental sinir içinde) ile sağlanır. Periferik nörojenik kontrolde adrenerjik, kolinerjik, nonadrenerjik nonkolinerjik (NANK) lifler rol alır. Helisin
arterler ve laküner boşlukları saran endotel hücreleri, sinusoidler norotransmitterleri salgılayarak penis düz kas tonusunu kontrol eder.
2.2.4.1 Kontraktil (antierektil) mediatorler: Noradrenalin (NA)
Penis düz kas kontraksiyonlarının ana düzenleyicileri α-1 adrenoreseptorlerdir. Üç alt tipi de(α-1 a-b-d) insan korpus kavernozumlarında bulunur. Noradrenalin α-1 adrenoreseptorleri; guanidin nukleotid bağlayıcı protein (G protein) aracılığı ile inositol trifosfat (IP3) ve diasilgliserol (DAG) kullanarak hücre içi kalsiyum düzeyinin artışına neden olmaktadır. Salınan NA penil damarlardaki hem α-adrenoreseptorleri hem de α-adrenoreseptorleri aktive eder. Fakat β-adrenoreseptorlerinin konsantrasyonu α-adrenoreseptorlere göre oldukça az olması nedeniyle helisin arterlerde ve korpus kavernozumda kontraksiyona neden olur (26).
Endotelin
Endotel hücreleri tarafından salgılanan, güçlü vazokonstruktor etkisi olan ve vasküler düz kasta mitojenik aktiviteyi arttıran bir peptitdir. ET-A reseptörleri vasküler düz kas hücrelerinde bulunur. Vazokonstruksiyon ve hücresel çoğalmayı indükler. ET-B reseptorleri ise endotelyal hücrelerde yer alır. Endotel bağımlı relaksan faktörler ve prostasiklin ile vazodilatasyonu sağlar (31).
Anjiotensin
Anjiotensin-1 anjiotensin konverting enzim tarafından Anjiotensin-2’ye dönüştürülür. İntrakavernözal dokuda konsantrasyonu artınca korpus kavernozumlarda kontraksiyona neden olur (32).
2.2.4.2 Relaksan (Erektil) Mediatorler Asetilkolin
Ereksiyon, S2-4 spinal segmentlerden köken alan parasempatik sinirlerdeki artmış sinirsel aktivite ile başlatılır. Preganglionik nörotransmitter olan asetilkolin; endotel hücrelerinden NO salınımını sağlar, presinaptik düzeyde adrenerjik sinir inhibisyonu yapıp muskarinik reseptörleri uyarır, noradrenalin salınımını inhibe eder böylece peniste tumesansa ve ereksiyona neden olur.
Düz kas hücrelerinde M2, endotel hücrelerinde ise M3 hâkimiyeti mevcuttur. Asetilkolin, sempatik sinirlerdeki presinaptik muskarinik reseptorler ile noradrenerjik vazokonstrüktor tonusu düzenler.
Vazoaktif İntestinal Peptid, Prostaglandinler ve diğerleri
Vazoaktif İntestinal Peptid (VIP) reseptörleri (tip1 ve 2) kavernözal dokuda yüksek konsantrasyonda bulunur. G protein aracılığı ile adenil siklazı stimule eder ve hücre içi cAMP düzeyini arttırır. cAMP, cAMP bağımlı protein kinazı aktive eder ve relaksasyon oluşturur. PGF2α, PGI2 korpus kavernosum ve korpus spongiozumda kontraksiyona, PGE1 ve PGE2 ise relaksasyona neden olur (33).
Purinerjik mekanizmalar
Düz kas P1 pürinoseptörleri adenozine yanıt vererek korpus kavernosumda gevşemeye neden olur. Endotel hücrelerinde ATP P2Y reseptörleri ile korpus kavernosumda gevşemeye neden olur (33, 34).
2.3 Priapizm 2.3.1 Tarihçe
Priapizm adını antik Yunan kültüründen bilinen ve erkeklik ve fertilitenin sembolü olan Priapus tanrısından almıştır. Priapizm çok eski zamanlardan beri bilinmekle birlikte, Yunan mitolojisi ve eski Mısır yazıtlarında adı geçmektedir (Şekil 2.5). Anadolu’da olan efsaneye göre, Olympos tanrıları arasına gelen Afrodit güzelliği ile herkesi büyülermiş, o kadar ki Zeus bile âşık olup onunla sevişmiş. Afrodit gebe kalınca, Zeus’un eşi (Hera) doğacak çocuğun babası kadar güçlü, annesi gibi güzel olmasından korktuğu için kem göz koymuş, çocuğun sakat doğmasını sağlamış. Doğan çocuğun penisi hemen hemen kendi boyu kadar ve sürekli ereksiyondaymış. Priapos kocaman bir fallos ile dünyaya gelince Afrodit oğlundan utanmış, tanrılara göstermemek için de onu kırlara bırakmış. Çobanlar bulup büyütmüşler ve erkekliğine tapınır olmuşlar. Kırlarda büyüyen priapus, tıpkı kendisi gibi toprakla büyüyen ve yetişen her şeye güç ve bereket vermiştir. Bu onu “Bereket Tanrısı” yapmış ve çok büyük olan penisi de güç sembolü haline gelmiştir (35,36,37). Eski Mısır Ebers papirüslerinde priapizmle ilgili bilgiler ve tedavi için reçeteler bulunmaktadır (38). Priapizm ilk kez 1616’da Petraens tarafından “Gonorrhoea, Satyriasis et Priapisme” başlıklı bir makalede tanımlanmıştır (39). İlk İngilizce literatür ise 1845‘te Tripe tarafından seksüel uyarı sonrasında veya bağımsız olarak gelişen, devamlı penil ereksiyon olarak tanımlanmıştır (40). Priapizm patofizyolojisi ile ilgili modern literatürde yayınlanmış ilk makale Hinman’a ait 1914 yılında
yayınlanan araştırmadır (39). Hinman priapizmi mekanik (%80) ve nörojenik (%20) olarak iki kategoriye ayırmıştır. Mekanik nedenler arasında hematolojik hastalıklar, pelvik abse, genital travma ve penil tümör, nörojenik sebepler olarakta sifiliz, beyin tümörü, epilepsi, beyin travması ve entoksikasyonlar bildirilmiştir (39). Daha sonra 1960 yılında Frank Hinman Jr. ışık mikroskopu kullanarak, korporal dokunun günler içerisinde kalınlaşarak, ödematoz ve fibrotik hale geldiğini göstermiştir (41). Spycher ve arkadaşları, elektron mikroskopunda priapizm oluşan dokuda 12. saatte sinüzoidal epitelde destrüksiyon, 24. saatte trombosit adheransı, 48. saatte sinuzoidal alanda trombüs ve düz kasta nekroz oluştuğunu bildirmişler ( 42 ).
Şekil 2.5: Toprağın bereket tanrısı Priapus (37) 2.3.2 Priapizm tanım
Priapizm tanım olarak cinsel istek, orgazm ve uyarıdan bağımsız uzamış ereksiyon halidir (1).
2.3.3 Epidemiyoloji ve etiyoloji
Priapizm, insidansı bütün yaş guruplarında 1.5/100.000’dir. Tipik olarak insidans 5-10 yaş arasında ve 20-50 yaş arasında iki kez pik yapar. Çocukluk çağında en sık neden orak hücreli anemi iken, erişkinlerde sıklıkla farmakolojik ajanlar nedeni ile priapizm gelişmektedir (38). Kumala ve ark, Fin popülasyonunda priapizm insidansını 1975- 1990 yılları süresince 0.3-1.1/100.000 arasında değiştiğini bildirmişlerdir (43). Hollanda’da Eland ve ark, toplam insidans oranını genel popülasyonda 1.5/1000.000 olarak hesaplamışlar. Kırk yaş ve üzeri için yaş spesifik insidans oranı yılda 2.9/100.000 olarak bildirilmektedir (44). Earle ve ark. Batı Avustralya da yıllık insidansı 0.84/ 100.000 olarak rapor etmişlerdir (45).
Etiyolojik faktörlerin görülme sıklığının araştırıldığı Pohl ve arkadaşlarının yaptıkları çalışmada; %40 idiyopatik, %21 ilaç tedavisi, %12 genital travma ve %11orak hücreli anemi olarak rapor edilmiştir (46).
A. İdiopatik Priapizm B. Sekonder Priapizm
• Tromboembolik patofizyoloji: Orak hücreli anemi, lösemiler, yağ embolileri, Henoch-Schonlein purpurası,
• Travmatik patofizyoloji: Perineal veya genital bölge travmalarına sekonder,
• Nörojenik Patofizyoloji: Spinal kord yaralanmaları, otonomik nöropatiler, anesteziye sekonder,
• Malign tümör penil tutulumları: Primer penil sarkomlar, renal, mesane, pulmoner, hepatik metaztazlar.
• Alkolizm, psikotik ajanlar (fenotiazin, klorpromazin), •Antihipertansifler: hydralazin, guanetidin
•Testosteron uygulamaları (52), Sildenafil sitrat (51)
•Alfa adrenerjik reseptör blokerleri: Tamsulosin (48), Doksazosin (2), Terazosin (49), Prazosin (50)
•Total parenteral nütrisyon, antidepresifler: trazodon, karbazepine, aripiprazol, ve lityum, • Bağımlılık yapıcı maddeler: Kokain, Etanol, Marihuana
•İntrakavernozal enjekte edilebilen ilaçlar: Papaverin, Prostoglandin E1, fentolamin • İnfeksiyon: prostat absesi (47).
Tablo 2.1. Priapizmde etiyolojik sınıflama 2.3.4 Priapizm Patofizyolojisi
Kavernozal dokuların iskemik hasarı erektil disfonksiyona neden olacağından dolayı priapizmin erken değerlendirilmesi ve tedavisi önemlidir. Bu nedenden dolayı priapizmin tipinin belirlenmesi hayati önem taşımaktadır.
Priapizm, patofizyolojik olarak 3 grupta incelenmektedir: 1. Düşük akımlı, iskemik, anoksik veya veno-okluziv priapizm,
2. Yüksek akımlı, non-iskemik, iyi oksijenizasyonlu veya arterial priapizm, 3. Tekrarlayan, açılıp kapanan veya “stuttering” priapizm.
1.İskemik priapizm: İskemik priapizm en yaygın tip olup; klinik olarak kavernöz
kan akımının yokluğu ile karakterize, genellikle ağrılı bir rijid ereksiyondur. Dört saatten fazla süren iskemik priapizm acil tıbbi müdahale gerektiren bir kompartman sendromudur. Kavernozal kan koyu renklidir ve kan gazı analizleri sıklıkla hipoksi (PO2<30 mmHg), hiperkapni (PCO2>60 mmHg) ve asidoz (pH<7.25) ile karakterizedir. Acil tedavi gerektirir ve non-iskemik priapizme göre prognozu kötüdür. İskemik priapizmde, kavernozal düz kasta ultrastruktural değişiklikler 12 saat sonra interstisiyel ödem olarak kendini gösterirken, 24 saate kadar sinüzoidal endotel hücre hasarı, bazal membran parçalanması ve trombosit adezyonu görülmektedir. 48 saat sonunda sinüzoidlerde trombüs gösterilirken, fibroblast benzeri hücrelerinde görülmesi düz kas nekrozunun başladığını göstermektedir. Tedavi edilmezse veya tedavide geç kalınırsa (>24 saat) kavernozal düz kaslarda nekroz, irreversibl korporal fibrozis ve erektil disfonksiyon meydana gelir (1).
Vücuttaki tüm düz kaslar istirahatte relaksasyon, fonksiyonel durumda kontraksiyon halinde bulunurlar. Bu durumun tek istisnası penistir. Penil düz kaslar istirahat halinde yani günün yaklaşık 23 saatinde kontrakte şekilde bulunurlar. Ancak penisin fonksiyonel olarak aktif hali olan ereksiyonda, düz kaslar relaksasyona uğramaktadırlar. Dolayısıyla peniste gerek tümesans, gerekse detümesans oluşmasında penis düz kas fonksiyonu etkin rol oynamaktadır. Pek çok mekanizmalarla regüle edilen penil düz kas tonusunda, kontraksiyona eğilimin artması erektil disfonksiyonla, relaksasyona eğilimin artması priapizmle sonuçlanabilmektedir. Kavernozal düz kaslarda relaksasyon sağlayan başlıca yolaklar; nitrik oksit-siklik guanozinmonofosfat (NO-cGMP) yolağı, adenozin yolağı ve hemoksijenaz 1-karbonmonoksit (HO1-CO yolağıdır. Kontraksiyonu etkileyen olası mekanizmalar ise; fosfodiesteraz tip 5 (PDE5) enzim aktivitesi, norepinefrin (NE), endotelin-1 (ET) ve Rho-kinaz cevabıdır. Penisin anatomik yapısı ve fonksiyonel özelliklerinin optimum olarak korunması için, düz kas tonusunun regülasyonunda etkili olan bu mekanizmaların dengeli bir şekilde fonksiyon
göstermesi gerekmektedir. Dolayısıyla priapizm etyopatogenezinde penis düz kas dokusunda kontraksiyonda etkin olan mekanizmalar azalmış, relaksasyonda etkin olan mekanizmalarda ise artmış bir fonksiyon beklenmektedir (53,54).
Şekil:2.6 İskemik priapizmde patofizyoloji
2-Non İskemik Priapizm: Non iskemik priapizm (arteriyel priapizm) iskemik priapizmden daha nadir gözükür. Hastalık ilk olarak 1960 yılında Burt ve ark. tarafından rapor edilmiştir (55). Her yaşta görülebilmekle beraber prepubertal dönemde nadirdir (56). Genellikle perineal veya penil künt travma, nadiren de penetran travma, penil revaskülarizasyon veya shunt cerrahisi, Nesbitt korporoplasti, transuretral cerrahi, uretral travma, vazoaktif ilaç kullanımı, kalıtsal metabolik hastalıklar (Fabry Hastalığı gibi), nörolojik/hematolojik hastalıklar (orak hücreli anemi, lösemi gibi) ve konjenital arteriyel malformasyonlar nedeniyle oluşur (57). Travma sonucu kavernozal arterde yaralanma olur ve arterio-laküner bir fistül veya fistüller oluşur. Sonuçta, kan peniste yüksek fizyolojik vasküler rezistanstan sorumlu helisin arterleri bypass ederek laküner boşluğa dolar. Aşırı kan girişi sonucu korporeal sinüsler gerilir. Kanın endotele sürtünmesi ve yüksek oksijen konsantrasyonu nedeniyle nitrik oksit (NO) sentez ve salınımı artar; arteriyel ve trabeküler dilatasyon meydana gelir (58). Subtunikal venöz kompresyon
olmadığından kan akımının bir kısmı devam eder ve parsiyel bir ereksiyon oluşur. İyileşme döneminde pıhtı ve nekrotik düz kas hücreleri ortadan kalkar ve psödokapsül oluşur. Bu süreç aylarca sürebilir. Non iskemik priapizm (Yüksek akımlı priapizm) iskemik priapizmin medikal veya cerrahi tedavisinden sonra da oluşabilmekle beraber mekanizması net bilinmemektedir (1). Muhtemel nedenleri arteriyel veya sinüzoidal yapıda yırtılma ve iskemi sonrası ortaya çıkan vazodilatatör/ vazokonstriktör faktörlerin disregülasyonudur (59). Renkli Doppler USG’de arteriolar- sinüzoidal fistül veya nadiren fistül olmaksızın kavernozal arterde yüksek akım vardır (1). Eğer bir iskemik priapizm hastasında hastalığın tedavisi sonrasında kısa sürede bir rekürrens gelişir ise, kısmi penil rijidite ile devam eden bir priapizm var ise veya ağrısız, tekrarlayan bir priapizm var ise bu yüksek akımlı priapizm alt tipinden şüphelenilmelidir (59).
3-Tekrarlayan priapizm: Tekrarlayan priapizm sıklıkla idiyopatik olan ender
görülen bir durumdur ve patofizyolojisi henüz aydınlatılamamıştır. Tekrarlayan priapizm çocuklarda sıklıkla hematolojik hastalıklar ile ilişkili iken, erişkinlerde ise genellikle idiopatiktir (62). Stuttering ataklar terimi ilk olarak Emond ve ark tarafından kullanılmıştır. Emond ve ark multipl, kendini kısıtlayıcı tekrarlayan priapizmi orak hücre hastalığı olan erkeklerde saptamışlardır (63).
İstenmeyen ağrılı ereksiyon epizodları arasında detümesans periyotları ile seyretmektedir. Sadece orak hücre anemili ( OHA) erkeklere özgü olmayıp patofizyolojisi henüz aydınlatılamamıştır. OHA’lı hastalarda genellikle priapizm tipi aralıklıdır. Dehidratasyon, ateş ve soğuğa maruziyet uzamış sabah ereksiyonuna (priapizm) neden olmaktadır (61). Uzamış ereksiyon sıklıkla uykuda başlar ve detümesans uyanmakla hemen gerçekleşmez. Mekanizması net olarak anlaşılmasa da bu hastalarda anormal noktürnal penil tümesans paterni görülebilir. Hastalar remisyon öncesi birkaç saat tekrarlayan ağrılı ataklar yaşarlar. Etkilenen genç hastalar utangaçlıktan, uyku düzensizliğinden ve performans anksiyetesinden yakınmaktadırlar (60).
2.3.5 Tanı Hikâye
Hikayede, priapizm süresi, ağrının süresi (iskemik priapizm tipik olarak ağrılıdır ve ağrı genellikle episodun ilk saatinde başlar), perineal (özellikle ata biner tarzda) veya
penil travma araştırılmalıdır. Ayrıca, travma sonrası priapizm epizodların başlaması tipik olarak birkaç gün gecikir. Priapizmin en sık nedeni yüksek dozda intrakavernozal ajanların kullanılmasıdır (papaverin, prostaglandin E1 (PgE1),
fentolamin ve benzer vazoaktif ajanlar). Uzamış ereksiyon süresi ajanın tipine ve kullanım dozuna bağlı olarak %1 ile %21 arasında değişmektedir (63,64). İlaç hikâyesi soruşturulmalıdır, anhihipertansifler, antikoagulanlar, antidepresanlar, antipisikotikler gibi birçok oral kullanılan ilaç priapizm ile ilişkili olabilir (43). Orak hücre anemisi, β talasemi gibi diğer hemoglobinopatiler, löseminin bazı formları ve total parenteral beslenme priapizme neden olabilir.
Fizik Muayene:
Non iskemik priapizmin göstergesi olabilecek yeni travmaların saptanması için genital organlar ve perine değerlendirilmelidir. Tam rijid korpus kavernozum iskemik priapizmde, semirijid bir korpus kavernozum ise non iskemik priapizmde görülmektedir. Çocuklarda detümesans ile sonuçlanan perineal kompresyon non-iskemik priapizmin habercisi olabilir (59). İskemik priapizme neden olabilen malignitenin varlığını dışlamak için abdominal ve rektal muayene yapılmalıdır.
Laboratuvar Testleri:
Korporal aspirasyon ve kan gazı analizi bütün hastalara yapılmalıdır. İskemik priapizmde kan gazı değerleri hipoksik ve asidotiktir ve aspire edilen kanın rengi hipoksi nedeniyle koyu kırmızıdır. Glukopeni ile hipoksi kombinasyonunun korpus kavernozum düz kas hücrelerinin irreversibl disfonksiyonu ile ilişkili bulunmasından dolayı kan gazı aspirasyonunda glukoz seviyesinin değerlendirmeside önerilmiştir (66). Non iskemik priapizmde kan gazı değerleri arterial kana benzerdir ve aspirasyon kanının rengi ise açık kırmızıdır. Düşük akımlı ve yüksek akımlı priapizm ayrımı tablo 2.2’de özetlenmiştir (67,38,54).
Yüksek akımlı priapizm Düşük akımlı
O2 >30 mmHg <30 mmHg
pCO2 <60 mmHg >60 mmHg
pH >7.25 ≤7.25
Ağrı - ++
Pulsasyon ++
-Palpasyon Elastik Rijid
Arteryel akım Yüksek Düşük
Venöz akım Var Yok
Viskozite Düşük Yüksek
Tablo 2.2: Düşük ve yüksek akımlı priapizmin ayırıcı tanısı (64,38,54). Radyolojik değerlendirme:
Renkli Doppler Ultrasonografi (RDU): RDU yapılması priapizmin
değerlendirmesinde kan gazı analizine yardımcı olabilir. Bununla birlikte, özellikle perineal travmalı hastalarda, kavernozal arter fistülü veya psödoanevrizma gibi anormallikleri göstermede kritik öneme sahiptir. Kavernozal kan akımı non-iskemik priapizmde sıklıkla normaldir veya biraz artmıştır. RDU İskemik priapizmde kavernozal arterlerdeki kan akım seviyesinin düşük olduğunu veya kan akımının olmadığını gösterir.
Penil arteriografi: Non iskemik priapizmli hastalarda kavernozal arterde fistül yeri
gösterilebilir ve buraya penil arteriografi ile selektif embolizasyon yapılabilir.
2.3.6 Tedavi
Priapizmli hastaların tedavisinde amaç erektil fonksiyonun korunması ve ağrının ortadan kaldırılması için detümesansın sağlanmasıdır. Priapizme neden olan olası etiyolojik faktörler müdahale edilmeden önce elde edilebilen verilere göre değerlendirilmelidir ve tedavi direkt olarak altta yatan etiyolojik faktöre yapılmalıdır. Orak hücre anemisinde, hidrasyon, alkalizasyon, transfüzyon ve oksijenasyon var olan tedavi alternatifleridir. Hematolojik malignitelerde kemoterapi ve radyoterapi priapizmin rezerve edilmesinde yardımcı olabilir (43,54,55).
2.3.6.1 İskemik priapizm tedavisi:
Spesifik tedavi öncesi, priapizmin erken evresinde, buz torbaları veya soğuk duş vazokonstriktif refleksi indükleyerek priapizmi hafifletebilir. Priapizme yaklaşımda
en az invaziv olandan başlanması (korporal kan aspirasyon) ve daha fazla invaziv olana doğru ilerlenmesi (şant prosedürleri veya penil protez implantasyonu) önerilmektedir (43).
Aspirasyon ± İrrigasyon:
Hipoksik, asidik ve glukopenik kanın aspirasyonu iskemik priapizmin rezolüsyonu için çoğu kez ilk basamaktır. İskemik priapizmde, 19 G kelebek iğne ile 20 ml kan aspire edilmeli ve aspirasyon enjektörde açık kırmızı kan gözlemlenene kadar sürdürülmelidir. Diğer taraftan, hipoksik kanın temizlenmesi için izotonik ile irrigasyon yapılabilir. İrrigasyonlu veya irrigasyonsuz aspirasyonun etkisi yaklaşık olarak %30’dur (54). Rezolüsyonun sağlanması için 5 dk. beklenmesi önerilir. Eğer detümesans sağlanmazsa intrakavernozal ajanlar kullanılabilir.
İntrakavernozal ajanlar:
Epinefrin, norepinefrin, fenilefrin, efedrin ve metaraminol intrakavernozal injeksiyon için kullanılan alfa adrenerjik ajanlardır. İskemik priapizmli hastalarda başarı oranları epinefrin, metaraminol, norepinefrin, ve fenilefrin için sırasıyla %81, % 70, %43, %65 olarak rapor edilmiştir (54). Fenilefrin epinefrin ile karşılaştırıldığında etkisinin daha düşük olmasına karşın, minimal kardiovasküler riski nedeniyle intrakavernozal injeksiyon için tercih edilen ajan olmalıdır. Eğer bir saat içinde detümesans tekrarlayan alfa adrenerjik ajanların intrakavernozal injeksiyonu ile sağlanamazsa, cerrahi tedavi seçenekleri düşünülmelidir. Tablo 2.3’te priaizm tedavisinde kullanılabilecek çeşitli ilaçlar ve dozları verilmiştir.
İlaç Doz
İntrakavernozal uygulama
Epinefrin 0.03-0.05 mg Etilnefrin 2-20 mg Fenilefrin 0.1-1 mg Norepinefrin 0.01-0.02 mg Metilen mavisi 50 mg İntravenöz/oral uygulama Dopamin 2-4µg/kg i.v.
Terbütalin sülfat 5 mg oral
Ketamin hidroklorür 1 mg/kg i.v. veya i.m.
Tablo 2.3. Priapizm tedavisinde kullanılabilecek çeşitli ilaçlar, dozları ve uygulama
yöntemleri (67,54).
Cerrahi tedavi:
İskemik priapizmin cerrahi tedavisi ile korpus kavernozumda birikmiş eski kanın drenajı için yeni yollar oluşturarak detümesansın sağlanması amaçlanmaktadır. Distal şantlar (Winter, Eb-behoj, Al-Ghorab) baslangıçta cerrahi prosedür olarak tercih edilmelidir. Eğer bu yöntemlerle başarı sağlanamaz ise, proksimal şant (Quackel, Grayhack) prosedürleri uygulanabilir. Winter, Ebbehoj, Al-Ghorab Distal şant prosedürleri için başarı oranları sırasıyla %66, %73 ve %74 olarak rapor edilmiştir. Proksimal şantlar olan Quackel şantları için %77 iken Grayhack için bu oran %76’dır (54). Korporal aspirasyon ve intrakavernozal adrenerjik ajan enjeksiyonu ile priapizm süresi 12 saatten az olan olguların hepsinde, 12-24 saat arasında olanların %78’inde ve 24-36 saat arasında olanların %44’ünde erektil fonksiyonun spontan olarak ya da sildenafil ile korunabildiği bildirilmiştir. Ancak 36 saatten uzun süren ataklarda, erektil fonksiyonun hiç bir hastada korunamadığı vurgulanmıştır (3). Priapizm tedavisindeki başarısızlık önemli kavernozal fibrozise neden olmakta ve buda daha sonra yapılacak olan penil protez implantasyonunu yüksek istenmeyen yan etki oranları nedeniyle zorlaştırmaktadır. Bunun sonucu olarak, son zamanlarda iskemik priapizm tedavisinde erken dönemde penil protez implantasyonu önerilmiştir (68).
2.3.6.2 Non iskemik priapizm tedavisi:
bildirilmektedir (43). Tıbbı acil bir durum olmadığından bu hastalar konservatif kalınarak takip edilebilir ve rüptür yerlerin kendiliğinden kapanması beklenebilir (69,70). Detümesansa ulaşmak için, erken dönemde vazospazma ve lazere arterin tromboze olmasına neden olabilecek buz veya baskı torbaları yardımcı olabilir (71). Olguların yaklaşık yarısında hastalığın kesin tedavisi arterio-sinusoidal fistülün selektif anjiyografik embolizasyonudur. Non-iskemik priapizmin emici ve emici olmayan gereçler ile rezolüsyon ve ED oranları sırasıyla 78%, 39% ve 74%, 5% olarak rapor edilmiştir (54). Anjiyografik girişim sonuçsuz kalırsa tekrar embolizasyon yapılabilir veya son olarak rüptüre arterin intraoperatif renkli Doppler ultrasonografi yardımıyla açık cerrahi ligasyonu gerekebilir.
2.3.6.3 Tekrarlayan priapizm tedavisi:
Tekrarlayan priapizmli hastalarında tedavinin amacı iskemik priapizm episodlarının spesifik tedavilerini yapmak ve yeni priapizm episodlarını önlemek için bazı önlemler almaktır. Priapizmi önleyici tedaviler için antipisikotik ilaçlar, ağızdan etilefrin, dietilstilbestrol, baklofen terbutalin, antiandrojenler ve gabapentin ve digoksin kullanılmıştır (72,73).
2.4 İskemi ve Reperfüzyon 2.4.1 Mekanizmalar
Bir dokuya giden kan akımı kesildiğinde, o dokuda hücrelerin fonksiyon bozukluğu ile başlayan ve hücre ölümüne kadar ilerleyen bir dizi kimyasal olay gerçekleşir. Hücresel fonksiyonların gerçekleşebilmesi için gerekli temel yakıt oksijendir. Normal hücre fonksiyonları için gerekli olan yüksek enerjili fosfat bağları aerobik metabolizma ile sağlanır. Oksijen yetersizliği durumunda anaerobik metabolizma devreye girer. Bu da laktik asit ve toksik metabolitlerin birikimi ile sonuçlanır. Ortaya çıkan asidoz nedeniyle normal enzim kinetiği değişir ve yüksek enerjili fosfat bağlarının yapımı azalır. Bu durumda hücre kendi homeostazı için gerekli olan enerjiden yoksun kalır (74).
Hücresel homeostaz için gerekli olan enerji kaynaklarının, özellikle ATP’nin tüketimi, hücre membranında iyon dengesizliğine yol açar. Na+ ve Ca++ iyon dengesi bozulur. Oksijen seviyesi düştüğünde oksidatif fosforilasyon sona erer ve
hücrede enerji üretimi glikoliz ile sağlanır. Glikojen depolarının tüketilmesi ise laktik asit ve inorganik fosfatların birikimi ile sonuçlanır. Mitokondrial fonksiyon bozulur, hücre membran permeabilitesi artar. Hücrenin ana hatları; ultra strüktürel özelliklerinin kaybı ve hücre yüzeyinde kabarcıkların oluşumu ile bozulur. Osmotik regülasyonun kaybı nedeniyle hidropik dejenerasyon – vakuoler dejenerasyon izlenir. Hücre çekirdeğinde kromatin kümelenmesi ve piknozis gibi histolojik bulgular görülür (74,75,76,77).
Reperfüzyon, iskemiye neden olan etkenin ortadan kaldırılarak dokuya kan akımının yeniden düzenlenmesidir. Reperfüzyonun, dokuda iki önemli etkisi vardır. Bunlar iskemik dokuda enerji ihtiyacının sağlanması ve toksik metabolitlerin uzaklaştırılmasıdır. Böylece reperfüzyon iskemik hasarın düzeltilebilmesi için gerekli bir süreçtir. Ancak oksijenlenmiş kanın iskemik dokuya dönüşü dokuyu daha fazla zedeleyen bir reaksiyon sürecini başlatır (74). Reperfüzyon hasarı serbest oksijen radikalleri, endotelial faktörler ve nötrofillerin eşlik ettiği karmaşık bir mekanizmayla gerçekleşir.
Reperfüzyon hasarına doğrudan veya dolaylı olarak katılan pek çok madde ve biyokimyasal reaksiyon tanımlanmıştır. Bu maddelerin birbiriyle etkileşimi sonucunda iskemi reperfüzyon hasarının reperfüzyon kısmının mediatörleri olan serbest oksijen radikalleri ortaya çıkar. İskemi reperfüzyonun yol açtığı mikrovasküler hasar için nötrofil ve endotel ilişkisi gerekmektedir. İskemi sırasında ve daha ağırlıklı olarak bunu takip eden reperfüzyon döneminde postkapiller venüllerde endotele artmış nötrofil adhezyonu görülür. Araşidonik asit metabolitleri, özellikle lökotrienler kapiller permeabiliteyi ve lökositlerin endotele adezyonunu arttırırlar. Endotele giderek artan ilgiyle bağlanan lökositler, lizozimleri aktive eder, reaktif oksijen radikalleri üretir ve diğer lökositler için kemotaktik ajanlar salınmasına neden olur. İskemi ve reperfüzyon sürecinde aktive olan lizozim proteolitik enzimlerin salınmasını sağlarken Fosfolipaz A2 hücre membran lipidlerini araşidonik aside dönüştürür. Araşidonik asit lökotrienler ve prostaglandinler gibi inflamatuar mediatörlerin prekürsörüdür (4).
Serbest radikaller, en dış yörüngesinde tek sayıda elektron içeren, ileri derecede reaktif, kısa ömürlü ve stabil olmayan moleküllerdir. Moleküler oksijenin indirgenmesi ve uyarılması ile çok değişik oksijen serbest radikalleri üretilebilir (5). Oksijenin redüksiyonu ve aerobik hücrelerin enzimatik oksidasyonu sırasında negatif yüklü bir ara ürün olan süperoksit radikali (O2¯) oluşur. Süperoksit radikalinden enzimatik yolla veya spontan dismutasyonla ikinci bir ara ürün olan hidrojen peroksit radikali (H2O2) oluşur. Daha sonra özellikle mitokondride diğer bir ürün olan hidroksil radikali (OH¯) oluşur (Şekil 1). Diğerleriyle karşılaştırıldığında O2¯ radikali yüksek elektron aktivitesine sahiptir ve çok reaktiftir. Ancak oksijen radikallerinden en aktif olanı OH¯ radikalidir. Lipid peroksidasyonu, sulfidril grupların oksidasyonu ve membran potansiyellerinin indirgenmesi gibi etkilerden başlıca sorumlu olan radikaldir (74,4).
Hücreler serbest oksijen radikallerinin hasarına bağışık değildir. Ancak genellikle glutatyon ve katalaz gibi endojen etkenler ile oksijen hasarına karşı korunmuşlardır. İskemik dokularda, serbest oksijen radikali üreten intraselüler mekanizmalar tam aktive edilmiş durumdadır. Ancak oksijen sağlanmasındaki eksiklikten dolayı fonksiyon görmezler. Kan akımı ve oksijen sağlanmasının restorasyonu ile büyük miktarlarda serbest oksijen radikali üretilerek reperfüzyon hasarı indüklenir. Organizmada serbest oksijen radikalleri ortaya çıktıktan sonra radikal reaksiyon dizileri başlar. Eğer bir serbest radikal, radikal olmayan bir molekülle reaksiyona girerse, binlerce reaksiyondan oluşan reaksiyon zincirlerini başlatır. Serbest oksijen radikalleri paylaşılmamış elektronlarından dolayı lipid, protein, karbonhidrat, nükleik asit gibi çeşitli makromoleküllerin oksidatif hasarına neden olurlar (4,5).
2.4.2.1 Serbest radikal türleri
2.4.2.1.1 Reaktif Oksijen Türleri (ROS)
Oksijen doğada dioksijen olarak bulunan kararsız bir elementtir. Bu kararsız yapısını giderebilmek için başka bir oksijen atomunun dış yörüngesindeki iki elektronu ortaklaşa kullanarak “Oksijen Radikalleri”ni oluşturur (78).
Radikaller Radikal Olmayanlar
Hidroksil (HO) Alkoksil (RO) Peroksil (ROO)
Hidrojen Peroksit (H2O2) Singlet Oksijen (O2) Ozon (O3)
Superoksit (O2) Nitrik oksit (NO) Azot dioksit (NO2)
Hipoklorid (HOCl)
Lipid hidroperoksit (LOOH) Peroksinitrit (ONOO) Tablo 4. Oksijen türevi bileşikler
Süperoksit Radikalleri (O2)
Süperoksit radikali, hemen tüm aerobik hücrelerde oluşan, indirgen ve orta derecede yükseltgen olan bir ajandır. Esas önemi, hidrojen perokside kaynaklık etmesi ve geçiş metal iyonlarının indirgeyicisi olmasıdır. Uzun bir yarı ömre sahip olup, lipofilik özellik gösterir. Bu özelliğinden dolayı da oluştuğu yerden uzak bölgelere difüzyonla yayılabilmektedir. Ancak doğrudan doğruya hasar yapıcı etkisi çok fazla değildir (79).
Hidrojen Peroksit (H2O2)
Hidrojen peroksit, süperoksit dismutaz tarafından katalizlenen dismutasyon reaksiyonu sonucu ortaya çıkar. İki süperoksit molekülü iki proton alarak H2O2ve moleküler oksijeni oluştururlar. Reaksiyon sonucu radikal olmayan ürünler meydana geldiğinden bu bir dismutasyon reaksiyonu olarak bilinir.
H2o2 membranlardan geçebilen uzun ömürlü oksidandır. Kendisi eşleşmemiş elektronu olmadığından bir serbest radikal olarak kabul edilmediği halde, reaktif oksijen türleri içine girer ve serbest radikal biyokimyaşında önemli bir rol oynar. Geçiş metal iyonları varlığında daha da hızla gerçekleşen bir reaksiyonla süperoksit anyon radikali ile birlikte en reaktif radikal olan hidroksil radikalini oluşturur (80).
Hidroksil Radikalleri (HO.)
Hidroksil radikali (HO.), biyolojik sistemlerde bulunan en güçlü serbest radikaldir. Hidroksil radikali, hidrojen peroksitin geçiş metalleri varlığında indirgenmesi ile oluşan son derece reaktif bir radikaldir. Ayrıca hidrojen peroksitin süperoksit radikali ile reaksiyonu sonucunda da meydana gelir. OH. radikalleri başta lipid, protein ve nükleik asitler (DNA ve RNA) olmak üzere hemen hemen bütün hücresel moleküllerle reaksiyona girebilmektedirler.
Singlet Oksijen (O2↑↓)
Singlet oksijen, ortaklanmamış elektronu olmadığı için radikal sayılmamıştır ancak serbest radikal reaksiyonlarını başlattığı için radikal sınıfına sokulan reaktif oksijen molekülüdür. Oksijenin yüksek enerjili ve mutajenik formudur(81)
Hipoklorik Asit (HOCI)
Hipokloröz asit radikal olmadığı halde reaktif oksijen türleri (ROS) içinde yer almaktadır. Fagositik hücrelerin bakterileri öldürülmesinde önemli rol oynarlar. Aktive olan nötrofiller, monositler, makrofajlar ve eozinofiller süperoksit radikallerini üretirler.
2.4.2.1.2 Reaktif Nitrojen Türleri (RNS (NO, NO2, NO+, NO ) )
Düşük konsantrasyonlarda iken, ortamda oksijen varlığında dahi stabilitesini koruyabilen NO, bilinen en düşük molekül ağırlıklı, biyoaktif memeli hücresi sekresyon ürünüdür Diğer radikallerden farklı olarak düşük dozlarda toksik değildir ve çok önemli fizyolojik işlevleri gerçekleştirir NO. bir atom azot ile bir atom oksijenin çiftleşmemiş elektron vererek birleşmesinden meydana gelmiştir ve bu yüzden radikal tanımına uymaktadır (82). Bu lipofilik serbest radikal damar endotel hücrelerinde Nitrik Oksid Sentaz (NOS) enzimi aracılığıyla L-arjininden sentezlenir.
2.4.2.2. Başlıca Serbest Radikal Üretim Kaynakları
Serbest radikaller organizmada normal olarak meydana gelen oksidasyon ve redüksiyon reaksiyonları sırasında oluştuğu gibi çeşitli dış kaynaklı etkilerin etkisiyle de oluşabilir. Hücre organellerinin her biri farklı miktarda radikal oluşumuna sebep olurlar. Bunların yanı sıra radyasyon, stres ve ksenobiyotikler aktive olmuş fagositlerde serbest radikal üretimini arttırırlar. Sitokrom P450, sitokrom b5, ksantin oksidaz, triptofan dioksijenaz, lipooksijenaz, prostoglandin sentetaz, hemoglobin, flavoproteinler, lipid peroksidasyonu, oksidatif stress yapan iskemi, travma ve intoksikasyon gibi durumlar, mitokondrial elektron transport sistemi (ETS), moleküler otooksidasyon yapan tiol, hidrokinon, katekolamin, flavin ve antibiyotik gibi moleküllerin hepsi hücresel serbest radikalleri oluştururlar (83,84) . Serbest radikal oluşturan kaynaklar endojen ve ekzojen olmak üzere iki gruba ayrılabilir.
Endojen Serbest Radikal Üretim Kaynakları
Normal olarak metabolizmada, bazı biyokimyasal olayların çeşitli basamaklarında serbest radikaller oluşmaktadır. Her ne kadar serbest radikal yapısına sahip maddelerin organizmaya zarar verme potansiyelleri varsa da, bazı metabolik olayların ilerleyebilmesi için bunların oluşması kaçınılmazdır.
Serbest radikaller, ekzojen nedenlerle de oluşabilir. Radyasyon, sigara dumanı, zehirli gazlar, bazlaçlar, kanserojen maddeler ve pestisitler en önemli ekzojen serbest radikal üretim kaynakları olarak bilinirler (85).
2.4.2.3. Serbest Radikallerin Vücuttaki Etkileri Serbest Radikallerin Lipitlere Etkileri
Serbest radikallerin hücrede başlattığı en önemli ve zararlı etki lipid peroksidasyonudur. Çoklu doymamış yağ asitlerinin serbest radikaller ile oksidasyonu lipid peroksidasyonu olarak tanımlanır. Lipid peroksidasyonu, organizmada oluşan kuvvetli yükseltgen bir radikalin etkisiyle membran yapısındaki çoklu doymamış yağ asidi zincirindeki alfa metilen gruplarından bir hidrojen atomunun uzaklaştırılması ile başlamaktadır. Biyolojik sistemlerde bu radikalin süperoksid ile hidroksil radikalinin olduğu kabul edilmektedir. Yağ asidi, zincirinden bir hidrojen atomunun uzaklaştırılması sonucu zincir radikal niteliğini kazanır. Bunun sonucunda oluşan radikal alkil radikali olup dayanıksız bir türevdir ve bir dizi değişikliğe uğrar. Özellikle molekül içi çift bağ aktarılması ile dien konjugatları ve daha sonra lipid radikalinin moleküler oksijenle etkileşimi sonucunda lipid peroksid radikali (LOO-) oluşur. Lipid peroksid radikali zar yapısındaki diğer çoklu doymamış yağ asitlerini etkileyerek lipid hidroperoksit (ROOH) ve yeni bir alkil radikali oluşturur (86,79).
Lipid peroksidasyonu biyolojik membranlarda akıcılığın kaybına, membran potansiyelinde azalmaya, hidrojen ve diğer iyonlara karşı geçirgenliğin artışı neticesinde hücrenin hasarına ve içeriğinin serbestleşmesine neden olur. Lizozomal ve mitokondrial membranların etkilenmesi ile organel içi enzimler hücre içine salınır. Lizozomal proteolitik enzimlerin sitoplazmaya salınması ile proteoliz hızlanır, doku hasarı şiddetlenir. Membran geçirgenliğinin bozulması ile membran elektrolit dengeleri değişir ve protein sentezi inhibe olur (79).
Lipid peroksidasyonu sırasında, karbon bağların kopması ile aldehid yapıda yıkım ürünleri oluşmaktadır. Malondialdehit (MDA) membran bileşenlerinin polimerizasyonuna ve çapraz bağ yapmalarına yol açar. Bu da, hücre yüzeyinin durumunu, enzim aktivitesini, iyon transportunu etkiler (86). Malondialdehit (MDA benzeri, tiyobarbitürik asit ile reaksiyon veren maddeler (TBARS) lipid
peroksidasyonunun dolayısıyla iskemi reperfüzyon hasarının en duyarlı göstergelerindendir (79).
Serbest Radikallerin Proteinlere Etkileri
Serbest radikallerin aminoasitler ile etkileşimi sonucu hücrenin protein yapıları hasar görmektedir. Protein oksidasyonunun kimyasal sonucu olarak metionin sülfokside, histidin oksihistidine veya aspargine, tirozin ditirozine ve sistein disülfitlere dönüşür. Enzim veya reseptör fonksiyonuna sahip membran proteinleri serbest radikallere daha duyarlı oldukları için meydana gelen değişiklikler proteinlerin bağlanma özelliklerinde ve enzim aktivitelerinde farklılaşmaya neden olarak hücre fonksiyonlarında bozulmalara yol açar (86).
Serbest radikallerin DNA’ya etkileri
Serbest oksijen radikalleri nükleotid yapısı içinde yer alan adenin ve guanin ile etkileşime girerek DNA’nın yapısını değiştirebilir ve mutasyonlara yol açabilir(87).
2.4.3. Antioksidan savunma sistemleri
Reaktif oksijen türlerinin oluşumunu ve bunların meydana getirdiği hasarı önlemek için vücutta “antioksidan savunma sistemi” adı verilen birçok savunma mekanizmaları gelişmiştir. Bütün hücreler güçlü savunma sistemlerinin varlığı ile oksidatif strese karşı savaşmaktadırlar. Savunma sistemlerini serbest radikal tutucuları ve bazı enzimler oluşturmaktadır ve savunma sisteminde öncelikle enzim sistemi etkili olmaktadır(88).
2.4.3.1. Enzimatik antioksidanlar
Serbest radikalleri, biyolojik önemi olan moleküllerle etkileşmeden önce daha zararsız bileşiklere dönüştürerek veya başka moleküllerden radikal üretimini engelleyerek etkilerini gösterirler (89,86).
Süperoksit dismutaz
Süperoksid radikalinin hidrojen peroksit ve moleküler oksijene dönüşümünü katalizler, böylece hücre içinde süperoksid radikal düzeyi azaltılır (90,91).
2O2- + 2H+ ---> 2H2O + O2
Katalaz
Hidrojen peroksidi oksijen ve suya parçalayan reaksiyonu katalizler. Katalaz enzimi peroksizomlara yerleşmiştir, peroksidaz aktivitesi vardır ve hidrojen peroksit gibi küçük moleküllere etki ederken lipid hidroperoksitlere etki etmez (5).
2H2O2 ---> 2H2O + O2
Sitokrom oksidaz
Süperoksid radikalininin suya dönüşümünü sağlar (89). 4O2- + 4H+ + 4e- ---> 2H2O
Glutatyon peroksidaz:
Hidrojen peroksid ve organik hidroperoksitlerin (ROOH) indirgenmesini sağlayan reaksiyonları katalizler (79).
H2O2 + 2GSH ---> GSSG + 2H2O
ROOH + 2GSH ---> GSSG + ROH + H2O
Glutatyon transferazlar
Sitozolde bulunur ve yabancı maddelerin glutatyon ile konjugasyonunu katalizleyere biyotransformasyonunu sağlar.
R-X + GSH ---> GS-R + HX
2.4.3.2. Enzimatik olmayan antioksidanlar Vitamin C (Askorbik Asit):
Lipid peroksidasyonunu başlatıcı radikalleri temizleyerek lipidleri ve membranları oksidatif hasara karşı korur (92).
Vitamin E (α-Tokoferol):
Lipid peroksitlerini etkisizleştirerek peroksidasyon zincir reaksiyonunu sonlandırır. Membran fosfolipidlerinin yapısındaki çoklu doymamış yağ asitlerini serbest radikallerin etkisinden korur (79,93).
Melatonin:
Melatonin en zararlı serbest radikal olan hidroksil serbest radikalini ortadan kaldıran çok güçlü bir antioksidandır.
β -Karoten (Vitamin A ön maddesi)
β-karoten yağda çözünen bir antioksidan olarak serbest radikaller biyolojik hedeflerle interaksiyonuna girmeden önce direkt olarak onları yakalayabilir ve aynı zamanda zincir kıran bir antioksidan olarak etki ederek de peroksit radikalleri oluşumunu önler (94).
Seruloplazmin, albumin, ürik asit, bilirubin, sistein, transferin ve laktoferrin diğer antioksidanlardır.
2.5 CURCUMİN (TURMERIC)
Turmeric (Curcuma longa), zencefil ailesine ait çok yıllık otsu bir bitkidir. Bu bitkinin köklerinden elde edilen turmerik Hindistan'da yüzyıllardır yaygın olarak kullanılmaktadır ve yaygın olarak güney ve güneydoğu tropikal Asya’da yetiştirilmektedir. Turmeric’in aktif bileşeni olan curcumin, baharatın %2 ile %5’ini oluşturmaktadır. Curcuminden dolayı sarı renk karakterindeki Turmeric, ilk kez 1842 yılında Vogel tarafından izole edilmiştir. Curcumin neredeyse su içerisinde hiç çözünmeyen turuncu-sarı kristal gibi bir tozdur (95,96). Curcumin (diferuloylmethan) portakal sarısı rengi ile gıda boyası olarak da kullanılmaktadır. Çok iyi bilinen ve sıklıkla kullanılan köri baharatının ana komponentidir. Curcuminin antioksidan özelliğinin yanı sıra antiinflamatuar, immunomodulatuar, antitümoral ve antipsöriyatik etkinliği gösterilmiştir (7).
ŞEKİL 2.7 Curcuminin kimyasal yapısı (95) 2.5.1 Metabolizması
Curcumin suda çözünmez, hücre membranının hidrofobik ceplerinde lokalize olur. Curcumin moleküler özellikleri nedeniyle hücrelere hızlıca penetre olmakta, plazma membranından kolayca geçerek sitozole girmektedir. Stoplazmada biriken Curcumin çekirdeğe girmez. Lipofilik özelliklerinden dolayı plazma membranı, endoplazmik retikulum ve çekirdek kılıfı gibi memranöz yapıların içinde yoğunlaşmaktadır. Curcumin dolaşımda çok düşük düzeyde veya hiç bulunmamaktadır (97). Curcumin bağırsaklardan emilimi sırasında renksiz ve daha az polar olan tetrahidrocurcumin adlı metabolitine dönüşmektedir. Tetrahidrocurcumin bağırsaklardan emilerek tüm dokulara dağılmaktadır. Tetrahidrocurcumin karaciğerde glukuronlanarak safra yolu