Oksijen konsantrasyonunun implantasyon öncesi embriyo gelişimi ve gebelik oranı üzerine etkisi
Tam metin
Şekil
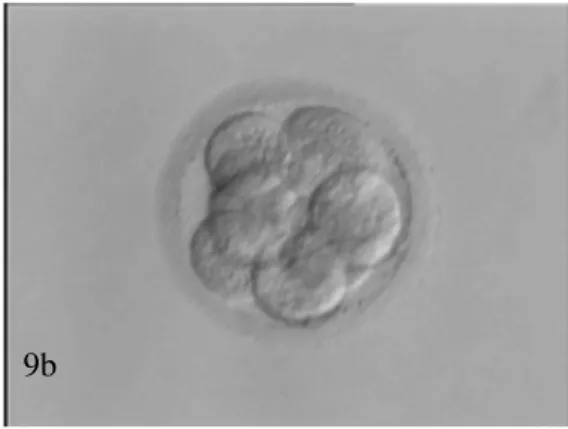


Benzer Belgeler
2-) Elif okula ulaştığında saat 08.30 ‘dur. Ev ile okul arasındaki uzaklık 40 dakika sürdüğüne göre Elif evden saat kaçta çıkmıştır?. 3-) Karagöz ile Hacivat
Yoğun tanıtım çalışmalarının gerçekleştirildiği 2011 yılında toplam geceleme sayısında bir önceki yıla göre %12 düzeyinde bir artış kaydeden Altın Yunus’un
Halk GYO (HLGYO, EÜ, Fiyat:0.96TL, Piyasa Değeri TL758mn): Halk GYO, Halk Bankası ile Ataşehir Finans Kule binası için kira sözleşmesini 01.04.2017 tarihinden itibaren geçerli
İSKİ Genel Müdürlüğü’nden alınan bilgiye göre; son üç günde yağan yağmur, barajlardaki doluluk oranını 2 milyon metreküp art ırdı.. İstanbul’un günde 2
Phileas Fogg, oyunda yirmi bin İngiliz sterlini kazandıktan sonra saat yediyi yirmi beş geçe arkadaşlarından izin isteyip Reform klüpten ayrıldı.. Uşak, Bay Fogg’un
— Türkiye Cumhuriyeti Hükümeti ile Özbekistan Cumhuriyeti Hükümeti Arasında Hava Taşımacılığı Anlaşmasının Onaylanmasının Uygun Bulunduğuna Dair Kanun Tasarısı
Öğretim Yaklaşım, Strateji, Yöntem Ve Tekniklerinin Kullanıldığı Öğrenme
108 günlük felç devresinin ardından 3 Temmuz 2020’de açılmasına izin verilen sinema işletmeleri, 10 Eylül 2020’ye dek tamamlanan on haftada 300.230 adet bilet satışı