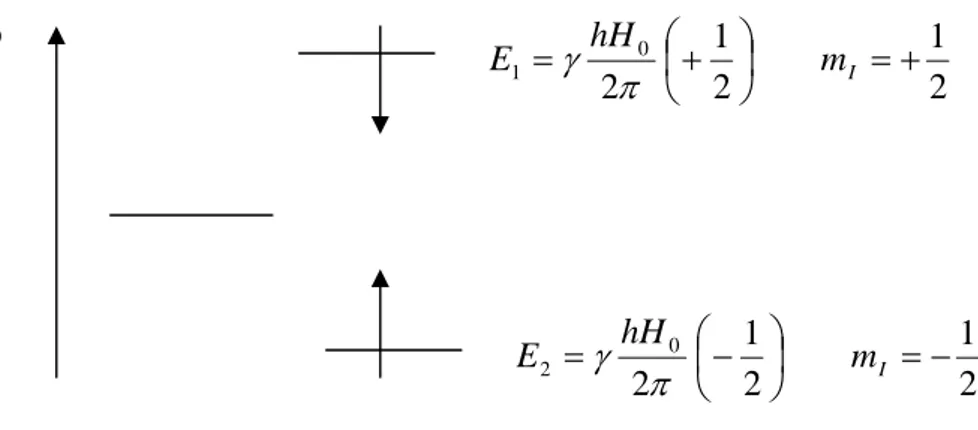FEN BĠLĠMLERĠ ENSTĠTÜSÜ
BAZI MOLEKÜLLERĠN NMR PARAMETRELERĠNĠN HF POST HF VE DFT METOTLARI ĠLE
HESAPLANMASI
Halil Uğur TAġDEMĠR Yüksek Lisans Tezi
Ortaöğretim Fen ve Matematik Alanlar Eğitimi Fizik Eğitimi A.B. Dalı
ORTAÖĞRETĠM FEN VE MATEMATĠK ALANLAR EĞĠTĠMĠ FĠZĠK EĞĠTĠMĠ ANABĠLĠM DALI
BAZI MOLEKÜLLERĠN NMR PARAMETRELERĠNĠN HF POST HF VE DFT METOTLARI ĠLE
HESAPLANMASI YÜKSEK LĠSANS TEZĠ
HAZIRLAYAN
Halil Uğur Taşdemir
DANIġMAN
Yrd. Doç. Dr. Ercan TÜRKKAN
ÖZET
YÜKSEK LİSANS TEZİ
BAZI MOLEKÜLLERİN NMR PARAMETRELERİNİN HF POST HF VE DFT METOTLARI İLE HESAPLANMASI
Halil Uğur TAŞDEMİR Selçuk Üniversitesi Fen Bilimleri Enstitüsü
Fizik Anabilim Dalı
Danışman: Yrd. Doç. Dr. Ercan TÜRKKAN 2010, 105 Sayfa
Bu çalışmada glioksim molekülünün ve dimetil glioksim molekülünün konformasyon analizi yarı deneysel metot olan PM3 metodu ile yapılmıştır. Ortaya çıkan konformasyonlar B3LYP/ 6-311G++(d,p) metot ve baz seti kullanılarak optimize edilmişlerdir. Optimizasyon sonucunda en kararlı yapıların (anti-, amphi- ve syn-) NMR parametreleri GIAO yöntemi ile Hartree Fock(HF), Moller Pleasent (MP2), Density Functional Theory (DFT) metot ve 31g(d,p), 31+g(d,p), 6-31++g(d,p), 6-311g(d,p), 6-311+g(d,p), 6-311++g(d,p) baz setleri kullanılarak hesaplanmıştır. Hesaplanan NMR parametreleri ile deneysel NMR parametre değerleri ile karşılaştırılarak glioksim ve dimetil glioksim moleküllerinin yapı analizleri yapılmıştır.
ABSTRACT Master Thesis
CALCULATION OF NMR PARAMETERS OF SOME MOLECULES USING HF, POST HF AND DFT METHODS
Halil Uğur TAŞDEMİR Selcuk University
Graduate School of Natural and Applied Sciences Department of Physics
Supervisor: Asst. Prof. Dr. Ercan TÜRKKAN 2010, 105 Pages
In this study conformational analysis of glyoxime (GO), and dimethyl-glyoxime (DMG) molecules have been carried out with semi-empirical PM3 method. Geometries of conformers have been optimized using B3LYP method and 6-311++G(d,p) Gaussian basis sets. NMR parameters calculations of the most stable structures of the calculated optimized structure (anti-, amphi-, syn-) carried out with GIAO method and Hartree Fock (HF), Moller Pleasent (MP2), Density Functional Theory (DFT) method and using 6-31g(d,p), 6-31+g(d,p), 6-31++g(d,p), 6-311g(d,p), 6-311+g(d,p), 6-311++g(d,p) basis sets. The structure analysises of Glyoxime and Dimethy glyoime molecules have been done using calculated NMR parameters and experimental NMR results.
ÖNSÖZ
Bu tez çalışması S.Ü. Ahmet Keleşoğlu Eğitim Fakültesi Fizik Öğretmenliği Bölümü Öğretim Üyelerinden Yrd. Doç. Dr. Ercan Türkkan yönetiminde hazırlanarak, S.Ü. Fen Bilimleri Enstitüsü’ne yüksek lisans tezi olarak sunulmuştur.
Öncelikle yüksek lisans çalışmalarım süresince bana desteğini hiçbir zaman esirgemeyen, ilgi, alaka ve sabrıyla her zaman beni çalışmalarıma motive eden çok değerli danışmanım Yrd. Doç. Dr. Ercan TÜRKKAN’ a teşekkürü bir borç bilir, saygılarımı sunarım.
Tez çalışmalarım esnasında bilgi ve tecrübelerini benimle paylaşmaktan çekinmeyen, hesaplamalarda yadımlarını esirgemeyen çok değerli Hocam Yrd. Doç. Dr. Ömer DERELİ’ye sonsuz teşekkürlerimi sunarım. Ayrıca oxim bileşiklerinin sentezinde ve NMR ölçümlerinde yardımlarını esirgemeyen Öğr. Gör. Fatih SEVGİ ye teşekkürlerimi bir borç bilirim. Bununla birlikte maddi, manevi hiçbir destekten kaçınmayan biricik aileme çok teşekkür eder, saygılarımı sunarım.
İÇİNDEKİLER
ÖZET………ii
ABSTRACT………iii
ÖNSÖZ………iv
KISALTMALARIN LİSTESİ………vii
ŞEKİL VE TABLOLARIN LİSTESİ………viii
1. GİRİŞ………... ….1
2. NÜKLEER MANYETİK REZONANS TEMELLERİ………4
2.1. Çekirdeğin Spin Kuantum Sayısı………...4
2.2. Atom Çekirdeklerinin Manyetik Alanda Davranışı………...5
2.3. Manyetik bir Dipolün Manyetik Alanda Enerjisi………..7
2.4. Rezonans Olayı ve Rezonans Koşulu………8
2.5. Enerji Seviyelerinin Dağılımı………..10
2.6. Durulma Olayı……….11
2.7. Kimyasal Kayma………..12
2.8. Pik Yerlerinin Belirlenmesi ve NMR Spektrumlarında Skala………14
2.9. 13C NMR spektroskopisi………..18
2.9.1. 1H ve 13C Çekirdeklerinin Karşılaştırılması……….18
2.9.2. 13C Çekirdeklerinin Duyarlılığını Etkileyen Faktörler………19
2.9.2.1. Doğada 13C ve 1H Çekirdeklerinin Dağılımı………19
2.9.2.2. 13C ve 1H Çekirdeklerinin Jiromanyetik Sabitleri………20
2.9.2.3. Durulma ( Rölaksasyon) Zamanları……….22
2.9.3. 13C Spektroskopisinde Ölçüm Hassasiyetini Arttırmak için Uygulanan yöntemler………... 22
2.9.3.1 Ölçüm Hacminin ve Numune Miktarının Artırılması……….22
2.9.3.2. Sıcaklığın Düşürülmesi………..23
2.9.3.3. Manyetik Alan Şiddetinin Artırılması………...23
2.9.3.4. 13C ile İşaretleme………...24
2.9.3.5. Spektrum Toplama( Akümülasyon)………...24
3. TEORİK TEMELLER………26
3.1. Schrödinger Denklemi……….27
3.3. Çok Elektronlu Sistemlerde Elektronik Schrödinger Denkleminin Yaklaşık
Çözümleri ve Elektronik Yapı Teorisi Metodları………...30
3.4. Ab Initio Moleküler Orbital Teori Metodları………...32
3.4.1. Hartree-Fock Metodu………32
3.4.2. Slater Determinantları………...34
3.4.3. Spin Sınırsız Hartee-Fock Metodu………39
3.5. Elektron Korelasyonu ve Configuration Inteaction Metodu………40
3.5.1. Sınırlandırılmış Configuration Interaction Metodu………..45
3.6. Yoğunluk Fonksiyonelleri Teorisi………...46
3.7. Baz Setleri………51
3.7.1. Gaussiyen Tipi Orbitaller………..53
3.7.2. Gaussiyen Baz Setleri………...57
3.7.2.1. Küçük Ölçekli Baz Setleri (STO-NG)………..59
3.7.2.2. Genişletilmiş Baz Setleri………60
3.7.2.2.1. Bütün Orbitalleri Çok Zetalı Olan Baz Setleri………60
3.7.2.2.2. Değerlik Orbitalleri Çok Zetalı Olan Baz Setleri………...60
3.7.2.2.3. Polarizasyon Fonksiyonu İçeren Baz Setleri………..61
3.7.2.2.4. Difüzyon Fonksiyonları İçeren Baz Setleri……….61
4. GEOMETRİ OPTİMİZASYONU………..63
5.DENEYSEL ÖLÇÜMLER VE TEORİK HESAPLAMALAR………..66
5.1. Deneysel Kısım………....66
5.2. Teorik Kısım………....66
5.3. Glioksim Molekülü………..68
5.4. Dimetil glioksim molekülü………..75
6. TARTIŞMA VE SONUÇ………...89
6.1. Glioksim anti 1 Konformasyonunun Yapısal Analizi……….89
6.2. Glioksim amphi 1 Konformasyonunun Yapısal Analizi………..92
6.3. Glioksim syn 1 Konformasyonunun Yapısal Analizi………..94
6.4. Dimetil Glioksim anti 1 Konformasyonunun Yapısal Analizi………95
6.5. Dimetil Glioksim amphi 1 Konformasyonunun Yapısal Analizi………97
6.6. Dimetil Glioksim syn 1 Konformasyonunun Yapısal Analizi………98
KISALTMALAR DİZİNİ GO: Glioksim
DMG: Dimetil-glioksim
SCF: Öz Uyumlu Alan Yöntemi HF: Hartree-Fock Yöntemi MO: Moleküler Orbital
CI: Konfigurasyon Etkileşmeleri(Configuration Interaction) Yöntemi MP: Moller-Plessent Pertürbasyon Teorisi Metodu
DFT: Yoğunluk Fonksiyonelleri Teorisi (Density Functional Theory) PEY: Potansiyel Enerji Yüzeyleri
LCAO: Atomik Orbitallerin Lineer Toplamı
MO-LCAO: Moleküler Orbitallerin, Atomik Orbitallerin Lineer Toplamı cinsinden ifade edilmesi
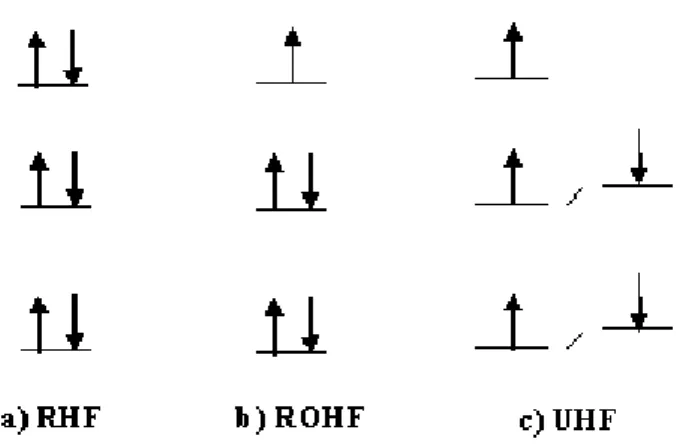
RHF: Spin Sınırlı Hartree-Fock Yöntemi
ROHF: Spin Sınırlı Açık Kabuk Hartree-Fock Yöntemi UHF: Spin Sınırsız Hartree-Fock Yöntemi
HK: Hohenberg ve Kohn KS: Kohn ve Sham
LDA: Yerel Yoğunluk Yaklaşımı (Local Density Approximation)
LSDA: Yerel Spin Yoğunlukları Yaklaşımı (Local Spin Density Approximation) GGA: Genelleştirilmiş Gradyent Yaklaşımı (General Gradient Approximation) LYP: Lee, Yang ve Parr
ETO: Üstel Tipte Orbital (Exponential Type Orbitals) GTO: Gaussiyen Tipi Orbital (Gaussian Type Orbitals) STO: Slater Tipi Orbital (Slater Type Orbitals)
CGF: Daraltılmış Gaussiyen Fonksiyonu (Contracted Gaussian Functions) AO: Atomik Orbital
B3LYP: Becke (B) Lee-Yang-Parr (LYP) Yöntemi
DFT B3LYP: Density Functional Theory Becke (B) Lee-Yang-Parr (LYP) Yöntemi PM3: Parametrizasyon Metodu 3
ŞEKİL VE TABLOLARIN LİSTESİ Şekiller
1-Şekil 2.1 Bir çekirdeğin Manyetik Alana getirildiğinde enerji seviyelerinde ki
yarılmalar………...8
2-Şekil 2.2 Tetrametilsilan molekülünün şekli………..15
3-Şekil 2.3. Metilbenzilnitrilin’ in 60 MHz lik ve 100 MHz lik ölçüm sonuçları…17 4-Şekil 3.1 Orbitallerdeki elektron yerleşimi ve enerji seviyelerinin şematik gösterimi………..39
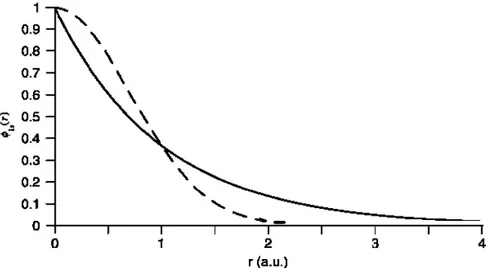
5-Şekil 3.2 Hidrojen atomunun 1s orbitali için STO (düz çizgili) ile Gaussiyen ilkel fonksiyonların (kesik çizgili) karşılaştırılması………..56
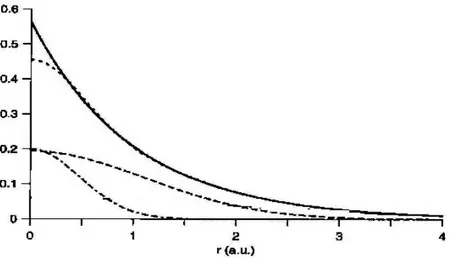
6- Şekil 3.3 Hidrojen atomunun 1s orbitali için farklı üslere sahip iki GTO (kesik çizgili, altta) nun lineer kombinasyonunun (kesik çizgili, üstte) bir STO’ya (düz çizgili, üstte) uydurulması………..57
7-Şekil 4.1Geometri Optimizasyonuna ait noktaların şematik gösterimi………….63
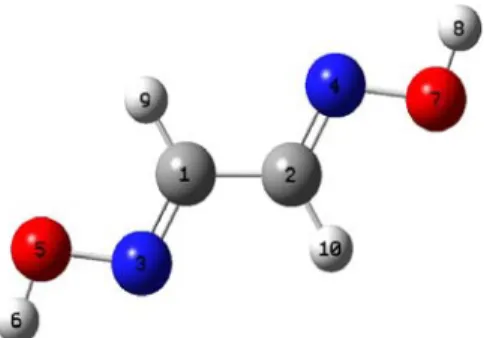
8- Şekil 5.1 Glioksim Anti1 konformerinin yapısı……….70
9-Şekil 5.2 Glioksim Amphi1 konformerinin yapısı……….70
10-Şekil 5.3 Glioksim Syn1 konformerinin yapısı………....70
11-Şekil 5.4 Dimetiglioksim Anti1 konformerinin yapısı……….76
12-Şekil 5.5 Dimetilglioksim Amphi1 konformerinin yapısı………76
13-Şekil 5.6 Dimetilglioksim Syn1 konformerinin yapısı………76
14- Şekil 5.7 Glioksim molekülünün deneysel 1H NMR kimyasal kayma spektrumu………... 85
15- Şekil 5.8 Glioksim molekülünün deneysel 13C NMR kimyasal kayma spektrumu………86
16- Şekil 5.9 Dimetilglioksim molekülünün deneysel 1H NMR kimyasal kayma spektrumu………87
17- Şekil 5.10 Dimetilglioksim molekülünün deneysel 13C NMR kimyasal kayma spektrumu………87
Tablolar
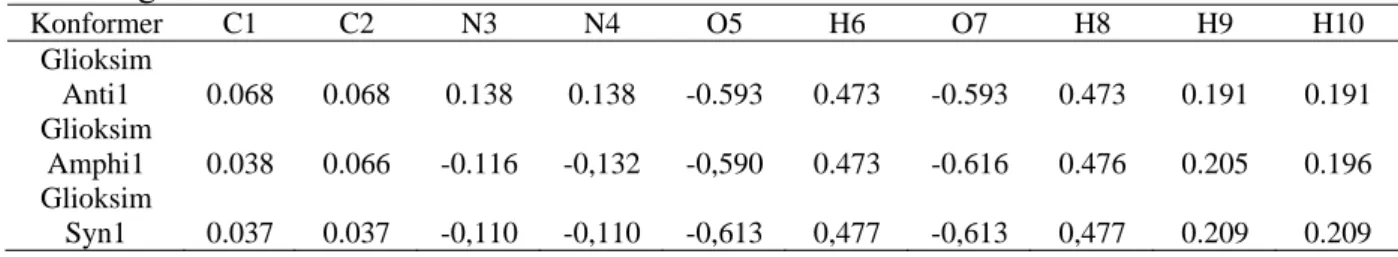
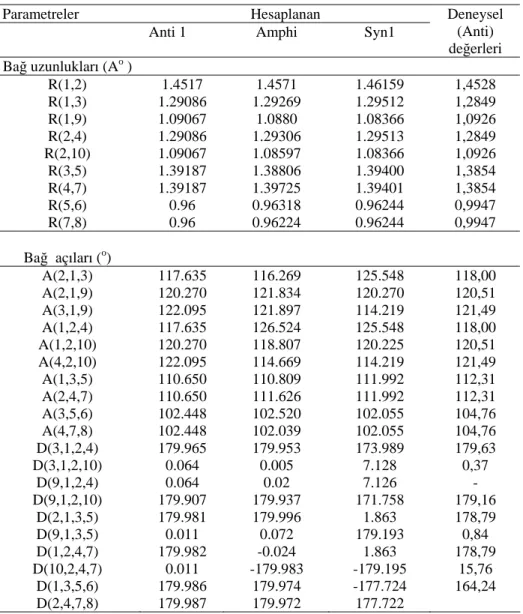
1-Tablo 5.1 Glioksim molekülünün konformerlerinin hesaplanan enerji ve dipol momentleri………...68 2-Tablo 5.2 Glioksim molekülünün konformerlerinin hesaplanan NBO yükleri…..68 3-Tablo 5.3 En kararlı konformerlerin hesaplanan geometrik parametreleri ve
deneysel X- ray değerleri………69 4-Tablo 5.4 Glioksim anti1 konformasyonunun değişik metot ve baz setlerine göre
çözelti (DMSO) içinde ki ve gaz fazında ki kimyasal
kayma değerleri……….. 71 5-Tablo 5.5 Glioksim amphi1 konformasyonunun değişik metot ve baz setlerine göre
çözelti (DMSO) içinde ki ve gaz fazında ki kimyasal
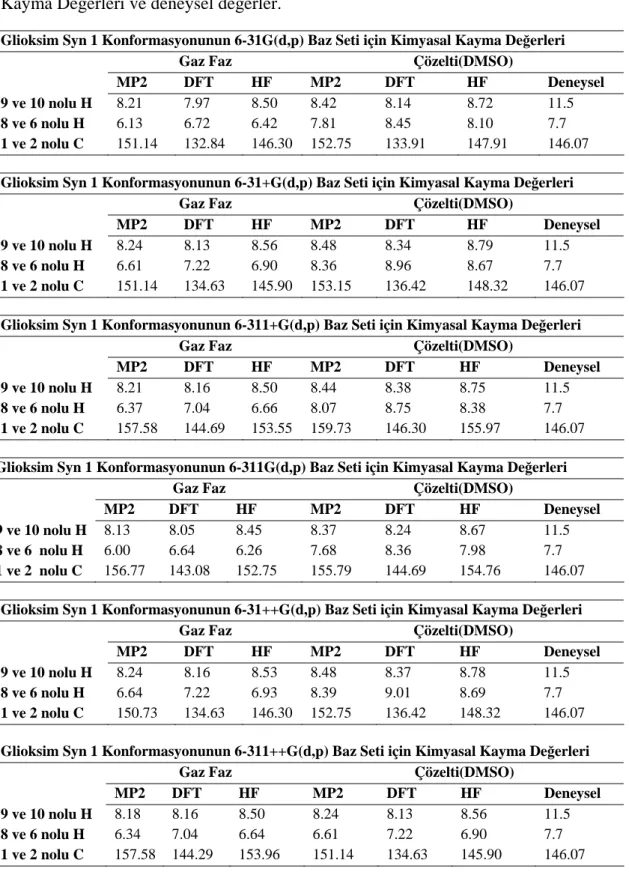
kayma değerleri………..72 6-Tablo 5.6 Glioksim syn1 konformasyonunun değişik metot ve baz setlerine göre
çözelti (DMSO) içinde ki ve gaz fazında ki kimyasal
kayma değerleri………..74
7-Tablo 5.7 Dimetilglioksim molekülünün konformerlerinin hesaplanan enerji ve dipol moment değerleri………...75 8-Tablo 5.8 Dimetilglioksim molekülünün konformerlerinin hesaplanan NBO
yükleri……….77 9-Tablo 5.9 Dimetilglioksim molekülünün konformerlerinin geometrik parametreleri
ve deneysel X-ray değerleri……….78 10-Tablo 5.10 Dimetilglioksim anti1 konformasyonunun değişik metot ve baz
setlerine göre gaz fazında ve çözelti içinde ki
kimyasal kayma değerleri………79
11-Tablo 5.11 Dimetilglioksim amphi1 konformasyonunun değişik metot ve baz setlerine göre gaz fazında ve çözelti içinde ki
kimyasal kayma değerleri………81 12-Tablo 5.12 Dimetilglioksim syn1 konformasyonunun değişik metot ve baz
setlerine göre gaz fazında ve çözelti içinde ki
1.GİRİŞ
Nükleer manyetik rezonans (NMR) fen ve doğa bilimlerinde yararlanılan çok önemli bir spektroskopik yöntemdir (1). NMR spektroskopisinin birçok kimyasal uygulamalarda kullanılışının artmasının sebebi de moleküllerin bileşimlerde, geometrilerinde, konformasyonlarında (aynı molekülün uzayda farklı geometri ile dizilişleri) ve çevrelerinde hassas olmasından dolayıdır. Ayrıca NMR spektroskopisi çekirdeklerin etrafındaki elektronlar hakkında değerli bilgiler verir ve böylece sistemin parçalarını tanımlamak için; organik, inorganik hatta biomoleküllerin üç boyutlu yapılarını tanımlamak için geniş bir şekilde kullanılmaktadır (2). NMR sinyalinin başarılı bir şekilde belirlenmesinden sonra belki de en önemli keşif nükleer rezonans frekansının, gözlenen çekirdeğin elektronik çevresine bağlı olmasıdır (3,4). Nükleer manyetik rezonans şimdiler de çözelti içinde ki organik ve biomoleküllerin yapısal problemlerini çözmede kullanılan başlıca bir teknik olmuştur (5). Son yirmi yıl içerisinde NMR parametrelerinin ab-inito hesaplamalarında önemli gelişmeler sağlanmıştır(6-13).Ab- inito moleküler orbital çalışmaları bir çok küçük ve orta büyüklükte molekülün moleküler yapılarını tanımlamakta başarılı olduğunu kanıtlamıştır (14-17). Küçük ve orta büyüklükte ki moleküller için de NMR perdeleme sabitlerinin ab-inito hesaplamalarının güvenilir sonuçlar vermekte olduğu tespit edilmiştir.(18-22). Nükleer manyetik rezonans moleküler yapıları ve konformasyonları tanımlamak için temel bir araçtır. Çünkü NMR spektroskopisi ile elde edilen nükleer perdeleme sabiti ve skaler spin-spin çiftlenme sabiti moleküllerin elektronik yapılarının belirlenmesine büyük katkılar sağlar (23-27). Son yirmi yıldır moleküldeki çekirdeklere ait kimyasal kayma ve mutlak perdeleme sabiti olarak bilinen NMR parametrelerinin teorik hesaplamaları aktif bir araştırma alanı olmuştur(28-30). Modern yüksek çözünürlüklü nükleer manyetik rezonans spektroskopisi biomoleküllerin hem çözelti içinde hem de katı halde dinamikleri ve yapıları hakkında bilgi sağlamaktadır (31-33). Eğer teorik hesaplama sonuçları deneysel verilerle uyumlu ise nükleer spin-spin çiftlenme sabitlerinin kayda değer bir potansiyeli vardır. Nükleer spin-spin çiftlenme sabitleri moleküllerin elektronik yapılar hakkında önemli bilgiler içerir (34).
Elektronik yapı teorisi hesaplamalarıyla, çok elektronlu sistemlerin elektronik Schrödinger denkleminin yaklaşık çözümleri yapılmaktadır (15). Elektronik yapı teorisi hesaplamaları, yarı deneysel teknikler ve ab-initio hesaplama teknikleri olmak üzere iki farklı hesaplama tekniği kullanmaktadır. Yarı deneysel hesaplama tekniklerinde bir takım deneysel ölçümler hesaplamalara katılmaktadır.
Ab-initio hesaplama tekniklerinde ise hiçbir deneysel veri kullanmaksızın, kuantum
mekaniğinin kanunları ve bir takım matematiksel yaklaşım teknikleri kullanılarak tamamıyla teorik hesaplamalar yapılmaktadır. Literatürde yarı deneysel veya
Ab-initio hesaplama tekniklerini kullanarak çok elektronlu sistemlerin elektronik
Schrödinger denkleminin tam çözümüne, yaklaşık çözümler veren pek çok hesaplama metodu vardır. Ab-initio metodlarının temeli 1928 yılında Hartree’nin yaptığı çalışmaya dayanmaktadır (35). Hartree bu çalışmasında çok elektronlu sistemler için elektronların bireysel tek elektron dalga denklemlerini yazmış ve (Self Consistent Field ) Öz Uyumlu Alan (SCF) yöntemiyle bu denklemleri çözmüştür. Sonra Slater 1930 yılında çok elektronlu sistemlerin tam dalga fonksiyonlarını yani Slater determinant dalga fonksiyonlarını yazmıştır (36). Fock daha sonra Hartree ve Slater’in yaptığı çalışmaları sistematik bir şekilde birleştirerek Hartree-Fock (HF) denklemlerini yazmıştır (37-38). Roothaan ve Hall tarafından moleküler orbitallerin atomik orbitallerin lineer kombinasyonu şeklinde yazılmasıyla HF denklemlerinin analitik çözümleri yapılabilmiştir (39-40). Bütün bu çalışmaların birleşimi bugün literatürde HF metodu olarak bilinen metodu geliştirmiştir. HF metodu eksiklikleri olmakla birlikte kendisinden sonra geliştirilen bütün metodlara temel teşkil etmektedir. HF metodunun en büyük eksikliği HF Hamiltoniyenindeki elektron-elektron Coulomb etkileşmesi teriminin, elektron-elektron korelasyon etkilerini ifade edememesidir. Bu eksikliği gidermek amacıyla literatürde pek çok yeni metod geliştirilmiştir. Bu metodlar Ab-initio Moleküler Orbital Teori (ab-initio-MO) metodları diye adlandırılan (Configuration Interaction) Konfigürasyon Etkileşmeleri Metodu (CI) (41-43), (Moller-Plessent Perturbation Theory ) Moller-Plessent Perturbasyon Teorisi Metodu (MP) (44-47) ve (Density Functional Theory) Yoğunluk Fonksiyoneli Teorisi (DFT) metodlarıdır (48-50).
Ab-initio-MO Teori metodlarıyla bilgisayar ortamında yapılan moleküler
ve hesaplama süreleri de aynı ölçüde artmaktadır. Bu nedenle bu metodlarla yapılacak olan hesaplamalarda araştırmacının sınırlarını elindeki bilgisayarların kalitesi ve hesaplamayı yapacağı sistemin büyüklüğü belirlemektedir. Bu sıkıntılar bu alanda çalışanları yeni metod arayışlarına itmiştir. DFT’ nin gelişimi de bu sebeple olmuştur. Özellikle büyük moleküllerde yapılan hesaplamalarda araştırmacılar mecburen DFT metodlarını kullanmak zorunda kalmaktadır. Bununla birlikte DFT metodları halen gelişim sürecindedir ve hesaplamalardaki hassasiyeti artırmak amacıyla metodlar geliştirilmeye ve denenmeye devam etmektedir. Bütün
ab-initio hesaplamalarında moleküler orbitaller tam set olan bazı fonksiyonlar
cinsinden yazılabilir. Bu baz setleri genellikle Slater tipi fonksiyonlardan ya da Gaussiyen tipi fonksiyonlardan oluşmaktadır. Slater tipi fonksiyonlarla yapılan moleküler hesaplamalarda ortaya çıkan çok merkezli integrallerin hesaplanmasında karşılaşılan sıkıntılar nedeniyle, moleküler hesaplamalarda Gaussiyen tipi fonksiyonlar ve bu fonksiyonlardan oluşturulan Gaussiyen baz setleri tercih edilmektedir.
Koordinasyon bileşiklerinden olan vic-dioksim kompleksleri, teknikte, ilaç kimyasında boyar madde olarak ve daha birçok alanda kullanıldığından çokça üretilmekte, ayrıca yeni sentezlerin yapılması yönünde de yoğun çalışmalar sürdürülmektedir (51-58). Koordinasyon bileşiklerinin biyolojik yapılardaki önemi de gün geçtikçe artmaktadır. Son zamanlarda kanser araştırmalarında anti-tümör etkilerinin bulunması özellikle vic-dioksim kompleksleri üzerindeki araştırmaların yoğunlaşmasına sebep olmuştur (59). Vic-dioksim kompleksleri, vitamin B12 ve
bitkilerin klorofil renk maddesine benzerliğinden dolayı biyolojik yapıların aydınlatılmasında kullanılmaktadır (52). Oksimler sağlık alanında da, ağrı kesici, lokal anestezik etkileri nedeniyle kullanılmaktadır (60-63). Bir çok oksim antimikrobiyal etkilere sahiptir ve antibiyotik olarak kullanılmaya başlanmıştır(64-66). Bazı oksim türevleri parazit öldürücü etkiye sahiptir (67,68). Aritmi gibi bazı kalp rahatsızlıklarında, göz içi tansiyonunu düşürmekte, bazı psikiyatri hastalıklarının tedavisinde oksimlerden faydalanılmaktadır (69-71).
2. NÜKLEER MANYETİK REZONANS
Nükleer Manyetik Rezonans spektroskopisinin temeli çekirdeğin manyetik özelliğine dayanır. Atom çekirdeğindeki manyetizmayı basit bir şekilde şöyle açıklayabiliriz. Atom çekirdeğini küre biçiminde ve merkezinden geçen eksen etrafında dönen bir cisim olarak düşünebiliriz. Çekirdekte proton bulunduğundan çekirdek kendi ekseni etrafında döndüğünde pozitif yükte (proton) bu eksen etrafında bulunan dairesel yörüngelerde hareket edecektir. Bu yükün belli bir yörünge üzerinde hareketi, elektrik akımından başka bir şey değildir. Her elektrik akımı çevresinde manyetik alan oluşturur. Ekseni etrafında dönen atom çekirdeği de çevresinde bir manyetik alan meydana getirir. Bu nedenle atom çekirdekleri bir mıknatıs gibi davranırlar. Çekirdeğin oluşturduğu manyetik alanın momenti vardır.
Klasik fizikten bilindiği üzere kendi ekseni etrafında dönen bir cisim Lr gibi bir açısal momentuma sahiptir. Atom çekirdeği de kendi ekseni etrafında döndüğünden çekirdeğinde açısal momentumu vardır. Çekirdeğin kendi ekseni etrafında dönmesi olayına çekirdek spini denir. Bir çekirdeğin açısal momentumu ile manyetik momenti arasında
L
r
r
γ
μ
=
(2-1) ilişkisi vardır. Buradaμ
r
manyetik moment,L
r
açısal momentum veγ
ise jiromanyetik sabitidir. Jiromanyetik sabiti γ her element için ayrı değere sahiptir.2.1. Çekirdeğin Spin Kuantum Sayısı
Bir elementin NMR da aktif olup olmaması ( NMR ile incelenebilmesi) ilgili çekirdeğin spin kuantum sayısına bağlıdır. Elektronda olduğu gibi atom çekirdeğinin de spin kuantum sayısı vardır. Çekirdeğin spin kuantum sayısı I, çekirdekte bulunan proton ve nötronların sayısına göre değişmektedir. Çekirdekte bulunan proton ve nötronların sayısına göre spin kuantum sayıları belirlenemez. Ancak proton ve nötronların sayısı ile spin kuantum sayısı arasında geçerli olan bazı kurallar vardır.
1) Çift-çift çekirdekler: Bu elementler NMR spektroskopisinde aktif değildirler. Spin kuantum sayıları I=0 dır. Kütle numarası ve atom numarası çift olan elementlerdir. Örneğin 16O atomunda 8 proton ve 8 nötron vardır. 2) a. Tek- tek çekirdekler: Kütle numarası ve atom numarası tek olan
elementlerdir. Bu gruba dahil elementlerin proton sayısı tek nötron sayısı çifttir. Örneğin 19F atomunun 9 protonu 10 nötronu vardır.
2) b. Tek-Çift çekirdekler: Kütle numarası tek atom numarası çift olan elementlerdir. Bu gruba ait olan elementlerin proton sayısı çift nötron sayısı tektir. Örneğin 13C atomunun 6 protonu 7 nötronu vardır.
Genel olarak ikinci gruba dahil olan elementlerin spin kuantum sayıları
2 1 =
I ve tek katlarıdır. Yani
,... 2 5 , 2 3 , 2 1 = I
3) Çift-tek çekirdekler: Kütle numarası çift, atom numarası tek olan elementlerdir. Bu gruba dahil olan izotopların nötron ve proton sayısı tektir. Örneğin 14N atomunda 7 proton ve 7 nötron vardır. Bu grupta bulunan elementlerin spin kuantum sayıları I =1,2,3,... şeklindedir.
Bir elementin NMR spektroskopisinde gözlenebilmesi için o elementin spin kuantum sayısının I>0 olması gerekir.
2.2. Atom Çekirdeklerinin Manyetik Alanda Davranışı
Atom çekirdeklerinin en önemli özelliklerinden birisi çekirdeğin kendi ekseni etrafında dönmesi sonucu oluşan manyetik moment ve açısal momentumdur. Açısal momentumun alabileceği değerler kuantumludur. Kuantum fiziğinde açısal momentum büyüklüğünün ifadesi
π
2
I
hm
L
=
(2-2)bağıntısı ile verilir. Burada
h
Planck sabiti mI ise çekirdek spin manyetik kuantumkuantum sayısına bağlıdır. Bir çekirdeğin spin manyetik kuantum sayısı ile spin kuantum sayısı arasında
)
1
2
(
+
= I
m
I (2-3) bağıntısı vardır ki bu bağıntı çekirdek spin çokkatlılığını ifade eder. Spin kuantum sayısı2 1 =
I olan protonun manyetik kuantum sayısı bu değerin (2-3) denkleminde
yerine yazılması ile kolayca bulunur.
2
1
2
1
2
+
=
=
Im
Bu değer (mI =2) manyetik kuantum sayısının 2 olduğu anlamına gelmez; bu sayı
protonun iki farklı manyetik kuantum sayısına sahip olduğunu gösterir. mI =2 ifadesi manyetik alan içerisine getirilen bir çekirdeğin iki farklı enerji seviyesine yarılacağı anlamına gelir. Manyetik kuantum sayıları, +I ve –I değerleri arasında bulunan değerleri alırlar. Ancak iki kuantum sayısı arasındaki fark Δm = 1 olabilir. Açısal momentum manyetik kuantum sayısına göre değişmektedir:
π
2
I
hm
L
=
(2-2)denkleminde manyetik kuantum sayısı mI nın değerlerini yerine yazarsak açısal
momentumun değerleri bulunur. Açısal momentum ile manyetik dipol moment arasındaki bağıntıyı daha önce vermiştik.
L
r
r
γ
μ
=
(2-1)π
γ
μ
2
Ihm
=
(2-4)Bu denkleme göre manyetik moment değerlerinin manyetik kuantum sayısına bağlı olduğu görülmektedir. Bu da bize manyetik momentinde kuantumlu olduğunu gösterir.
2.3. Manyetik bir Dipolün Manyetik Alanda Enerjisi
Manyetik bir dipol şiddeti Hr0 olan manyetik bir alan içerisine getirildiği
zaman dipolün belirli bir potansiyel enerjisi oluşur. Bu enerji manyetik alan şiddetine ( Hr0 ) ve dipolün manyetik momentine (
μ
r
) bağlı olup0
.H
E
=
μ
r
r
Δ
(2-5)şeklinde ifade edilir. Manyetik momentin (2-4) denklemindeki değerini (2-5) denkleminde yerine yazarsak
π
γ
2
0m
IhH
E
=
Δ
(2-6)elde edilir. (2-6) denklemine göre bir dipolün manyetik alan içerisinde alabileceği enerji değerleri kuantumludur. Başka bir deyimle manyetik bir dipol manyetik alan içerisine getirildiği zaman yalnız belirli enerji seviyelerine sahip olabilir. Dipolün sahip olabileceği enerji seviyesi sayısı manyetik kuantum sayısına dolayısıyla spin kuantum sayısına bağlıdır. Bir atom çekirdeğinin manyetik alanda farklı enerji seviyelerinde bulunması nasıl oluşur? Bu olayı proton için açıklamaya çalışalım. Protonun bir manyetik momenti vardır ve bu moment bir vektördür. Proton homojen ve statik bir manyetik alan içerisine getirildiği zaman manyetik moment gelişi güzel yönlenemez. Manyetik momentin manyetik alanda yönlemesi kuantumludur. Uygulanan dış manyetik alanın (H0) belli bir yönü olduğundan protonun manyetik momenti manyetik alanın yönü ile paralel veya antiparalel olarak yönlenir. Böylece protonun manyetik momentinin manyetik alanda iki farklı yönlenmesi mümkündür. Manyetik bir alan olmadığı zaman manyetik moment gelişi güzel her iki istikamette yönlenir. Bu durumda tüm protonların enerji seviyesi dejeneredir. Genel olarak çekirdeklerin spin kuantum sayısı dolayısıyla manyetik kuantum sayısı o çekirdeğin manyetik alan içerisinde kaç farklı enerji seviyesine yarılacağını belirler.
Şekil 2.1.Bir çekirdeğin manyetik alana getirildiğinde enerji seviyelerindeki yarılmaların şematik gösterimi
2.4. Rezonans Olayı ve Rezonans Koşulu
Rezonans ile olayı uygulanan bir dış manyetik alan ile paralel yönlenmiş manyetik momentin dışarıdan verilen uygun enerji ile antiparalel konuma geçmesidir. O halde bu iki enerji seviyesi arasında ki fark rezonans açısından önem kazanmaktadır. Enerji seviyeleri arasındaki fark
⎟
⎠
⎞
⎜
⎝
⎛−
=
=
Δ
2
1
2
-2
1
2
-
0 0π
γ
π
γ
hH
hH
E
E
E
antipelel parelel (2-7) şeklindedir ve buradanπ
γ
2
0hH
E
=
Δ
(2-8)şeklinde ifade edilmiş olur.
2 1 2 1 2 0 1 ⎟ =+ ⎠ ⎞ ⎜ ⎝ ⎛+ = mI hH E π γ 2 1 2 1 2 0 2 ⎟ =− ⎠ ⎞ ⎜ ⎝ ⎛− = hH mI E π γ H0
Elde ettiğimiz bu denklem protonun manyetik alanda bulunduğu enerji seviyeleri arasındaki farkı göstermektedir. Planck sabiti
h
ve jiromanyetik sabitγ
değişmeyeceğine göre değişken parametre olarak yalnız manyetik alan şiddeti H0 karşımıza çıkmaktadır. O halde protonun enerji seviyeleri arasındaki enerji farkı doğrudan manyetik alan şiddetine bağlıdır. Proton veya herhangi bir çekirdek manyetik alan içerisinde bulunmadığı zaman (2-8) denkleminden (H0 =0)0
=
ΔE
olacağından enerji seviyeleri arasında herhangi bir fark olamayacaktır. Böylece enerji seviyelerinin dejenere olduğu sonucu ortaya çıkmaktadır. Protonların rezonansa gelebilmesi için çekirdeklerin alt enerji seviyesinden üst enerji seviyesine geçmesi gerekir. Bunun için protona dışarıdan ΔE kadar bir enerjinin verilmesi gerekir. Bu enerji elektromanyetik radyasyon olarak verileceğinden elektromanyetik dalga enerjisinin ΔE ye eşit olması gerekir. Elektromanyetik dalga enerjisi ve frekansıυ
h
E
=
Δ
(2-9) denklemiile belirlenir. Rezonans koşulu için (2-8) ve (2-9) deki enerji denklemlerinieşitlersek
π
γ
υ
2
0hH
h
E
=
=
Δ
(2-10)π
γ
υ
2
0H
=
(2-11)rezonans denklemini elde ederiz. Bu denklem NMR deneylerinde rezonans için gerekli koşulu ortaya koymaktadır.
Tüm NMR deneyleri, alt enerji seviyesinde bulunan bir çekirdeğin (homojen bir manyetik alan içerisinde) dışarıdan verilen bir enerji ile üst enerji seviyesine geçmesi ile başlar. Proton manyetik alan içerisine getirildiği zaman I=1/2 olduğundan çekirdeğin enerji seviyesi iki faklı enerji seviyesine yarılır. Alt enerji
seviyesinde bulunan proton (manyetik momenti dış manyetik alan ile paralel olan) enerji alarak üst enerji seviyeye geçer. Protonun manyetik momenti dış manyetik alanın yönü ile antiparalel yönlenir. Bu olaya spin çevrilmesi veya genel olarak rezonans denir. Rezonans için dışarıdan verilen enerji miktarı iki seviye arasındaki enerji kadar olmalıdır. Denklem (2-11) de verilen rezonans denklemi incelendiğinde iki değişken parametrenin olduğunu görmekteyiz.
Bu parametrelerden biri uygulanan manyetik alan şiddeti H diğeri ise 0
numune üzerine gönderilen ışının frekansı
υ
dür. Rezonans olayının gerçekleşebilmesi için şöyle hareket edilir. Numune homojen ve sabit bir manyetik alan içerisine getirilir daha sonra elektromanyetik dalga gönderilir. Elektromanyetik dalganın gönderilmesi esnasında dalganın frekansı sürekli olarak değiştirilir rezonans için gerekli frekans yakalanırsa bu enerji alt seviyeden üst seviyeye geçen protonlar tarafından absorblanır. Bu absorbsiyon olayı sinyal olarak kaydedilir. Rezonans için ikinci bir yöntem de numune üzerine sabit frekanslı elektromanyetik dalga gönderilir, manyetik alanın şiddeti sürekli olarak değiştirilir.2.5. Enerji Seviyelerinin Dağılımı
Bir numune manyetik alanın içerisine getirildiği zaman protonların bir kısmının uygulanan manyetik alanla paralel bir kısmının ise antiparalel yönlendiğini biliyoruz. Yani protonların bir kısmı alt seviyede bir kısmı da üst seviyede bulunur. Rezonans olayında çekirdekler alt enerji seviyesinden üst enerji seviyesine geçiş yaptıklarından alt enerji seviyesinde bulunan çekirdek sayısının üst enerji seviyesinde bulunan çekirdek sayısından daha fazla olmasını isteriz. Seviyelerin doldurulması Boltzmann dağılım yasasına göre olur:
kT E
e
N
N
−Δ=
β α (2-12)α
N = Üst seviyede (antiparelel ) olan protonların sayısı
β
N = Alt seviyede ( parelel) olan protonları sayısı E
Δ = İki seviye arasındaki enerji farkı
k = Boltzmann sabiti
T
= SıcaklıkE
Δ nin değerini (2-9) denkleminde yerine yazarsak ve seriye açarsak
T
k
hH
e
N
N
hHkTπ
γ
π γ β α2
1
0 2 0−
=
=
− (2-13)elde ederiz. Rezonans olayında enerji absorpsiyonu ile alt seviyede bulunan bir proton üst seviyeye geçer. Bu nedenle alt seviyede bulunan protonların sayısı üst seviyeye göre ne kadar fazla olursa rezonans olasılığı o oranda artar. Ne kadar fazla proton rezonans olursa sinyalin şiddeti de (pik şiddeti) o oranda artar. Bu nedenle çekirdeklerin popülasyonunu değiştirmemiz gerekir. (2-13) denklemine göre bu oranı değiştirebilecek iki parametre vardır. Bunlar sıcaklık (T) ve manyetik alan şiddeti
0
H dır. Eğer sıcaklık düşürülürse
β α
N
N
oranı azalır. Yani alt seviyede bulunan proton sayısı artar. O halde düşük sıcaklıklarda NMR spektrumu kaydetmekle hassasiyet arttırılmış olacaktır. Ancak NMR spektrumu kaydedilecek madde herhangi bir çözücü içerisinde çözündükten sonra spektrum kaydı yapıldığı için numune soğutulunca çözünürlük problemi ile karşılaşılacaktır. Ayrıca numune içerisinde var olan dinamik dengelerin (bağ dönmesi, halka çevrilmesi…) statik hale geçmesi de problem oluşturacaktır. Yani sıcaklığın düşürülmesi hassasiyeti arttırmak için uygun bir yöntem değildir. Buradan popülasyonu etkileyecek tek parametre kalır ki o da
0
H
manyetik alan şiddetini arttırmaktır.2.6. Durulma Olayı (Relaksasyon)
NMR spektroskopisinde rezonans olayının, alt enerji seviyesinde bulunan bir protonun enerji soğurarak üst seviyeye geçmesi ile oluştuğunu söyledik. Rezonans sonucu protonlar alt seviyeden üst seviyeye geçtiğinden enerji seviyelerinin
popülasyonu değişmektedir. Sistemdeki dengenin tekrar sağlanabilmesi için üst enerji seviyesine geçmiş protonların fazla enerjilerini dışarıya vererek tekrar eski konumlarına yani alt enerji seviyelerine dönmeleri gerekir. Protonların üst seviyede iken fazla enerjilerini dışarıya vererek tekrar alt seviyeye dönmelerine durulma denir. Durulma için geçen zamana durulma zamanı denir. İki çeşit durulma vardır:
1) Spin-örgü durulması T1
2) Spin-spin durulması T2
Protonun üst seviyeden alt seviyeye geçerken fazla enerjisini (soğurduğu enerji) ışın halinde dışarıya vermesi söz konusu değildir. Işın yayma olasılığı yayılan ışının dalga boyu ile ters orantılı olduğundan bu olasılık radyo dalgaları bölgesinde olanaksızdır. Çözelti içerisinde bulunan her türlü parçacığa( gaz, sıvı, katı, çözücü molekülleri) örgü denir. Bu moleküller termal hareketler sonucu çeşitli manyetik alanlar meydana getirirler. Bu yüklü taneciklerin kendilerine mahsus dönme hareketleri vardır. Bu oluşan alanların bazılarının frekansı çekirdeğin presesyon hareketinin ( kendi ekseni etrafında dönmesi) frekansına uyar ve rezonans koşulu oluştuğunda fazla enerji örgüye verilir. Örgüye verilen enerji termal harekete yani kinetik enerjiye çevrilir. Spin örgü durulması için geçen zaman T1 dir.
Spinler arasında ikinci bir etkileşim ise spin-spin durulmasıdır. Spin– spin durulmasında temel halden uyarılmış düzeye çıkan çekirdek almış olduğu enerjiyi komşusu olan çekirdeğin spini ile etkileşerek aktarır.
2.7. Kimyasal Kayma
Rezonans olayının meydana gelebilmesi için (2-11) denkleminin sağlanması gerekir. Jiromanyetik sabiti
γ
her element için ayrı bir değere sahiptir. Her proton için jiromanyetik sabit aynı değerdir. (2-11) nolu rezonans denklemini protonlara uyguladığımızda sabit bir manyetik alan içerisinde bulunan herhangi bir numunenin tüm protonları aynı yerde belli bir frekansta rezonansa gelmeleri gerekirdi. Böyle bir durumda NMR spektroskopisi bize yalnız molekül içinde proton olup olmadığı hakkında bilgi veren bir spektroskopik yöntem olurdu. Protonların aynı frekansta rezonans olmaması gerçeği NMR spektroskopisini geliştirmiştir. Protonlar bağlı oldukları atomlara ve uzaydaki konumlarına göre farklı bölgelerde rezonans olurlar.Her ne kadar protonlar homojen ve kararlı bir manyetik alan içerisinde bulunsalar da protonların etkisi altında bulundukları manyetik alan dış manyetik alandan farklıdır. O halde her proton farklı manyetik alanın etkisi altında kalmaktadır. Bu nedenle (2-11) denklemine göre protonların rezonans frekansları farklı olacaktır çünkü her protonun etki altında kaldığı manyetik alan farklı olacaktır. Böylece protonları NMR aracılığı ile tanımak mümkün olmaktadır. Protonların çevresinde bulunan manyetik alan neden dış manyetik alandan farklıdır? sorusu akla geliyor. Rezonans olayını incelerken şimdiye kadar çekirdeklerin çevresinde bulunan elektronları dikkate almadık. Bu elektronların oluşturdukları sekonder manyetik alanlarla dış manyetik alanın etkisini azaltır veya arttırırlar. Elektronlar yüklü tanecikler olduklarından manyetik alanın içine getirildiği zaman uygulanan manyetik alanın etkisi ile ilave hareketler yaparlar.
Lenz yasasına göre dış manyetik alan elektron akımı ile ikinci bir manyetik alan (sekonder manyetik alan) meydana getirirse oluşan manyetik alanın yönü dış manyetik alanın yönü ile zıttır. Elektron sirkülasyonu ile oluşan manyetik alanın yönü dış manyetik alan ile zıt olduğunda, dış manyetik alanın şiddeti H0, çekirdek etrafında azalır. Dış manyetik alanın etkisinin çekirdek etrafında azalmasına perdeleme denir. Bir molekül her ne kadar homojen bir manyetik alan içine getirilse de çekirdekler oluşan sekonder manyetik alanlardan dolayı dış manyetik alandan farklı bir manyetik alanın etkisi altında kalırlar. Bazı durumlarda protonun konumuna göre elektronlar tarafından oluşturulan sekonder manyetik alan dış manyetik alan ile aynı yönde olabilir. Bu durumda çekirdek dış manyetik alandan daha kuvvetli bir manyetik alan etkisi altında kalır. Sonuçta rezonans koşulunun sağlanması için manyetik alan şiddetinin azaltılması gerekir. Bu olaya antiperdeleme denir. Elektronların meydana getirdiği sekonder manyetik alan dış manyetik alanın etkisiyle meydana gelmektedir. Dolayısıyla oluşan sekonder manyetik alanın şiddeti
H
SEKile dış manyetik alanH
0arasında0
H
H
r
SEK=
σ
r
(2-14)SEK
H = Sekonder manyetik alan
0
H = Dış manyetik alan
σ
= Perdeleme sabitidir.Orantı sabiti
σ
ya perdeleme sabiti denir. Perdeleme sabitini etkileyen en önemli faktör protonların etrafında bulunan elektron yoğunluğudur. Protonların etkisi altında kaldığı toplam manyetik alana lokal manyetik alan denir vesek
lok
H
H
H
r
=
r
0-
r
(2-15)Sekonder manyetik alanın değerini (2-15) denkleminde yerine yazarsak
(
σ
)
σ
−
=
=
1
-0 0 0H
H
H
H
H
lok lokr
r
r
r
r
(2-16)denklemini elde ederiz. Sonuçta rezonans olayında protonun çevresinde bulunan lokal manyetik alan önemlidir. Lokal manyetik alan şiddeti (2-16) denkleminden anlaşılacağı gibi perdeleme sabitine bağlıdır. Lokal manyetik alan elektron yoğunluğuna bağlı olarak her proton etrafında farklı değere sahiptir. Bu da protonların çevresindeki elektron yoğunluğuna bağlı olarak farklı bölgelerde rezonans olacağını göstermektedir. Protonların farklı bölgelerde rezonans olmalarına kimyasal kayma denir.
2.8. Pik Yerlerinin Belirlenmesi ve NMR Spektrumlarında Skala
Rezonans yerlerinin belirlenmesi için standart bir sinyal alınır ve diğer rezonans frekanslarının standart sinyalinden olan uzaklığı Hz (Hertz) cinsinden verilir. Böylece sinyallerin yeri saptanmış olur. NMR ölçümlerinde standart sinyal için tetrametilsilan (TMS) molekülüne ait sinyallar kullanılır.
TMS nin kullanılma sebepleri:
1) TMS ucuz olup temin edilmesi kolaydır.
3) TMS nin kaynama noktası 27 0C olduğundan spektrum kaydından sonra numunenin hafif ısıtılması ile TMS ortamdan kolayca uzaklaştırılabilir dolayısıyla TMS safsızlık oluşturmaz.
4) TMS nin 12 tane eşdeğer protonu olduğundan konsantrasyonu düşük tutulsa bile şiddetli bir sinyal elde edilir.
Şekil 2.2. Tetrametilsilan molekülünün şekli
Spektrumu kaydedilecek bileşiğin çözeltisine TMS ilave edilir ve NMR spektrumu kaydedilir. Herhangi bir protonun rezonans frekansının standardın (TMS) rezonans frekansına olan uzaklığına kimyasal kayma denir.
π
γ
υ
2
0H
=
(2-11)Rezonans denkleminden hatırlanacağı gibi bir protonun rezonans frekansı manyetik alan şiddetine bağlıdır. Manyetik alan şiddeti farklı olan cihazlarla çalışıldığı zaman protonların rezonans frekansları da farklı olacaktır. Sonuçta farklı cihazlarla çalışılınca kimyasal kayma değerleri farklı olacağından bir karışıklık ortaya çıkacaktır. Bu güçlüğün ortadan kaldırılması için manyetik alan şiddetine bağlı
olmayan bir skalanın oluşturulması gerekmektedir. Kimyasal kayma, bir protonun rezonans frekansı ile standartın (TMS) rezonans frekansı arasındaki fark olarak tanımlanmıştır. standart
ν
ν
ν
=
−
Δ
numune (2-17) Bu fark NMR cihazının alan şiddetine göre değişecektir. Değişim alan şiddeti ile doğru orantılı olacaktır. Yani manyetik alanın büyüklüğü ne kadar fazla ise bu fark o oranda artacaktır. Bu fark cihazın çalıştığı sabit frekansa bölünür ve bu değer 106 ile çarpılırsa tüm cihazlar için geçerli olan değişmeyen kimyasal kayma denklemi ortaya çıkar. 6 tan10
cihaz s numυ
υ
υ
δ
=
−
(2-18) Burada;δ
= Kimyasal kayma numuneυ
= Numunenin rezonans frekansıstandart
υ
= Standardın rezonans frekansıcihaz
υ
= Cihazı çalıştığı frekanstır.Standardın rezonans frekansını
υ
standart = 0 olarak kabul edersek, kimyasalkaymayı 6
10
cihaz numuneυ
υ
δ
=
(2-19) şeklinde yazabiliriz.Şekil 2.3.a. Metilbenzilnitrilin’ in60 MHz lik NMR ölçümünün sonuçları Şekil 2.3.b. Metilbenzilnitrilin’ in 100 MHz lik ölçümün sonuçları
Her iki spektrumda da sinyallerin standart sinyalinden olan uzaklığı Hz cinsinden verilmiştir. 60MHz için 100MHz için 2,35ppm 10 60MHz 141Hz δ 6 CH3 = = 100MHz10 2,35ppm 235Hz δ 6 CH3 = = 3,70ppm 10 60MHz 222Hz δ 6 CH2 = = 10 3,70ppm 100MHz 370Hz δ 6 CH2 = = Şekil 2.3.a Şekil 2.3.b
7,18ppm 10 60MHz 431Hz δ 6 arom = = 10 7,18ppm 100MHz 718Hz δ 6 arom = =
Protonların farklı bölgelerde rezonans olmaları iki önemli nedene dayandırılmaktadır.
1. Protonların çevresinde elektronların oluşturduğu bulunan lokal diamanyetik etki 2. Komşu atom ve atom gruplarının meydana getirdiği manyetik alanların etkisi Buraya kadar analatılanlar proton (1H) Nükleer Manyetik Rezonansı için geçerlidir.
13C Nükleer Manyetik Rezonans spektroskopisi de temelde proton Nükleer Manyetik
Rezonans spektroskopisi ile aynıdır.
2.9. 13C NMR spektroskopisi
13C NMR spektroskopisi son yirmi yıl içerisinde önemli gelişmeler
kaydederek yapı tayininde organik kimyanın vazgeçilmez yöntemlerinden biri haline gelmiştir. İlk NMR deneyinin 1945 yılında yapılmış olmasına rağmen bir bileşiğin yapısının NMR ile incelenmesi ilk kez 1951 yılında gerçekleşti. Öncelikle proton çekirdeklerinin vermiş olduğu sinyaller incelendi. 13C çekirdeğinin ilk sinyali 1957 yılında Lauterbur tarafından gözlendi . Ancak 13C çekirdeğinin duyarlılığının protona oranla az oluşu 13C NMR spektroskopisinin gelişimini bir süre ertelemiştir. 13C NMR
cihazları artık organik kimya bölümlerinde ve fizik bölümlerinde sıradan bir şekilde kullanılmaktadır. İlk çıkan cihazlarda yalnız proton veya karbon çekirdeklerinin NMR spektrumları ölçülürdü. Daha sonra geliştirilen cihazlarla her iki çekirdek birden ölçülmeye başlanmıştır.
2.9.1. 1H ve 13C Çekirdeklerinin Karşılaştırılması
13C NMR spektroskopisi yukarıda bahsettiğimiz gibi 1H NMR
spektroskopisinden yaklaşık olarak 20 yıl sonra gelişmeye başaldı. Yapı analizinde bu kadar önemli olan bir yöntemin geç gelişmesinin nedeni 13C çekirdeklerinin yapısında aramak gerekir. Karbon ve proton çekirdeklerinde gözlenen farklılıkları
incelemeden önce bu iki çekirdeğin ortak noktaları üzerinde duralım. Bir çekirdeğin NMR spektroskopisinde aktif olabilmesi için spin kuantum sayısının sıfırdan farklı olması gerekir. 13C çekirdeğinin spin kuantum sayısı protonda olduğu gibi
2 1 = C I ve 2 1 = H I
dir. O halde 13C çekirdekleri
1 2 + = I m
denklemine göre (m=2) iki tane çekirdek spin çokkatlılığına sahiptir. Bu sayılar
2 1 1 =+ m ve 2 1 2 =− m
dir. Buradan 13C çekirdeklerinin manyetik alanda protonda olduğu gibi iki ayrı enerji seviyesine yarılacağı anlaşılmaktadır.
2.9.2. 13C Çekirdeklerinin Duyarlılığını Etkileyen Faktörler
2.9.2.1. Doğada 13C ve 1H Çekirdeklerinin Dağılımı
Karbon atomunun doğada bulunan iki önemli izotopu vardır. Bu izotoplar doğada
12C = % 98,70 13C = % 1,108
oranında bulunurlar. 12C çekirdeğinin spin kuantum sayısı I=0 olduğundan 12C çekirdekleri NMR da aktif değildir. Çünkü I=0 değerini (2.3) denkleminde yerine yazdığımız zaman m=1 elde etmekteyiz. Bu da 12C çekirdeklerinin manyetik alanda
tek bir yönlenmeye sahip olduklarını diğer bir deyimle çekirdeğin enerji seviyelerinde herhangi bir yarılmanın olmadığını ortaya koyar. O halde karbon NMR spektroskopisinde aktif olan 13C çekirdekleridir. Bu izotopun doğada % 1,1 oranında yaygın olması 13C NMR spektroskopisinin gelişmesini bir süre engellemiştir. Proton ve karbon çekirdekleri spin kuantum sayıları ve NMR da aktif olan izotopların doğada dağılım oranları açısından karşılaştırıldığında protonun karbona göre NMR da yaklaşık olarak yüz katı kadar daha aktif olduğu ortaya çıkmaktadır.
2.9.2.2 13C ve 1H Çekirdeklerinin Jiromanyetik Sabitleri
1H NMR bölümünde belirtildiği gibi çekirdeklerin jiromanyetik sabitleri
NMR açısından önemlidir. Rezonans koşulu denkleminden (2.11) anlaşılacağı gibi sabit bir manyetik alan içerisinde rezonans olacak çekirdeğin rezonans frekansını jiromanyetik sabit belirler. Örneğin sabit bir manyetik alan içerisine getirilen iki farklı çekirdeğin jiromanyetik sabitleri farklı ise bu iki çekirdeğin rezonans frekansları da farklı olacaktır.
13C ve 1H çekirdeklerini göz önüne aldığımızda bu çekirdeklerin jiromanyetik
sabitleri:
γ
H = 2,674 . 108 s-1 T-1γ
C = 0,672 . 108 s-1 T-1şeklindedir. Yukarıda verilen değerlerden her iki çekirdeğin jiromanyetik sabitleri arasındaki oranın yaklaşık olarak 4 olduğu görülmektedir. 1H çekirdeklerinin manyetik alan şiddeti 14100 Gauss ( piyasada kullanılan en düşük NMR cihazı) olan bir alanda
MHz
60
2
14100
10
674
.
2
2
8 0=
=
=
π
π
γ
υ
H
denklemine göre rezonansları için 60 MHz lik bir enerjiye ihtiyaç duyulur. Halbuki aynı manyetik alan içerisine 13C çekirdekleri getirildiğinde yukarıda ki denklemde γ = 0,672. 108 s-1 T-1 değeri yerine yazıldığında gerekli rezonans için 15 MHz lik bir enerjiye ihtiyaç olduğunu görürüz. Bu da bize 1H ve 13C çekirdeklerinin farklı bölgelerde rezonans olduklarını gösterir. Eğer bir cihaz 400 MHz ise 1H çekirdeklerinin rezonansı için 400 MHz kadar bir enerjiye ihtiyaç vardır. Aynı cihazda 13C çekirdekleri ölçülürse rezonans için gerekli enerji 100 MHz dir. Bu durumda 13C çekirdeklerinin 100 MHz lik bir cihazda ölçüldüğünden bahsedilir. Özet olarak şunu söyleyebiliriz: Jiromanyetik sabitleri sabit bir manyetik alanda çekirdeklerin rezonans frekanslarını belirler.
13C çekirdeğinin protonda olduğu gibi manyetik alanda iki farklı enerji
seviyesine yarıldığından bahsettik. Boltzmann enerji dağılımı yasasına göre bu enerji seviyeleri arasındaki populasyon farklı iki parametreye bağlıdır. Bunlar (2-14) denklemimden görüldüğü gibi sıcaklık T ve iki enerji seviyesi arasındaki enerji farkı ΔE dir. ΔE sabit manyetik alan içinde jiromanyetik sabitine bağlıdır. Buna göre 13C ve 1H çekirdeklerinin belli bir manyetik alan içinde oluşturacakları enerji seviyeleri arasındaki enerji farkları değişik olacak ve protonun enerji seviyeleri arasındaki enerji farkı, karbon çekirdeklerinin enerji seviyeleri arasındaki enerji farkının 4 katı daha fazla olacaktır.
Enerji seviyeleri arasında oluşan fark spektruma ne şekilde yansır? Boltzmann enerji dağılım yasasına göre alt ve üst enerji seviyeleri arasındaki fark ne kadar fazla olursa alt seviyede bulunan çekirdek sayısı üst seviyeye göre o oranda fazla olur. Alt seviyede çekirdeklerin fazla olması rezonans olma olasılığını daha fazla artırmaktadır. Rezonans olma olasılığının artması spektrumda gözlenen pikin şiddetinin artması anlamına gelir. Başka bir deyimle çekirdeğin rezonans için gerekli olan duyarlılığını ifade eder. Sonuçta, bir çekirdeğin jiromanyetik sabiti o çekirdeğin rezonans için ne kadar duyarlı olduğunu gösterir. Çekirdeklerin jiromanyetik sabitleri ile duyarlılıkları arasında bir bağlantı vardır. Rezonans olan bir çekirdeğin duyarlılığı jiromanyetik sabiti olan γ değerinin küpü ile orantılıdır. Buna göre
C
denkleminden 13C çekirdeklerinin duyarlılığının, protona göre (0,2514)3 = 0,0159 kadar daha az olduğu ortaya çıkmaktadır. Bu ifade şu anlama gelmektedir: 13C ve 1H izotopları doğada aynı oranda bulunmuş olsaydı o zaman protonun duyarlılığı karbon çekirdeğinin duyarlılığının 1/0,0159 = 63 katı olurdu.
2.9.2.3.Durulma ( Rölaksasyon) Zamanları
13C çekirdeğinin proton ile kıyaslandığı zaman gözlenen diğer bir farklılığı T 1
ile ifade edilen longitudinal durulma zamanıdır. 13C çekirdeklerinin durulma
zamanları genelde uzundur. Durulma zamanları uzun olan çekirdekler çabuk doygunluğa ulaştıklarından duyarlılıkları da azdır.
Yukarıda sıralanan tüm faktörler : 1. İzotopların doğada yaygınlığı 2. Jiromanyetik sabitlerin değerleri 3. Durulma zamanları
Şeklinde göz önüne alındığı zaman 13C çekirdeğinin duyarlılığının 1H çekirdeğinin duyarlılığına oranı 1/5700 olduğu ortaya çıkmaktadır. Bu durum 13C NMR spektroskopisinin neden daha geç geliştiğini ortaya koymaktadır. 13C çekirdeğinin doğal duyarlılığı artırılamayacağına göre 13C ölçüm yönteminin geliştirilmesi yoluna gidilmiştir.
2.9.3. 13C Spektroskopisinde Ölçüm Hassasiyetini Arttırmak için Uygulanan Yöntemler
2.9.3.1. Ölçüm Hacminin ve Numune Miktarının Artırılması
Bir spektrumda gözlenen sinyallerin şiddeti numunede bulunan çekirdek sayısı ile doğrudan orantılı olduğundan iyi bir spektrum kaydı için ölçümü yapılan numunenin miktarının artırılması gerekir. Ancak numune miktarının artırılması sınırlıdır. Numune miktarı en fazla birkaç katına çıkarılabilir. Sabit bir çözücü içerisinde numune miktarını artırmak isteyince çözünürlük problemi ve çözelti
vizkozitesinin artması gibi iki sorun karşımıza çıkar. Çözelti vizkozitesinin artması ile çekirdeklerin durulma süreleri kısalır bunun akabinde cihazın rezolüsyonolüsyonu azalır ( pikler genişler) ve ince yarılmalar gözlenmez. O halde maddenin çözünürlüğü çok iyi olsa dahi konsantrasyon artışı sınırlıdır.
2.9.3.2. Sıcaklığın Düşürülmesi
Boltzmann dağılım yasası göz önüne alınırsa, manyetik alan varlığında oluşan iki farklı enerji seviyesi arasında gözlenen populasyon farkını etkileyen faktörlerden birinin de sıcaklık olduğu (2.14) denkleminden görülmektedir. Bu denkleme göre sıcaklığın düşürülmesi alt seviyede bulunan çekirdeklerin oranını artıracaktır. Alt enerji seviyesinde bulunan çekirdeklerin sayılarının artması rezonans olasılığını ve bunun sonucunda da pik şiddetini artırır. Ancak bir çekirdeğin ölçüm hassasiyetinin artırılması için sıcaklığın düşürülmesi uygun bir yöntem değildir. Bu yöntemin populasyon dağılımını olumlu yönde etkilemesinin yanı sıra sakıncalı tarafları da vardır. Sıcaklığın düşürülmesi ile maddenin çözünürlüğü azalacak dolayısıyla çözünürlük problemi ortaya çıkacaktır. Ayrıca moleküllerde mevcut olan çeşitli dinamik süreçler (bağ dönmesi, halka inversiyonu, v.s.) statik hale geçeceklerinden sıcaklığın düşürülmesi ile normal gözlenmesi gereken spektrumlar yerine daha değişik spektrumlar gözlenecektir. Sonuç olarak sıcaklığın düşürülmesi teorik olarak her ne kadar çekirdeklerin duyarlılığını artıran bir yöntem ise de beraberinde getirdiği çözünürlük probleminden dolayı pratikte uygulanmaz.
2.9.3.3. Manyetik Alan Şiddetinin Artırılması
Çekirdeklerin manyetik alan içerisinde oluşturmuş oldukları enerji seviyeleri arasında ki farkın populasyonu etkilediğini (2-14) denkleminden görmekteyiz. Bir çekirdeğin manyetik alan içinde oluşturduğu enerji seviyeleri arasındaki enerji farkının jiromanyetik sabitin yanı sıra manyetik alan şiddetine de (H0) bağlı olduğu
Manyetik alan şiddeti ne kadar fazla olursa bir çekirdeğin manyetik alan içerisinde oluşturduğu enerji seviyeleri arasındaki enerji farkı da o oranda fazla olur. Enerji seviye farkı doğrudan seviyeler arasında ki populasyon farkını etkileyeceğinden pik şiddetleri de artar.
Sonuç olarak şunu vurgulamak gerekir ki ölçüm hassasiyetinin artırılması ve birleşik olan piklerin yarılmalarını (rezolüsyonu) elde edebilmek için mümkün olduğu kadar manyetik alan şiddeti yüksek olan cihazlarla çalışmak gerekmektedir.
2.9.3.4. 13C ile İşaretleme
13C çekirdeği doğada % 1,1 oranında bulunmaktadır. Bu nedenle molekülün
bazı karbon atomları 13C izotopları ile işaretlenebilir. İyi bir 13C NMR spektrumu elde etmek için karbon atomlarını işaretlemek doğru bir iş olmadığı gibi kolayda değildir. Yalnız reaksiyon mekanizmalarının incelenmesinde belli bir karbon atomunun davranışını kontrol etmek açısından tek bir karbon atomunu işaretlemek doğru ve akılcı bir iştir.
2.9.3.5. Spektrum Toplama( Akümülasyon)
Yukarıda 13C çekirdeğinin duyarlılığının çok az olduğundan söz ettik. Bir numunenin 13C spektrumunu kısa bir sürede alabilmemiz için neler yapabiliriz? Spektrumlarda gözlenen emisyon ve absorpsiyondan oluşan gürültü (temel çizgi) istatistiksel bir şekilde dağılmıştır. Böylece gürültü bilgisayar aracılığı ile toplanırken elimine edilir. Numuneye ait olan pikler her zaman için absorpsiyon pikleri olduklarından bunlar toplama sonucunda artar ve sonuçta kaydedilen spektrum sayısına bağlı olarak sinyal/gürültü oranı artmaya başlar. Kaydedilen spektrum sayısı ile sinyal/gürültü arasında
n
bağıntısı vardır. Burada;
S = sinyal büyüklüğü N = gürültü büyüklüğü
n = kaydedilen spektrum sayısıdır.
Örneğin bir numuneden 100 spektrum kaydedildiği zaman S/N oranında
10
100
=
=
N
S
3. TEORİK TEMELLER
Kuantum mekaniğinin birinci postülası bir sistemin durumunun Ψ dalga 0
fonksiyonu ile tanımlanabileceğini ifade eder. İkinci postülasına göre her fiziksel niceliğe karşılık gelen bir Oˆ operatörü vardır. Üçüncü postülasına göre ise bir operatörün öz fonksiyonları o operatörün işleyeceği uzayı geren baz vektörlerini oluştururlar. Baz vektörleri yani Ψ dalga fonksiyonları normalize değilse 0
operatörün beklenen değeri
∫
∫
=
dv
dv
ˆ
ˆ
0 * 0 0 * 0 0 0Ψ
Ψ
Ψ
O
Ψ
Ψ
O
Ψ
(3.1)ile tanımlanır. Ψ ’ler normalize fonksiyonlar iseler bu ifade
∫
= ˆ dv ˆ 0 * 0 0 0 OΨ Ψ OΨ Ψşeklinde olur. Moleküler bir sistemde herhangi bir fiziksel niceliği hesaplamak için öncelikle o fiziksel niceliğe karşılık gelen operatör belirlenir. Daha sonra o moleküler sisteme ait Schrödinger denkleminin çözümünden elde edilen, normalize edilmiş dalga fonksiyonları kullanılarak Denk.(3-1)’deki integraller hesaplanır. Kuantum mekaniğine göre, bir sisteme ait Schrödinger denklemi tam olarak çözülebilirse, sistemin enerjisi ve buna bağlı olarak diğer fiziksel özellikleri hesaplanabilmektedir. Hidrojen atomu için Schrödinger denklemi tam olarak çözülebilir. Fakat çok elektronlu sistemler için Schrödinger denkleminin tam çözümü yapılamamaktadır. Elektronik yapı teorisi çok elektronlu sistemlerde bazı matematiksel yaklaşıklıkları kullanarak Schrödinger denklemine yaklaşık çözümler sağlamayı amaçlayan bir teoridir. Schrödinger denkleminin yazılmasında ve çözülmesinde ise molekülün geometrisi önem taşımaktadır
Elektronik yapı teorisinde hesaplama metotları iki ana başlık altında toplanabilir:
• Yarı deneysel metotlar
Yarı deneysel metotlarda bilinen bazı deneysel parametreler teorik hesaplamalarda kullanılarak Schrödinger denklemine yaklaşık çözümler elde edilmeye çalışılmaktadır.
Ab-initio metodlarında ise hiçbir deneysel veri kullanılmaksızın kuantum
mekaniğinin ilkeleri ve matematiksel yaklaşımlar kullanılarak tamamıyla teorik hesaplamalar yapılmaktadır. Ab-initio metodları, Ab-initio Moleküler Orbital Teori (Ab-initio MO) ve Yoğunluk Fonksiyoneli Teorisi (Density Functional Theory DFT) olmak üzere iki farklı teoriye dayandırılarak türetilen metotlardan oluşmaktadır.
3.1. Schrödinger Denklemi
Moleküllerin kuantum mekaniksel hesaplamalarında öncelikle moleküle ait,
)
(
Ψ
E
(
Ψ
0r,
R)
=
0r,
R
H
(3-2)şeklindeki zamandan bağımsız Schrödinger denkleminin çözümlerinin bilinmesi gerekir(74). Burada r elektronların, R çekirdeklerin konum vektörlerini temsil etmektedir. H hamiltoniyen operatörü, E sistemin enerjisi, Ψ( Rr, ) ise sistemin dalga fonksiyonlarıdır. Genel olarak bir sistemin hamiltoniyen operatörü, sistemin toplam kinetik enerjisi,
∑
∇
−
=
i 2 i i 2 2m
8π
h
T
(3-3)ile potansiyel enerjisi,
∑
〈=
j i ij j ir
q
q
V
(3-4)V
T
+
=
H
(3-5)∑
∑
〈+
∇
−
=
j i ij j i i 2 i i 2 2r
q
q
m
8π
h
H
(3-6)şeklindedir. Buradaki toplamlar bütün parçacıklar üzerindendir. m parçacıkların i
kütlesi, h Planck sabiti, r iki parçacık arasındaki mesafe, ij q ve i q sırasıyla j
parçacıkların yükleridir. Elektronlar için qi = −e çekirdekler içinse qi = +Zie’dir. elektron ve M çekirdekten oluşan bir molekülün Denklem (3-6)’daki hamiltoniyeni atomik birimlerde yazarsak
∑
∑ ∑
∑ ∑
∑ ∑
∑
= = = = 〉 = 〉 =+
+
−
∇
−
∇
−
=
M 1 A N 1 i M 1 A N 1 i N i j M 1 A M A B AB B A ij iA A 2 A A N 1 i 2 iR
Ζ
Ζ
r
1
r
Ζ
2M
1
2
1
H
(3-7)şeklinde olur. Burada riA = ri − rA , i.elektronla A. çekirdek arasındaki mesafe,
j i r
r − =
ij
r , i. elektronla j. elektron arasındaki mesafe, RAB = RA − RB , A ile B
çekirdeği arasındaki mesafe, M , A. çekirdeğin kütlesi ile elektron kütlesi A
arasındaki oran ve Z , A. çekirdeğin atom numarasıdır. Bu hamiltoniyendeki ilk A
terim elektronların kinetik enerjisini, ikinci terim atom çekirdeklerinin kinetik enerjisini, üçüncü terim elektronla atom çekirdekleri arasındaki Coulomb etkileşmesini, dördüncü terim elektron-elektron etkileşmesini, beşinci terim ise çekirdek-çekirdek etkileşmesini temsil eder.
3.2. Born-Oppenheimer Yaklaşımı
Çok elektronlu atom ve moleküllerin için yazılan Schrödinger denklemininin çözümünü yapabilmek amacıyla bazı yaklaşımlar yapılmaktadır. Bu yaklaşımlardan bir tanesi Born-Oppenheimer Yaklaşımıdır. Born ve Oppenheimer yaklaşımına göre; nükleer hareketlerle, elektronik hareketler birbirinden ayrılır(75).Born-Oppenhimer yaklaşımına göre çekirdeğin kütlesi elektronlarınkinden çok büyük olduğundan
çekirdekler elektronlardan çok daha yavaş hareket ederler. Bu nedenle elektronlar sabit bir çekirdeğin alanında hareket eden parçacıklar olarak kabul edilebilir. Bu durumda Hamiltoniyen ifadesi içindeki çekirdeklerin kinetik enerjisi terimi ihmal edilebilir. Çekirdekler arasındaki etkileşme ise bir sabit kabul edilir. Hamiltoniyenin kalan terimleri elektronik hamiltoniyen olarak tanımlanır. Elektronik hamiltoniyen M tane sabitlenmiş çekirdek yükü etrafında hareket eden N elektronu tanımlar.
∑
∑ ∑
∑ ∑
= = = = 〉+
−
∇
−
=
N i N i M A N i N i j ij iA A i electr
r
Z
H
1 1 1 1 21
2
1
(3-8)Bu durumda elektronik Schrödinger denklemi,
)
(
)
(
r
=
Ψ
r
Ψ
elekt elektE
H
(3-9)şeklinde yazılır. Burada çekirdeklerin koordinatları olan R hesaplara parametrik olarak katılır.Eelekt elektronik enerjidir. Sisteme ait toplam enerji ise,
∑ ∑
= 〉Ζ
Ζ
+
=
M A M A B AB B A elekt toplR
E
E
1)
(R
(3-10)Denk.(3-10) farklı çekirdek dizilişlerine karşılık gelen moleküler potansiyel enerji yüzeylerini tanımlar. Schrödinger denklemini çok elektronlu bir sistem için yazmak kolay olsa da He atomu gibi iki elektronlu bir sistem için bile denklemin tam çözümü yapmak imkansızdır. Bu imkansızlığın sebebi, hamiltoniyen içindeki elektron-elektron Coulomb etkileşim operatörüdür. Bu operatör çok elektronlu sistemlerde Şchrödinger denkleminin değişkenlerine ayrılmasını imkansız kılmaktadır. Çok elektronlu sistemlerin elektronik Schrödinger denklemine ancak bir takım yaklaşıklıklar yapılarak çözülebilir. Elektronik Schrödinger denkleminin yaklaşık çözümleri elektronik yapı teorisi hesaplamaları ile yapılır. Bu amaçla Elektronik yapı teorisi içerisinde pek çok farklı metod geliştirilmiştir. Bu metodlar ya varyasyonel metodlar ya da pertürbasyon metodlarıdır. Varyasyonel metotlar iteratif
yöntemlerle Schrödinger denklemine yaklaşık çözümler sağlar. Bu şekilde elde edilen yaklaşık çözümlerin enerjileri, gerçek enerjiye bir üst sınır olmaktadır.
3.3. Çok Elektronlu Sistemlerde Elektronik Schrödinger Denkleminin Yaklaşık Çözümleri ve Elektronik Yapı Teorisi Metodları
Yukarıda da bahsettiğimiz gibi çok elektronlu sistemlerin elektronik Schrödinger denkleminin tam çözümü yapılamamaktadır. Elektronik yapı teorisi çok elektronlu sistemlerde bazı matematiksel yaklaşımlar kullanarak Schrödinger denklemine yaklaşık çözümler sağlamayı amaçlayan bir teoridir. Elektronik yapı teorisinde hesaplama metodları ikiye ayrılır;
• Yarı deneysel metodlar
• Ab-initio metodları
Yarı deneysel metodlarda bilinen bazı deneysel ölçüm sonuçları teorik hesaplamalarda kullanılarak Schrödinger denklemine yaklaşık çözümler elde edilmeye çalışılmaktadır.
Ab-initio metodlarında ise hiçbir deneysel veri kullanılmaksızın kuantum
mekaniğinin kanunları kullanılarak teorik hesaplamalar yapılmaktadır. Ab-initio metodları, Ab-initio Moleküler Orbital Teori (Ab-initio MO) ve (Density Functional Theory) Yoğunluk Fonksiyoneli Teorisi (DFT) olmak üzere iki farklı teoriye dayandırılarak türetilen metodlardan oluşmaktadır. Her iki teorinin de temelinde elektronik Schrödinger denklemine yaklaşık çözümler sağlamak vardır. Bu çalışmada yapılan hesaplamalar tamamen teorik olduğundan yarı deneysel metodlardan bahsedilmeyecektir.
Ab-initio metodlarıyla hesaplama yapılırken öncelikle hesaplamanın
yapılacağı sisteme ve hesaplanacak özelliklere uygun olacak şekilde bir hesaplama yöntemi kurulmalıdır. Hesaplama yöntemi kurulurken dikkat edilmesi gereken iki önemli nokta vardır.
• Hesaplamanın yapılacağı metodun seçilmesi
• Hesaplamada kullanılacak olan baz setinin seçimi
Ab-initio metodlarıyla hesaplama yapmak demek, bu metodlardan herhangi