T.C.
SELÇUK ÜNİVERSİTESİ SAĞLIK BİLİMLERİ ENSTİTÜSÜ
KRONİK BÖBREK YETMEZLİĞİ OLAN HASTALARDA
HEMODİYALİZE GİRME SÜRESİNİN KARDİYOVASKÜLER
RİSK BELİRTEÇLERİ ÜZERİNE ETKİSİ
GÜL AKAR
YÜKSEK LİSANS TEZİ
BİYOKİMYA ANABİLİM DALI
Danışman
Prof. Dr. Sadık BÜYÜKBAŞ
T.C.
SELÇUK ÜNİVERSİTESİ SAĞLIK BİLİMLERİ ENSTİTÜSÜ
KRONİK BÖBREK YETMEZLİĞİ OLAN HASTALARDA
HEMODİYALİZE GİRME SÜRESİNİN KARDİYOVASKÜLER
RİSK BELİRTEÇLERİ ÜZERİNE ETKİSİ
GÜL AKAR
YÜKSEK LİSANS TEZİ
BİYOKİMYA ANABİLİM DALI
Danışman
Prof. Dr. Sadık BÜYÜKBAŞ
Bu araştırma Selçuk Üniversitesi Bilimsel Araştırma Projeleri Koordinatörlüğü tarafından 09202042 proje numarası ile desteklenmiştir.
i
ÖNSÖZ
Kronik böbrek yetmezliği olan hastalarda diyalize girme süresinin kardiyovasküler risk belirteçleri üzerine etkisi olup olmadığını ortaya koymayı amaçladığımız çalışmamız boyunca bilgi ve deneyimlerinden yararlandığım, ilgisine ve emeğine minnettar olduğum değerli hocam Yrd. Doç.Dr. Aysel KIYICI ve bölümümdeki diğer bütün saygıdeğer hocalarıma,
Beni bugünlere getiren, maddi ve manevi desteklerini esirgemeyen sevgili aileme ve kıymetli eşime,
Sonsuz teşekkürlerimi sunarım.
ii İÇİNDEKİLER ÖNSÖZ ... i İÇİNDEKİLER ...ii SİMGELER VE KISALTMALAR...iii 1.GİRİŞ ... 1
1.1. Kronik Böbrek Yetmezliği Tanımı ... 2
1.1.1. Kronik Böbrek Yetmezliğinin Evreleri ... 3
1.1.2. Kronik Böbrek Yetmezliği Nedenleri ... 5
1.1.3. Kronik Böbrek Yetmezliği Prevalansı... 6
1.1.4.Kronik Böbrek Yetmezliğinin Klinik Özellikleri... 7
1.1.5. Kronik Böbrek Yetmezliği Tedavisi ... 11
1.1.6. Kronik Böbrek Yetmezliği ve Kardiyovasküler Hastalık ... 14
1.2. Yüksek Duyarlıklı CRP (hsCRP)... 16
1.3. IL-6... 19
1.4 İskemi-Modifiye Albümin (IMA) ... 21
2. GEREÇ VE YÖNTEM ... 24
2.1. Çalışma Şekli... 24
2.2. Olgu Seçimi... 24
2.3. Örneklerin Toplanması ve Saklanması ... 24
2.4. Biyokimyasal Analizler... 25
2.4.1. hsCRP Ölçümü ... 25
2.4.2. IL-6 Ölçümü ... 25
2.4.3. İskemi-Modifiye Albümin Tayini ... 27
2.4.4. Diğer Biyokimyasal Ölçümler... 29
2.4.5. İstatistiksel Analiz ... 29 3. BULGULAR... 30 4. TARTIŞMA ... 34 5. SONUÇ VE ÖNERİLER ... 39 6. ÖZET ... 40 7. SUMMARY ... 41 8. KAYNAKLAR ... 42 9.ÖZGEÇMİŞ ... 46
iii
SİMGELER VE KISALTMALAR
ABSU : Absorbance Units (Absorbans Üniteleri) ACB : Albümin Kobalt Bağlanma Testi
ACS : Akut Coronary Sendrom (Akut Koroner Sendrom) AMİ : Akut Miyokard İnfarktüsü
APC : Antijen Presenting Cells (Antijen Sunan Hücreler) CAD : Coronary Artery Disease (Koroner Arter Hastalığı) cTnT : Troponin T
CRP : C-Reaktif Protein
CVD : Cardiovascular Disease (Kardiyovasküler Hastalık) D-IMA : Albümine Göre Düzeltilmiş İskemi-Modifiye Albümin
DM : Diabetes Mellitus
DTT : Dithiothreitol
ESRD : End-Stage Renal Disease (Son Dönem Böbrek Hastalığı) GFH : Glomerüler Filtrasyon Hızı
HD : Hemodiyaliz
HDL : High Density Lipoprotein (Yüksek Dansiteli Lipoprotein) HSA : Human Serum Albumin (İnsan Serum Albümin)
hsCRP : High Sensitive C-Reactive Protein (Yüksek Duyarlıklı C-reaktif Protein)
HT : Hipertansiyon IFN : İnterferon
IMA : İskemi-Modifiye Albümin IL-6 : İnterlöin-6
KBY : Kronik Böbrek Yetmezliği KVH : Kardiyovasküler Hastalık KVS : Kardiyovasküler Sistem
LDL : Low Density Lipoprotein (Düşük Dansiteli Lipoprotein)
MI : Miyokard Enfarktüsü
PD : Periton Diyaliz
RRT : Renal Replasman Tedavileri SDBY : Son Dönem Böbrek Yetersizliği TND : Türk Nefroloji Derneği
iv TNF-α : Tümör Nekröz Faktör Alfa
USRDS : United States Renal Data System (Birleşmiş Devletler Böbrek Veri Sistemi)
VLDL : Very Low Density Lipoprotein(Çok Düşük Dansiteli Lipoprotein)
1
1.GİRİŞ
Kronik böbrek yetmezliği (KBY) glomerüler filtrasyon değerinde azalmanın sonucu böbreğin sıvı solüt dengesini ayarlamada ve metabolik, endokrin fonksiyonlarda kronik, ilerleyici bozulma hali olarak tanımlanabilir. Böbreklerin en önemli görevi vücuttan atık maddelerin atılmasıdır. Kronik böbrek yetmezliğinde böbrekler görevlerini yerine getirmeyince kanda üre ve kreatinin gibi maddeler yükselir. Kandaki elektrolitlerin dengesi bozulur (Akpolat ve ark 2007).
Hemodiyaliz (HD), böbrek yetmezliği sebebiyle böbrek fonksiyonlarını kaybeden hastaların hayatlarını devam ettirebilmeleri için vücutta oluşan toksik madde ve sıvıların vücuttan atılmalarını sağlayan bir tedavi yöntemidir. Özel membranlar ile hastanın kanının makineler aracılığı ile temizlenmesi işlemidir. Hemodiyaliz işleminin gerçekleşmesi için yeterli kan akımı, bir membran ve hemodiyaliz makinesi sağlanmalıdır. Hemodiyaliz tedavisi hastanın böbrek yetmezliğinin şiddetine, çıkardığı idrar miktarına bağlı olmak üzere haftada 2 - 3 kez, 4 - 6 saat süre ile uygulanır (Ayköse 2006).
Yakın zamanda yapılan birçok çalışma sonuçları göstermiştir ki; kronik böbrek yetmezliği olan hastalarda kardiyovasküler hastalıklara yatkınlık artmakta ve unstabil angina, myokard infarktüsü (MI) gibi akut koroner sendromlar daha sık ortaya çıkmaktadır. Yine yapılan çalışmaların bir kısmında bu risk artşına kronik böbrek yetmezlikli hastaların diyabet, hipertansiyon gibi böbrek yetmezliği gelişiminin etiyolojik nedenlerinden çok bu hastalara uygulanan hemodiyaliz ya da periton diyalizi gibi işlemlerin neden olduğu öne sürülmektedir (Levy ve ark 2004).
Son yıllarda iskemi durumlarında serum albümin yapısında değişikliklerin oluştuğunun belirlenmesi yeni bir serum kardiyak iskemi belirtecinin bulunmasına olanak sağlamıştır. Albümin yapısındaki son amino terminali, kobalt, bakır ve nikel gibi geçiş metallerinin bağlandığı bölgedir. İskemi durumunda ortaya çıkan hipoksi, asidoz, serbest radikal hasarı ve membran bozulması gibi nedenler bu geçiş metallerinin albüminin N-terminaline bağlanmalarını azaltır. Yapısında değişiklik meydana gelmiş olan bu albümine “iskemi-modifiye albümin (IMA)” adı verilir ve albümin molekülündeki değişiklikler, hasta serumuna bir miktar kobalt eklenerek kolorimetrik olarak ölçülebilir. IMA konsantrasyonlarındaki artma miyokard
2 iskemisini gösteren erken bir belirteç olarak akut koroner sendromlu hastaların değerlendirilmesinde kullanılmaktadır (Pantazopoulos ve ark 2009).
C-reaktif protein (CRP), bir akut faz reaktanıdır. Bu protein adını pnömokok adlı bakterinin C polisakkaridi ile karşılaştığında, presipitasyon yapma niteliğinden almıştır. İnflamasyonun çok erken bir belirtecidir ve inflamasyon başlangıcından 2-4 saat sonra yükselir. Klinik çalışmalar, yüksek duyarlılıklı CRP (hs-CRP)’nin sağlıklı görünen kişilerde ileride gelişecek bir inme, MI ve periferik vasküler hastalık için güçlü ve bağımsız bir risk faktörü olduğunu göstermiştir (Punzi ve ark 2005).
Sitokin ailesinin üyesi olan interlökinler makrofaj ve lenfositlerden salgılanan, vücudun travma ve infeksiyona immünolojik ve metabolik cevabında rol oynayan hormon benzeri elemanlardır. Bu seriden olan interlökin-6 (IL-6) infeksiyöz veya inflamatuar bir uyarana karşı konağın verdiği akut yanıtta yer alan bir mediatördür. IL- 6 akut faz proteinlerin salgılanmasında da önemlidir (Daftarian ve ark 1996, Rader 2000).
Hemodiyaliz işleminin kronik böbrek yetmezlikli hastalarda inflamatuar mediatörlerin üretimini artırdığı bilinmektedir. Son yıllarda yapılan çalışmalarda da kronik böbrek yetmezlikli hastalarda görülen kardiyovasküler hastalık risk artışının hemodiyaliz işleminden kaynaklandığı öne sürülmektedir. Biz de çalışmamızda, kronik böbrek yetmezliği olan hastalarda hemodiyaliz süresinin kardiyovasküler risk belirteçleri üzerine etkisini bu belirteçlerden hsCRP, IL-6 ve yeni bir belirteç olan iskemi modifiye albümin düzeylerini ölçerek ortaya koymayı amaçladık.
1.1. Kronik Böbrek Yetmezliği Tanımı
Kronik böbrek yetmezliği glomerüler filtrasyon değerinde azalmanın sonucu böbreğin sıvı-solüt dengesini ayarlama ve metabolik-endokrin fonksiyonlarında kronik ve ilerleyici bozulma hali olarak tanımlanabilir. Üremi kronik böbrek yetmezliğinin neden olduğu tüm klinik ve biyokimyasal anormallikleri içeren bir deyimdir ve birçok kaynakta kronik böbrek yetmezliği ile eş anlamda kullanılmaktadır. KBY çeşitli nedenlere bağlı olarak, fonksiyonel nefronların ilerleyici kaybı sonucu ortaya çıkmaktadır. Bu kayıp süresince homeostazın sürdürülebilmesi için fonksiyonel nefronlarda çeşitli değişiklikler meydana gelmektedir. Ancak bir noktadan sonra bu değişiklikler yetersiz kalmakta ve son dönem böbrek yetmezliği (SDBY) ortaya çıkmaktadır. Glomerüler filtrasyon hızının
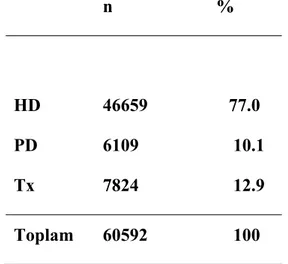
3 (GFR) zaman içersinde ilerleyen ve geriye dönüşsüz bir şekilde azalması, gelişmekte olan KBY’ nin en önemli göstergesidir (Akpolat ve ark 2007). Kronik böbrek yetmezliği medikal yönünün yanı sıra hastaların sosyal, ekonomik ve psikolojik durumlarını da etkilemektedir. Türk Nefroloji Derneği (TND) 2008 yılı verilerine göre ülkemizde kronik böbrek yetmezliği nedeniyle renal replasman tedavisi (RRT) gören hasta sayısının 754 diyaliz merkezinden toplanan verilere göre 60592 olduğu belirlenmiştir (Tablo 1.1).
Tablo 1.1. 31 Aralık 2008 itibarıyla kronik hemodiyaliz/periton diyalizi (HD/PD) programında izlenmekte olan veya fonksiyonel greftle izlenmekte olan tüm hastaların RRT tipine göre dağılımı
n % HD PD Tx 46659 77.0 6109 10.1 7824 12.9 Toplam 60592 100 1.1.1. Kronik Böbrek Yetmezliğinin Evreleri
KBY dünyada halk sağlığını ilgilendiren prevalansı her geçen gün artmakta olan bir hastalıktır. Kronik Böbrek Hastalığı (KBH); 3 ay veya daha uzun süreli böbrek hasarı veya GFR değerinde azalma durumunun olması olarak tanımlanmıştır (Sarnak ve ark 2003, Levey ve ark 2003). GFR birim zamanda glomerülden filtre edilen plazma miktarıdır. GFR genelde bütün fonksiyon gören nefronların toplam filtrasyon hızını belirtir. Normal GFR değeri erişkinlerde 125 mL/dk (mL/dk x 1.73m2) (Levey ve ark 2003, Lippi ve ark 2001). KBY evreleri Çizelge 1.1.1’ de gösterilmiştir.
4
Tablo 1.1.1. Kronik Böbrek Yetmezliğinin Evreleri (Ulusal Böbrek Vakfı (NKF))
Evre Tanımlama GFR ml/dk/1,73 m2
1 Böbrek hasarı var ama GFR normal veya artmış > 90 ml/dk 2 Böbrek hasarı var GFR hafif azalmış 60-89 ml/dk 3 Orta derecede azalmış GFR 30-59 ml/dk 4 Şiddetli derecede azalmış GFR 15-29 ml/dk 5 Son dönem böbrek yetmezliği < 15 ml/dk
Böbrek Fonksiyon Rezervinin Yitirilme Dönemi
GFR azalmasının başlangıcından, kreatinin ve üre gibi maddelerin kandaki düzeylerinin artmaya başlamasına kadar geçen evredir ve semptomlar henüz görülmemektedir. Bu dönemde GFR normal düzeyde olabildiği gibi artış da gösterebilmektedir (Parmar 2002).
Hafif Böbrek Yetmezliği Dönemi
Bu dönemde kreatinin klerensi 60–89 mL/dk düzeyindedir. GFR ise normalin %25-30’u kadardır. Ayrıca kanda üre ve kreatinin seviyesi normal değerlerin üst sınırında veya normalin biraz üzerindedir. İdrar konsantrasyon yeteneğinde azalma, poliüri, noktüri, hafif anemi ve arter basıncında artma görülmektedir. Bu dönemde böbrek ek yüke dayanıksızdır. GFR’ deki azalmalar kandaki kreatinin ve üre seviyesinde ani fakat geriye dönüşlü yükselmelere neden olabilmektedir (Parmar 2002) .
5
Belirgin Böbrek Yetmezliği ve Klinik Üremi Dönemi
GFR, normal değerin %25’nin altındadır. Kandaki üre ve kreatinin değerleri belirgin ve kalıcı bir şekilde yükselmiştir. Ayrıca anemi belirginleşmiş, poliüri yerleşmiş, hafif metabolik asidoz, hipokalsemi ve hiperfosfatemi eğilimi meydana gelmiştir. Bunun yanında kalsiyum emiliminde azalma, malnütrisyon, trigliserit konsantrasyonunda yükselme meydana gelebilmektedir. GFR ’nin azalması tüm organ sistemlerini özellikle de sindirim, dolaşım ve sinir sistemlerini etkileyen, üremi adı verilen klinik tabloyu beraberinde getirmektedir (Parmar 2002) .
Son Dönem Böbrek Yetmezliği
GFR % 5’in altına indiğinde terminal üremi dönemi başlamaktadır. Plazma kreatinin düzeyi (Pcr) 10 mg/dL ’nin ve üre 200 mg/dL’ nin üzerine çıkmaktadır. Üreminin tüm belirtileri şiddetlenmekte ve idrar miktarında azalma meydana gelmektedir. Ayrıca azotemi, hipertansiyon, kalp yetmezliği, perikardit, kanamalar ve komaya kadar varabilen bilinç bulanıklığı görülebilmektedir. Terminal üremi döneminde diyaliz dışı tedavi ve diyet önlemleri yetersiz kalmaktadır (Parmar 2002).
1.1.2. Kronik Böbrek Yetmezliği Nedenleri
KBY birçok nedenle gelişebilmektedir. Bunlardan bazıları aşağıda belirtilmiştir
1. Prerenal nedenler: Böbrek süzme fonksiyonlarının bozulmasıdır. Bunlar
ciddi, uzun süren renal arter stenozu, bilateral renal arter embolizmidir.
2. Renal nedenler: Kronik glomerulonefrit, kronik tübüler intersisyal nefrit,
diabetes mellutus, amiloidozis, hipertansiyon, kistik hastalıklar, neoplazi gibi böbreğin kendine özgü hastalıklarıdır.
3. Postrenal nedenler: Toplayıcı sistemdeki bozukluklardır. Bunların arasında
en sık görülen nedenler idrar yolu obstrüksiyonu, böbrek ve idrar yolarındaki tümör ve böbrek taşları oluşturmaktadır (Akpolat ve ark 2007).
Kronik Böbrek Yetmezliği çok farklı nedenlerle gelişebilmekte ve bu nedenlerin sıklığı ülkeden ülkeye, ırka ve cinsiyete bağlı olarak değişebilmektedir. Ülkemizde görülen en önemli etiyolojik faktörler arasında; diabetes mellitus (DM), hipertansiyon (HT), kronik glomerulonefrit ve ürolojik hastalıklar gelmektedir (Erek ve ark 2006, Akploat ve ark 2007).
6
Çizelge 1.1.2. Hemodiyaliz Hastalarında Etiyoloji (Türk Nefroloji Derneği)
1.1.3. Kronik Böbrek Yetmezliği Prevalansı
1990 yılından beri Türkiye’de diyaliz ve transplanstasyon kayıtları TND tarafından toplanmakta ve her yıl kitapçık halinde yayınlanmaktadır. 2008 yıl sonu itibariyle düzenli hemodiyaliz tedavisinde olan hasta sayısı 46659, düzenli periton diyaliz tedavisinde olan hasta sayısı 6109 ve böbrek transplantasyonu ile yaşayan hasta sayısı 7824 olarak bildirilmiştir (Türk Nefroloji Derneği registry raporu 2008).
2008 yılında Türkiye’de renal replasman tedavisi gerektiren son dönem kronik böbrek yetmezliği (SDBY) nokta prevalansı milyon nüfus başına 756 olarak saptanmıştır (TND registry raporu 2008). 2008 yılı için SDBY, tüm dünya üzerinde farklı prevalanslar göstermektedir (United States Renal Data System USDRS 2009).
7
Çizelge 1.1.3. SDBY Prevalansı, 2006 (USDRS 2008).
1.1.4.Kronik Böbrek Yetmezliğinin Klinik Özellikleri
Hastaların klinik semptom ve bulguları böbrek yetmezliğinin derecesi ve gelişme hızı ile yakından ilişkilidir. GFR değeri 35-50 ml/dk olana kadar hastalar semptomsuz olabilir. GFR 20-25 ml/dk olunca hastalarda üremik semptomlar ortaya çıkmaya başlar. GFR 15 ml/dk olduğunda SDBY bahsedilir ve hastalar diyaliz, renal transplantasyon gibi renal replasman tedavilerine gerek duyarlar (Akpolat ve ark 2007). KBY’ nin belirtileri, protein yıkım ürünlerinin kanda artması, sıvı- elektrolit ve asit-baz dengesi bozuklukları olarak ortaya çıkmaktadır. Bu bozukluklar tüm sistemleri etkilemektedir.
8
Su ve Elektrolit Atım Değişikliği
Hastalarda poliüri görülmektedir. Böbreğin idrarı konsantre etme yeteneği bozulmaktadır. KBY’ de plazma sodyum miktarı böbrek yetmezliğinin son evresine kadar normal düzeyde kalabilmektedir. Sağlam nefronlarla potasyum atımı hızlandığı için, terminal döneme kadar potasyum normal düzeydedir. Terminal dönemde ise hipernatremi, hiperpotasemi ve hiperfosfatemi görülmektedir. Hipernatremi ve hipoalbünemiye bağlı olarak ödem gelişebilmekte ve bu durumda da oligüri ve anüri olabilmektedir (Baysal ve ark 2002). Sıvı dengesi bozukluklarında poliüri, noktüri, polidipsi görülebilmektedir. Hipokalsemi genel bir bulgu olup hiperfosfatemi ile birlikte görülebilmektedir. Bunun yanı sıra, serum magnezyum değeri de yükselmektedir. KBY’ de proteinüri nedeniyle serum albümin ve dolayısıyla onkotik basıncın düşmesi, sodyum ve su retansiyonu nedeniyle hidrostatik basıncın artması ödem oluşumunun nedenleri arasındadır (Akpolat ve ark 2007).
Asit- Baz Dengesinin Bozulması
Vücudun asit-baz dengesini sağlamak böbreklerin önemli bir fonksiyonudur. KBY’ de böbrek fonksiyonları ileri derecede bozulduğu için metabolik asidoz gelişebilmektedir. Metabolik asidozun gelişmesinde, hidrojen iyon sekresyonu azaldığı için asit atılımı bozulur, bikarbonat geri emilimi azalmıştır, NH3 den NH4 yapımı azalmıştır ve sonuçta titre edilebilen asit yapımı azalmıştır. GFR çok düşerse (10 ml/dk’ nın daha da altına) asidosiz ağırlaşabilmekte ve kussmaul solunum ortaya çıkabilmektedir (Kazancı 2004, Akoğlu 2000).
Üremik Toksinlerin Birikmesi
KBY ‘de GFR’ nin 30 mL/ dk’ nın altına inmesi ile kanda çeşitli metabolitler, özellikle protein metabolizmasının son ürünleri birikmektedir. Üre, kreatinin, ürik asit, metil guanidin gibi üremik toksinler ile aminoasitler, indoller, parathormon, büyüme hormonu, gastrin, renin, kalsitonin ve prolaktinin organizmada birikmesi vücuttaki diğer organları da etkilemektedir ( Akpolat ve ark 2007).
9
Kardiyovasküler Belirtiler
Renin sekresyonunun artışı ve volüm fazlalığı nedeniyle oluşan hipertansiyona sıklıkla rastlanmaktadır. En önemli faktör hastalıklı böbreğin yeterli miktarda sodyumu atamaması nedeni ile vücuttaki suyunda artmasıdır. Hastalar normal ağırlıklarına indirildiği zaman büyük bir kısmında kan basıncını kontrol etmek mümkün olabilmektedir. KBY hastalarında hipertansiyona bağlı kardiyovasküler hasarlar ve hiperlipidemiler oluşabilmektedir. Konjestif kalp yetmezliği, akciğer ödemi ve üremik perikardit sık görülen komplikasyonlarıdır. Üremik perikarditin nedeni ürenin seröz zarlarda toplanmasıdır (Serdengeçti 1997).
Gastrointestinal Belirtiler
Sıklıkla görülen bulantı, kusma ve iştahsızlık terminal devreye doğru hastanın durumunu ağırlaştırmaktadır. Bu şikayetlerin nedeni kan üre düzeyinin yüksek olmasıdır. Ayrıca ağız mukozasında iltihaplanma, ağız kokusu, mide ülseri, gastrointestinal kanamalar, konstipasyon ve diyare görülebilmektedir. Üremik koku; tükürükteki üreden üreaz enzimi aracılığıyla oluşan NH3 oluşumu ve oral hijyen
bozukluğu nedeni ile oluşmaktadır. Anoreksi, bulantı, kusma, üreye ve üremik toksinlere bağlı gastrik irritasyon, dehidratasyon, elektrolit boşalması ve hipertansif ensefalopati buna katkıda bulunabilmektedir. Üremik gastroenterit; üreye veya üreden oluşan NH3 irritasyonunun yol açtığı mukoza ülserasyonları sonucu meydana
gelmektedir (Baysal ve ark 2002).
Hematolojik Belirtiler
Hastalarda anemi ve kalp pıhtılaşmasında bozukluk görülebilmektedir. Aneminin başlıca nedenleri eritrositlerin yapımının azalması, ömrünün kısalması ve kan kayıplarıdır. Eritrosit yapımının azalmasının nedeni; ertitropoetin (EPO) oluşumunda azalma, kemik iliğinin baskılanması, demir emilimi ve kullanımında meydana gelen bozukluk ve folik asit yetersizliğidir. Normal kişilerde eritrosit yaşam süresi 120 gün olmasına rağmen KBY olan hastalarda bu süre 70-80 gündür. Eritrosit ömrünün kısalmasına neden olan faktörler ise üremik toksinler ve mikroanjiyopatidir. KBY’ de anemiyi etkileyen diğer bir neden de diyalizat sıvısında bulunan bazı oksidan maddelerdir. Bu maddeler kloramin, bakır ve çinkodur. Kan kayıpları, burun kanamalarından ve gastrointestinal yolla olan kanamalardan kaynaklanabilmektedir. Ayrıca analiz için sıklıkla kan alınması ve hemodiyalizdeki
10 kayıplarda bu sonucu oluşturabilmektedir. KBY hastalarında oluşan kanamaların temel nedeni pıhtılaşma bozukluğudur. Trombosit sayısında bir azalma vardır fakat genellikle normalin alt sınırındadır. Trombosit agregasyonu ve yapışkanlığı bozulmuştur. Bu nedenler trombosit fonksiyon bozukluğu nedeniyle bu bireylerde pıhtılaşmada sorun meydana gelmekte kanama zamanlara uzamaktadır (Akoğlu 2000).
Dermatolojik Belirtiler
Hastaların hemen hemen hepsinde deri rengi kirli- koyu- kahverengidir. Ciltte idrarla atılamayan pigmentinin birikimi ve anemileri nedeni ile bu renkte bir görünümleri olur. Ciltte kolaylıkla morarmalar olmaktadır. Kaşıntı özellikle boyun, göğüs, bacak ve kollarda daha belirgindir. Üre yüksekliği ile paralel olarak, ter ile ürenin atılmasına bağlı olarak üremik frost adı verilen cilde tuz serpilmiş gibi zannedilen üre kristallerini fark etmek mümkündür. Cilt genellikle kurudur ve diyalizdeki hastalar da daha belirgindir (Akoğlu 2000).
Nörolojik Belirtiler
Hastalarda erken dönemde mental konsantrasyon kabiliyeti bozulmuştur. Üremik bulgular ilerledikçe hastalar baş dönmesinden, uykusuzluktan şikayet etmektedirler. Üremik bulgular ilerledikçe adale çekilmeleri, baş ağrıları, uykuya meyil ve konvulsüyonlar görülebilmektedir (Kazancı 2004).
Renal Osteodistrofi
Renal osteodistrofi erken dönemlerde genellikle klinik belirti vermemektedir. Ancak kontrol edilmezse diyaliz döneminde ağrıya yol açılabilmekte, hastanın aktivitesi ve mobilizasyonunu büyük ölçüde etkileyebilmektedir. Bu kemik bozuklukları grubu içinde osteitis fibroza, osteoskleroz, osteomalazi ve osteoporoz bulunmaktadır. Bu tablonun ortaya çıkış sebebi paratiroid hormonunun fazla salgılanmasıdır (Akoğlu 2000).
Sinir Sistemi Belirtileri
Oksijenin beyin tarafından kullanımının azalması, iyon konsantrasyonundaki değişimlere ve üremik toksinlere bağlı olarak konfusyon (bilinç bulanıklığı) ve konvülsiyon (istem dışı kasılma) oluşabilmektedir(Akpolat ve ark 2007).
11
1.1.5. Kronik Böbrek Yetmezliği Tedavisi
2002 yılında National Kidney Foundation (NKF) tarafından Amerika Birleşik Devletlerinde hazırlanan kılavuzda önerilen tedavi planı aşağıdaki gibi olmalıdır (Weiner ve ark 2007).
1. Altta yatan hastalığın tedavisi
2. Böbrek yetmezliğinin ilerlemesini hızlandıran faktörlerin kontrolü, böbrek yetmezliğinin yavaşlatılması
3. Böbrek fonksiyonlarında azalmanın yol açtığı sorunların önlenmesi ve tedavisi
4. Son dönem böbrek yetmezliği gelişen hastalarda renal replasman tedavisinin uygulanmasıdır.
SDBY olan hastalarda renal replasman tedavileri; hemodiyaliz, periton diyalizi ya da renal transplantasyondur. Türk Nefroloji Derneği’nin 2008 verilerine göre; Türkiye’de 2008 yıl sonu itibariyle mevcut SDBY hastalarının RRT tipleri, %74.9’u HD, %9.6 PD ve %14.4 renal transplantasyon olarak bildirilmiştir (Türk Nefroloji Derneği Registry Raporu, 2008). Kronik diyaliz tedavisine başlamak için kullanılan en objektif parametre glomeruler filtrasyon değeri olup glomeruler filtrasyon değerinin ölçülmesinde en sık kullanılan yöntem kreatinin klirensidir. Kreatinin klirensi 10 – 15 ml/dk düzeyine inince kronik diyaliz tedavisine başlanmaktadır.
Hemodiyaliz
Hemodiyaliz, hastadan alınan kanın antikoagulasyonla vücut dışında makine yardımıyla yarı geçirgen bir zardan geçirilerek, sıvı solüt içeriğinin yeniden düzenlenip hastaya geri verilmesi işlemidir. İlk olarak 1946 yılında Willem Koff tarafından akut böbrek yetmezliğinin tedavisinde, 1960’lardan itibaren de giderek KBY hastalarının tedavisinde uygulanmaya başlanmıştır. Normalde hastanelerin böbrek diyaliz ünitelerinde yapılır. Hastanın sağlık durumuna göre haftada 2-3 kez uygulanmalıdır. Her seans yaklaşık 4-6 saat sürmektedir (Levy ve ark 2004)
Hemodiyalizin gerçekleştirilmesi için küçük bir cerrahi operasyona ihtiyaç vardır. Bu operasyon hastaya yapılan hemodiyaliz işlemini hızlandırmak ve
12 kolaylaştırmak için uygulanır ve damarların birleştirilmesi şeklinde gerçekleştirilir. Hemodiyalizatık maddeleri vücuttan hızla ve başarıyla uzaklaştırır.
Hemodiyalizin Prensibi
Kan, diyalizör (yapay böbrek) olarak bilinen bir filtrede temizlenmek üzere vücut dışına çıkarılır. Diyalizör, selüloz veya benzer bir üründen yapılmış yarı-geçirgen bir membranın bir tarafından kanın diğer tarafına dializatın akması prensibine göre işler. Diyalizat, normalde vücutta bulunan fakat böbrek yetersizliliğinde aşırı miktarlara varan mineral ve tuzlardan ayarlanmış bir miktar içerir. Membranın değişik boyutlardaki küçük delikleri; kandaki fazla sıvı ve maddelerin değişik hızlarda küçük moleküller hızlı ve büyük olanlar daha yavaş, geçerek kanda doğru bir denge sağlanana kadar diyalizata aktarılmasını sağlar. Bir böbrek makinesi, kan akımını, basıncı ve değişim hızını ayarlar. Herhangi bir zaman diliminde diyalizörde çok az miktarda kan olduğu için, kan hastadan diyalizöre, dializörden de hastaya yaklaşık dört saatte dolaşır. Tedavi genellikle haftada üç keredir. Her hasta için diyalizin zamanı ve miktarı programlanabilir. Tedavinin sıklığı ve süresi elbette ki böbrek yetersizliğinin derecesine ve uzaklaştırılması gereken toksin ve sıvı miktarına bağlıdır. Diyaliz tedavisinin amacı uygun sıvı ve solüt değişimini sağlamaktır. Sıvı-solüt değişiminin difüzyon ve ultrafiltrasyon olmak üzere iki temel prensibi vardır. Difüzyon membranın iki yanındaki konsantrasyon farkı nedeniyle solutun konsantrasyonu yüksek olan taraftan düşük olan tarafa hareketidir. Difüzyon hızını ve yönünü etkileyen başlıca üç faktör vardır:
1. Konsantrasyon gradienti: İki taraf arasındaki konsantrasyon gradienti
arttıkça madde alışverişi hızlanacaktır.
2. Solütlerin molekül ağırlığı ve hızı: Porlardan geçen maddelerin
molekülleri ne kadar büyük ise membrandan geçen madde miktarı ve geçiş hızı o kadar azalır.
3. Membran direnci: Yarı geçirgen membran kalınlığının artması, porların
küçülmesi veya por sayısının azalması membranların madde alışverişine karşı direncini arttırır.
Ultrafiltrasyonda uygulanan basınç nedeni ile membranın bir yanından diğer yanına sıvı transferidir. Sıvı transferine solüt transferi de eşlik eder. Hemodiyalizde
13 ultrafiltrasyon hidrostatik basınç ile sağlanırken, sürekli ayaktan periton diyalizinde ozmotik basınç ile sağlanmaktadır (Daugirdas ve ark 2003).
Hemodiyalizin Avantajları
1. Atık maddeler vücuttan hızla ve başarı ile uzaklaştırılır.
2. Diyaliz ortamı hastanın diğer hastalar ile ilişki kurmasını sağlar. 3. Her gün değil, haftada iki veya üç kez uygulanır.
4. Malnütrisyon ile daha az karşılaşılır. 5. Hastaneye yatma gereksinimi daha az olur. 6. Karına ait komplikasyonlarla karşılaşılmaz. Hemodiyalizin Dezavantajları
1. Tedavi seansları arasında sıvı-elektrolit ve metabolik değişime bağlı olarak
diyaliz sonrası hastanın kendini iyi hissetmesi, ancak sonraki seansa kadar yavaş yavaş tekrar kötüleşmesi sonucu olaşan rahatsızlık hissedilmektedir.
2. Tedavi sırasında iğneler kullanılmaktadır.
3. Çeşitli sıvı ve gıdaların alınmasında kısıtlanmalar vardır. 4. Fistül için minör cerrahi bir girişim gerekmektedir. Hemodiyalizin Komplikasyonları
Hemodiyalizin komplikasyonları sık rastlanan ve daha az rastlanan fakat ciddi olan komplikasyonları olarak ikiye ayrılmaktadır. Sık görülen komplikasyonları; hipotansiyon, kas krampları, huzursuz bacak sendromu, bulantı, kusma, baş ağrısı, göğüs ve sırt ağrısı, kaşıntı, titreme ve ateştir. Daha az rastlanan fakat ciddi komplikasyonlar; disekilibrium sendromu, anafilaktik reaksiyonlar, aritmiler, kalp tamponadı, intrakranial kanama, konvülziyonlar, hemoliz, hava embolisi ve hipoksemidir (Ayköse 2006).
Periton Diyalizi (PD)
Son dönem böbrek yetmezlikli hastalarda böbrek fonksiyonlarının kesintisiz olarak, doğal bir membranla herhangi bir kuvvete veya alete gerek duyulmadan yerine koyma düşüncesinden periton diyalizi geliştirilmiştir. Periton boşluğundaki solüt ve su absorbsiyonu periton zarındaki kapiller dolaşım ve lenfatikler yardımıyla
14 olur. Periton zarı toksik maddeleri filtre eden yarı geçirgen zar vazifesi görür(Daugirdas ve ark 2003). Periton diyalizinde vücut ısısına kadar ısıtılmış genelde 2 litre diyaliz solüsyonu periton boşluğuna yerleştirilmiş olan kateter vasıtasıyla 10 dakika gibi bir sürede periton boşluğuna verilir. Periton diyaliz tipine göre değişen periyotta bu solüsyonlar periton boşluğunda bekletilir. Bekleme sürecinden yaklaşık 20 dakika içerisinde diyalizat periton boşluğundan geri alınır ve yeni bir diyalizat tekrar periton boşluğuna verilir.Bu işlem genel olarak günde 4 kez, haftanın 7 günü uygulanır (William ve Henrich, 1999). Periton diyaliz hastaları için altı farklı periton diyaliz yöntemi vardır. Bunlar; sürekli ayaktan periton diyalizi, aletli periton diyalizi, aralıklı periton diyalizi sürekli siklik periton diyalizi, gece periton diyalizi ve tidal periton diyalizidir. Hem hastanın sosyal şartlarına uygun hem de periton diyalizinin gerek solüt klirensi gerekse ultrafiltrasyon transferini en yükseğe çıkaracak olan bir periton diyaliz yöntemi seçilir (Ayköse 2006).
Transplantasyon
Transplantasyon, SDBY’nin seçkin tedavi şeklidir. Çünkü transplantasyon ile, diyaliz tedavilerinde olduğu gibi böbrek fonksiyonlarından bazıları değil tamamı yerine getirilir. Ayrıca diyaliz işleminin oluşturduğu fiziksel ve psikolojik zorluklar ortadan kalktığından yaşam kalitesi daha iyidir. Fakat transplantasyon yapılabilmesi için alıcının hayatı tehdit eden ekstarenal komplikasyonlarının olmaması gerekir. Primer oksaloz, tedavi edilemeyen psikoz, immünsupresif tedavi ile ilerleyici bir hastalığın olması transplantasyona engeldir. Yaygın damar harabiyeti olmadığı sürece diyabetes mellitus kesin kontrendikasyon değildir (Ayköse 2006).
1.1.6. Kronik Böbrek Yetmezliği ve Kardiyovasküler Hastalık
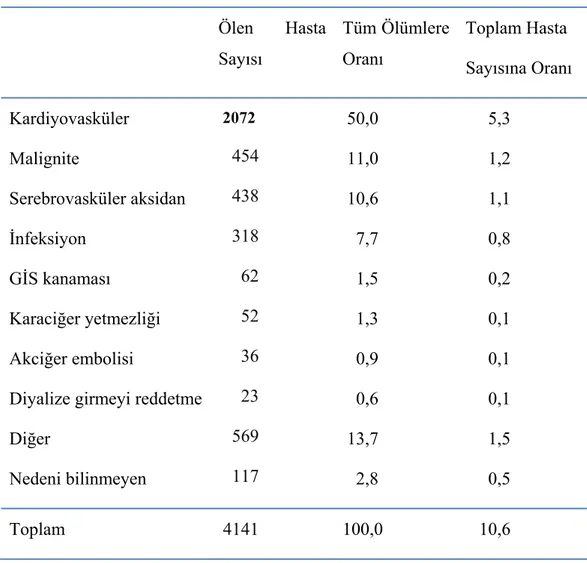
Kardiyovasküler hastalıklar koroner kalp hastalığı, serebrovasküler hastalık, artmış kan basıncı (hipertansiyon), periferal arter hastalığı, romatizmal kalp hastalığı, konjenital kalp hastalığı ve kalp yetmezliğini kapsamaktadır. SDBY olan hastalarda, genel popülasyona göre, en büyük risk faktörü kardiyovasküler hastalıklara (KVH) yakalanma riskinin yüksek olmasıdır. SDBY olan hastalarda ölüm nedenlerinin yaklaşık %50’si KVH’a bağlıdır (Türk Nefroloji Derneği Registry Raporu 2008). Bunu serebrovasküler hastalık, malignite ve infeksiyonlar izlemektedir (Çizelge1.1.6.). Diyaliz hastaları kardiyovasküler hastalıklar yönünden yüksek risk altındadır. Diyaliz hastalarının yaklaşık yarısında klinik açıdan önemli
15 kardiyovasküler komplikasyonlar görülebilmektedir. Konjestif kalp yetersizliği, iskemik kalp hastalıkları ve aritmiler diyaliz hastalarında en sık görülen kardiyovasküler komplikasyonlardır. Toplumdaki klasik kardiyovasküler risk faktörlerine, böbrek yetmezliği ve diyalize bağlı risk faktörlerinin eklenmesi mortalite ve morbitidenin artışı gözlemlenmiştir. Risk faktörlerinin ortadan kaldırılması, kalp yetersizliklerinin, aritmilerin ve koroner arter hastalıklarının erken tanısı ve tedavisi diyaliz hastalarında yaşam beklentisini ve kalitesini arttıracaktır (Aydınalp ve Müderrisoğlu 2006).
SDBY olan hastalarda KVH risk faktörleri geleneksel ve geleneksel olmayan risk faktörleri olmak üzere iki grupta incelenmektedir. Bu risk faktörleri ve KVH’ın özellikleri aşağıdaki tablo 1.1.6.2’de gösterilmektedir
Tablo 1.1.6.1. 2008 yılında ölen HD hastalarının ölüm nedenlerine göre dağılımı (690 adet tıbbi merkezden gelen sonuçlara göre)
Ölen Hasta Sayısı Tüm Ölümlere Oranı Toplam Hasta Sayısına Oranı Kardiyovasküler Malignite Serebrovasküler aksidan İnfeksiyon GİS kanaması Karaciğer yetmezliği Akciğer embolisi
Diyalize girmeyi reddetme Diğer Nedeni bilinmeyen 2072 454 438 318 62 52 36 23 569 117 50,0 11,0 10,6 7,7 1,5 1,3 0,9 0,6 13,7 2,8 5,3 1,2 1,1 0,8 0,2 0,1 0,1 0,1 1,5 0,5 Toplam 4141 100,0 10,6
16
Tablo 1.1.6.2. KVH risk faktörleri
GELENEKSEL GELENEKSEL OLMAYAN
Yaş Cinsiyet Total kolesterol LDL ↑ HDL ↓ Diabetes mellitus Hiper tansiyon Sigara Fiziksel aktivite Hiperhomosisteinemi Aile öyküsü GFR oranı Proteinüri Anemi Kalsiyum/fosfor metabolizması İnflamasyon Malnütrisyon Oksidatif stres Renin-anjiyotensin sistem 1.2. Yüksek Duyarlıklı CRP (hsCRP)
Yüksek duyarlıklı CRP (hsCRP), klasik CRP den farklı bir analit izlenimi yaratmasına rağmen gerçekte farklı değildir. Kullanılan ölçüm yönteminin daha düşük düzeyleri tespit edebildiğini belirten bir CRP ölçüm yöntemidir ( Punzi ve ark 2005)
CRP, 120 kDa ağırlığında, non-kovalent bağlı, beş özdeş polipeptid alt birimden meydana gelen, pentraksin ailesinden, bir prototip akut faz proteinidir. Her bir polipeptid ünitesi 206 aminoasit kalıntısı içerir. Bu beş protomer kovalent olmayan bağlarla halkasal biçimde bağlanarak pentamerik simetri oluştururlar (Thompson ve ark 1999). Her bir protomer iki katlı β tabakadan oluşan tipik lektin kıvrımı içermektedir (Pepys ve Hirschfield 2003).
17
Şekil 1.2. Her bir protomerin ligand bağlayıcı yerindeki iki kalsiyum atomu ve lektin kıvrımlarını gösteren kristal yapının şerit diyagramı (Pepys ve Hirschfield 2003)
Akut faz yanıtında hızlıca yükselmesi, 24-48 saat içinde binlerce kat artabilmesi, hızlıca eski seviyelerine inmesi, diürnal varyasyon göstermemesi, yaş ve cinsiyet farkı göstermemesi, diyetten etkilenmemesi CRP’nin çarpıcı biyolojik özelliklerindendir. İlk olarak 1930 yılında Tillet ve Frances, akut hastalığı olan bireylerin serumlarında, Streptococcus pneumoniae’nin hücre duvarındaki C-polisakkaride bağlanıp çökelti oluşturan bir madde tanımlamışlardır. 1941’de, bunun bir protein olduğu gösterilmiş ve C-reaktif protein (CRP) adı verilmiştir. İnflamatuar yanıtta artacak olan ilk akut faz reaktanlarındandır. Karaciğerde interlökin-6 (IL-6)'nın kontrolü altında sentezlenir. Polisakkaritlere bağlanma özelliği vardır. Kalsiyum iyonlarının varlığında fosforilkolin, fosfatidilkolin ve nükleik asitler gibi polianyonlara, kalsiyum iyonları yokluğunda ise histonlar gibi polikatyonlara bağlanabilir. CRP bu moleküllerden birine bağlandığında klasik kompleman yolunu aktive eder. İnflamasyonun nonspesifik bir göstergesidir. İnflamasyon, infeksiyon,
18 malignansi ve otoimmun hastalıklar gibi birçok durum serum CRP düzeylerinde artışa yol açar (Kurubacak 2007). Akut inflamasyonu olan hastalarda CRP düzeyi 1000 katına kadar artabilir. C-reaktif proteinin plazma yarı ömrü yaklaşık 19 saattir. Bu süre sağlık ve hastalıkta sabittir. Bu nedenle dolaşımdaki CRP düzeyinin tek belirleyicisi sentez hızıdır (Vigushin DM.ve ark. 1993). Sentez hızı da, CRP üretimini uyaran patolojik durumların şiddetini gösterir. Artmış üretimi yapan uyarı tümüyle bittiğinde dolaşımdaki CRP düzeyi hızla düşer, neredeyse plazmadaki CRP klirens değerine ulaşır . C-reaktif protein’in sentez hızına, duyarlılığına ve normal aralığına bakıldığında, genel toplumdaki her bir birey; travma, inflamasyon, küçük veya subklinik inflamasyonda olabilecek nadir yükselmeler dışında sabit bir CRP düzeyine sahiptir. Otoimmun hastalıklar ve malignansilerde CRP'deki artış uzun süre kalıcı olabilir. Sağlıklı bireylerin %90 kadarında CRP düzeyleri 0.3 mg/dl’nin altındadır. Kardiyovasküler risk saptanmasında CRP düzeyleri <1, 1-3, >3 mg/L; sırası ile düşük, orta ve yüksek risk gruplarını gösterir (Ridker ve Cook 2004). CRP yıllarca doku hasarı ve inflamasyonun teşhisinde kullanılmasına rağmen son yıllarda kardiyovasküler hastalıkların teşhisinde de kullanılmaya başlanmıştır. Bu da ateroskleroz ve akut koroner sendromların gelişiminde inflamasyonun rolünün daha iyi anlaşılması ile ortaya çıkmıştır. Laboratuar ve klinik bulgular aterosklerozun basit bir lipid depo hastalığı olmadığını, aterotrombotik gelişimde sistemik inflamasyonun da rol oynadığını göstermiştir. Arteriyel duvardaki ateromatoz plaklarda mononükleer hücrelere, makrofajlara ve T lenfositlere yoğun şekilde rastlanmaktadır. Aterosklerozun inflamatuar komponentlerinin anlaşılmasında CRP’ nin önemli bir rolü olduğu kanıtlanmıştır. Bununla birlikte, kardiyovasküler hastalıkların teşhisinde ve riskinin belirlenmesinde CRP’ nin kullanılabilmesi için daha hassas olarak ölçümüne gerek vardır. Bu amaçla hs-CRP ölçüm metodları geliştirilmiştir. Klinik çalışmalar hs-CRP’ nin sağlıklı görünen kişilerde ileride gelişecek bir inme, AMİ ve periferik vasküler hastalık için güçlü ve bağımsız bir risk faktörü olduğunu göstermiştir. Gelecekte oluşacak KKH riskini belirlemede hs-CRP'nin değeri, total kolesterol, HDL kolesterol, LDL kolesterol gibi geleneksel biyokimyasal göstergelerden veya lipoprotein a, homosistein, apolipoprotein A ve B gibi diğer göstergelerden önemli ölçüde daha yüksektir (Kurubacak 2007).
Zaman içinde hsCRP için immünokimyasal yöntemler ticari olarak geliştirilmiştir. Anti-CRP antikorların enzim ile işaretlenmesi (ELISA) veya floresan
19 bileşiklerle işaretlenmesi, monoklonal veya poliklonal antikorların polistren boncuklara yapıştırılması gibi yöntemler kullanılmıştır. Günümüzde kullanılan ölçüm yöntemleri arasında, ELISA’nın en yüksek duyarlılık ve özgüllüğe sahip olduğu belirtilmektedir (Rıfai ve Ridker 2001).
1.3. IL-6
İnterlökinler, sitokinler olarak bilinen daha geniş bir polipeptid sınıfının bir parçasıdır. Bunlar immün sistemin çeşitli hücreleri arasındaki sinyalleri ileten haberci moleküllerdir. Sitokinler, doğal ve spesifik immunütenin bir protein aracı grubudur. Genelde sitokinler bir inflamatuar veya antijenik etkileşime yanıt olarak sentezlenir. Sitokinler, lenfositlerin olgunlaşıp farklılaşmalarını sağlarlar. Kökenlerine göre sitokinler üç gruba ayrılabilir. Bunlardan birincisi, mononükleer fagositlerden köken alan monokinler, ikinci grup lenfositlerden köken alan lenfokinler, üçüncü grup ise lökositlerden köken alan interlökin grubu sitokinlerdir. Fonksiyonel olarak sitokinler sınıflandırıldığında infeksiyoz ajanlara karşı genelde mononükleer hücreler tarafından sentezlenen doğal immünite sitokinleri (TNF, IL-1, IL-12, IFN, IL-10, IL-6, IL-15, IL-8 ) ve yabancı antijenlerin spesifik tanımlanması sonrası cevapta genelde T lenfositleri tarafından sentezlenen adaptif immünite sitokinleri olarak sınıflandırılabilirler (Hall 1989).
IL-6, 21-30 kDa ağırlığında tek bir protein zincirinden oluşan, 212 aminoasit içeren O ve N- glikolizasyon ve fosforilasyon bölgeleri içeren bir polipeptiddir(Demirel Yıldırım 2009). IL-6 ilk olarak proaktivasyon halindeki normal insan lenfositleri ve Ebstein Barr virüsünce transformasyona uğratılmış B lenfositler tarafından
immunglobulin salgılatan bir faktör olarak tanımlanmıştır. Çok yönlü işleve sahip bir sitokin olarak hematopoezi, akut faz reaktanlarını, immun yanıtı düzenler ve konağın savunma mekanizmasında merkezi bir rol oynar. Dendritik hücreler,
monositler, makrofajlar ve aktive olmuş T hücreleri, endotel hücreleri, osteoblastlar, fibroblastlar, mast hücreleri, astrositler, keratinositler ve timositler tarafından
sentezlenir. Lenfosit, monosit, mesane ve akciğer hücerleri tarafından
oluşturulabildiği gibi kardiyak miksoma, myeloma ve hipernefroma gibi tümör hücrelerince de oluşturulabilmektedir (Naka ve ark 2002; Kishimoto ve ark 1995).
20
Şekil 1.3.1. IL–6’nın fizyolojik etkileri (Trikha ve ark 2003 )
Serum IL-6 seviyesi, yaralanmanın şiddetini yansıtır, bütün sitokinler arasında ve kısmen sepsiste en güvenilir prognostik göstergedir. IL-6, 7p21 yerleşimli IL-6 geni tarafından eksprese edilen proinflamatuar bir sitokindir. Doğal ve adaptif immünitede yer alır. İnflamasyon, vücut savunması, doku onarımı, glukoz ve yağ metabolizmasında yer alır. IL-6, çok değişik biyolojik etkileri olan bir immün sistem mediyatörüdür. Bakteriyel toksinler ve bakteri orjinli metalloproteinazlar IL-6’ nın aktive olmuş nötrofil ve monositlerden salınımını uyarırlar. IL-6, konak savunmasında pek çok fonksiyona aracılık eder. T lenfositleri aktive ederken, B lenfositleri için de bir farklılaşma faktörü olarak rol oynar. Kazanılmış immünitede B hücrelerinden antikor üretimini uyarır. IL-2 varlığında T hücrelerinin sitotoksik T hücrelerine farklılaşmasını ve timositlerin proliferasyonunu uyarır. Ayrıca aktive olmuş makrofajların ve lenfositlerin etkilerini düzenler (Ohno ve ark 1993; Rader 2000). IL-6 akut faz cevabı için merkezi bir uyarandır, hepatositlerde akut faz cevabın artmasında rol oynar. Bu etkisini CRP, haptoglobin, fibrinojen ve proteaz inhibitörleri gibi akut faz proteinlerinin üretimini arttırarak gerçekleştirir. IL-6, CRP’nin karaciğerde üretiminde primer belirleyicidir (Daftarian ve ark 1996; Rader 2000) IL-6 endotel hücrelerinde IL-1 ve TNF-α’ın sekresyonunu arttırırken, IL-1 ve
21 TNF-α ise IL-6 sekresyonunu arttırmaktadır. Ayrıca IL-6, T lenfositlerinde IL-10 üretimi uyarır. IL-10 ise posttranskripsiyonel mekanizma ile IL-6’nın sentez ve sekresyonunu baskılar (Daftarian ve ark 1996). Bu nedenle IL-6 doğal ve kazanılmış immünitede rol oynamaktadır (Burtis ve Ashwood 1999).
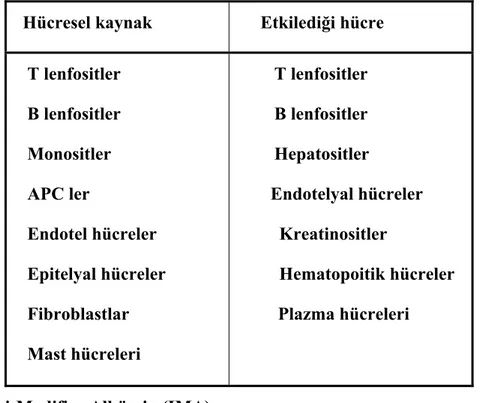
Tablo 1.3.2. IL-6’nın hücresel kaynakları ve etkilediği hücreler (Burtis ve Ashwood 1999)
Hücresel kaynak Etkilediği hücre T lenfositler B lenfositler Monositler APC ler Endotel hücreler Epitelyal hücreler Fibroblastlar Mast hücreleri T lenfositler B lenfositler Hepatositler Endotelyal hücreler Kreatinositler Hematopoitik hücreler Plazma hücreleri
1.4 İskemi-Modifiye Albümin (IMA)
İnsan serum albümini kanda en fazla bulunan proteindir ve serum albümin konsantrasyonu 3.5-5.3 g/dL dir. Karaciğerde sentezlenir ve plazma proteinlerinin %60’ını oluşturur. 585 amino asitlik primer zincirden meydana gelen insan serum albümini 17 disülfid köprüsü ve bir serbest sistein amino asitinden meydana gelmiştir (Sugio ve ark 1999). Plazma onkotik basıncının ayarlanmasında önemli olan albümin, kan pH’sının ayarlanmasında da tampon görevi görür. Amino asit deposu gibi görev yaparak karaciğerin protein sentezi aktivitesini destekler. Tiroksin, bilirübin, kortizol, östrojen, serbest yağ asitleri gibi endojen moleküllerin; varfarin ve penisilin gibi bir çok ilacın; kalsiyum, magnezyum, hemin gibi metabolizma için önemli ya da toksik olan organik veya inorganik bir çok maddenin taşınmasında görev alır (Smi ve ark 1993).
Miyokardiyal iskemi hastalarının serum albümini metal bağlama kapasitesinin, normal deneklerin serum albüminin kapasitesinden düşük olduğu
Bar-22 Or ve arkadaşları tarafından keşfedilmiştir. İnsanlarda; geçiş metallerinden olan bakır (II), nikel (II) ve kobalt’ın (II) primer yüksek affinite bağlama bölgesinin albüminin N-terminalinde lokalize olduğu ve ilk üç amino asitin (aspartik asit, alanin ve histidin) kobaltın koordinasyonunu sağladığı pek çok çalışmada kesin olarak kanıtlanmıştır. Albümine geçiş metallerinin ikinci bağlama bölgesi de tanımlanmıştır. Bakır ve nikel için bir diğer güçlü bağlama bölgesi ve tiyol, histidin, triptofan ve tirozinler gibi pek çok zayıf bağlama bölgesi vardır. Bakırın molar ekivalanlarıyla yapılan titrasyon deneyleri; birinci bağlama bölgesi (N-terminal) ile ikinci bağlama noktası arasında affinite farklılığı olduğunu göstermiştir. Böylece ikinci bağlama bölgesi, ancak birinci bağlama bölgesinin satürasyonu sonrası uygun olur (Bal ve ark 1998). Miyokardiyal iskemi hastalarında gözlenmiş olan metal bağlama olayındaki azalmadan, birinci bağlama bölgesindeki iskeminin neden olduğu modifikasyonların sorumlu olduğu kabul edilmiştir (Fagan ve ark 2002).
N-terminali hasarlı olan albümin, iskemi-modifiye albümin olarak adlandırılır. Sentetik peptidlerin kullanımıyla, albüminin N-terminalindeki mevcut aminoasitler temsil edilmektedir. Bar-Or ve arkadaşları, N-terminaldeki aspartat veya aspartat ve alanin rezidülerinin her ikisinin yer değiştirme ya da asetilasyonla elimine edilerek N-terminal tripeptidinin bağlama kapasitesini gösterebilmişlerdir. İki pozisyonundaki alanin ile prolinin substitüsyonu metal bağlamayı elemine eder. N-terminal bölgesine bağlı bakır, kobaltın bağlanmasını da engeller. Çünkü bakırın bağlama sabiti Ka = 1.5 x 10 16 L / Mol’dür ve bağlama sabiti Ka = 6.5 x 10 3 L / Mol olan kobalttan çok daha büyüktür. Denemenin inkübasyon süresi boyunca bu sabitlerde değişim meydana gelmez (Nandedkar ve ark 1974).
23 Doksanlı yılların sonunda akut koroner sendromlu hastaların serumunda bulunan insan serum albumininin, ekzojen kobaltı (Co) bağlamasında azalma olduğu tespit edilmiş ve ardından iskemi-modifiye albumin (IMA) olarak bilinen bu metabolik varyant, ‘Albümin Kobalt Bağlama’ (ACB) testi ile ölçülebilir hale getirilmiştir (Bar-Or ve ark 2000, Cichota ve ark 2008, Renda ve ark 2009).
Albümin kobalt bağlama testi (ACB) olarak adlandırılan test; serum albümini ile geçis metali olan kobaltın bağlanması esasına dayanır. Albümin kobalt bağlayıcı (ACB: Albumin Cobalt Binding) testi, insan albüminin N-terminaline bağlanabilen hücre dışı kobaltı ölçer (Carrage ve ark 2006, Sharma ve ark 2006). IMA, albümin kobalt bağlayıcı (ACB) test ile saptanır. Bu test ile yaklaşık olarak 30 dakikada sonuç elde edilir (Pantozopoulos ve ark 2009).
Endotel ve ekstrasellüler hipoksi, asidosiz, serbest radikal hasarı ve sodyum kalsiyum pompası bozukluğu ile oluşan iskemik olaylarda, albüminin N-terminal bölgesi ve buna bağlı olarak albümin kobalt bağlanması çok kısa süre içerisinde değişmektedir . Akut kroner sendromlu hastalarda kobalt Co (II) bağlanmasının azaldığı saptanmıştır. Bağlamadaki bu azalma; albüminin NH2 terminalindeki Co (II)
geçiş metalinin bağlanma bölgeleri için değişimi yansıtır (Bar-Or ve ark 2000, Chan ve ark 1995).
İskemi-modifiye albümin (IMA), son dönem böbrek yetmezlikli hastalarda miyokardial iskemi teşhisi için yeni bir belirteçdir (Sharma ve ark 2007). IMA düzeyi ESRD’li hastalarda mortaliteyi tahmin eder (Sharma ve ark 2006). Artan IMA seviyeleri, akut miyokard infarktüsü için de akut koroner sendromla bağlantılı olarak bulunmaktadır (Hacker ve ark 2007).
Hemodiyaliz (HD), son aşamalı böbrek hastalığı (ESRD) için en çok uygulanan tedavidir. Hemodiyaliz çoğunlukla, kardiyovasküler hastalıklar içinde, ateroskleroz (damar sertliği), kalp yetmezliği ve hipotansiyonu da kapsamaktadır. HD’nin beyin ve miyokardiyum (kalbin kas tabakası) gibi iç organlarda dahil olmak üzere birçok organda iskemiye sebep olduğu rapor edilmektedir (Carrage ve ark 2006).
24
2. GEREÇ VE YÖNTEM 2.1. Çalışma Şekli
Çalışmamız; özel bir diyaliz merkezinde hemodiyaliz programına alınan 60 kronik böbrek yetmezlikli hasta grubu ile yaş ve cinsiyet yönünden benzerlik gösteren 20 sağlıklı bireyden oluşan kontrol grubunda gerçekleştirildi. Selçuk Üniversitesi Tıp Fakültesi Etik Kurulu tarafından 26.09.2008 tarih ve 2008/278 numaralı kararı ile tez projesi olarak onaylandı. Daha sonra 09202042 numarası ile Selçuk Üniversitesi Bilimsel Araştırma Projeler Koordiantörlüğü tarafından desteklenmesine karar verildikten sonra çalışmaya başlandı.
2.2. Olgu Seçimi
Özel bir diyaliz merkezinde hemodiyaliz programına alınan 60 (30 kadın ve 30 erkek) son dönem böbrek yetmezliği olan hasta ile kontrol grubu olarak 20 sağlıklı birey (11 kadın, 9 erkek) çalışmaya dahil edildi. Hastalar diyalize girme sürelerine göre bir yıldır (1.grup) , iki-beş yıl arası (2.grup) ve beş yıldan uzun süredir (3.grup) hemodiyaliz programına alınan hastalar olarak yirmişer kişilik üç gruba ayrıldı. Kontrol grubu ile hasta grupları yaş ve cinsiyet dağılımı olarak benzerdi.
Çalışma hakkında bireylere projenin amacı ve kapsamını açıklayıcı bilgiler verildikten sonra kendilerinden yazılı aydınlatılmış onam belgesi alındı.
Özgeçmişlerinde kardiyovasküler olay hikayesi olanlar, akut yada kronik enfeksiyonu olanlar, sigara ve/veya alkol kullananlar ile çalışmaya katılmayı kabul etmeyenler çalışmaya alınmadı.
2.3. Örneklerin Toplanması ve Saklanması
Bireylerden hemodiyaliz işleminden önce sabah 12 saatlik açlık venöz kan örnekleri; herhangi bir koruyucu ve antikoagülan madde içermeyen tüplere alındı.
Alınan kan örnekleri Hettich marka santrifüj cihazı ile 4000 rpm hızla 10 dakika santrifüj edilerek serumları ayrıldı. Daha sonra çalışılacak biyokimyasal analizler için yeterli miktarda serum örneği ayrılarak -80° C’de derin dondurucuda analiz süresine kadar saklandı.
25
2.4. Biyokimyasal Analizler
Cihazlar ve Teknik Araç-Gereçler
Biotek ELX50 ELISA yıkama cihazı Biotek ELX800 ELISA okuma cihazı Spekol 1300 Spektrofotometre
Dimension Xpand (Siemens, Almanya) otoanalizörü DPC shaker
Thomas Scientific vorteks
Medispec mikropipetler (10-100 μl ve 100-1000 μl ayarlamalı)
Kimyasal Maddeler
Kobalt II klorid (CoCl2) (Katalog No:102539, Merck, Almanya)
Ditiyotreitol (DTT) (Katalog No:111474, Merck, Almanya) Sodyum klorür (NaCl) (Katalog No:106406, Merck, Almanya)
2.4.1. hsCRP Ölçümü
hsCRP konsantrasyonları Dimension Xpand (Siemens, Almanya) analizöründe orijinal Siemens kitleri kullanılarak ölçüldü. Nefelometrik yöntem ile ölçüm yapıldı. İnsan CRP’sine spesifik monoklonal antikorlarla kaplı polistiren partikülleri CRP içeren örneklerle karıştırıldığında agrege olur. Bu agregatlar örnekten geçirilen bir ışık demetinin dağılmasına yol açar. Dağılan ışığın şiddeti örnekteki ilgili proteinin konsantrasyonuyla orantılıdır. Numune konsantrasyonu bilinen bir standart ile karşılaştırma yapılarak değerlendirilir.
Yöntemin çalışma içi % CV değerleri 0,69 mg/l ve 14 mg/l konsantrasyonlarda sırasıyla %2,3 ve %2,0 şeklindedir. Çalışmalar arası % CV değerleri ise aynı düzeydeki standartlar için %2,3 ve %2,7 olarak belirlenmiştir. Saptayabildiği en düşük hsCRP konsantrasyonu ise 0,175 mg/l’dir.
2.4.2. IL-6 Ölçümü
Plazma IL-6 düzeyi analizi için AssayMax Human IL-6 ELISA kiti (AssayPro,USA, Katalog no: EI1006-1) kullanılarak enzim immunoassay yöntemi ile ölçüm yapıldı.
26 Yöntemin çalışma içi ve çalışmalar arası % CV değerleri sırasıyla %5,1 ve %7 şeklindedir. Saptayabildiği en düşük IL-6konsantrasyonu ise <10 pg/ml’ dir.
Kullanılan Malzemeler
IL-6 mikroplate: IL-6’ ya karşı mürin monoklonal antikorlarla kaplanmış 96 kuyucuklu polistiren mikroplate
Şeffaf plate kapatma bantları IL-6 standardı: 0,75 ng, liyofilize
Biyotinile IL-6 antikoru (100X): IL-6’ ya karşı biyotinile antikor, 80 µl Konsantre mix dilüent (10X): 30 ml
Konsantre yıkama tamponu (20X): 30 ml Streptavidin peroksidaz konjugat(100X): 90 µl Kromojen substrat: Tetrametil benzidin, 8 ml Stop solüsyonu: 0,5 N HCL, 12 ml
Deiyonize su
Reaktiflerin Hazırlanması
1. Tüm kit içeriğinin oda sıcaklığına gelmesi için beklenir. Reaktifler oda
sıcaklığında taze olarak hazırlanır.
2. Konsantre Mix Dilüent: Deiyonize su ile 1/10 oranında dilüe edilir.
2-8ºC’ de 1 ay saklanabilir.
3. IL-6 Standardı: 0,75 ng’ lık liyofilize IL-6 standardı 0,75 ml seyreltilmiş
mix dilüent ile sulandırılarak 1 ng/ml’ lik stok IL-6 standardı elde edilir.Çözeltinin homojen olarak dağılması için 10 dakika oda sıcaklığında beklenir. Daha sonra yedi adet polstiren tüp alınarak 0,5 ng/ml, 0,25 ng/ml, 0,125 ng/ml, 0,063 ng/ml, 0,031 ng/ml, 0,016 ng/ml konsantrasyonlarda standartlar seri dilüsyonlarla, seyreltilmiş mix dilüent kullanılarak elde edilir. Son tüpe ise sadece seyreltilmiş mix dilüent konulur ve bu da 0 ng/ml’ lik standart olarak kullanılır.
4. Biyotinile IL-6 Antikoru: Antikor içeren viyal çevrilir ve 50µl konsantre
27
5. Konsantre Yıkama Tamponu: Konsantre yıkama tamponu deiyonize su
ile 1/100 oranında seyreltilir.
6. Streptavidin Peroksidaz Konjugat: Konsantre Streptavidin peroksidaz
konjugat içeren viyal çevrilir ve 50µl konsantre Streptavidin peroksidaz konjugat alınarak seyreltilmiş mix dilüent ile 1/100 oranında seyreltilir.
Çalışma Prosedürü
1. Her kuyucuğa 50’şer µl serum veya standarttan pipetlendi. 2. Plate şeffaf koruyucu ile kapatılıp 2 saat inkübe edildi.
3. 200 µl yıkama tamponu ile 5 kez yıkandı. Plate kurutma kağıdına 4-5 kez
vurularak içinde su kalmaması sağlandı.
4. Her kuyucuğa 50 µl Biotinylated IL-6 antikoru pipetlendi ve 2 saat inkübe
edildi.
5. 200 µl yıkama tamponu ile beş kez yıkandı.
6. Her kuyucuğa 50µl Streptavidin-Peroksidaz konjugat pipetlendi ve 30
dakika inkübe edildi.
7. 200µl yıkama tamponu ile beş kez yıkandı.
8. Her kuyucuğa 50µl kromojen substrat pipetlendi ve optimal mavi renk
oluşuncaya kadar (yaklaşık 12 dakika) beklendi.
9. Her kuyucuğa 50µl stop solüsyonu konuldu. Renk maviden sarıya döndü. 10. Plate ELISA okuyucuda 450 nm’de bekletilmeden okundu.
Hesaplama
Standartların konsantrasyonlarına (x ekseni) karşı standartların 450 nm’ deki absorbansları (y ekseni) kullanılarak standart eğrisi elde edildi ve bu eğriden elde edilen denklemde örneklerin absorbans değerleri girilerek konsantrasyonları pg/ml olarak hesaplandı.
2.4.3. İskemi-Modifiye Albümin Tayini
IMA düzeyleri Bar-Or ve arkadaşlarının geliştirdiği metoda göre kolorimetrik yöntem ile ölçüldü (Bar-Or ve ark 2000). Ölçümler için Spekol 1300 marka spektrofotometre kullanıldı.
28
Kullanılan Çözeltiler
Kobalt II klorür (CoCl2) Çözeltisi (1g/l)
Dithiothreitol (DTT) Çözeltisi (1,5 g/l) İzotonik NaCl Çözeltisi (9.0 g/l)
Çalışma Prosedürü
Örnek Kör
Serum 200 μL 200 μL
CoCl2 50 μL 50 μL
Oda sıcaklığında 10 dakika inkübasyon
DTT 50 μL 50 μL
Oda sıcaklığında 2 dakika inkübasyon
NaCl 1000 μL 1000 μL
Numune tüplerinin absorbansı, kör tüpüne karsı 470 nm dalga boyunda ölçüldü. Sonuçlar, absorbans üniteleri şeklinde rapor edildi (ABSUs).
Hesaplama
IMA sonuçları örneğin (hastanın) albümin değeri ve o grubun (hasta grubunun) median albümin değeri kullanılarak düzeltilir. Çünkü albümin düzeyi düştükçe IMA artar. Bu IMA değerine albümine göre düzeltilmiş ya da uyarlanmış IMA düzeyi (D-IMA) denir. Uyarlanmış IMA (D-IMA), Lippi ve arkadaşlarının önerdiği formüle göre hesaplanır (Lippi ve ark 2007).
D-IMA = Örneğin IMA Düzeyi × Örneğin AlbüminKonsantrasyonu
29
2.4.4. Diğer Biyokimyasal Ölçümler
Glukoz, trigliserid, total kolesterol, HDL-kolesterol konsantrasyonları enzimatik yöntemlerle Dimension Xpand (Siemens, Almanya) analizöründe orijinal Siemens kitleri kullanılarak ölçüldü. LDL-kolesterol düzeyleri Friedewald formülü ile aşağıdaki şekilde hesaplandı:
Total kolesterol (mg/dl) = HDL-kolesterol + VLDL ([Trig]/5) + LDL-kolesterol. 2.4.5. İstatistiksel Analiz
Bulguların istatistiksel olarak değerlendirilmesinde SPSS 15.0 for Windows istatistik paket programı kullanıldı. Önce kronik böbrek yetmezlikli hasta grupları ile kontrol grubuna ait analitik verilerin dağılımları Shapiro Wilk dağılım analizi ile incelendi. Normal dağılım gösteren parametreler (yaş, total kolesterol, HDL-kolesterol, IMA ve D-IMA) için One Way ANOVA varyans analizi ve post-hoc Tukey HSD testleri yapıldı. Normal dağılım göstermeyen parametrelerin (trigliserit, hsCRP ve IL-6) çoklu karşılaştırmaları için Kruskal Wallis, ikişerli karşılaştırmaları için ise Mann Whitney U testi testi kullanıldı. Parametreler arası ilişkiler, ikişerli olarak Spearman ve Pearson korelasyon analizleri yapılarak değerlendirildi. Sonuçlar Ortalama± Standart Sapma olarak verildi. p<0.05 değeri istatistiksel olarak anlamlı kabul edildi.
30
3. BULGULAR
Grupların yaş ortalamaları karşılaştırıldığında kontrol grubu ile hasta grupları arasında ve hasta gruplarının kendi aralarında yaş ortalamalarının benzer (Tukey HSD testi post hoc testi ile ikişerli karşılaştırmalar yapıldığında p>0,05) olduğu görülmüştür (Çizelge 3.1).
Grupların trigliserit düzeyleri karşılaştırıldığında her üç hasta grubunun ortalama trigliserit düzeylerinin kontrol grubundan daha yüksek (p<0,05) olduğu; 1.grupla 2. grup arasında, 1. grupla 3. grup arasında ve 2. grupla 3. grup arasında ortalama trigliserit düzeyleri açısından bir fark olmadığı (p>0,05) görülmüştür (Çizelge 3.1).
Grupların ortalama total kolesterol, HDL-kolesterol ve LDL-kolesterol düzeyleri karşılaştırıldığında gruplar arasında bu parametreler açısından anlamlı bir fark olmadığı (sırasıyla p>0,05) görülmüştür (Çizelge 3.1).
Grupların ortalama hsCRP düzeyleri karşılaştırıldığında gruplar arasında anlamlı bir fark olmadığı (p>0,05) görülmüştür (Çizelge 3.1).Fakat 1,2 ve 3. grupların ortalama değerlerine bakıldığında kardiyovasküler riskin orta düzeyde olduğu görülmektedir.
Grupların IL-6 düzeyleri karşılaştırıldığında üç hasta grubunun ortalama IL-6 düzeylerinin kontrol grubundan daha yüksek (p<0,05) olduğu; 1.grupla 2. grup arasında ortalama IL-6 düzeyleri açısından bir fark olmadığı (p>0,05), 1. grubun ortalama IL-6 düzeylerinin 3. gruptan anlamlı olarak yüksek olduğu (p<0,05) ve 2. grubun ortalama IL-6 düzeylerinin de 3. gruptan anlamlı olarak yüksek olduğu (p<0,05) görülmüştür (Çizelge 3.1).
Grupların IMA düzeyleri karşılaştırıldığında her üç hasta grubunun ortalama IMA düzeylerinin kontrol grubundan yüksek (p<0,05) olduğu; 1.grupla 2. grup arasında, 1. grupla 3. grup arasında ve 2. grupla 3. grup arasında ortalama IMA düzeyleri açısından bir fark olmadığı (p>0,05) görülmüştür (Çizelge 3.1).
Grupların D-IMA düzeyleri karşılaştırıldığında her üç hasta grubunun ortalama D-IMA düzeylerinin kontrol grubundan yüksek (p<0,05) olduğu; 1.grupla 2. grup arasında, 1. grupla 3. grup arasında ve 2. grupla 3. grup arasında ortalama D-IMA düzeyleri açısından bir fark olmadığı (p>0,05) görülmüştür (Çizelge 3.1).
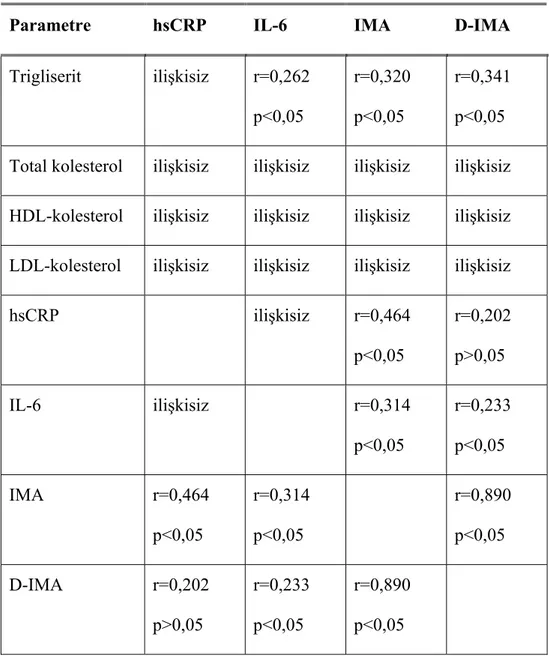
31 Parametreler arasındaki ilişkiler ikişerli olarak değerlendirildiğinde; hsCRP düzeyleri ile IMA (r=0,464; p<0,05) arasında pozitif korelasyon bulundu (Çizelge 3.2).Ancak bu analiz sonuçlarına göre hsCRP düzeyleri ile trigliserit, total kolesterol, HDL-kolesterol, LDL-kolesterol ve IL-6 düzeyleri arasında anlamlı bir ilişki bulunamadı. Ancak IL-6 düzeyleri ile trigliserit (r=0,262; p<0,05), IMA (r=0,314; p<0,05) ve D-IMA (r=0,233; p<0,05) arasında pozitif korelasyonlar bulundu (Çizelge 3.2). Fakat IL-6 düzeyleri ile total kolesterol, HDL-kolesterol, LDL-kolesterol ve IL-6 arasında anlamlı bir ilişki bulunamadı.
IMA düzeyleri ile trigliserit (r=0,320, p<0,05), hsCRP (r=0,464; p<0,05), IL-6 (r=0,314; p<0,05) ve D-IMA (r=0,890; p<0,05) arasında pozitif korelasyonlar bulundu (Çizelge 3.2). Ancak IMA düzeyleri ile total kolesterol, HDL-kolesterol, LDL-kolesterol arasında anlamlı bir ilişki bulunamadı.
D-IMA düzeyleri ile trigliserit (r=0,341; p<0,05), hsCRP (r=0,202; p>0,05), IL-6 (r=0,233; p<0,05) ve IMA (r=0,890; p<0,05) arasında pozitif korelasyonlar bulundu (Çizelge 3.2). Ancak D-IMA düzeyleri ile total kolesterol, HDL-kolesterol, LDL-kolesterol arasında anlamlı bir ilişki bulunamadı.
Bu ilişkiler içinde özellikle IMA ile hsCRP, IL-6 ve D-IMA’nın pozitif korelasyonu bu çalışmanın önemli bir sonucu olup daha önce yapılan çalışmalarda göze çarpmaması nedeniyle orjinaldir.
32
Çizelge 3.1. Hasta ve kontrol gruplarına ait demografik ve biyokimyasal veriler
Parametre Grup 1 Grup 2 Grup 3 Kontrol p
N 20 20 20 20 10 9 11 9 Erkek Kadın 10 11 9 11 Yaş 61,32±14,58 58,70±13,09 50,95±15,48 51,10±11,13 p>0,05 Trigliserit (mg/dl) 161,8±65,5 167,2±88,5 171±99,7 101,8±40,4a p<0,05 Total kolesterol (mg/dl) 193,1±59,6 165,2±36,7 163,4±37,2 179,4±35,3 p>0,05 HDL-kolesterol (mg/dl) 44,7±10,7 37,7±6,8 43,6±15,8 47,1±14,3 p>0,05 LDL-kolesterol (mg/dl) 116,1±52,5 94,3±25,9 92,5±34,2 109,2±31,1 p>0,05 hsCRP (mg/l) 0,6 (0,1-4) 0,7 (0,1-3,3) 0,55 (0,1-5,5) 0,35 (0,1-2) p>0,05 IL-6 (pg/ml) 83,07±21,35b 85,95±18,26c 75,46±10,65d 69,67±15,34e p<0,05 IMA (ABSU) 1,040±0,122 1,008±0,114 1,025±0,151 0,410±0,069f p<0,05 D-IMA (ABSU) 0,980±0,114 0,961±0,192 1,006±0,178 0,402±0,067g p<0,05
a= Her üç hasta grubunun da ortalama trigliserit düzeyleri kontrol grubundan anlamlı olarak yüksek bulundu, ancak hasta grupları arasında ise anlamlı bir fark bulunamadı.
b= 1.Grubun ortalama IL-6 düzeyleri 3.grup ve kontrol grubundan anlamlı olarak yüksek bulundu, 2.grup ile aralarında ise anlamlı bir fark bulunamadı.
33
c= 2.Grubun ortalama IL-6 düzeyleri 3. Grup ve kontrol grubundan anlamlı olarak yüksek bulundu, 1.grupla ise aralarında anlamlı bir fark bulunamadı.
d= 3.Grubun ortalama IL-6 düzeyleri 1. ve 2. gruplardan anlamlı olarak düşük, kontrol grubundan anlamlı olarak yüksek bulundu.
e= Kontrol grubunun ortalama IL-6 düzeyleri her üç hasta grubundan da düşük bulundu. f= Her üç hasta grubunun da ortalama IMA düzeyleri kontrol grubundan anlamlı olarak yüksek bulundu, ancak hasta grupları arasında ise anlamlı bir fark bulunamadı.
g= Her üç hasta grubunun da ortalama D-IMA düzeyleri kontrol grubundan anlamlı olarak yüksek bulundu, ancak hasta grupları arasında ise anlamlı bir fark bulunamadı.
Çizelge 3.2. IMA, D-IMA Seviyeleri ile Diğer Parametreler Arasındaki Korelasyon Analiz Sonuçları
Parametre hsCRP IL-6 IMA D-IMA
Trigliserit ilişkisiz r=0,262 p<0,05 r=0,320 p<0,05 r=0,341 p<0,05 Total kolesterol ilişkisiz ilişkisiz ilişkisiz ilişkisiz HDL-kolesterol ilişkisiz ilişkisiz ilişkisiz ilişkisiz LDL-kolesterol ilişkisiz ilişkisiz ilişkisiz ilişkisiz hsCRP ilişkisiz r=0,464 p<0,05 r=0,202 p>0,05 IL-6 ilişkisiz r=0,314 p<0,05 r=0,233 p<0,05 IMA r=0,464 p<0,05 r=0,314 p<0,05 r=0,890 p<0,05 D-IMA r=0,202 p>0,05 r=0,233 p<0,05 r=0,890 p<0,05
34
4. TARTIŞMA
Bizim çalışmamızda gruplar arasında hsCRP düzeyleri açısından anlamlı bir fark bulunamamıştır. Her ne kadar hasta gruplarındaki hsCRP düzeyleri kontrol grubundan yüksekmiş gibi görünse de bu fark istatistiksel olarak anlamlı değildir. Diyalize girme süresinin hsCRP üzerinde kronik bir etkisinin olmadığı görülmüştür.Fakat hsCRP değerlerinin hasta gruplarında 1mg/l civarında olması; 1,2 ve 3. Grup hastalaımızın kardiyovasküler riskinin orta düzeyde olduğunu göstermiştir.
Çalışmamızda IL-6 düzeylerinin hasta gruplarının hepsinde kontrol grubundan anlamlı olarak yüksek olduğu, hasta grupları arası karşılaştırmada ise 1 yıldır HD’ ye giren hastalarda 2-5 yıldır girenlere; 2-5 yıldır girenlerde de 5 yıldan daha uzun süredir girenlere göre anlamlı olarak yüksek olduğu görülmüştür. Bu sonuçlar bize bir inflamatuar belirteç olan IL-6’ nın daha çok akut inflamasyonla arttığını ve hemodiyalize girme süresi uzadıkça ise azaldığını göstermektedir.
Bu konuda daha önce yapılan çalışmalarda hsCRP ve IL-6 düzeyleri, daha çok HD ve kontrol grubu ya da HD işleminin öncesi ve sonrası arasında fark olup olmadığını ortaya koymaya yöneliktir ve sonuçları da birbirinden farklıdır.
181 hemodiyaliz hastası (erkek: 97; ortalama yaş, 56,3 yıl) 3 yıl boyunca izlenmiş ve bu dönem içerisinde 41 hastanın öldüğü gözlemlenmiştir. Ölümün temel nedenlerinin enfeksiyon ve kardiyovasküler hastalıktan olduğu saptanmıştır. hsCRP'nin ve albüminin serum düzeylerinin yükselmesinin ve ileri yaşın ölümle bir hayli ilişkili olduğu gözlenmiştir (Tsai ve ark 2007).
Ortalama yaşları 73 yıl, HD tedavisi gördüğü ortalama süre 44,4 ay olan 128 (80 erkek, 48 bayan) HD hastasının incelendiği çalışmada hastalar, hsCRP düzeyinde yükselme, hiperhomosisteinemi, HD ile geçen zaman, solüt aşırı birikimi ve yaş, cinsiyet, sigara içme, diyabet, hipertansiyon, sol vertiküler hipertrofisi, sekonder hiperparatroidizm (SHP) ve inflamasyon yönünden değerlendirilmişlerdir. 48 (%37) hastaya koroner arter hastalığı (KAH) teşhisi konulmuştur. KAH ile artan yaş arasında istatiksel olarak anlamlı bir korelasyon bulunmuştur ve yaşlı HD hastalarındaki koroner kalp hastalığının; yaş, erkek cinsiyet, diyabet, SHP, hipertansiyon, CRP düzeyinin artması, hiperhomosisteinemi, sigara içme, HD'ye
35 maruz kalınan süre ve HD'nin yetersizliğiyle arttığı sonucuna varmışlardır (Soubassi ve ark 2006).
Kaliforniya’da farklı ırktan 97 hemodiyaliz hastasını içeren bir grupla ilgili çalışma yapmışlardır. hsCRP düzeyleri ölçülmüştür. Aterosklerotik vasküler (koroner arter, serebrovasküler ve çevresel vasküler) hastalıkların yaygınlığını saptamışlar ve katılımcıları olaylar ve mortalite bakımından 1 yıl süreyle izlemişlerdir. hsCRP’nin aterosklerotik vasküler hastalık ve izleme dönemi sırasındaki mortalitenin anlamlı bağımsız bir değişkeni olduğunu saptamışlardır (Lentine ve ark 2006).
Yapılan bir çalışmada yaşları 58±1 olan ve 13± 1 yıldır HD hastası olan, 97’si erkek ve 59’u bayan toplam 156 kişinin karotid aterosklerotik değişiklikler ve IL-6 arasındaki bağıntı araştırılmıştır. Herbir hastada, IL-6 ve karotid arterlerin intima-media kalınlığı (IMT) ölçülmüştür. HD hastalarında, IL-6 serum düzeyleri benzer yaş aralığındaki normal kontrol grubuyla karşılaştırıldığında anlamlı derecede yüksek bulunmuştur. Bu bulgular, IL–6’nın HD hastalarındaki karotid aterosklerozun şiddetiyle ilişkili olduğunu belirlemiştir (Kato ve ark 2002).
Yaş, cinsiyet ve toplam adipoz doku kütlesi bakımından eşleştirilen 30 HD hastası, 30 sürekli peritonal diyaliz (CAPD) hastası ve 30 kişilik kontrol grubunda, diyaliz modalitesinin serum leptini, adiponektin, rezistin, IL-6 ve tümör nekroz faktörü -α (TNF-α) düzeyleri üzerindeki etkisini incelenmiş ve bu adipokinlerle ve dislipidemi ve insülin direnci arasındaki ilişki değerlendirilmiştir. Serum rezistin, adiponektin, IL-6, TNF-α ve hsCRP, kontrol grubuyla karşılaştırıldığında diyaliz hastalarında anlamlı derecede artmıştır (Taskapan ve ark 2007).
Kronik HD tedavisi alan son dönem böbrek yetmezliği hastalarında, hemodiyaliz işleminin, IL-6, IL-1β ve TNF–α, ve IL-8'in plazma düzeylerinde çok önemli bir akut değişmeye neden olup olmadığını belirlemeyi amaçlanan çalışmaya, kronik hemodiyalize maruz kalan 21 hasta (12 erkek/8 bayan) dahil edilmiştir. Serum sitokin konsantrasyonları üzerindeki hemodiyaliz işleminin akut etkisi, hemodiyaliz öncesi ve hemodiyaliz sonrası ölçümlerin karşılaştırılmasıyla değerlendirilmiştir. IL-1β, IL-6, TNF-α konsantrasyonları için anlamlı bir fark gözlenmemiştir. Hemodiyaliz işleminin IL-8 konsantrasyonunu belirgin bir şekilde düşürdüğünü gösterilmiştir (Tarakçıoğlu ve ark 2003).