T.C.
SELÇUK ÜNİVERSİTESİ FEN BİLİMLERİ ENSTİTÜSÜ
FERROSEN TÜREVLİ SCHİFF BAZLARININ SENTEZİ VE YAPILARININ
SPEKTROSKOPİK YÖNTEMLERLE AYDINLATILMASI
Asuman UÇAR DOKTORA TEZİ Kimya Anabilim Dalı
Haziran-2014 KONYA Her Hakkı Saklıdır
TEZ BİLDİRİMİ
Bu tezdeki bütün bilgilerin etik davranış ve akademik kurallar çerçevesinde elde edildiğini ve tez yazım kurallarına uygun olarak hazırlanan bu çalışmada bana ait olmayan her türlü ifade ve bilginin kaynağına eksiksiz atıf yapıldığını bildiririm.
DECLARATION PAGE
I hereby declare that all information in this document has been obtained and presented in accordance with academic rules and ethical conduct. I also declare that, as required by these rules and conduct, I have fully cited and referenced all material and results that are not original to this work.
İmza Asuman UÇAR
iv
ÖZET DOKTORA TEZİ
FERROSEN TÜREVLİ SCHİFF BAZLARININ SENTEZİ VE YAPILARININ SPEKTROSKOPİK YÖNTEMLERLE AYDINLATILMASI
Asuman UÇAR
Selçuk Üniversitesi Fen Bilimleri Enstitüsü Kimya Anabilim Dalı
Danışman: Prof. Dr. Emine ÖZCAN 2. Danışman: Doç. Dr. Ersin Güler
2014, 135 Sayfa Jüri
Prof. Dr. Emine ÖZCAN Prof. Dr. Emin KARAPINAR
Doç. Dr. Zafer YAZICIGİL Doç. Dr. Ersin GÜLER Doç. Dr. Haluk BİNGÖL
Bu çalışmada öncelikle aldehitlerle (4-hidroksibenzaldehit, vanilin) aminoasit metilesterlerinin (glisin metilester hidroklorür, alanin metilester hidroklorür, fenilalanin metilester hidroklorür, L-valin metilester hidroklorür) reaksiyonuyla schiff bazları elde edilmiştir. Schiff bazları ile α-klorasetilferrosenin reaksiyonundan yeni ürünler elde edilmiştir. Elde edilen bileşiklerin yapıları elementel analiz, FT-IR, UV-Vis, 1H NMR, 13C NMR spektroskopisi ve DSC tekniği kullanılarak karekterize edilmiştir. Bunlara ek olarak sentezlenen ürünlerin Dönüşümlü Voltametri (CV) tekniği ile elektrokimyasal özellikleri incelenmiştir. Elektrokimyasal çalışmalarda GC elektrot kullanılarak önceden sentezlenen bileşiklerin 10-3
M asetonitrilde hazırlanan çözeltilerinin elektrokimyasal karakterizasyon voltamogramları incelenmiştir. Referans elektrot olarak Ag/Ag+, karşıt elektrot olarak platin tel elektrot kullanılmıştır.
Anahtar Kelimeler: schiff bazı, α-klorasetilferrosen, amino asit metilester, dönüşümlü voltametri (CV).
v
ABSTRACT Ph.D THESIS
SYNTHESIS AND CHARACTERIZATION OF SCHIFF BASES DERIVED FROM FERROCENE WITH SPECTROSCOPIC METHODS
Asuman UÇAR
THE GRADUATE SCHOOL OF NATURAL AND APPLIED SCIENCE OF SELÇUK UNIVERSITY
THE DEGREE OF DOCTOR OF PHILOSOPHY IN MECHANICAL ENGINEERING
Advisor: Prof. Dr. Emine ÖZCAN Advisor: Assoc. Prof. Dr. Ersin GÜLER
2014, 135 Pages Jury
Prof. Dr. Emine ÖZCAN Prof. Dr. Emin KARAPINAR Assoc. Prof. Dr. Zafer YAZICIGİL
Assoc. Prof. Dr. Ersin GÜLER Assoc. Prof. Dr. Haluk BİNGÖL
In this study, firstly, Schiff bases were synthesized from the reaction of aldehydes (4-hydroxybenzaldehyde and vanilin) and amino acid methylesters (glycine methylester hydrochloride, L-alanine methylester hydrochloride, L-phenylL-alanine methylester hydrochloride, L-valine methylester hydrochloride). New compounds were obtained by the reaction of synthesized Schiff bases and α-chloroacetylferrocene. The structures of the obtained compounds were characterized by using elemental analysis, FT-IR, UV-Vis, 1H NMR, 13C NMR spectroscopy and DSC technics. In addition electrochemical properties of the synthesized products were examined using Cyclic voltammetry (CV) technique. In Electrochemical studies electrochemical characterization voltammograms were investigated using GC electrode, in 10-3 M acetonitrile solution of previously synthesized compounds. As the reference electrode Ag / Ag + and as a counter electrode platinum wire electrode were used.
vi
ÖNSÖZ
Bu çalışma Selçuk Üniversitesi Fen Fakültesi Kimya Bölümü Öğretim Üyelerinden Prof. Dr. Emine ÖZCAN ve Doç. Dr. Ersin Güler yönetiminde hazırlanarak, Selçuk Üniversitesi Fen Bilimleri Enstitüsü’ne Doktora tezi olarak sunulmuştur. Ayrıca bu çalışma S.Ü. BAP Koordinatörlüğü tarafından 13201020 numaralı proje olarak desteklenmiştir.
Yüksek Lisans Tezimi yöneten ve çalışmamın her safhasında yakın ilgi ve yardımlarını esirgemeyen değerli danışman hocam Prof. Dr. Emine ÖZCAN’a sonsuz saygı ve şükranlarımı sunarım.
Tez çalışmalarım boyunca laboratuarında çalışma imkanı sağlayan ve tezimin danışmanlığını üstlenen Doç. Dr.Ersin Güler’e, bilgi ve tecrübeleriyle yol gösteren her an yardımcı olan değerli hocalarım Prof. Dr. H. İsmet UÇAN ve Prof. Dr. Mustafa Yılmaz’a teşekkür ederim.
Tez süresince çalışmalarımı izleyen, yönlendiren ve çalışmalarımla ilgili bilgi ve önerilerinden her zaman faydalandığım, kimyasal olarak destek sağlayan Doç. Dr. Haluk Bingöl’e ve Tez İzleme Komitesi Üyelerinden Prof. Dr. Zafer Yazıcıgil’e teşekkür ederim.
Elektrokimya çalışmalarında yardımcı olan Doç. Dr. İmren Hatay PITIR, Arş. Gör. Dr. Salih Zeki BAŞ ve laboratuarında çalışma imkanı sağlayan Prof. Dr. Mustafa Ersöz’e ve her an desteğini esirgemeyen Arş. Gör. Dr. Mustafa ÖZMEN’e teşekkür ederim.
Bu zorlu süreçte her daim yanimda olan, her engeli beraber aştığım, yol arkadaşım Mükerrem Fındık’ a teşekkür ederim.
Ayrıca bütün tahsil hayatım boyunca maddi ve manevi yardımlarıyla bana her zaman destek olan aileme sonsuz teşekkür ederim.
Asuman UÇAR KONYA-2014
vii İÇİNDEKİLER ÖZET ... iv ABSTRACT ... v ÖNSÖZ ... vi İÇİNDEKİLER ... vii 1. GİRİŞ ... 1 1.1. Schiff Bazları ... 1
1.1.1. Schiff Bazlarının özellikleri ... 1
1.1.2. Schiff Bazlarının Oluşum Mekanizması ... 2
1.1.3. Schiff Bazlarının Biyolojik Aktivitesi ... 4
1.1.4. Schiff Bazlarının Metal Kompleksleri ... 5
1.1.5. Schiff Bazlarının Önemi ... 9
1.2. Amino Asitler ... 10
1.2.1. Amino Asitlerin Genel Özellikleri ... 10
1.2.2. Amino Asitlerin Yapıları ... 11
1.2.3. Amino Asitlerin Sınıflandırılması ... 13
1.2.4. Amino Asitlerin Fiziksel Özellikleri ... 16
1.2.5. Amino Asitlerin Kimyasal Özellikleri ... 16
1.3. Ferrosen ... 17
1.3.1. Ferrosenin Yapısı ... 17
1.3.2. Ferrosenin Genel Özellikleri ... 19
1.3.3. Ferrosenin Bileşiğinin Sentezi ... 19
1.3.4. Ferrosenin Uygulama Alanları ... 20
1.4. Elektrokimyasal Teknikler ... 21
1.4.1. Voltametride Kullanılan Elektrotlar ... 22
1.4.2. Dönüşümlü Voltametri (CV) ... 25
1.5. Modifiye Elektrotlar ... 27
1.5.1. Modifikasyon Metodları ... 28
1.5.2. Modifiye Yüzeylerin Karakterizasyonu ... 32
2. KAYNAK ARAŞTIRMASI ... 33
3. MATERYAL VE YÖNTEM ... 38
3.1. Kullanılan Kimyasallar ve Cihazlar ... 38
3.1.1. Kulllanılan Cihazlar ... 38
3.1.2. Kullanılan Kimyasalar ... 39
3.1.3. Elektrokimya Çalışmaları için Kullanılan Cihaz ve Elektrotlar ... 39
l kullanılmıştır. Elektrot temizliği için Buehler P-4000 zımpara kağıdı, 0,1 μm ve 0,05 μm tanecik boyutuna sahip alümina süspansiyonu kullanılmıştır. ... 39
viii 4.1. Kimyasal Sentezler ... 40 4.1.1. α-Klorasetilferrosen Sentezi (1) ... 40 4.1.2. N-(4-hidroksibenziliden)-fenilaleninmetilester (2) ... 40 4.1.3. N-(4-hidroksi-3-metoksi-benziliden)-fenilaleninmetilester (3) ... 41 4.1.4. N-(4-hidroksibenziliden)-glisinmetilester (4) ... 42 4.1.5. N-(4-hidroksi-3-metoksi-benziliden)-glisinmetilester (5) ... 42 4.1.6. N-(4-hidroksibenziliden)-alaninmetilester (6) ... 43 4.1.7. N-(4-hidroksi-3-metoksi-benziliden)-alaninmetilester (7) ... 43 4.1.8. N-(4-hidroksibenziliden)-vanilinmetilester (8) ... 44 4.1.9. N-(4-hidroksi-3-metoksi-benziliden)-vanilinmetilester (9) ... 44 4.1.10. (E)-metil 2-[4-(2-oxo-2-ferroseniletoksi)benzilidenamino]-3-fenilpropanat (10) ... 45 4.1.11. (E)-metil 2-[3-metoksi-4-(2-oxo-2-ferroseniletoksi)benzilidenamino]-3-fenilpropanat (11) ... 46 4.1.12. (E)-metil 2-[4-(2-oxo-2-ferroseniletoksi]benzilidenamino)asetat (12)... 47 4.1.13. (E)-metil 2-[3-metoksi-4-(2-oxo-2-ferroseniletoksi]benzilidenamino)asetat (13) ... 48 4.1.14. (E)-metil 2-[4-(2-oxo-2-ferroseniletoksi)benzilidenamino]propanat (14) .. 49 4.1.15.(E)-metil2-[3-metoksi-4-(2-oxo-2-ferroseniletoksi)benzilidenamino]propanat (15) ... 50 4.1.16. (E)-metil 3-metil-2-[4-(2-oxo-2-ferroseniletoksi)benzilidenamino]bütanat (16) ... 51 4.1.17. (E)-metil 2-[3-metoksi-4-(2-oxo-2-ferroseniletoksi)benzilidenamino]-3-metil bütanat (17) ... 52 4.2. Elektrokimyasal Çalışmalar ... 53
5. ARAŞTIRMA SONUÇLARI VE TARTIŞMA ... 54
5.1. Sentezlenen Bileşiklerin Element Analizi Sonuçları ... 54
5.2. Spektral Analiz Yorumları ... 55
5.2.1. FT-IR spektrumları ile ilgili yorumlar ... 55
5.2.2. 1H-NMR spektrumları ile ilgili yorumlar ... 59
5.2.3. 13C-NMR spektrumları ile ilgili yorumlar ... 63
5.2.4. UV-vis spektrumları ile ilgili yorumlar ... 67
5.2.5. Elektrokimyasal Çalışmalar ile ilgili yorumlar ... 68
6. SONUÇLAR VE ÖNERİLER ... 71
KAYNAKLAR ... 72
EKLER ... 79
ix SİMGELER VE KISALTMALAR Simgeler 1 α-Klorasetilferrosen 2 N-(4-hidroksibenziliden)-fenilaleninmetilester 3 N-(4-hidroksi-3-metoksi-benziliden)-fenilaleninmetilester 4 N-(4-hidroksibenziliden)-glisinmetilester 5 N-(4-hidroksi-3-metoksi-benziliden)-glisinmetilester 6 N-(4-hidroksibenziliden)-L-alaninmetilester 7 N-(4-hidroksi-3-metoksi-benziliden)-L-alaninmetilester 8 N-(4-hidroksibenziliden)-L-vanilinmetilester 9 N-(4-hidroksi-3-metoksi-benziliden)-L-vanilinmetilester 10 (E)-metil-2-[4-(2-oxo-2-feroseniletoksi)benzilidenamino]-3-fenilpropanat 11 (E)-metil-2-[3-metoksi-4-(2-oxo-2-feroseniletoksi)benzilidenamino]-3- fenilpropanat 12 metil- 2-[4-(2-oxo-2-feroseniletoksi]benzilidenamino)asetat 13 metil -2-[3-metoksi-4-(2-oxo-2-feroseniletoksi]benzilidenamino)asetat 14 (E)-metil 2-[4-(2-oxo-2-feroseniletoksi)benzilidenamino]propanat 15 (E)-metil-2-[3-metoksi-4-(2-oxo-2-feroseniletoksi)benzilidenamino]propanat 16 (E)-metil 3-metil-2-[4-(2-oxo-2-feroseniletoksi)benzilidenamino]bütanat 17 (E)-metil 2-[3-metoksi-4-(2-oxo-2-feroseniletoksi)benzilidenamino]-3-metil bütanat
x Kısaltmalar ACN Asetonitril DMSO Dimetilsülfoksit CV Dönüşümlü voltametri GC Camsı karbon
Uv-vis Ultraviyole visible spektroskopisi
FTIR Fourier transform infrared spektroskopisi
mL Mililitre
mmol Milimol
NMR Nükleer Magnetik Rezonans e.n. Erime Noktası
NMR Nükleer Magnetik Rezonans TGA Termal Gravimetrik Analiz DTA Diferansiyel Termal Analiz AFM Atomik Kuvvet Mikroskobu DSC Diferansiyel Taramalı Kalorimetri
1. GİRİŞ
Schiff bazı ligandları ile metal kompleksleri Koordinasyon Kimyasında önemli bir rol oynamaktadır. Özellikle sıvı kristaller ve katalitik işlemler gibi organik kimyada uygulamalarından dolayı bu ligandalar ile geçiş metal komplekslerinin sentezi ve karakterizasyonu üzerinde bir hayli çalışma yapılmaktadır (Sousa-Pedrares ve ark., 2008).
Schiff bazlarının elektrokimyasal olarak ne türde reaksiyonlar verdiğine dair bir çalışmaya 1932-1970’li yıllar arasında literatürde çok az rastlanmaktadır. İlk izlere 1976-1980 arasında rastlanır. Ancak bu yıllardaki literatürlerde amfiprotik çözücüler kullanıldıklarından bu ilk çalışmalarda reaksiyonların amin ve aldehit ile sonuçlandığı ortaya atılmış ve çok fazlada üstüne düşülmeden öyle bırakılmıştır. Bu maddelerin aprotik çözücülerdeki reaksiyonlarına ilk ciddi elektrokimyasal araştırmalara 1995’ten sonra rastlanmaktadır (Kale, C., 2004).
1.1. Schiff Bazları
1.1.1. Schiff Bazlarının özellikleri
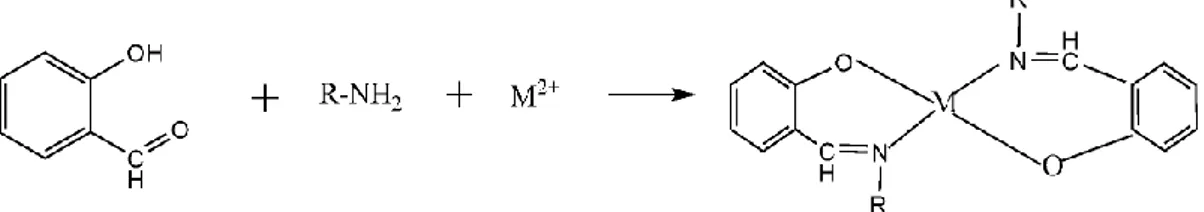
Aldehit ve ketonların uygun reaksiyon şartlarında primer aminlerle kondenzasyonu sonucu meydana gelen ve yapılarında -CH=N bulunan bileşiklere “Schiff bazları” denir. Genel olarak yapılarında -CH=N bulunan bileşiklere “azometin ya da imin bileşikleri” ve -CH=N bağından olusan fonksiyonel gruba da “Azometin grubu” denir. Schiff bazları ilk defa 1864 yılında Alman kimyager H. Schiff tarafından sentezlenmiştir. Salisilaldehit ile stokiyometrik orandan biraz fazla alınan herhangi bir alifatik primer aminle, alkollü veya sulu-alkollü ortamda, az miktardaki sodyum hidroksit veya sodyum asetat varlığında geçiş metalleri ile geri soğutucu altında ısıtılması sonucu N-alkil salisilaldiminlerin metal kompleksleri elde edilmiştir (Schiff, 1869).
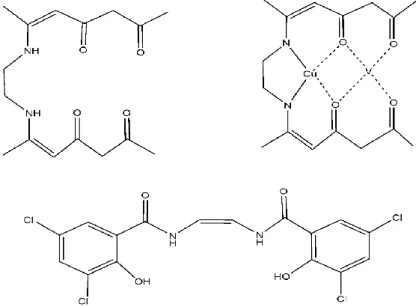
Schiff bazlarında bulunan molekül içi hidrojen bağları hakkında Chearetti, polar çözücülerde molekül içi hidrojen bağı oluşmasının ve molekül içi hidrojen bağı açılmasının mümkün olduğunu açıklamıştır (Sekil 1.2). Burada temel olarak naftalin ve fenantrolin türevleri örneklendirilmiştir. Bu moleküllerin özellikle sıcaklık ve çözücü değişiminde NH/OH tautomerik dengesinin önemli oranda etkilendiği belirtilmiştir (Patai, 1970; Dede, 2007).
Şekil 1.2. Bazı Schiff bazlarında görülen molekül içi hidrojen bağları.
1.1.2. Schiff Bazlarının Oluşum Mekanizması
İmin oluşumu çok düşük ve çok yüksek pH’da yavaştır ve genel olarak pH 4 ve 5 arasında en hızlı gerçekleşir. Eğer imin oluşumu için önerilen mekanizma dikkate alınırsa neden asit katalizörün gerekli olduğu anlaşılabilir. Önemli basamak, protonlanmış alkolün bir su molekülü kaybederek iminyum iyonu haline geldiği basamaktır. Asit, alkol grubunu protonlayarak, zayıf ayrılan bir grubu (-OH), iyi ayrılan bir gruba (H2O) çevirir. Eğer hidronyum iyonu derişimi çok yüksekse tepkime daha yavaş ilerler, çünkü aminin kendisi de önemli oranda protonlanır ve bu da ilk basamakta gerekli nükleofil derişimini azaltacak bir etkendir. Hidronyum iyon derişimi çok az ise, tepkime yine yavaşlar; çünkü protonlanmış aminoalkol derişimi azalır. En uygun koşul 4-5 arasındaki bir pH değeridir (Solomon, 2002).
Şekil 1.3. Schiff bazlarının oluşum mekanizması
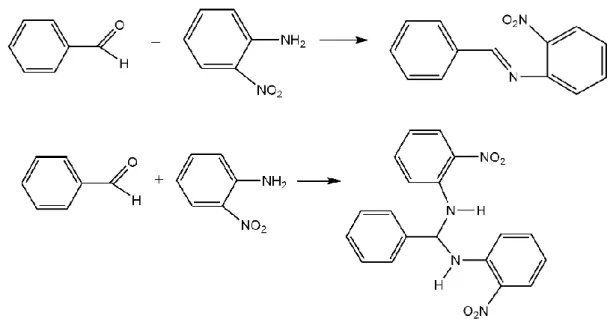
Schiff bazlarının olusumunda reaksiyon şartlarının etkisi kadar, kullanılan aldehit/amin oranının da önemli olduğu anlaşılmıştır. Örneğin o-nitroanilin benzaldehitle molar oranındaki reaksiyonundan (Sekil 1.4.) Schiff bazı meydana gelirken, o-nitroanilinin aşırısı ile yapıldığında ise Schiff bazı oluşmamaktadır (Öztürk, 1998).
1.1.3. Schiff Bazlarının Biyolojik Aktivitesi
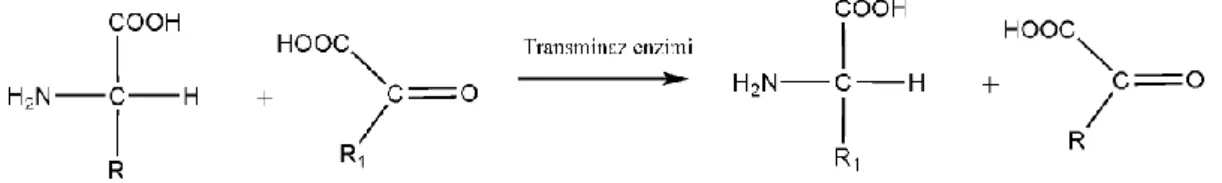
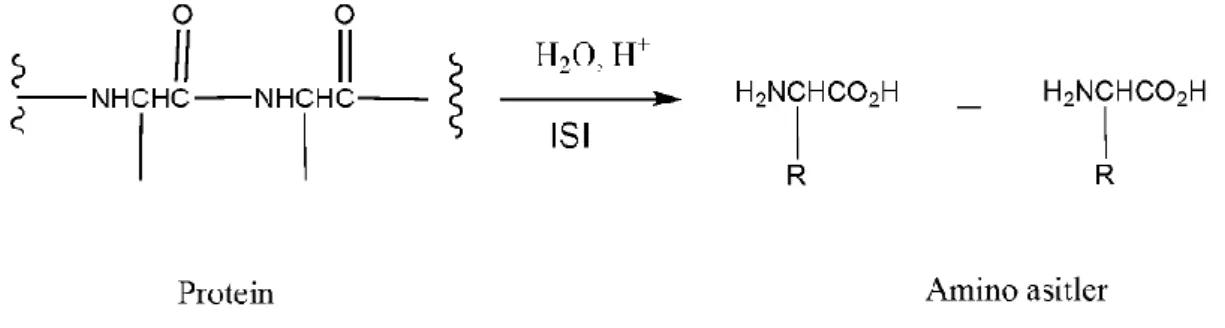
Günümüzde Schiff bazlarının biyolojik sistemlerdeki önemi gün geçtikçe artmaktadır. Schiff bazlarının en önemli biyolojik aktivitesi aminoasit biyosentezinde oynadıkları roldür. Schiff bazları α-aminoasitlerin, RCH(NH2)COOH, biyosentezinde önemli ara bileşiklerdir. α-aminoasitlerin, organizmada proteinlerin sentezinde kullanılmaktadır. Yiyeceklerin, yeterli miktarda, alınması zorunlu aminoasit içermemesi halinde organizma bazı durumlarda ihtiyaç fazlası bir aminoasiti transaminasyon tepkimesiyle gereksinim duyduğu aminoasite dönüştürür. İhtiyaç fazlası aminoasitin amino grubu, bir seri imin ara ürünü üzerinden bir keto-aside taşınır (Fessenden, 1992).
Şekil 1.5. N-alkil- Salisilaldehitin schiff bazı reaksiyonu
Ayrıca Schiff bazı verebilen N-alkil-Salisilaldehit yapısı pridoksal (Şekil 1.6) için önemli özellikleri olan temel moleküllere ışık tutmuştur.
Şekil 1.6. Pridoksal (B6 vitamini)
Pridoksal, fosfat ile birleşerek pridoksal fosfatı oluşturur ki bu yapıdan da aldehit grubu ile enzim içindeki aminoasit, Schiff bazı meydana getirir. Ayrıca fosfat grubu da enzimin başka bir yerine bağlanır, böylece enzim sistemine bir aminoasit etki ederek Schiff bazı bağını açar ve kendisi bağlanır, böylece yeni bir Schiff bazı oluşur. Oluşan Schiff bazı hidroliz olur ve pridoksamini oluşturur (Daniel, V. P., ve ark., 2008). Schiff bazları, enzimlerin karbonil ve azot gruplu substratlarla etkileşimini içeren çeşitli enzimatik reaksiyonlarda da önemli ara maddelerdir (Yazıcı, A. ve ark., 1988).
1.1.4. Schiff Bazlarının Metal Kompleksleri
Ligandlar, merkezi atoma elektron çiftleri verebilen Lewis bazlarıdır. İmin yapısındaki azot atomu çiftlenmemiş elektron bulundurduğu için elektron verici olup bazik karakterdedir. Azometin azotu olarak da tanımlanabilen bu atom bir Schiff bazı için öncelikli koordinasyon noktasıdır. (Dede, 2007). Azot atomunun bir çift bağ ile bağlanmış olduğu azometin sistemi de π- orbitalleri sayesinde geri bağlanmaya uygun d-metal iyonları için koordinasyon bölgesi olabilir. Sonuç olarak, azot atomunun da bulunduğu bu grup hem σ–donör hem de π- donör akseptör fonksiyonu gösterebilmektedir. Bu durum, Schiff bazlarının oluşturduğu metal komplekslerinin yüksek kararlılıklarının nedenidir (Canpolat, 2003). Azometin grubunun ligand olarak kararlı kompleksler oluşturabilmesinde ikinci önemli faktör, molekülde hidrojen atomunun kolay uzaklaştırılabildiği azometin bağına yakın bir fonksiyonel grup bulundurmasıdır. Böylece meydana gelen beşli veya altılı şelat halkaları ortaya çıkar ki, bu kompleksler metalin kantitatif bağlandığı yapılardır(Öztürk, 1998).
1.1.4.1. Schiff Bazı Komplekslerinin Sınıflandırılması
Schiff bazlarının metal komplekslerinin sınıflandırılması, bileşiğin sahip olduğu donör atomlar dikkate alınarak yapılır. Buna göre en çok rastlanan metal kompleksleri: N-O, O-N-O, O-N-S, N-N-O, O-N-N-O, N-N-N-N donör atom sistemine sahip olanlardır. (Dede, 2007). Bu türden Schiff bazlarının oluşturduğu metal komplekslerine ait örnekler aşağıda gösterilmistir.
1.1.4.1.1. N-O Tipi Schiff Bazları
p-N,N’-dimetilanilinin Salisilaldehit Schiff bazı, Ag+ iyonu ile iki dişli N-O
tipinde kompleks oluşturur (Erk ve Baran, 1990).
1.1.4.1.2. O-N-O Tipi Schiff Bazları
Pirimidinamin’in sübstitüe salisilaldehitler kullanılarak Schiff bazları elde edilmiş ve bunların Cu(II), Ni(II), Zn(II) ve Cd(II) metal kompleksleri sentezlenmiştir (Levent, 2001).
Şekil 1.8. Primidinamin-Salisilaldehit Schiff Bazı bakır kompleksi
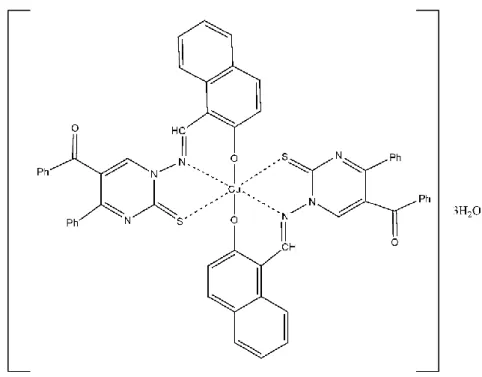
1.1.4.1.3. O-N-S Tipi Schiff Bazları
Pirimidintiyonamin bileşiğinin 2-hidroksinaftaldehit ile kondenzasyonu sonucu elde edilen Zn(II) kompleksi ONS tipi olarak değerlendirilebilir (Sönmez ve ark., 2009).
Şekil 1.9. O-N-S tipi Schiff bazı Zn (II) kompleksi 1.1.4.1.4. N-N-O Tipi Schiff Bazları
4-Klorometil-2-(2-Hidorksinaftilidenhidrazin) tiyazol ve onun Cr(III), Co(II), Ni(II), Cu(II) kompleksleri (Sekil 1.10) örnek verilebilir (Saydam ve Yılmaz.,2005).
1.1.4.1.5. O-N-N-O Tipi Schiff Bazları
Diasetil veya benzilin, 1-amino-5-benzoil-4-fenil-1H-pirimidin-2-on ile template çalışmaları yapılarak (Sekil 1.11) asiklik yapıda N2O2 yapısında Fe(III) ve Cr(III) kompleksleri elde edilmiştir (Sönmez, 2004).
Şekil 1.11. O- N-N-O tipi Schiff bazı mononükleer metal kompleksi 1.1.4.1.6. N-N-N-N Tipi Schiff Bazları
Bu gruba N,N’-bis(2-aminobenzoil)etilendiamin ile salisilaldehitten oluşan N,N’ bis(2-salisilideniminobenzoil)etilendiamin’in Fe2+ kompleksi örnek olarak verilebilir (Dede, 2007).
1.1.4.1.7. Compartmental Türündeki Schiff Bazları
Ayrıca Schiff baz ligandları Mn(II)-Mn(II) ya da Mn(II)-Mn(III) metalleri gibi iki metali bir arada tutabilirler. Metalleri yan yana tutabilen ligand çeşitleri “Compartmental” olarak adlandırılır (Sekil 1.13). Bu tip ligandlar 1,3,5-triketonların α,ω-etilendiaminlerle kondensasyonu sonucu elde edilebilir (Dede, 2007).
Şekil 1.13. Metalleri yan yana tutabilen “ Compartmental” ligand çeşitleri 1.1.5. Schiff Bazlarının Önemi
Schiff bazları, tıpta ve eczacılıkta, bazı ilaçların hazırlanmasında, biyolojik sistemlerde, boyar maddelerin üretiminde, kozmetikte, tarım alanında, polimerlerin üretiminde, plastik sanayisinde, elektronik endüstrisinde, uçak sanayisinde, analitik kimyada ve sıvı kristal teknolojisi gibi çeşitli dallarda gittikçe artan öneme sahip maddelerdir. Schiff bazları biyolojik ve yapısal önemleri yüzünden üzerinde çok çalışılan bileşiklerdir (Helmut, S.,1976, Metzler, C.M. ve ark., 1980)
Özellikle salisilaldehit ile alkil ve aril aminlerin kondenzasyonundan oluşan N-R ve N-Ar salisilidenaminler çok komplike bir sistem olan pridoksal ve B1 vitaminlerinin yapısının anlaşılmasında kullanılan birer model olmuştur (Murthy, A.S.N. ve ark., 1981).
Kemoterapik özelliği nedeniyle ilaç sanayinde kullanım alanının olduğu da bilinmektedir. Özellikleri arasında en çok önemli olanı biyolojik sistemlerdeki
aktiviteleridir. Bu aktiviteleri de eser elementlerle yaptıkları şelatlardan kaynaklanmaktadır. Buna bağlı olarak; çok geniş farmokolojik aktiviteye sahiptir (Yazıcı, A. ve ark., 1988, Ansell, B.A., 1982).
Schiff bazları, genellikle renkli ve saydam katılardır. Bu özelliklerinden yararlanılarak boya endüstrisinde kullanılmaktadır. Ayrıca parfüm endüstrisinde de kullanım alanı bulmuştur. Bunun yanında özellikle biyokimya ve analitik kimya açısından da gittikçe artan öneme sahip maddelerdir. Bu bileşiklerin sentetik oksijen taşıyıcı, enzimatik reaksiyonlarda ara ürün oluşturucu, antitümör oluşturucu gibi özelliklerinin yanında bazı metal iyonlarına karşı seçici ve spesifik reaksiyon vererek spektrofotometrik reaktif olarak analitik kimyada kullanımları da önem taşımaktadır (Burger, K., 1973, Orthmer, K., 1968). Bunun dışında elektronik gösteri sistemleri içinde sıvı kristal olarak, kauçuk hızlandırıcı olarak da kullanılabilmektedir.
Schiff bazları kesin erime noktalarına sahip oldukları için karbonil bileşiklerinin tanınmasında ve metallerle kompleks verebilme özelliklerine sahip olmaları nedeniyle metal miktarlarının tayininde kullanılmaktadır. Ayrıca bazı Schiff bazları fungisid ve böcek öldürücü ilaçların bileşiminde de bulunabilmektedir (Yazıcı, A. ve ark., 1988). Salisilaldehitin etilendiamin ve propilendiamin gibi alkilen diaminlerle kondenzasyonu sonucu meydana gelen Schiff bazları metal deaktivatörü olarak kullanılmaktadır.
Disalisilidenpropilendiamin, PVC’nin kararlılığı için kullanılmaktadır. Ayrıca bunların nikel şelatının termoplastik reçineler için ışık stabilizatörü olarak kullanıldığı bilinmektedir.
1.2. Amino Asitler
1.2.1. Amino Asitlerin Genel Özellikleri
Doğada, canlı organizmaların farklı kesimlerinde 150 kadar amino asit bulunur. Bu amino asitlerin 25 kadarı, sudan sonra insan vücudunda en çok bulunan maddeler olup molekül ağırlıkları 6 000 ile 1 000 000 arasında değişen proteinlerin yapı taşıdırlar (Tüzün, 1998). Diğer grup amino asitler ise, vücuttaki metabolizma tepkimelerinde yer alırlar veya yapısal madde olarak bulunurlar. Bu 25 amino asidin 20 tanesi DNA üzerinde kodlanmıştır ve kod sisteminin transkripsiyonu ve çevirisiyle doğrudan doğruya proteinlerin bileşimine girerler. Bu amino asitler; kas, deri, tırnak, tüy, ipek, hemoglobin, enzim, antikor ve pek çok hormonu oluşturmak üzere değişik şekilerde
birleşebilirler. Geri kalan ise, protein sentezi tamamlandıktan sonra, aşağıdaki, reaksiyonda görüldüğü gibi biyokimyasal reaksiyonlarda protein üzerinde sonradan oluşurlar. (Uyar, 1990).
Şekil 1.14. Amino asit oluşumu
Vücut için gerekli amino asitlerin yaklaşık olarak %80’i karaciğer tarafından üretilirken, geri kalan %20’sinin ise dış kaynaklardan sağlanması gerekmektedir. Temel amino asitler vücut içerisinde sentezlenemezler ve bu nedenle diyet yapılarak sağlanması gerekmektedir. Temel amino asitler; izolösin, lösin, lizin, metionin, fenilalanin, treonin, triptofan ve valindir. Aspartik asit, asparagin, glutamik asit, glutamin, pirolin, serin, tirozin ise vücut tarafından sentezlenebilen aminoasitlerdir ve temel olmayan amino asitler olarak isimlendirilirler. Arginin ve histidin ise bu iki gruba da girmeyen amino asitlerdir ve büyüme evresinde, vücut yeterli miktarda arginin ve histidin amino asitlerini üretmediğinde büyüme ile ilgili bazı problemler ortaya çıkar ve bu nedenle bu amino asitlerin dış kaynaklardan ayrıca alınması gerekir (Uyar, 1990).
1.2.2. Amino Asitlerin Yapıları
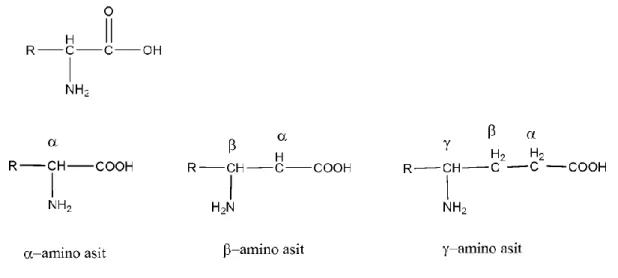
Amino asitler aslında bir tür karboksilli asitlerdir. Ancak, bu asitlerde karboksil grubuna komşu olan karbon atomuna bir amino grubu bağlı bulunmaktadır. Amino grubu molekül içinde karboksilik asit grubuna göre, α-,β-,γ- yerlerinde bulunabileceği gibi fonksiyonel grupları birden çok da olabilir (Uyar, 1990). Amino asitlerin genel formülü,
şeklindedir. Amino asitlerde, amino (-NH2) grubu bulunur. Amino asitler düşük pH’larda, elektrik alanında negatif kutba doğru hareket eden katyonlar halinde bulunurlar (Uyar, 1990).
Şekil 1.15. Düşük pH’larda amino asitler
Amino asitler yüksek pH’larda anyon halinde bulunurlar ve elektrik alanında pozitif kutba doğru hareket ederler.
Şekil 1.16. Yüksek pH’larda amino asitler
Amino asitlerde iç nötralleşme ile bir dipolar iyon (iç tuz, zwitteriyon) oluşur (Uyar, 1990).
Belirli bir amino asidin molekül yapısına bağımlı olan asit ve baz kuvvetleri çoğunlukla birbirine eşit değildir. İç nötralleşmenin tam olarak gerçekleştiği pH değerine izoelektrik nokta denir. İzoelektrik noktalarda tüm amino asit molekülleri dipolar iyon yapısındadırlar ve bu iyonlar, elektrik alanında pozitif ve negatif kutupları tarafından eşit miktarda çekildikleri için, ne negatif ne de pozitif kutba doğru hareket edebilirler. Yapılan incelemeler, katı halde bulunan amino asitlerin tamamen dipolar iyon yani zwitteriyon şeklinde bulunduğunu göstermiştir. Çözeltide ise her ikisi arasında denge kurulabilir, ama yine de dipolar iyon şeklinin yüksüz molekül şeklinden daha baskın oldugu kanıtlanmıştır. Amino asitlerin dipol momentlerinin yüksek olması (μ=4.0 D), erime noktalarının yüksekliği, uçucu olmaması, çözündüğü zaman suyun polarlığını arttırması ve suda çok çözünmeleri gibi fiziksel özellikleri de dipolar iyon yapısında olmalarından kaynaklanmaktadır (Tüzün, 1997). Dikarboksilik amino asitlerde iki tane –COOH grubu vardır. Bu asitlerin suda çözeltileri asidiktir, izoelektrik noktaları pH=3 dolayındadır. Bazik amino asitler ise birden fazla amino grubu içerirler. Bunların saf sudaki çözeltileri baziktir. Nötral amino asitlerin sudaki çözeltileri nötraldir ve izoelektrik noktaları pH=6 dolayındadır. Belirli pH’ta ise tüm amino asit molekülleri nötral olurlar ve elektrolizde göç etmezler. Bu pH’a amino asidin izoelektrik pH’ı denir. İzoelektrik nokta her bir amino asit için karakteristik olup aşağıdaki formül ile hesaplanır.
P1=
PK1+PK2 2
1.2.3. Amino Asitlerin Sınıflandırılması
Amino asitler yapısal özelliklerine göre değişik şekilde sınıflandırılırlar. Reaksiyonlara göre amino asitler, nötral, asidik ve bazik amino asit olarak 3 sınıfa ayrılırlar. Kolay öğrenmek bakımından amino asitler aşağıdaki şekilde sınıflandırılabilir.
1. Alifatik Amino Asitler 2. Aromatik Amino Asitler 3. Kükürtlü Amino Asitler 4. Asidik Amino Asitler 5. Bazik Amino Asitler
6. İmino Asitler
1.2.3.1. Alifatik Amino Asitler
Glisin: En basit ve asimetrik karbon atomu ihtiva etmeyen tek amino asittir. Bu sebeple
opikçe aktif değildir. Organizmada sentezlenebilir. Serin amino asidi ile glisin birbirine dönüşebilir. Glisin, benzeoik asit ve diğer bazı asitlerle birleşerek detoksifiksiyon mekanizmasında rol alır. Bundan başka kreatinin yapımında kullanılır. Nükleik asit sentezine katılır. Doğuştan glisin metabolizması bozukluğundan, bu amino asitin böbreklerden geri emilmesinin sonucunda, idrarda fazla miktarda glisin çıkar, diğer bir deyişle glisinüri görülür.
Alanin: Organizmada hemen her proteinde esansiyel olmayan yani endojen bir amino
asitidir. Özel bir görevi yoktur.
Valin: Eksojen yani esansiyel bir amino asittir. Çeşitli proteinlerin yapısında bulunur. Lösin ve İzolösin: Proteinlerde bulunan esansiyel amino asitlerdir. Vücuttaki
metabolizmeleri aynı yolla izlediklerinden beraber incelenir.
Serin: Glisin amino asiti ile birbirine dönüşebilirler.
Treonin: Birçok proteinlerde bulunur. Vücutta yapılamaz. Metabolize olması için
piridoksal fosfat'a ihtiyaç vardır.
1.2.3.2. Aromatik Amino Asitler
Fenilalanin ve tirozin: Bazı maddelerin sentezinde benzer bir şekilde bir role sahip
olduklarından beraber incelenirler. Fenilalanin tirozine dönüşebilir fakat tirozin fenilalanine dönüşemez. Bundan dolayı fenilalanin esansiyel bir amino asitdir. Yani dışarıdan besinlerle alınması gerekir. Fenilalanin'in tirozine dönüşümü genetik bir bozukluk dolayısıyla fenilalanin hidroksilaz enziminin bulunmamasına bağlı olarak durduğu taktirde, kanda fenilalanin ve bazı metabolitlerinin birikimi ve idrarda bu maddelerin atıldığı görülür. Küçük çocuklarda görülen bu kalıtsal hastalık "fenilketonüri" olarak adlandırılır. Zeka geriliği ve gelişme noksanlığı görülür. Tirozin adrenal medulladan sentezlenen epirefrin ve norepinefrin ile tiroid bezinden salınan trioksin'in ön maddesini oluşturur. Tirozin metabolizması bozukluğundan cildin rengini veren melanin denen pigmetin oluşumundaki yetersizlikten kaynaklanan "Albinizm" hastalığı görülür. Bu hastalarda cilt ve kıllar beyaz olur.
Triptofan: Hem besin değeri yönünden, hem de hücre için önemli birçok bileşiklerin
kaynağını oluşturduğundan önemli bir amino asitdir. Triptofan oksijean bir amino asit olup, birçok proteinden oluşur. Niyasin isimli vitaminin ve birçok fizyolojik görevi bulunan seretonunu'in sentezinde kullanılır. Şizofreni hastalırnda krizler esnasında bu amino asitin parçalanma ürünleri idrara çıkar.
1.2.3.3. Kükürtlü Amino Asitler
Sistein: Birçok proteinlerde ve özellikle kreatininde desistinde (sistin) şeklinde fazla
miktarda bulunur. Sistein, glutatyonuun bileşimine girer. Organizmada metiyonin bulunduğu taktirde vücutta yapılabilir. Metiyonin varlığında serin'den teşekkül eder.
Metiyonun: Birçok proteinde bulunur. Esansiyel bir amino asittir. Metiyonin
organizmada hem metil (-CH3), hem sülfhidril (-SH) grubu vericisidir.
Sistin: Saç, tırnak ve boynuz gibi yapılarda bulunur.
1.2.3.4. Asidik Amino Asitler
Aspartik asit ve Glutamik asit: Endojen amino asitlerdendir. Bu iki amino asit
transaminasyon reaksiyonlarında rol alırlar. Ayrıca glutamik asit, folik asit denilen vitaminin yapısında rol alır.
1.2.3.5. Bazik Amino Asitler
Lizin: Özellikle hayvansal kaynaklı proteinlerde bulunur. Bazik bir amino asit olup,
organizmada teşekkül edemez, yani esansiyeldir.
Hidroksilizin: Lizin amino asidinin bir (OH-) grubu taşıyan şeklidir.
Histidin: Birçok proteinlerde % 1-2 oranında ve hemoglobinde % 10 oranında bulunur.
Endojen bir amino asittir.
Arginin: Birçok proteinde özellikle proitaminde çok bulunur. Organizmada glutamik
1.2.3.6. İmino Asitler
Prolin ve Hidroksiprolin: Ençok prolamin grubundan proteinlerde bulunur. Amino
grubu yerine imino grubu bulunur. Prolin ve hidroksiprolin endojen maddelerdir. Prolin, bağ dokusunun yapıtaşı olan kollajen'in yapısında bulunur.
1.2.3.7. Esansiyel Amino Asitler
Organizmada sentezlenemeyen, besinlerle dışarıdan alınması gerekli amino asitlere esansiyel amino asitler denir. Bunlar: Valin, lösin, izolösin, treonin, ketiyonin, fenil alanin, triptofan ve lizin alino asitleridir.
1.2.4. Amino Asitlerin Fiziksel Özellikleri
Amino asitler genellikle suda, seyreltik asit ve bazlarda çözünürler, buna karşılık etil alkol ve diğer organik çözücülerde çözünemezler.
Glisin amino asiti dışında bütün amino asitlerin karon atomları asimektirktir. Bu nedenle optik aktivite gösterirler.
Amino asitler amfoter özellik gösteren maddelerdir. Yani asidik ortamda baz, bazık ortamda asit gibi davranırlar.
İzoelektrik noktada iyonlaşmış bulunan pozitif ve negatif gruplar denge halindedir. Bir elektrik akımı uygulandığında amino asit molekülleri ne pozitif ne de negatif kutba göç ederler. Proteinler bu özelliklerinden dolayı elektroforez denilen aletle kolayca birbirinden ayrılırlar ve miktarları da belirlenebilir.
1.2.5. Amino Asitlerin Kimyasal Özellikleri
Bir amino asidin -COOH grubu ile bir başka amino asitin -NH2 grubu birleşerek aralarında peptid bağı oluştururlar.
Şekil 1.18 Peptid bağı oluşumu
Böylece amino asitler birbirleriyle peptid bağları yaparak peptid zincirleri yaparlar. Peptid zincirleri proteinlerin primer yapısını meydana getirir.
Amino asitler susuz HCI karşısında etil ve metil alkolle esterler yaparlar.
Amino asit esterleri alkolik veya anhidröz amonyakla muamele edilirse amino asitlerin amidleri meydana getirirler.
Amino asitlerin amin grupları bir solüsyon içerisinde metil iyodür veya dimetil sülfat ile muamele edilirse, kolaylıkla metilleşebilirler.
Prolin ve hidroksiprolin dışındaki amino asitler nitröz asitlerle reaksiyona girerek azot açığa çıkmasını sağlarlar. Amino asitlearin bu özelliklerin yararlanarak protein miktar tayını yapılır.
Amino asitlerin formaldehit ile muamelesiyle amino asit miktarı tayini yapılabilir.
Amino asitlerden glisin, sistein ve flutamin organizmada yabancı maddelerle birleşerek organizma için zararsız hale getirilirler. Böyle maddelere konjugasyon ajanı denir. Örneğin glisin, benzoik asitle birleşerek hippürik asiti meydana getirir. Hipürik asit idrarla atılır.
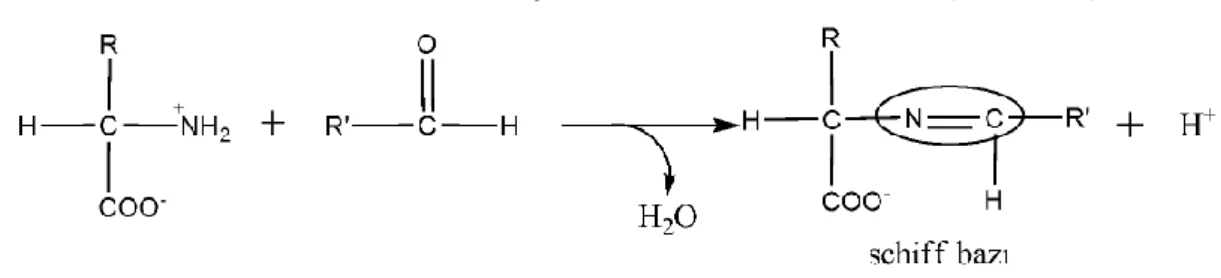
Amino asitlerin aldehitlerle reaksiyonu sonucunda Schiff bazı (−N=CH−) olusur.
Şekil 1.19 Amino asitlerle aldehitlerin genel reaksiyonu. 1.3. Ferrosen
1.3.1. Ferrosenin Yapısı
P. Pauson ve S. A. Miller, 1951 yılında yaptıkları çalışmada, ferrosen denilen Fe(C5H5)2 formülündeki bileşiği sentezlemişler. Aynı zamanda Miller, Tebboth ve Tremanie iki siklopentadienil grubunu içeren demirin çözünür bir bileşiğini elde
etmişlerdir. Bu çalışmalar tesadüfi ve birbirinden bağımsızdır. Bir tanesi, amonyak sentezinde kullanılan demir katalizöründen 300°C’da siklopentadien ve azot karışımının geçirilmesi ile diğeri ise siklopentadienil-magnezyum bromürün demirklorür ile muamele edilmesiyle elde edilmiştir. Ferrosen, sandviç kompleks yapıları olarak nitelenen organometalik bileşiklerin ilk örneğidir. Bütün sandviç yapısındaki bileşiklerde aromatik bir halka bir geçiş metaline bağlanmaktadır. Bu bağlanmada metalin halkadaki tüm karbon atomlarına uzaklığı aşağı yukarı aynıdır. Metal, her iki halkadaki karbon atomları ile etkileşime girer ve böylece son derece kararlı bileşikler oluşur. Sandviç bileşikleri genelde metalin bir tuzu veya karbonil bileşiğinin aromatik bileşikle uzun süre kaynatılması sonucu oluşmaktadır. Genelde kararlı katı bileşiklerdir ve çok yaygın olarak kullanılmaktadır.
Şekil 1.20 Ferrosenin genel yapısı
Bis(siklopentadienil)demir kompleksindeki demir atomlarının +2 yükseltgenme basamağındadır. Elektronların bir çifti her iki halka ile bağ oluşturmakta ve bu bağ belli bir karbon atomu ile Fe atomu arasında değil, demir ile halka arasında delokalize olmuş bir bağ şeklindedir. Bu bağa Wilkinson sandviç, diğerleri ise ferrosen bağı adını vermişlerdir. Ferrosen adı bis(siklopentadienil)demirin aromatikliğini vurgulamak için Woodward tarafından verilmiş, önce Kealy ve Pauson, C5H5MgBr ile FeCl3 arasında meydana gelen
reaksiyon sonucunda elde edilen bileşikteki iki metal-karbon σ bağı olduğunu düşünmüşler ve sonra ferrosenin yapısı X-ışınları difraksiyon yöntemi ile belirlenmiştir.
Ferrosen metalosen diye anılan “sandwich” bileşiklerin örneklerindendir. (ŋ5-C5H5)2Fe → Ferrosen
(ŋ5-C5H5)2Co → Kobaltosen (ŋ5-C5H5)2Ni → Nikelosen
1.3.2. Ferrosenin Genel Özellikleri
Ferrosen, sahip olduğu siklopentadienil halkaları sayesinde aromatik bir bileşiktir, ayrıca kendisi Fe(II) iyonlarından aldığı elektron desteği ile benzen halkasına göre elektronca daha zengindir ve bu da ona aromatik katılma tepkimelerine kolayca girmelerini sağlamaktadır. Fe(II)`nin yarı dolu d orbitalleri sayesinde ferrosen bileşikleri genelde kırmızı ve turuncumsu bir rengi var olup iğne şeklinde kristallere sahiptir. Ferrosenin erime noktası 173-174°C, kaynama noktası 249°C‟dır. Suda çözünmez, birçok organik çözücüde kolaylıkla çözünmektedir.
1.3.3. Ferrosenin Bileşiğinin Sentezi
Bis(siklopentadienil)demir (II) elde edilen ilk geçiş metali organometalik bileşiklerden birisidir ve iki η5-siklopentadienil (Cp) ligandına bağlı Fe2+ atomundan oluşmaktadır. Ferrosen birçok farklı tepkime neticesinde elde edilebilmektedir. Bunların bazıları;
1.Siklopentadienil-magnezyum bromürün demir klorür ile reaksiyonu,
2.Demir metali ile siklopentadienin doğrudan termal reaksiyonu, 3.Demir karbonil ile siklopentadienin doğrudan etkileşmesi, 4.Demir oksit ile siklopentadienin krom oksit içinde etkileşmesi,
5.Sodyum siklopentadienin demir klorür ile sıvı amonyak içerisindeki reaksiyonu, 6.Demir asetilaseton-dipiridin kompleksi ile siklopentadienin reaksiyonu,
Bunların dışında;
Metalik sodyum Metodu;
Ferrosen ayrıca metalik sodyum metodu yani Wilkinson sentezine göre elde edilmektedir.
1.3.4. Ferrosenin Uygulama Alanları
Roket yakıtlarında fuel katalisti olarak kullanılır. (yanma hızını 1-4 katına ulaştırır, çıkış borularındaki sıcaklığı düşürür ve ısı ışımaları gibi durumlar söz konusu olmaz.)
Dizel oil, fuel oil, ağır ve hafif yağlarda kullanıldığında duman çıkışın önler, enerjiyi korur ve hava kirliliğini azaltır.
Dizel yağa % 0,1 Ferrosen ilave etmek yağ sarfiyatını %10-14, duman çıkışını %30-70 azaltır ve % 10 daha fazla güçlendirir. Etrafa herhangi bir olumsuz geri dönüşümü olmaz.
Fuel oil’in günümüz koşullarında bu kadar kullanışlı olmasında ferrosen’in önemli katkıları vardır. Koruyucu ve düzenleyici olarak kullanılır.
Polimerin yumuşama noktasını, sıcaklık dayanıklılığını, plastik ve selülozik özelliğini arttırır. Polipropen, poliester gibi polimerik malzemelerin ultraviole ışımalarına karşı dayanıklılığını arttırır.
Işıklandırma hassasiyetinde olan malzemelerde kullanılır, film üzerinde gümüş ile yer değiştirir.
Geniş skalalı devre tahtalarının yapımında kullanılır, 4 kat daha fazla ışık hassasiyeti vardır, doğrulama hassasiyetini arttırır, basit bir teknolojiye sahiptir ve kirliliği azaltır.
Foto hassasiyet katalisti olduğu için foto kimyasal plastik filmlerin çözünmesini arttırır, beyaz kirlenmeyi azaltır.
Anti kanser, antibiyotik ve kan toniği gibi ilaçların yapımında kullanılır. Gübre yapımında kullanılır.
Kaliteli karbonil selüloz yapımında kullanılır. Biyokimyasal ve analitik madde olarak kullanılır.
1.4. Elektrokimyasal Teknikler
Elektrokimyasal teknikler, elektrot-çözelti sistemine bir elektriksel etki yapılarak sistemin verdiği cevabın ölçülmesi esasına dayanır. Genellikle akım olarak ortaya çıkan bu cevap, sistemin özellikleri hakkında bilgi verir. Bir elektrokimyasal tekniğin adına bakılarak sistemin verdiği cevabın türü ve elektriksel etki tam olarak anlaşılmayabilir.
Genel olarak bütün elektrokimyasal tekniklerde potansiyel, akım ve zaman parametreleri bulunur ve bu parametreler de elektrokimyasal tekniğin adını belirler. Örneğin, elektrokimyasal tekniklerden olan voltametride potansiyel-akım, kronoamperometride zaman-akım ve kronokulometride zaman-yük parametreleri bulunmaktadır ( Menekşe, H., 2012).
Potensiyotat
Hücre
Çalışma Elektrotu Ref erans Elektrot Karşıt Elektrot Veri Toplayaıcı Hücre ve Elektrot Kontrolü Kontrol Yazılımı Mikro İşlemci Bilgisayar
Şekil 1.21. Elektrokimyasal yöntemlerin gerçekleştiği düzenek 1.4.1. Voltametride Kullanılan Elektrotlar
1.4.1.1. Civa Elektrot
Hg, –39 °C’nin üzerindeki sıcaklıklarda sıvı halde bulunan bir metaldir. Bu elektrodun en önemli özelliği diğer metallerin yüzeyine ince bir film şeklinde kaplanabilmesidir. Bu şekilde yapılan cıva film elektrotlar diğer Hg elektrotlarla eşdeğer özellik gösterir. Akan ve damlayan Hg elektrotlar kullanılarak sürekli taze bir yüzey elde edilebildiğinden elektrot reaksiyonu sonucu oluşan ürünlerin veya ortamda bulunan diğer maddelerin adsorpsiyonuyla elektrot yüzeyinin kirlenmesi önlenir. Bunun yanısıra, Hg ve Hg film yüzeyi düzgün olduğundan, katı elektrotlardaki mgibi yüzeyin parlatılması gibi bir ön işleme gerek kalmaz. Bu şekilde düzgün ve temiz bir sıvı yüzeyinin olması ve hidrojen çıkışı aşırı gerilimin yüksekliği katodik reaksiyonlarda Hg’yı vazgeçilmez bir elektrot konumuna getirmektedir. Hg elektrodun sağladığı diğer bir avantaj da kolay temizlenebilmesi ve çok saf olarak elde edilebilmesidir. Bu temizleme işlemi HNO3 ile yapılır. Çünkü indirgenme potansiyeli Hgdan daha negatif olan bütün metaller HNO3 ile kolayca yükseltgenerek uzaklaştırılır. Sadece nikel; Hg ile metaller arasında bileşik yapar ve çok zor uzaklaştırılabilir. Civanın daha soy metallerden ayrılarak saflaştırılması damıtma yapılarak gerçekleştirilir. Bu elektrodun tek dezavantajı kükürt içeren bileşiklerde olduğu gibi bazı bileşiklerin Hg yüzeyine çok kolay adsorbe olmasıdır (Menekşe, H., 2012).
1.4.1.2. Platin, Altın Ve Diğer Soy Metal (Pd, Rh, Ir) Elektrotlar
En çok kullanılan soy metal elektrotlar Pt ve Au’dur. Bu metallerin en önemli kullanılma sebebi çok yüksek saflıkta hazırlanabilir, kolay işlenebilir ve istenilen geometrik şekillerde imal edilebilir olmaları ve açık atmosferde uzun süre oksitlenmemeleridir. Pt ve Pd’un hidrojen çıkışı aşırı gerilimi çok düşük olduğundan tersinir hidrojen elektrotların yapımında kullanılmaktadırlar (Menekşe, H., 2012). Pt, hidrojeni kolaylıkla adsorbe eder, dolayısıyla adsorplanmış hidrojen miktarından yola çıkılarak Pt’ın gerçek yüzey alanı kolaylıkla hesaplanabilir. Pd, sulu ortamlarda voltametrik çalışmalara uygun değildir; çünkü hidrojen Pd metali içerisinde çözünür. Au, hidrojen aşırı gerilimi yüksek olduğu için ve hidrojeni fazla adsorbe etmediğinden katodik çalışmalarda tercih edilir. Sayılan metaller içerisinde en fazla kullanılanı Pt’dir. Bu tercihin birinci sebebinin alışkanlık olmasının yanısıra altına göre platinin daha kolay işlenmesi gösterilebilir.
1.4.1.3. Karbon Elektrotlar
Karbon elektrot yapımında kullanılan ve oldukça tercih edilen bir elementtir. Bunun sebebi sert bir element olması, geniş bir potansiyel penceresine sahip olması, elektriği iyi iletmesi, kolay işlenebilir olması, ucuz ve elektrot yüzeyinin kolayca yenilenebilmesi olarak sayılabilir (Dryhust and McAllister 1984). Karbonun pek çok türü elektrot materyali olarak kullanılmaktadır. En çok rastlanan türleri tek kristalli grafit, yüksek düzenlilikte pirolitik grafit (HOPG), toz haline getirilmiş grafit, karbon siyahı, karbon pasta elektrot ve camsı veya seramik karbondur (McCreery 1991). Grafit, hekzagonal karbonlar içeren levhaların içinde tabakalı bir yapıya sahiptir ve anizotropiktir. HOPG (Yüksek düzenlilikte pirolitik grafit) polikristalin bir materyaldir; fakat yüksek derecede düzenli yapılanma gösterir. Bu yüzden X-ışını monokromotorlarının yapılmasında kullanılır. Bu materyalin taze yüzeyleri adhesif şerit ile üst tabakaları kesilerek oluşturulur, bu yüzeylerin çok düzgün olduğu STM ile yapılan topografik taramalar ile de gözlenebilir. Bunun yanısıra yüzey, engebeler, kusurlar ve çeşitli özellikler içerir. Normal pirolitik grafit daha az düzenli bir yapıdadır ve ince liflerin yapımı için uygundur. Bu yüzden ultra mikro elektrotların yapımında kullanılabilir.
Toz halindeki grafitin değişik türleri elektroliz yapılırken, gözenekli yatak
olarak veya mineral yağları ile karıştırılarak karbon pasta elektrotların yapımında kullanılabilir.
Karbon siyahı, bazen izole polimerlerle karıştırılarak iletken matriksler
oluşturulur ve karbon elektrot yapılır.
Karbon siyahı, teflon ve Pt ile karıştırılarak bir kısım yakıt pillerinde
gaz-difüzyon elektrotu olarak da kullanılır.
Camsı veya seramik karbon su veya hava geçirmez, amorf bir materyaldir ve
analitik uygulamalarda kullanılır. Karbon materyal modifikasyondan önce veya elektrot olarak kullanılırken temizlenmelidir. Çünkü karbon en kolay okside olabilen türdür. Karbon elektrotların oksidasyonu oksijen içeren atmosferde ısıtma veya oksijen içeren plazma veya lazer ışınına maruz kalma sonucunda meydana gelir. Bu durumda elektrot olduğu gibi ya da modifiye edilmek üzere kullanılsa da kullanılmadan önce yüzeyi prosedüre uygun olarak temizlenmelidir.
1.4.1.4. Yarı İletken ve Diğer Metak Elektrotlar
Kalay oksit kaplı cam elektrot, elektrokimyasal spektroskopide elektrot olarak
kullanılmaktadır. Kalay oksitin antimon ile karıştırılmasıyla n-tipi yarı iletken yapmak mümkündür. Oluşan yüzey kimyasal olarak inert ve görünür bölge spektrumunda görülebilecek kadar geçirgendir. Ancak bu iki özellik içerisinde optikçe geçirgen olma özelliği bu materyalin elektrot yapım malzemesi olarak daha fazla tercih sebebi olmasını sağlar.
Yarı iletken elektrotların akım-potansiyel eğrileri, elektrot yapısını oluşturan metal türüne göre değişir. Bunun temel sebebi iç direnç ve elektrodun düzenli olmayan iç potansiyeli yüzündendir. Çözelti direncinin aksine pozitif geri beslenme ile bu değişimin elektronik olarak giderilmesi mümkün değildir.
Metal ve yarı iletken materyallerin voltametrik elektrot olarak kullanılması ile ilgili literatürde çok sayıda çalışma bulunmaktadır. Bütün metal ve yarı iletken elektrotlar test edilmiş ve aşağıdaki kriterler yardımıyla çeşitli özellikleri belirlenmiştir. • SCE’ye karşı pozitif potansiyel aralığının sınırı
• Artık akımların tekrarlanabilirliği,
elektronlu tersinir bir yükseltgenme yapılması ve tekrarlanabilirliğine bakılmak suretiyle belirlenmiştir.
Elde edilen sonuçlara göre; krom ve tungsten karbür materyalleri dışında hiçbir materyalin camsı karbon ile kıyaslanamayacağı bulunmuştur. Cr’un düşük pozitif potansiyel aralıktaki ölçümler için alınan voltamogramların yorumlanabilir ve tekrarlanabilir olmasına rağmen neden platin elektrodun yerine kullanılamayacağına dair bir sebep bulunamamıştır. Titanyum geniş pozitif potansiyel aralığında kullanılma özelliğine sahip olmasına rağmen elektrot materyali olarak çok az kullanılmaktadır. Elde edilen voltamogramlar tekrarlanabilirliği olmayan ve elektrodun kullanımıyla zamanla kullanım ve ortam şartlarından etkilenen bir özelliğe sahiptir. Zirkonyum, tantalyum, niyobiyum ve molibden klasik bir pozitiflenme özelliğine sahiptir ve bu materyaller ile yapılan bir elektrot ile Fe (II) için yükseltgenme pikleri elde edilemez. Kurşun, organik elektrosentezde katot materyali olarak daha fazla kullanılır. Yüksek bir hidrojen dalgasına sahiptir ve mekanik olarak çalışılması kolaydır. Ancak voltametrik çalışmalarda camsı karbon veya platin kadar kullanışlı görünmemektedir (Sawyer et al. 1995).
Bunların dışında yarı iletken polimerler yaygın bir şekilde kimyasal sensör olarak kullanılmaktadır. Kimyasal sensörler otomotiv endüstrisinde hava yakıt karışımının indirgenme ve yükseltgenme özelliğini belirlemek ve maksimum etkinlikte en az kirlenmeye yol açacak olan hava yakıt karışımının motorun gereklerine adapte edilmesini sağlamaktadır. Medikal alanda ise iletken polimer sensörler kanın pH'sını ve kandaki potasyum, kalsiyum ve glikoz konsantrasyonlarını incelemek amacı ile kullanılmaktadır. İletken polimerlerin en ümit veren yakın gelecek uygulamalarından biri de şarj edilebilir bataryalardır. Bunlar polimerleri aktif elektrotlar olarak kullanabileceklerdir.
1.4.2. Dönüşümlü Voltametri (CV)
Dönüşümlü voltametrinin temel prensibi bir çözeltideki kimyasal türlerin bir elektrot yüzeyinde yükseltgenme ve indirgenmesine dayanır (Gosser 1994). CV’de tarama hızının değiştirilmesi suretiyle pik yüksekliklerinin tarama hızı ile farklı şekilde değişmesinden dolayı adsorpsiyon, difüzyon ve elektron aktarım reaksiyonuna eşlik eden kimyasal reaksiyon olaylarının varlığı ve tabiatı belirlenebilir. Bunun yanısıra ileri
ve geri tarama piklerinden reaksiyon mekanizması belirlenebildiği gibi kinetik veriler de bulunabilir. CV’de genellikle katodik ve anodik yöndeki tarama hızları eşit alınır. Dönüşümlü voltametride (CV) uygulanan potansiyelin zamanla değişim grafiği Şekil 1.22’de gösterilmiştir.
Şekil 1.22. Tipik bir voltamogram gösterimi
Potansiyel taraması E1 ve E2 arasında yapıldığı takdirde metodun adı “Doğrusal
taramalı voltametri” (LSV) adını alınır.
Dönüşümlü voltametride akım, potansiyele karşı grafiğe geçirilir. Tarama hızı 5 mV/s’den 100 V/s’ye kadar değiştirilebilir. Ancak burada önemli bir nokta, çok yüksek tarama hızlarında çift tabaka yüklenmesi ve IR düşmesi gibi çeşitli problemlerin ortaya çıkmasıdır. Bu problem mikro elektrot kullanılarak en az düzeye çekilebilir. CV’de katodik ve anodik yönlerdeki tarama hızları genellikle eşit alınır. Fakat özellikle hızlı ve homojen olan kimyasal reaksiyonlar mevcut ise anodik ve katodik tarama hızları farklı alınabilir.
Örneğin;
O + ne
- kfkb
R
şeklinde tersinir elektrot reaksiyonunun olduğunu ve başlangıçta çözeltide sadece O maddesinin bulunduğunu kabul edelim. Eğer tarama hızı çok yavaş olursa i–E grafiği kararlı hâldeki gibidir. Bu durumda belli bir potansiyelden sonra sınır akımına ulaşılır ve akım potansiyelden bağımsız bir hâl alır. Potansiyel tarama hızı arttırıldığında i–E
grafiği pik hâlinde gözlenir ve Şekil 1.23’de de görüldüğü üzere tarama hızıyla pik yüksekliği doğru orantılı olarak değişir. Bunun sebebi O maddesinin konsantrasyon potansiyel profili incelendiğinde anlaşılabilir.
Şekil 1.23. CV’de potansiyelin tarma hızı ile değişimini gösteren örnek voltamogram
Dönüşümlü voltametride pik akımı Randles-Sevcik eşitliği ile elde edilir. Randles-Sevcik eşitliği aşağıda verilmiştir.
i p =2,686 x 105 n3/2 Ac0 D1/2 v1/2
Burada ip: pik akımı (A), n: aktarılan elektron sayısı, A: elektrot yüzey alanı (cm2), D: difüzyon katsayısı (cm2/s), C: elektroaktif türün derişimi (mol/cm3) ve v: tarama hızı (V/s)’dır. Bu eşitlikten görüldüğü gibi pik akımı, tarama hızının karekök değeri ve elektroaktif türün derişimi ile doğru orantılıdır (Bard and Faulkner 2001).
1.5. Modifiye Elektrotlar
Katı elektrotların elektrokimyadaki kullanımı son yıllarda gittikçe önem kazanmakta ve çok çeşitli uygulama alanları bulmaktadır (McCreery 1991). Katı elektrotların yüzeylerinin modifiye edilebilmeleri bu elektrotları Hg elektroda göre daha üstün kılmaktadır. Bir katı elektrot yüzeyinde istenmeyen olaylar ve reaksiyonlar yüzey modifikasyonu ile engellenebilir veya bazı reaksiyonların cereyan etmesi sağlanabilir (Murray 1984, Finklea et al. 1996). Modifiye edilmemiş katı elektrotların yüzeyleri bazı
maddelere karşı katalitik özellik göstermeyebilir. Bazı katı elektrotların yüzeyleri ise zamanla değişikliğe uğrayabilir ve böyle yüzeylerde tekrarlanabilir sonuçların elde edilmesi mümkün olmayabilir. Elektrot yüzeyinde meydana gelmesi istenen reaksiyon bir süre sonra yüzeyde meydana gelen oksitlenme ve kirlenme sebebiyle engellenebilir veya farklı mekanizmaya göre yürüyebilir. Kimi zaman da analiz örneğindeki birden çok analit, benzer elektrokimyasal davranış gösterdikleri için birbirleri ile girişim yapar ve bu analitlerin aynı anda analizleri pratikçe imkânsız hale gelir. Bunu önlemek için katı elektrotların yüzeyleri modifiye edilir (Chia et al. 1984). Kimyasal olarak modifiye edilen elektrotların sadece yüzeyinde değişiklik yapılır ve elektrodun iç kısımları bu değişikliklerden etkilenmez.
1.5.1. Modifikasyon Metodları
Yüzeye bağlanan moleküllere ‘modifiye edici’ adı verilir. Bir modifikasyon işleminde modifiye edicinin seçimi çalışma amacına bağlıdır. Modifikasyon ile elektrotların yüzeylerine uygun moleküller bağlanarak yüzeyin elektrokimyasal karakteri değiştirilir. Böylece yüzey, hem kimyasal hem de elektrokimyasal bakımdan kısmi bir değişime uğrar. Elektrot modifikasyonunda moleküllerin yüzeye tutturulması işlemi üç farklı şekilde yapılır. Bunlar;
(i) Fiziksel adsorpsiyon, (ii) Kimyasal adsorpsiyon
(iii) İletken film halinde yüzeyde biriktirmedir.
Fiziksel adsorpsiyonda modifiye edici, elektrot yüzeyine fiziksel kuvvetlerle tutturulur. Bu işlem sırasında kovalent bağ meydana gelmez. Bu tür bağlanma, modifiye edicinin ve elektrot materyalinin özelliğine göre çok zayıf olabileceği gibi (tersinir adsorpsiyon) çok kuvvetli de olabilir (tersinmez adsorpsiyon). Tersinmez fiziksel adsorpsiyon bazen kimyasal adsorpsiyon olarak da adlandırılır (Soriaga et al. 1982, Durst et al. 1997). Kimyasal adsorpsiyonda modifiye edici, elektrot yüzeyine kovalent bağlarla bağlanır. Film halinde biriktirmede ise bir dimer veya polimer oluşumu ile çeşitli kalınlıkta tabakalar elektrot yüzeyine fiziksel veya kimyasal olarak tutturulur (McCreery 1991, Lyons 1994, Fagan et al. 1985).
Karbon elektrotlar, yüzey atomları bir kimyasal bağ oluşturmaya çok yatkın olduğu için, bu alanda en çok kullanılan elektrotlar arasındadır (McCreery 1991). Özellikle camsı karbon (GC) ve karbon fiber elektrotlar modifiye elektrot elde edilmesine çok uygundurlar.
Camsı karbon elektrot, mekanik olarak ve çözücü kullanılarak temizlenmeye, yüksek vakum altında çalışmaya, ısıl işlem uygulamaya ve kimyasal reaksiyonlara girmeye çok yatkındır. Ancak camsı karbon elektrodu modifiye etmeden kullanmanın, karbonun çok kuvvetli adsorbe etme özelliği sebebiyle kısa sürede kirlenmesi ve özelliğini kaybetmesi gibi bir takım dezavantajları da mevcuttur. Bu elektrot kolaylıkla temizlenebilir, ancak her temizlik işleminin uygulanmasında aynı özellikte yüzey elde etmek mümkün olmayabilir. Bu sebeple elde edilen sonuçların tekrarlanabilirliği bazen çok da iyi olmayabilir (Hu et al. 1985, Allongue et al. 1997). Bu problemler modifikasyon işlemleri ile giderilebilir.
Elektrotların modifikasyonunda çeşitli metotlar kullanılmaktadır. Bu metotlar ile modifiye edici tür yüzeye ya kovalent olarak bağlanır ya da kuvvetli adsorpsiyon sonucu yüzeyde biriktirilir. Karbon ve metal yüzeylerinin kovalent bağlanma sonucu modifikasyonu; alkol oksidasyonu, amin oksidasyonu ve diazonyum tuzu indirgemesi ile yapılır.
Alkol oksidasyonu ile modifikasyonda primer alifatik alkol içeren bir anhidrür
çözeltisindeki camsı karbon elektroda 2 V kadar yüksek bir potansiyel uygulandığı zaman (0,1 veya 1 M H2SO4 veya 0,1 M LiClO4 elektrolitleri varlığında) elektrot hemen hemen tamamen pasivize olur. Elektrokimyasal olarak karbon elektrotları modifiye etmek için kullanılan alkollere örnek olarak; metanol, etanol, 1-propanol, 1-butanol, trietilen glikol, etilen glikol, 1,2-propandiol verilebilir. Oluşturulan bu modifiye yüzeyler elektrokimyasal ve spektroskopik metotlarla karakterize edilebilir.
Amin oksidasyonunda karbon ve karbon fiber yüzeylerinin susuz etanol veya
asetonitril elektrolit çözeltilerindeki primer veya sekonder aminler ile oksidasyonu sonucu modifiye edilebilir. CV taramaları veya potansiyel kontrollü elektroliz veya CV taramaları ile tersinmez amin oksidasyon pikleri elde edilerek yüzey modifikasyonu yapılması mümkündür. Modifikasyonda kullanılan aminlere örnek olarak etilen diamin, sistein, imidazol, butilamin ve dopamin verilebilir. Bu modifiye yüzeyler elektrokimyasal ve spektroskopik metotlarla karakterize edilebilir ( Pinson et al. 2005).
İnorganik modifikasyonda, örnek bir çalışmada 4-aminobenzoik asit (4-ABA)
Modifikasyon işleminde modifiye ediciden 0,1 M KCl ortamında elektrooksidasyon ile bir amin katyonu oluşturulmuş ve bu şekilde 4-ABA’nın yüzeye kaplanması sağlanmıştır. Asitli pH’larda yüzeydeki Fe(CN)63– ’ye ait elektron aktarımları incelenmiş ve yüzey oluşturulduktan sonra Cu2+
iyonu yüzeye tutturularak CuHCF tek tabakası oluşturulmuştur. Yüzey CV ve EIS ile karakterize edilmiştir (Yang et al. 2000). Karbon elektrotların modifikasyonunda en çok başvurulan metot, bir diazonyum tuzunun sulu veya susuz ortamlarda indirgenmesiyle çözeltide bir aril radikali oluşturulması ve bu radikallerin karbon elektrot yüzeyine kovalent bağlarla bağlanmasıdır (Allongue et al. 1997). Bu reaksiyonda diazonyum tuzu indirgendiğinde, bir aril radikali ve azot molekülü meydana gelir. Diazonyum tuzu kullanarak elektrot yüzeylerinin modifikasyonundaki kimyasal reaksiyon mekanizması aşağıda gösterilmiştir.
Şekil 1.24. Diazonyum tuzu kullanarak elektrot yüzeylerinin modifikasyonundaki kimyasal reaksiyon mekanizması
Farklı diazonyum tuzları kullanılarak istenen özellikte elektrot yüzeyleri oluşturulabilir. Oluşan yüzey atmosfere dayanıklı, sulu ve organik ortamlarda modifiye yüzeyin özelliğine göre farklı kararlı yapılar göstermektedir. Bir çalışmada yüzeye tutturulan nitrofenil radikalinin, yüzeyden kopartılabilmesi için 700 oC sıcaklığa kadar
ısıtılması gerektiği ifade edilmektedir (Liu and McCreery 1995).
Diazonyum tuzu kullanılarak yapılan modifikasyonlar hem susuz ortamda hem
de sulu ortamda yapılabilmektedir.
Susuz ortamda, TBATFB gibi destek elektrolit içeren organik çözücülerde, aril
diazonyum tuzu kullanılarak karbon elektrot yüzeyinde tek elektronlu aril diazonyum tuzunun indirgenmesi ile yüzeye aril grupları tutturulur. Diazonyum tuzunun indirgenmesi CV ve potansiyel kontrollü elektroliz ile yapılabilir ve camsı karbon elektrot, HOPG (yüksek oranda düzenli grafit), HGC (hidrojenlenmiş camsı karbon)
başarı ile modifiye edilir (Delamar et al. 1992,). Başlıca modifiye edici aril diazonyum tuzlarına örnek olarak 4-nitrofenil, 1-naftil, fenil, benzoilfenil ve benzo[c]sinnolin (İsbir et al. 2005) verilebilir. Bu modifiye edilen yüzeyler yine çeşitli elektrokimyasal ve spektroskopik metotlarla karakterize edilebilir.
Sulu ortamda ise, diazonyum tuzunun izole edilemediği durumlarda, seyreltik
asidik ortamda + 4°C’ta çıkış maddesi olan amin ve NaNO2 deney hücresinde (in situ olarak) bir süre karıştırlarak diazonyum tuzu meydana getirilir ve diazonyum tuzu CV yardımı ile indirgenerek karbon yüzeye tutturulur. Modifiye edici diazonyum tuzlarının oluşturulması için örnek çıkış maddeleri olarak benzo-15-taç-5 eter ve glikol-bis(2- aminofenil) eter verilebilir. Bu yüzeyler de çeşitli elektrokimyasal ve spektroskopik metotlar ile karakterize edilir. (Morita et al. 2004, İsbir et al. 2006).
Kendiliğinden oluşan modifiye yüzeyler, (SAMs) için genellikle metal
yüzeylere tiyol grupları tutturulur. Bunun için temiz metal yüzeyleri tiyol çözeltilerine oda sıcaklığında daldırılarak belli saat veya gün bekletilir. Bu tür yüzeylerin korozyona karşı koruma, aşınma, paslanma gibi dış etkilere karşı koruma özelliğinin olması, yapımının ve karakterizasyonunun kolay olması ve oda sıcaklığında kararlı olması gibi özelliklerinden dolayı oldukça fazla tercih edilmekte ve çalışılmaktadır (Garg et al. 2002).
Langmuir-Blodgett filmler, (LB) özellikle elektronik olarak iletken tellerin ya
da başka bir deyişle köprülerin yapımında (nanowire) kullanılmaktadır. SAMs gibi kolay hazırlanması ve kolay karakterizasyonu sayesinde tercih sebebidir. SAMs’lerin yapımına benzer şekilde hazırlanırlar (Miyahara and Kurihara 2004).
Polimerizasyon ile yapılan modifikasyonlarda modifiye edilecek substrat yüzeyi
normal prosedure bağlı kalınarak modifiye edildikten sonra organik çözücü ve asitler ile safsızlıklardan arındırılır. Daha sonra polimer oluşturmak üzere seçilen monomer ile genellikle çoklu CV taraması yapılarak yüzeyde polimer oluşturulur (Jin et al. 2005).
Bunun yanısıra elde edilen bir modifiye elektrodun yüzeyine, çeşitli kimyasal reaksiyonlarla çok çeşitli maddeler de tutturulabilir. Böylece çok geniş bir elektrot modifikasyon alanı elde edilir (Bourdillon et al. 1992).
1.5.2. Modifiye Yüzeylerin Karakterizasyonu
1.5.2.1. Elektrokimyasal Metotlar
Modifiye edilen yüzeyler elektrokimyasal olarak dönüşümlü voltametri (CV), elektrokimyasal impedans spektroskopisi (EIS) , temas açısı, kronoamperometri (CA), kronokulometri (CC) yöntemlerinin yanısıra elektrokimyasal kuartz kristal mikrobalans (EQCM) yöntemi de kullanılmaktadır.
1.5.2.2. Spektroskopi Metotları
Modifiye edilen yüzeyler spektroskopik olarak; X-ışınları fotoelektron spektroskopisi (XPS) (Ranganathan et al. 1999), Raman spektroskopisi (Liu et al. 1995, Ranganathan et al. 1999), reflektans IR (Ref-IR) (Skoda et al. 2007), atomik kuvvet mikroskopisi (AFM) (Ranganathan and McCreery 2001), taramalı elektron mikroskopisi (SEM) (Kuo and McCreery 1999), ikincil iyon kütle spektroskopisi (SIMS) (Vase et al. 2007), yüzey plazmon rezonans spektroskopisi (SPR) (Sheridan ,A.K., et al. 2006) vb. tekniklerle karakterize edilebilir.
2. KAYNAK ARAŞTIRMASI
Syamal ve ark., (1985) Salisilaldehit türevleri ve 2-hidroksi-1-naftaldehitin o- aminofenol ile kondenzasyonundan elde edilen Schiff bazlarının Zr+4 iyonu ile metal şelatlarını sentezlemişlerdir. Bu komplekslerde Schiff bazları üç dişli ligandlar gibi davranarak koordinasyonun O-N-O donör sistemiyle gerçekleşmiştir. Kompleksler değişik reaksiyon ortamlarında 1:1 ve 1:2 metal-ligand oranında sentezlenmiş ve sentezlenen komplekslerin monomer yapıda ve diamagnetik olduğunu tespit etmişlerdir. Taguchi ve ark., (1988) schiff bazı komplekslerinin antikanser aktivitesi göstermesi özelliğinden dolayı da tıp dünyasındaki önemi giderek arttığını ve kanserle mücadelede reaktif olarak kullanılması hususunda araştırmaların devam ettiğini belirtmektedir.
Bahrens ve ark., (1996) yaptıkları çalışmalarda schiff bazlarının yapılarında oksokrom gruplar bulunduğu taktirde, elde edilen metal kompleksleri renkli maddeler olduklarından boya endüstrisinde, özellikle tekstil boyacılığında pigment boyar maddesi olarak kullanıldığını ifade etmektedir .
Sarı N. (1999), Bazı heterosiklik aldehit ve amino asitlerden yola çıkarak yeni Schiff bazları sentezlemiştir. Heterosiklik aldehit olarak; furan-2-karboksaldehit, tiyofen-2-karboksaldehit ve piridin-2- karboksaldehit, amino asit olarak; alanin, valin ve fenilalanin kullanmıştır. Schiff bazlarının yapılarını element analizi, FTIR, 1
H-NMR, 13
C-NMR, UV-GB spektrumları ve iletkenlik ölçümleri ile aydınlatmıştır. Çalışmanın ikinci bölümünde Schiff bazlarının Cu(II) ve Ni(II) komplekslerini template metodu kullanarak elde etmiştir. Komplekslerin yapılarını element analizleri, magnetik duyarlık ve iletkenlik ölçümleri, FTIR, UV-GB spektrumlan ve termal analizler (DTA, TGA) ile aydınlatılmıştır. Bütün komplekslerde Schiff bazlarının metal iyonuna imin azotu ve karbonil oksijeninden bağlanarak iki dişli şelat olarak davrandığı ve yine bütün komplekslerde M:L oranının 1:1 olduğunu gözlemlemiştir. Ni(II) komplekslerinin tamamının oktahedral yapıya sahip olduğunu görmüştür. Cu(II) komplekslerinin ise iki tanesininin altılı diğer dört tanesinin ise dörtlü koordinasyona sahip olduğunu belirlemiştir.
Emregül, K.C. ve ark., (2003): Salisilaldehit ile o-toluidin, metoksianilin ve 2-nitroanilin kullanılarak elde ettikleri Schiff bazlarının, elektrokimyasal teknikleri kullanarak korozyonu önleyici özelliklerini incelemişlerdir. N-(2-hidroksifenil)salisilaldimin, N-(2-metilfenil)salisilaldimin, N-(2
metoksifenil)salisilaldimin ligandlarının çok iyi anodik inhibitör olarak kullanılabileceklerini gözlemlemişlerdir. N-(2-nitrofenil) salisilaldimin hidroklorür hariç diğerlerinin N-(2-metoksifenil)salisilaldimin > N-(2-hidroksifenil) salisilaldimin > N-(2-metilfenil)salisilaldimin sırasına göre korozyon önleyici etki gösterdiklerini söylemişlerdir.
Xu, T.ve arkadaşlarının (2005)yaptığı çalışmada Glisin ve o-vanilinin mutlak alkol ortamında 1:1 oranında reaksiyonundan [N-(3- metoksisalisiliden)glisin] ligandı sentezlenmiştir.
Şekil 2.1. [N-(3-metoksisalisiliden)glisin] ligandı
Abbo H.S. ve ark.,(2005) 4-(naftalin-1-yliminometil)-fenol ve ve 4-(napftalin-2-yliminometil)-fenol bileşiklerinin 4-hidriksialdehit ile reaksiyonundan yeni bir schiff bazı sentezlemişlerdir. Bu üründen yola çıkarak Fe(III) komplekslerini elde etmişlerdir.
Şekil 2.2. Oluşan ürünler
Shi, L.ve ark., (2006) yaptığı çalışmada Salisilaldehit türevlerinden sentezlenen bileşiklerde, aromatik halkada bir veya daha fazla halojen atomu bulunduğunda, schiff bazlarının antifungal ve antibakteriyel aktiflik gibi çeşitli biyolojik aktivite gösterdikleri belirlenmiştir. Özellikle 5-klorsalisilaldehitten bir seri schiff bazı sentezlenmiş ve bunların antimikrobiyal özellikleri belirlenmiştir.