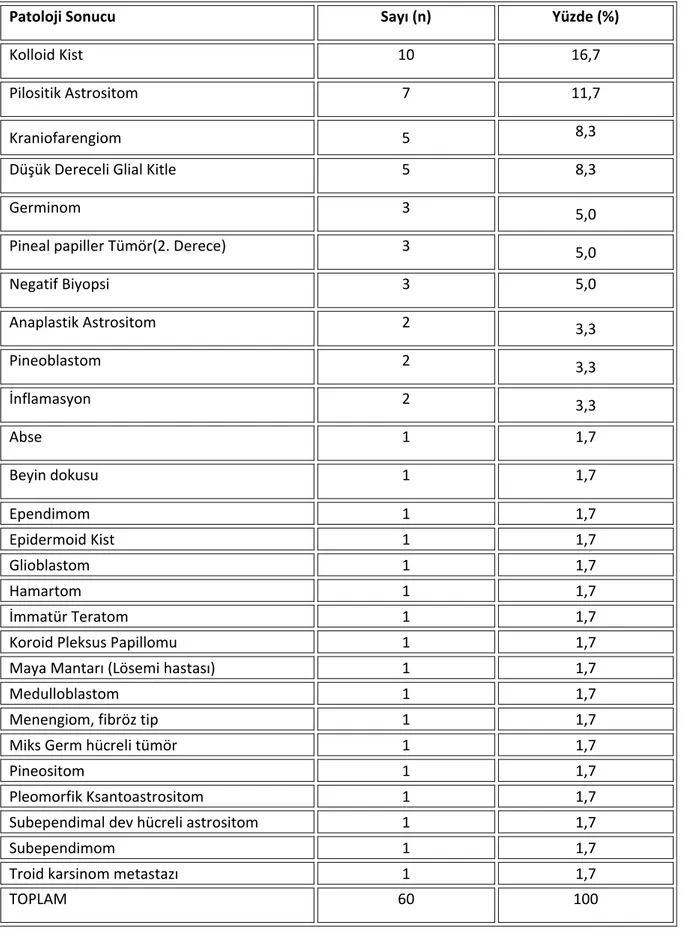
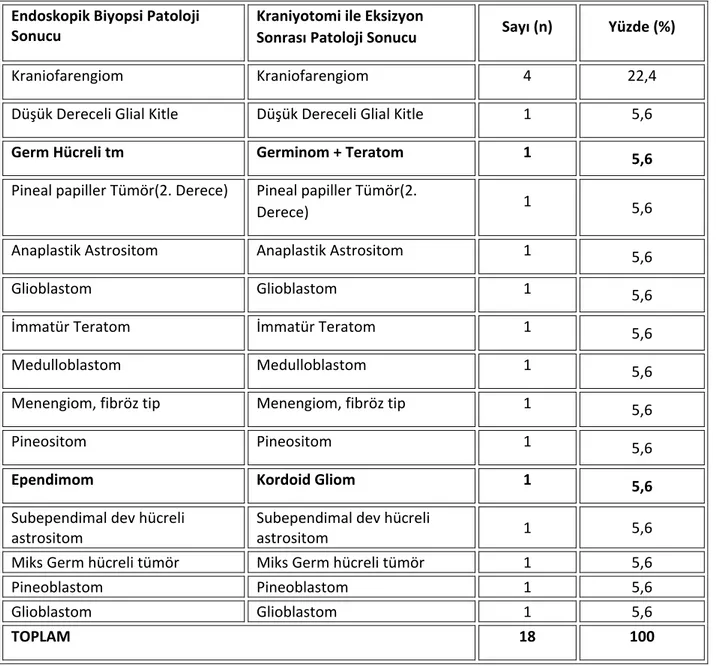
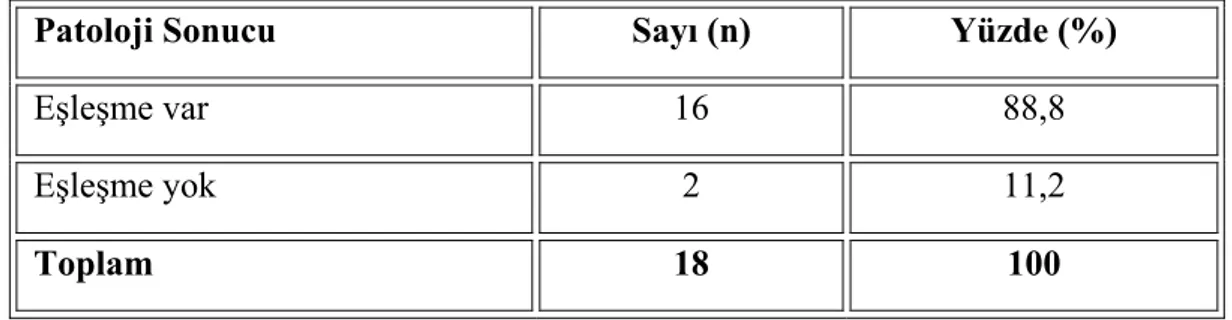
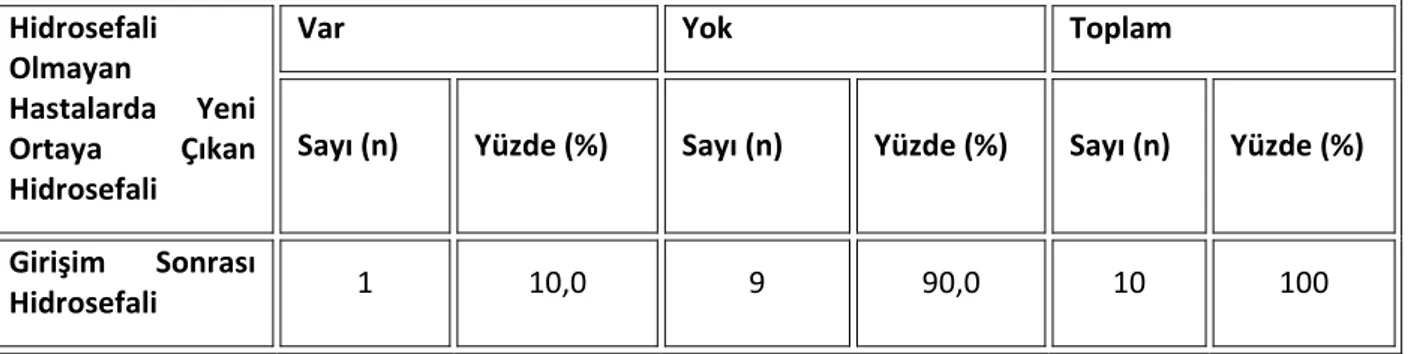
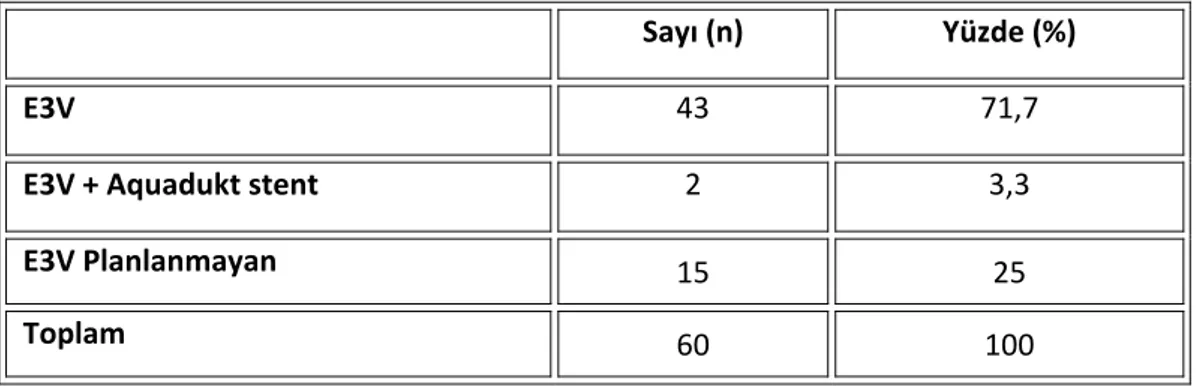
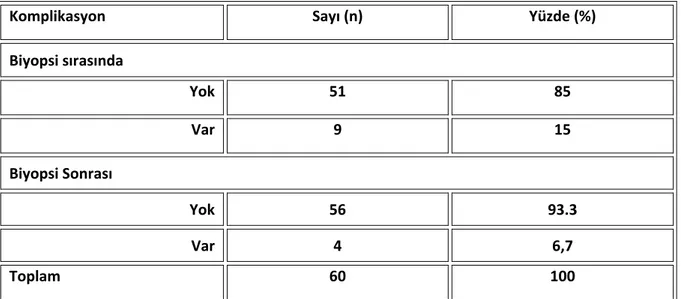
İntraventriküler endoskopik yolla alınan biyopsilerin değerlendirilmesi
Tam metin
Şekil

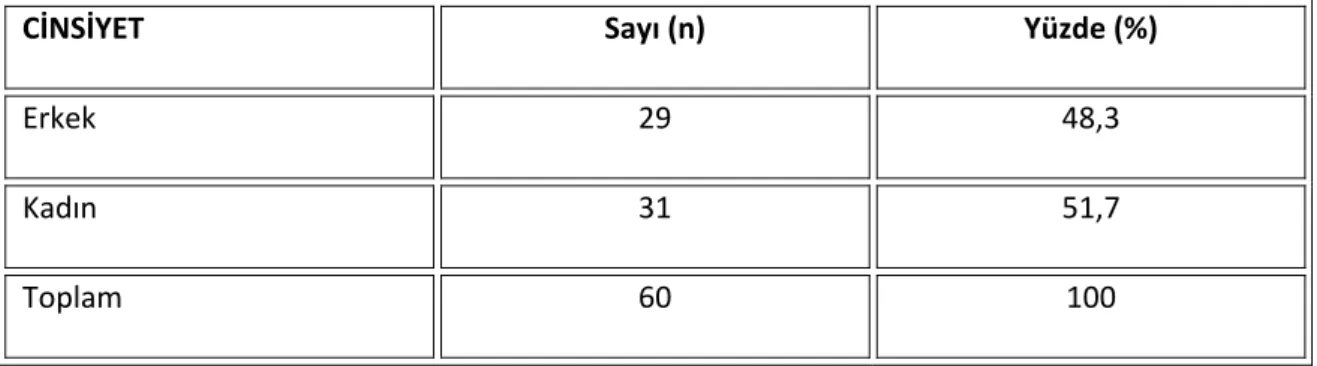
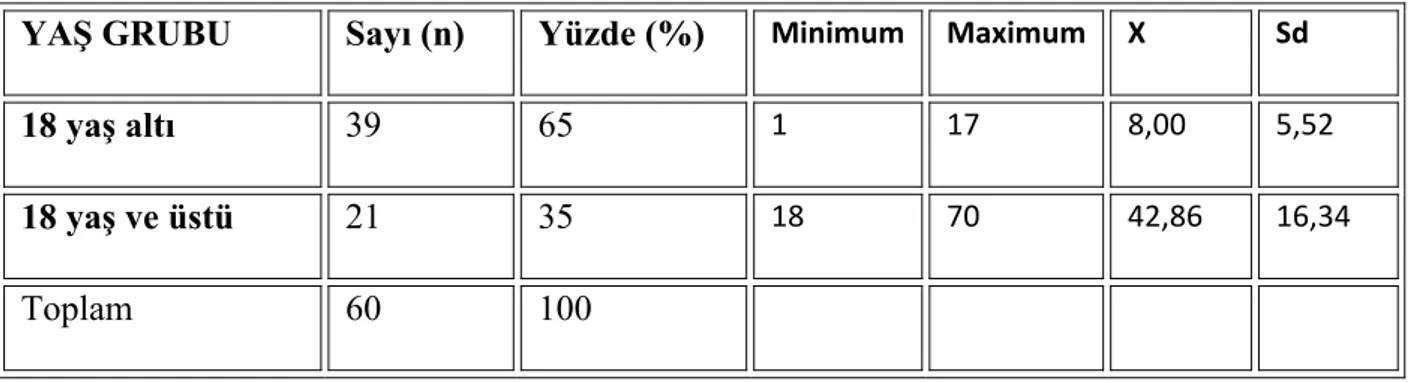

Benzer Belgeler
4 — Belediye İstimlâk Kanununun dördüncü madde si, istimlâk bedeli karşılığı temin edilmiş mıntakalarda başlanılan işler tamamlanmadıkça,
Kro- nik sinüzit ve kontrol gruplarý arasýnda septum deviasyonu, lamellar konka bulloza, bülböz konka bulloza, haller hücresi, ve agger nazi hücresi oranlarý açýsýndan anlamlý
Böbrek ya da üreter taş cerrahisi, gebeliğe bağlı hidronefroz, üreter patolojileri, ESWL, malignensi ve retroperitoneal fibrozis nedeni ile gelişen darlıklar
Bu çalışmada; Bakırköy Ruh ve Sinir Hastalıkları Eğitim ve Araştırma Hastanesi Beyin ve Sinir Cerrahisi Kliniği’ne Ocak 1995-Ocak 2005 yılları arasında baş- vuran
Sonuç olarak alt GİS endoskopisi ile erken tanı; sağ kalım, bireysel refah ve sosyoekonomik unsurlar açısından başta maligniteler olmak üzere, enflamatuar
Enhancement EP- CI Image Clustering using Efficient Fuzzy C Means Adaptive Image Thresholding Segmented Image Parameters estimation... efficiency of adaptive filters is
Therefore, women's career officials see that their position in public office is not contradictory to the verse, (2) the harmony of women household career officers in general
the proposed protocol works well in the DDMUAV network provides good throughput, average delay and reduced packet loss ratio compared to the epidemic protocol available in